|
2018-2019 |
|
ПО ХИМИИ
ШКОЛЬНЫЙ ЭТАП
1 | К 265 г раствора нитрата свинца (II) с массовой долей соли 15% добавили цинковые опилки. Через некоторое время массовая доля нитрата свинца (II) в растворе стала равна 12,6 %. Вычислите массу выделившегося свинца. (6 баллов) |
2 | Какую пространственную конфигурацию имеют молекулы SO2, SO3, CO2, NH3? Какие из этих молекул полярны (диполи)? (4 балла) |
3 | При некоторой температуре равновесие в системе СО2+Н2↔СО+Н2О (г) установилось при концентрациях 2,6,3 и 4моль/л соответственно. После этого водяной пар убрали из системы водопоглощающим средством. Рассчитайте новые равновесные концентрации. (5 баллов) |
4 | Вычислите процентное содержание KIO3 в растворе, если при взаимодействии 3,21 г этого раствора с избытком KI в разбавленном сернокислом растворе, образуется 0,635 г йода. (3 балла) |
5 | Какую массу 10%-ного раствора гидрокарбоната натрия необходимо добавить к 150 г 8%-ного раствора соляной кислоты, чтобы уменьшить ее массовую долю в 2 раза? (5 баллов) |
6 | В каком объёме воды можно растворить 4,2 г карбоната магния (ПР=2,1*10 -5)? (2 балла) |
|
2018-2019 |
|
ПО ХИМИИ
ШКОЛЬНЫЙ ЭТАП
1. |
АЛХИМИЯ И ГЁТЕ Алхимики не знали состава используемых веществ, не умели их анализировать и химические взаимодействия записывали словами. Вещества, участвующие в химических реакциях они называли, не руководствуясь никакими правилами, и поэтому понять, что они делали, было очень трудно. Гѐте в «Фаусте» дал пример записи алхимической процедуры: «Являлся красный лев – и был он женихом, И в тёплой жидкости они его венчали 5 С прекрасной лилией, и грели их огнём, И из сосуда их в сосуд перемещали…» Зная особое пристрастие алхимиков к соединениям ртути, можно предположить, что «Красный лев» - это красный оксид ртути HgO, а «прекрасная лилия» - хлороводородная кислота HCl. Вопросы: 1) Составьте уравнение химической реакции между «красным львом» и «прекрасной лилией». 2) Сколько г «красного льва» может прореагировать с 100 г 36,5%-ного раствора «прекрасной лилии»? 3) Кроме ртути людям с древности было известно ещѐ 6 металлов. Назовите любые 3 металла (кроме ртути), известные людям с древности (5 баллов) |
2. |
ЯДЫ И ОТРАВЛЕНИЯ А) Известно, что по официальной версии Наполеон умер от рака желудка. Спустя 140 лет ученые пришли к выводу, что, скорее всего он был отравлен ядовитыми соединениями элемента Х. Вероятно, Наполеону длительное время в пищу подмешивали вещество Х2О3 в малых дозах.
Б) 17 декабря 1916 года князь Феликс Юсупов с сообщниками пытался отравить приближенного к семье последнего российского императора, одну из самых одиозных фигур российской истории - Григория Распутина, добавив яд «Y» в пирожные. Однако яд не подействовал. Проведённый анализ позволил определить состав яда: калий - 60%, углерод - 18,46% и азот – 21,54%. Вопросы: 1) Установите элемент «Х», если известно, что его массовая доля в оксиде составляет75,7%. 2) К металлам или неметаллам относится элемент «Х»? 3) Выведите формулу вещества, которым пытались отравить Распутина. (5 баллов) |
3. |
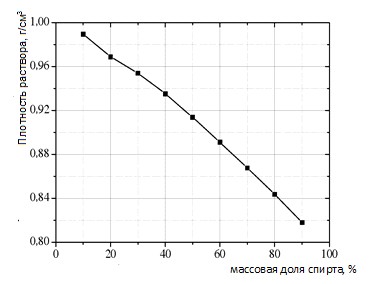
Дмитрий Иванович Менделеев изучал свойства водных растворов этилового спирта C2H6O, пытаясь доказать, что в этих растворах образуются химические соединения. Найденная Менделеевым зависимость плотности растворов спирта от массовой доли спирта имеет вид: В одном из опытов он смешал 500 мл воды и 500 мл спирта. Чему равен объем полученного раствора? Плотность воды примите равной 1,00 г/мл, а спирта – 0,79 г/мл. (4 балла) |
4. | Смесь трёх простых газообразных веществ, взятых в равном мольном соотношении. Число атомов азота в смеси в 1,5 раза меньше числа атомов кислорода и в 2 раза больше числа атомов гелия. Определите молярную массу смеси. (5 баллов) |
5. | Массовая доля металла в его гидроксиде составляет 52,3%. Определите формулу гидроксида, напишите 2 уравнения, иллюстрирующие его свойства. (5 баллов) |
6. | 13 см3 металла содержит 12*10 23 валентных электронов (плотность металла 8,64 г/см 3). Определите металл. Его электронная конфигурация? (3 балла) |
|
2018-2019 |
|
ПО ХИМИИ
ШКОЛЬНЫЙ ЭТАП
(8 баллов) Вещества А и Б - бесцветные жидкости состава С4Н10О. Жидкость А реагирует с натрием, выделяя водород, а также с HI (образуется вещество В, вступающее в реакции замещения) и с концентрированной серной кислотой (образуется вещество Г, обесцвечивающее бромную воду). Б не реагирует с натрием, но реагирует с НI, образуя вещество Д, по химическим свойствам похожее на вещество В. 1. Назовите вещества А и Б. 2. Напишите уравнения всех упомянутых реакций. |
(5 баллов) Навеску смеси гидрида лития и нитрида бария разделили на две равные части. Одну часть растворили в воде, вторую – в избытке соляной кислоты. Объём газов, выделившихся в реакции с водой, в полтора раза больше, чем в реакции с соляной кислотой. Определите массовую долю гидрида лития в исходной смеси. (10 баллов) |
(10баллов) Напишите уравнения реакций, соответствующие следующей схеме превращений: C7H9N → C7H8N2O2 → C6H3N2O4K → C5H4N2O2 → C5H6N2 В уравнениях укажите структурные формулы веществ и условиях реакций. |
(3 балла) Равновесие реакции окисления оксида азота(II) кислородом до оксида азота(IV) установилось при следующих концентрациях реагирующих веществ: С(NO)= 0,5 моль/л; С(О2) = 0,7 моль/л; С(NO2) = 2,1 моль/л. 1. Определите исходные концентрации оксида азота (II) и кислорода. 2. Как изменятся скорости прямой и обратной реакций, если в системе уменьшить общее давление в два раза? 3. Произойдет ли при этом смещение равновесия реакции? |
(4 балла) Колбу заполнили аммиаком при нормальных условиях, затем ее заполнили водой, причем весь аммиак растворился. Определите рН полученного раствора. Кд(NH4OH)=10-5 |
(4 балла) Для полного сгорания некоторого объёма углеводорода потребовалось 0,85 объёма кислорода, необходимого для сгорания такого же объёма следующего члена гомологического ряда. Установите формулы углеводородов. |
|
2018-2019 |
|
1.Бинарное соединение X образовано элементами одной группы периодической системы. Масса формульной единицы X равна 3.984 *10-23 г. Соединение X добавили к раствору сильной одноосновной кислоты, массовая доля водорода в которой равна 0. 995%. Запишите формулу образующейся соли.
2.При полном сгорании углеводорода расходуется в 2.5 раза меньше кислорода, чем при полном сгорании такого же объема его гомолога, содержащего на 22 атома углерода больше. Установите формулы углеводородов. В ответе запишите относительную молекулярную массу более тяжелого углеводорода (с точностью до целых).
3.Смесь для воздушного шара объемом 112 м3 (н. у.) состоит из водорода и гелия. При нормальных условиях шар способен оторвать от земли одного воздухоплавателя массой 75 кг. Масса незаполненного шара с корзиной составляет 55 кг. Чтобы шар оторвался от земли, необходимо, чтобы его общая масса не превышала 145 кг. Определите объем водорода (в м3) в смеси, в ответе укажите только число с точностью до целых.
4.Для очистки воды в Москве используют гипохлорит натрия, который получают электролизом раствора вещества X. Определите X. В ответе приведите его формулу.
5.Белое вещество A может быть получено сжиганием порошка переходного металла X в кислороде. При обработке хлором смеси A с углем образуется бесцветная жидкость Б, содержащая 25.24 масс.% элемента X. Определите X. В ответе укажите его порядковый номер.
6.При обработке 3.00 г минерала M избытком сильной кислоты выделяется 0.4313 л углекислого газа (при 298 К и давлении 11 бар). M содержит 55.31% меди (по массе) и состоит из четырех элементов. Примите, что все атомы меди имеют степень окисления +2. Сколько молей кислорода содержится в одном моле M?
7.Вещество A представляет собой ядовитый газ с резким запахом, он тяжелее воздуха, но его плотность по воздуху меньше 2. При взаимодействии газа A со щелочью образуются вода и две соли, одна из которых содержит кислород, а другая нет. Газ A хорошо горит в кислороде, при этом образуются только два газа (при н. у.), входящие в состав воздуха. Установите формулу A. В ответе приведите его относительную молекулярную массу, округленную до ближайшего целого.
8.Соляную кислоту добавляли к 10 мл 0.2 М раствора алюмината натрия. Одно и то же количества осадка выпало при добавлении как 10 мл, так и 20 мл раствора HCl. Чему равна молярная концентрация раствора HCl (в моль/л)?
9.При взаимодействии фторида трехвалентного металла с парами воды при 4000C образовались смешанный оксид металла, содержащий 26.56% кислорода по массе, и смесь двух газов. Во сколько раз одного из двух газов в этой смеси больше, чем другого, по числу молекул?
10.В ящике находится 501 монета. Все монеты одинаковы и сделаны из сплава серебра и золота. Масса одной монеты равна 4.13г. Одну из монет растворили в 12.6 г 50%-ной азотной кислоты, при этом выделился бурый газ, а после реакции осталось 0.06 моль непрореагировавшей азотной кислоты. Сколько рублей стоит ящик с монетами после эксперимента, если 1 моль золота стоит 5 рублей (дореволюционных), а 1 моль серебра – 2 рубля?
11.При получении ацетилена пиролизом метана в реактор поступает чистый метан, а выходит из него газовая смесь, содержащая продукты реакции (ацетилен и водород) и непрореагировавший метан. Анализ газовой смеси на выходе из реактора показал, что ее плотность по водороду равна 5.0. Сколько процентов метана вступило в реакцию?