УДК54.062
Тематическое направление: Аналитическая химия.
Химико-токсикологическое исследование амитриптилина в моче
©Супрунчук1Анастасия Александровна, Киричек1, 2+ Александр Васильевич, Шабалина2* Ангелина Эдуардовна, Петухов3, 4 Алексей Евгеньевич, Смирнов3 Алексей Витальевич, Родионова4 Галина Михайловна, Стрельникова5 Татьяна Анатольевна, Тюрин5 Игорь Александрович
1Кафедра «Экспертиза в допинг - и наркоконтроле». Российский химико-технологический университет им. . Ул. Героев Панфиловцев, д. 20. г. Москва, 125480. Россия. Тел. (495)4952426. E-mail:*****@***ru
2Отдел судебно-химической экспертизы. 111 Главный государственный центр судебно-медицинских и криминалистических экспертиз Министерства обороны Российской Федерации. Госпитальная площадь, д. 3. г. Москва. 105229. Россия. Тел.: (499)2635798. E-mail:*****@***ru, E-mail:*****@***ru
3Химико-токсикологическая лаборатория. Московский научно-практический центр наркологии Департамента здравоохранения г. Москвы. Ул. Болотниковская, д. 16. г. Москва, 113149. Россия. Тел.(499)6196049. E-mail:*****@***ru, E-mail:*****@***ru
4Кафедра фармацевтической и токсикологической химии им. . ФГАОУ ВО«Первый Московский государственный медицинский университет имени » Минздрава России (Сеченовский Университет). Ул. Трубецкая,. г. Москва. 119991. Россия. Тел.(495)690-17-57.E-mail:*****@***ru
5Химико-токсикологическая лаборатория. Научно-исследовательский институт скорой помощи им. Департамента здравоохранения города Москвы. Большая Сухаревская пл., д. 3. г. Москва, 129090. Россия. Тел. (499)620-11-66. E-mail: *****@***ru, E-mail: *****@***ru
_______________________________________________
*Ведущий направление; +Поддерживающий переписку
Ключевые слова: трициклические антидепрессанты, амитриптилин, химико-токсикологическое исследование, хромато-масс-спектрометрия.
Аннотация
На территории Российской Федерации среди всех антидепрессантов наиболее широко применяются препараты группы трициклических антидепрессантов. Наиболее распространенным среди лекарственных средств данной группы является амитриптилин. Он оказывает тимолептическое, антидепрессивное, анксиолитическое, седативное действие. Ингибирует обратный захват нейромедиаторов (норадреналина, серотонина) пресинаптическими нервными окончаниями нейронов, вызывает накопление моноаминов в синаптической щели и усиливает постсинаптическую импульсацию. При длительном применении снижает функциональную активность (десенситизация) бета-адренергических и серотониновых рецепторов мозга, нормализует адренергическую и серотонинергическую передачу, восстанавливает равновесие этих систем, нарушенное при депрессивных состояниях. Блокирует м-холино - и гистаминовые рецепторы центральной нервной системы. Широта терапевтического применения препарата обусловливает относительно большое количество лиц, принимающих его и, в свою очередь, довольно большой процент случаев отравлений, в том числе смертельных, данным веществом. Наиболее часто встречаются случаи случайных отравлений при несоблюдении рекомендованных дозировок и суицидальные отравления. С мочой выводится большая часть введенной дозы препарата, поэтому моча является важным объектом в химико-токсикологическом анализе, судебно-химической экспертизе и допинг-контроле. В данной работе использован метод изолирования и экстракции амитриптилина из мочи с использованием готовых экстракционных трубок TOXI-PROBES, имеющих комбинированный экстрагент, и позволяющих проводить одновременно с экстракцией очистку проб. В работе подобраны наиболее эффективные системы для разделения амитриптилина методом хроматографии в тонком слое сорбента, рассчитаны величины Rf в различных системах растворителей, подобраны реактивы для окрашивания. Получены спектры амитриптилина различными физико-химическими методами (УФ-спектроскопия, ГХ/МС). Методом хромато-масс-спектрометрии рассчитаны концентрации амитриптилина при терапевтическом приеме данного лекарственного средства, а также концентрации при передозировках. Высокие концентрации препарата коррелировали со степенью тяжести отравления, где имели место осложнения после интоксикации. Все наблюдаемые случаи имели относительно благоприятный исход в лечении, но при неоказании или несвоевременном оказании помощи возможен летальный исход.
UDC 54.062
Theme: Analytical Chemistry.
Chemical-toxicological study of amitriptyline in urine
©Suprunchuk1 Anastasiya Aleksandrovna, Kirichek1, 2+Aleksandr Vasilevich, Shabalina2*Angelina Eduardovna, Petukhov3, 4 Aleksey Yevgenyevich, Smirnov3 Aleksey Vitalevich, Rodionova4 Galina Mikhailovna, Strelnikova5 Tatiana Anatoliyevna, Tyurin5 Igor Aleksandrovich
1 Department of Expert Evaluation in Doping Control and Drug Control. D. Mendeleyev University of Chemical Technology of Russia. 20 Geroev Panfilovtsev str., Moscow, 125480. Russia. Tel.: (495) 495-24-26. E-mail: *****@***ru
2 Department of forensic chemical examination. State-owned Federal State Institution 111th Main Federal Center of medical and forensic examination of the Ministry of Defense of the Russian Federation. 3 Gospitalnaya square, Moscow, 105229. Russia. Tel.: (499) 263-57-98. E-mail: *****@***ru, E-mail:*****@***ru
3 Moscow scientific and practical center for narcology of the Department of health of Moscow. Doctor of clinical laboratory diagnostics.16Bolotnikovskaya square, Moscow, 113149. Russia. Tel.: (499)6196049. E-mail: *****@***ru, E-mail:*****@***ru
4 Department of Pharmaceutical and Toxicology Chem. A. P. Arzamastseva. Federal State Autonomous Educational Institution of Higher Education I. M. Sechenov First Moscow State Medical University of the Ministry of Health of the Russian Federation (Sechenov University). 2-4 Bolshaya Pirogovskaya st., Moscow, 119991. Russia. Tel.: (495)690-17-57. E-mail: *****@***ru
5 Chemical and toxicological laboratory. State budgetary institution of public health of Moscow "Research Institute of First Aid to them. NV Sklifosovsky Department of Health of Moscow ". kharevskaya pl., 3, Moscow, 129090. Russia. Tel.: (499)620-11-66. E-mail: *****@***ru, E-mail: *****@***ru
_____________________________________________
*Leading researcher; +Correspondent author
Key words: tricyclic antidepressants, amitriptyline, chemical-toxicological study, chromatography-mass spectrometry.
Abstract
Among all antidepressants, the preparations of the tricyclic antidepressant group are most widely used in the territory of the Russian Federation. Amitriptyline is the most popular among the medicinal product of this group. The one acts as thymoleptic, antidepressant, anxiolytic, sedative agent. This preparation inhibits reuptake of neuromediators (noradrenaline, serotonin) with presynaptic neural endings of neurons and causes accumulation of monoamines in the synaptic cleft, and enhances postsynaptic input. With prolonged use, the one reduces functional activity (desensitization) of beta-adrenergic, serotonin receptors of the brain, normalizes adrenergic and serotonergic transmission, and restores these systems balance, disturbed during depressive states. This preparation blocks m-choline - and histamine receptors of the central nervous system. The range of therapeutic use of the preparation accounts for relatively large number of persons, taking it, and in turn, a rather large percentage of poisoning occurrence, among other things fatal, with this substance. The cases of accidental poisoning, in case of non-compliance with the recommended dosages and suicidal poisoning are the most common. The most part of preparation-administered dose is excreted, so urine is an important object in the following: chemico-toxicological analysis, chemical evidence in court and doping control. In this paper, the method of isolating and extracting of amitriptyline from urine in connection with TOXI-PROBES ready-made extraction tubes, which have a combined extraction fluid, and permitting to do sample purification simultaneously with extraction, is used. The most effective systems for amitriptyline separation by chromatography in a thin layer of sorbent were picked up, the values of Rf in various solvent systems were calculated, and reagents for staining were picked up. Amitriptyline spectra were obtained by means of different physicochemical methods (UV-spectroscopy, gas chromatography-mass spectrometry). The concentrations of amitriptyline while therapeutic administration of this preparation, as well as the concentrations in overdoses were calculated by chromatography-mass spectrometry. High concentrations of the preparation were correlated with severity of poisoning; the complications have taken place after intoxication. All observed cases had a relatively favorable treatment outcome, but with failure to provide medical attention or untimely delivery of care, the fatality is possible.
Введение
В настоящее время на территории Российской Федерации среди всех лекарственных средств - антидепрессантов наиболее широко используются трициклические антидепрессанты, а среди них более всего амитриптилин. Как и все трициклические антидепрессанты, амитриптилин предотвращает обратный захват нейромедиаторов. Влияет на вегетативную нервную систему, поэтому вызывает множество эффектов, в том числе побочные. На основе индекса смертельной токсичности данный препарат относят к средствам с «недопустимым риском», т. е. после применения случается более 40 смертельных случаев на 1 млн выписанных рецептов. Максимальная токсичность проявляется в первые 6 часов после передозировки. У амитриптилина связывание с белками плазмы 94%, объем распределения 5-22 л/кг, период полувыведения 3-36 часов. Основной метаболит амитриптилина - N-деметилнортриптилин [1]. Предшествует ему нортриптилин - активный метаболит амитриптилина. 35% введенной дозы выделяется с мочой за 24 ч. в виде метаболитов, за 11 дней выводится почти 80% дозы и только 0,2% препарата находится в неизмененном виде [2].
Экспериментальная часть
Для качественного обнаружения предложен предварительный метод хроматографии в тонком слое сорбента. В ходе исследования был проведен подбор оптимальных условий с целью обнаружения амитриптилина. Хроматографирование проводили в каждой системе растворителей трижды с усреднением результатов.
Проводили детекцию пятен в ультрафиолетовом свете при длинах волн 264 и 365 нм, а также подбирали реактивы для окрашивания амитриптилина, используя общеалкалоидные осадительные реактивы Драгендорфа (по Мунье), Фреде, Марки, Эрлиха модифицированный, Манделина, растворы йодплатината подкисленного, прочного черного К и нингидрина в ацетоне, детекцию в парах йода.
Для подтверждения предварительных данных использовали метод спектрометрии в ультрафиолетовой области спектра (УФ-спектрометрия). Для исследования использовали прибор «Agilent Technologies 8453». Снимали УФ-спектр относительно раствора сравнения. Раствор сравнения - дистиллированная вода.
Идентификацию амитриптилина и его количественное определение выполняли методом газовой хроматографии - масс-спектрометрии. Хроматографирование проводили на хромато-масс-спектрометре «Маэстро ГХ – Маэстро МСД» (Россия), работавшем в режиме ионизации электронным ударом при 70 эВ и оборудованном капиллярной колонкой НР-5МS длиной 30 м и внутренним диаметром 0,25 мм. В качестве газа-носителя использовали гелий, поток составлял 1,0 мл/мин. Температура инжектора и интерфейса составляли 280°С. Температура колонки программировалась от 90°С (выдержка 1 мин.), затем до 310°С со скоростью 35°С/мин. Время анализа 24 мин. Ввод образцов объемом 1 мкл осуществляли методом без деления потока газа-носителя.
Масс-спектрометр работал в режиме сканирования спектров электронного удара при 70 эВ в диапазоне от 31 до 550 дальтон. Напряжение электронного умножителя устанавливали по результатам работы программы AUTOTUNE из стандартного пакета математического обеспечения фирмы-производителя.
После проведения хроматографирования масс-спектры, соответствующие вершинам хроматографических пиков, сравнивали по стандартной методике с масс-спектрами библиотек «PMW_TOX3», «NIST14» и «Wiley7N». Масс-спектры считали идентифицированными при совпадении масс-спектров исследуемого вещества с библиотечным с коэффициентом подобия, рассчитанным по стандартной методике, превышающим 80%.
Количественное определение проводили методом хромато-масс-спектрометрии по иону 58,1 дальтон, в качестве подтверждающих ионов использовали ионы 202,1; 59,05; и 203,1 дальтон. Расчеты проводили методом внешнего стандарта. Для этого в пробу мочи человека, не содержащую амитриптилин, вносили данную субстанцию из расчета получения концентрации 30,4; 60,9; 121,8; 243,7; 487,5; 975,0; 1950,0; 3900,0; 7810,0; 15625,0 и 31250,0 нг/мл.
Для пробоподготовки использовали метод изолирования и экстракции амитриптилина из мочи с использованием готовых экстракционных флаконов TOXI-PROBES (производства компании «Интерлаб», Россия). Пипеткой отбирали пробу мочи и вносили во флакон с буферным раствором «TOXI-PROBES A» до метки 5 мл. При заполнении флакона до уровня органического растворителя объем пробы мочи составляет 5 мл. Встряхивали в течение 5 минут, центрифугировали при 4500 об/мин в течение 10 минут. Верхний слой органического раствора из флакона «TOXI-PROBES A» (щелочное извлечение) отбирали пипеткой, каждое в отдельности, испаряли при комнатной температуре досуха и восстанавливали смесью хлороформ-этанол (1:1) до объема 0,5 мл для дальнейшего исследования на хромато-масс-спектрометре. Исследовали на хромато-масс-спектрометре при вышеописанных настройках прибора. Строили калибровку зависимости площади хроматографического пика иона 58,1 дальтон от количества добавленного амитриптилина. Каждую концентрацию измеряли с применением автоматического дозатора образцов трижды с последующим усреднением результатов. В представленном диапазоне концентраций график калибровочной зависимости линеен. Коэффициент корреляции составил 0,998.
Исследовали мочу пациентов, поступивших в центр острых отравлений с подозрением на отравление психотропными веществами, в частности трициклическими антидепрессантами.
Результаты и их обсуждение
В таблице ниже представлены данные хроматографической подвижности (величины Rf) амитриптилина, полученных нами на пластинках ПТСХ-А-АФ-УФ «Sorbfil» и HPTLС-Si-60 F254 («Merck», Германия) размерами 10х10 см в различных системах растворителей.
Табл. 1. Значения коэффициента Rf амитриптилина в различных системах растворителей на разных пластинках
Системы растворителей | Значение коэффициента Rf ±∆X | ||
соотношение | пластинка «Sorbfil» | пластинка «Merck» | |
метанол: 25% раствор аммиака | 100:1,5 | 0,56±(0,03ч0,04) | 0,51±(0,02ч0,05) |
толуол: ацетон: этанол: 25% раствор аммиака | 45:45:7:3 | 0,71±(0,01ч0,04) | 0,65±(0,02ч0,05) |
хлороформ: ацетон: этанол: 25% раствор аммиака | 20:20:3:1 | 0,65±(0,01ч0,02) | 0,65±(0,01ч0,02) |
Также была изучена хроматографическая подвижность имипрамина, выбранного в качестве стандарта по отношению к амитриптилину, который элюировался на одной и той же пластинке вместе с амитриптилином. Рассчитана величина Rs для амитриптилина в сравнении с имипрамином в экспериментах с различными подвижными фазами и различными пластинками. Результаты представлены в таблице ниже.
Табл. 2. Значения коэффициента Rs амитриптилина при исследовании с выбранным в качестве вещества сравнения имипрамином в различных системах растворителей на различных пластинках
Системы растворителей | Значение коэффициента Rs±∆X | ||
соотношение | пластинка Sorbfil | пластинка Merck | |
метанол: 25% раствор аммиака | 100:1,5 | 1,06±(0,01ч0,04) | 1,11±(0,02ч0,05) |
толуол: ацетон: этанол: 25% раствор аммиака | 45:45:7:3 | 1,06±(0,01ч0,02) | 1,06±(0,02ч0,03) |
хлороформ: ацетон: этанол: 25% раствор аммиака | 20:20:3:1 | 1,11±(0,01ч0,02) | 0,94±(0,01ч0,02) |
Результаты окрашивания реактивами приведены в таблице 3.
Табл. 3. Окрашивание амитриптилина различными реактивами
Реактив | Окрашивание |
Реактив Фреде | оранжевое окрашивание |
Раствор йодплатината подкисленного | бурое окрашивание |
Реактив Драгендорфа (по Мунье) | розовое окрашивание |
Реактив Марки | коричневое окрашивание |
Проявление парами йода | оранжевое окрашивание |
С реактивами Манделина и Эрлиха модифицированным, раствором прочного черного К и нингидрина в ацетоне амитриптилин окрашивания не даёт.
В результате исследования методом УФ-спектрометрии был получен ультрафиолетовый спектр амитриптилина, характеризуемый максимумом абсорбции при длине волны 239 нм. Полученный УФ-спектр представлен на рисунке 1 ниже.
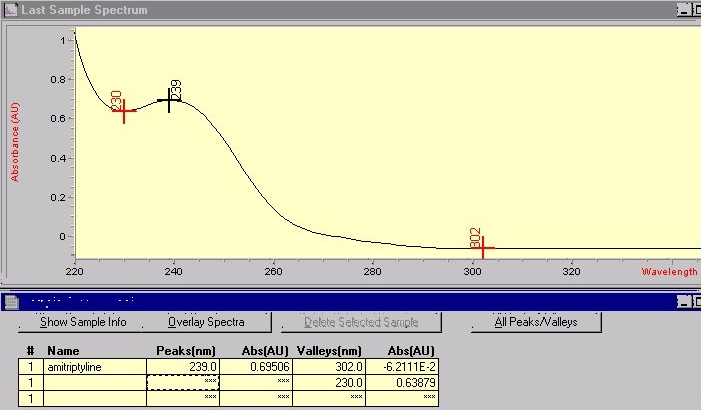
Рис. 1. УФ-спектр амитриптилина относительно раствора сравнения - дистиллированная вода.
При исследовании методом хромато-масс-спектрометрии получены хроматограммы и масс-спектр амитриптилина. Характеристические ионы 58, 59, 202, 42, 203, 214, 217 m/z. На рисунке 2 представлен фрагмент хроматограммы экстракта мочи человека с обнаруженными амитриптилином и его метаболитом нортриптилином.
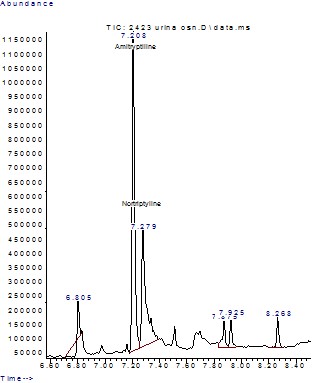
Рис. 2. Фрагмент хроматограммы экстракта мочи человека, в которой обнаружены амитриптилин и его метаболит нортриптилин.
В результате количественного определения получены концентрации амитриптилина в моче пациентов, поступивших с отравлением данным препаратом, представленные в таблице 4.
Табл. 4. Данные количественного определения амитриптилина в моче при отравлениях
№ п/п | Концентрация амитриптилина в моче, мкг/л | № п/п | Концентрация амитриптилина в моче, мкг/л | № п/п | Концентрация амитриптилина в моче, мкг/л |
1 | 16086,75 | 10 | 489,05 | 19 | 15208,40 |
2 | 20157,19 | 11 | 3505,71 | 20 | 2659,44 |
3 | 3955,00 | 12 | 6474,81 | 21 | 317,69 |
4 | 15166,09 | 13 | 366,61 | 22 | 477,63 |
5 | 2903,21 | 14 | 5311,16 | 23 | 4108,62 |
6 | 1423,35 | 15 | 26986,92 | 24 | 1129,88 |
7 | 3765,18 | 16 | 3065,55 | 25 | 902,63 |
8 | 2874,54 | 17 | 18755,48 | 26 | 1193,06 |
9 | 4297,39 | 18 | 3443,88 | 27 | 8527,99 |
В соответствии с литературными данными [3, 4] обнаруженные посмертные концентрации амитриптилина в моче составляли от 400 до 28000 (в среднем 3400) мкг/л. Относительно низкие (субтоксические и токсические) концентрации наблюдали у пациентов под № 13 и 21. В остальных случаях концентрации были очень высокие. Данные концентрации амитриптилина коррелировали со степенью тяжести пациентов. При неоказании или при несвоевременном оказании медицинской помощи в данных случаях отравлений не исключено наступление летального исхода. Кроме того, в некоторых случаях имело место сочетанное отравление амитриптилином и другими веществами, что также обусловливает тяжесть отравления.
Выводы
В представленной работе изложена методика исследования мочи по обнаружению амитриптилина и количественного его определения.
В результате:
Были подобраны системы растворителей для разделения амитриптилина и реактивы для окрашивания методом хроматографии в тонком слое сорбента и для предварительного обнаружения качественными цветными реакциями. Получены спектры амитриптилина различными физико-химическими методами (УФ-спектроскопия, ГХ/МС). Методом газовой хромато-масс-спектрометрии определены токсические концентрации амитриптилина в моче. В случаях определения подобных высоких концентраций у трупов их можно рассматривать как летальные, что соответствует литературным данным.Литература
[1] Медицинская токсикология: диагностика и лечение отравлений у человека. Т. 1: пер. с анг. М.: Медицина. 2003. 647-685с.
[2] , Токсикологическая химия. Метаболизм и анализ токсикантов. М.: ГЭОТАР-Медиа. 2008. 678-688с.
[3] Anthony C Moffat, M David Osselton, Brian Widdop. Clarke's Analysis of Drugs and Poisons. Fourth edition. London-Chicago: The Pharmaceutical Press. 2011. P.887-889.
[4] Randall C. Baselt. Disposition of Toxic Drugs and Chemicals in Man. Seventh edition. Foster city, California: Biomedical Publications. 2004. P.55-59.
References:
[1] Matthew J. Ellenhorn. Ellenhorn's Medical Toxycology: Diagnosis and Treatment of Human Poisoning. Vol. 1: translation from Eng. М.: Medicina. 2003. P.647-685.
[2] Afanas'eva E. Yu., Borisova E. Ya., Verstakova O. L., Gerasimov V. B., Eremin S. A., Eremin S. K., Ivanova G. F., Kaletin G. I., Kaletina N. I., Mishchikhin V. A., Pavlovskaya N. A., Radysh I. V., Rodchenkov G. M., Naidenova L. F., Simonov E. A., Skal'naya M. G., Skal'nyi A. V., Smirnov A. V., Syubaev R. D., Khabriev R. U., Chel'tsov V. V., Chukarin A. V., Yagudina R. I. Toxicological chemistry. Metabolism and the analysis of toxicants. - M.: GEOTAR-Media. 2008. P. 678-688.
[3] Anthony C Moffat, M David Osselton, Brian Widdop. Clarke's Analysis of Drugs and Poisons. Fourth edition. London-Chicago: The Pharmaceutical Press. 2011. P.887-889.
[4] Randall C. Baselt. Disposition of Toxic Drugs and Chemicals in Man. Seventh edition. Foster city, California: Biomedical Publications. 2004. P.55-59.



