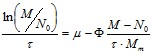 (4.1)
(4.1)
или
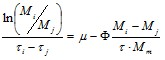
![]() (4.2)
(4.2)
до степени конверсии 0,4-0,6, то можно определить значения м и Ц. В том случае, если найденное Ц отрицательно, можно с уверенностью говорить, что процесс протекает с ингибированием избытком субстрата.
Цель работы: Изучить влияние концентрации субстрата на рост микроорганизмов.
З а д а ч и:
приготовить питательную среду с известной концентрацией субстрата S0, приготовить посевной материал с известным титром клеток, произвести засев питательной среды, рассчитать количество клеток N0 в единице объема среды, производить подсчет количества клеток в культуральной жидкости каждые 30 минут, произвести окончательный подсчет количества клеток через 24 часа после начала процесса культивирования, рассчитать удельную скорость роста м, на основании своих данных и данных полученными другими группами построить график зависимости м от S0, на основании своих данных с использованием уравнений 4.1 и 4.2 определить параметр Ф, сделать соответствующие выводы.М а т е р и а л ы и о б о р у д о в а н и е: дрожжи прессованные, сахар, сульфат аммония, фосфорнокислый калий одно - или двухзамещенный, камера Горяева, колбы конические на 250 см3, пробки ватно-марлевые.
Х о д р а б о т ы:
1) Каждая группа готовит питательную среду с определенной концентрацией сахара по заданию преподавателя в количестве не менее 150 см3.
2) В среду вносятся минеральные источники азота и фосфора. Сульфат аммония – 1% и фосфорнокислый калий – 0,5% от массы среды.
3) Готовится посевной материал на все группы. В 100 см3 теплой воды разводится 5 г прессованных дрожжей и в камере Горяева подсчитывается титр дрожжевых клеток.
4) В питательную среду вносится посевной материал в количестве 5% об.
5) Засеянная питательная среда разливается в 3 конические колбы по 50 см3. Колбы закрываются пробками и ставятся на качалку.
6) Через каждые 30 минут из колб с культуральной жидкостью отбираются пробы для подсчета титра клеток.
7) Культивирование прекращают через 24 часа после начала процесса.
8) В дальнейшем выполняют пункты 7, 8, 9, 10 задач лабораторной работы.
Вопросы на защиту лабораторной работы:
Сделайте вывод интегрального уравнения Моно. Как можно выявить механизм ингибирования роста микроорганизмов? В каких случаях используются уравнения 4.1 и 4.2? Раскройте сущность параметра Ф. В каких случаях используются параметры Ф и ц?Рекомендуемая литература:
М. Н.,, и тд. «Микобиологическое производство биологически активных веществ и препаратов"».-Москва.- «Высшая школа».-1987. , «Современные методы создания промышленных штаммов микроорганизмов».- Москва.- «Высшая школа».-1988. , и тд. «Производство белковых веществ».- Москва.- «Высшая школа».-1987. Maehara N., Komatsu H., Shimoda K. et al. Enhance of production of virus - inhibiting factor (interferon) in human diploid cells by ultraviolet irradiation and temperature shift-down after stimulation with Newcastle disease virus // Microbiol. Immunol. – 1980. – Vol. 24. – P.907-914. Schleicher J. B., Multisurface tacked plate propagation //Tissue culture: Methods and applications. – New York, Acad. Press, 1973. – P.333.Практическая работа №2
Тема. Определение скорости разбавления
Порядок выполнения работы:
При непрерывном культивировании микроорганизмов в режиме хемостата одним из основных параметров процесса является скорость разбавления D. При достижении в хемостате стационарного состояния удельная скорость роста микроорганизмов равна скорости разбавления (м=D).
Скорость разбавления можно определить как отношение объемной скорости истечения среды из ферментера к ее объему (5.1)
![]() , (5.1)
, (5.1)
где v – объемная скорость (см3/мин), V - объем среды (см3).
Так же скорость разбавления можно определить по скорости вымывания определенного вещества. Скорость вымывания вещества А можно выразить следующим образом
![]() , (5.2)
, (5.2)
где А – концентрация вещества, k – удельная скорость вымывания вещества. Знак « - « говорит о том, что концентрация вещества со временем убывает.
Приведя уравнение 5.2 к разделяющимся переменным получим
![]() . (5.3)
. (5.3)
Интегрируя 5.3 с учетом того, что при t=0 A=A0 получаем
![]() (5.4)
(5.4)
где А0 – начальная концентрация вещества.
Построив график зависимости lnA/A0 от времени t по тангенсу угла наклона линейной зависимости мы можем определить удельную скорость вымывания k или скорость разбавления D.
Цель работы: определить скорость разбавления в проточном реакторе полного смешения.
Задачи:
определить скорость разбавления по скорости вымывания вещества; определить скорость разбавления по объемной скорости истечения жидкости.Материалы и оборудование: вода, краситель метиленовый синий, фотоэлектроколориметр, модель проточного реактора полного смешения.
Ход работы:
В сосуд 3 заливается вода чуть выше уровня трубки 4 при закрытом зажиме 5. Сосуд устанавливается на магнитную мешалку 6. В сосуд 3 с водой добавляют несколько капель красителя и включают мешалку. После полного перемешивания красителя с водой открывают зажим 5 и излишек подкрашенной воды самотеком сливается в стакан 7. В полученной пробе измеряется оптическая плотность на фотоэлектроколориметре (А0). К сосуду 3 присоединяется сосуд 1 как показано на рис. 5.1. Открывается зажим 2 таким образом, чтобы вода из сосуда 1 поступала в сосуд 3 по каплям. Затем каждые 5 минут производится отбор пробы жидкости вытекающей из сосуда 3, пробы колориметрируются и результаты записываются. Отбор проб проводится до тех пор, пока показания колориметра не станут одинаковыми. По полученным данным строят график зависимости логарифма отношения оптической плотности в начальный момент времени к оптической плотности в момент времени t от времени t. По тангенсу угла наклона линейной зависимости находят скорость вымывания (скорость разбавления) При помощи мерного цилиндра определяется объемная скорость истечения жидкости v из сосуда 3 (см3/мин). Зажим 2 закрывается и сосуд 1 отсоединяется от сосуда 3. При помощи мерного цилиндра измеряется объем жидкости V в сосуде 3. По формуле 5.1 вычисляется скорость разбавления.Вопросы на защиту:
Способы определения скорости разбавления. Сравните экспериментальные значения скорости разбавления, полученные различными способами. Какой из них, по вашему мнению, является более точным? Напишите уравнения, описывающие стационарное состояние в хемостате. Дайте определение величины Dк. Что будет происходить в хемостате при м< Dк и при м> Dк?Рекомендуемая литература:
, Химия 8 класс. «Просвещение» . Москва.: 1995, С. 33-42. Биотехнология растений. - Алматы : Конжык -1996, -264 с Культура изолированных тканей и физиология морфогенеза растений.-М.:Наука, -1964, -272 с , Клеточная инженерия. - М.: Высшая школа, -1987, -127 с.Практическая работа № 3: Приобретение навыков приготовления и расчетов концентраций растворов.
Цель: Усвоить основные принципы расчетов и приготовления питательных сред для культивирования биологических объектов.
План:
Определение молярности раствора. Вычисление массовой доли раствора. Определение концентрации раствора. Чему равна молярная концентрация?Каждую химическую реакцию мы рассматриваем с качественной стороны, т. е. определяем какие вещества вступают в реакцию, и с количественной стороны, т. е. в каких массовых отношениях реагируют эти вещества без остатка. Рассматривая химическую реакцию с количественной точки зрения, нас интересуют не только массовые отношения, но и отношение числа частиц (атомов, молекул), вступивших в данную реакцию.
Если какую-либо химическую реакцию рассматривают с точки зрения числа частиц, то применяют физическую величину «количество вещества». Единицей количества вещества является моль.
Моль – это количество вещества, содержащее столько же частиц, сколько содержит атом углерода в 0,012 кг углерода.
Моль – это количество вещества, содержащее 6,02х1023 молекул, атомов или других частиц.
Молярная масса М вещества равна отношению массы m вещества к соответствующему количеству вещества ν (читается «ню»):
М= m/ν
Ход работы:
Задание 1. Приготовить раствор 500 см3 содержащий 0,6 М NaOH.
Пример расчета:
Если известна молярная концентрация раствора, то можно расчитать количество вещества в растворе по формуле: ν(NaOH) =с (NaOH) х V(раствора) = 0,6 х 0,5 = 0,3 моль (V - измеряется в литрах). Тогда масса NaOH в растворе составит m (NaOH) = ν (NaOH) х М (NaOH) = 0,3 х 40 = 12 грамм.
Задание 2. Приготовить раствора 50 см3 содержащий 0,1 М NaOH. Этот раствор используется для растворения фитогормонов.
Задание 3. При растворении кристаллогидрата CaCl2 x 6H2O массой 219 грамм в 1000 граммах воды образуется раствор. Какова массовая доля (%) хлорида кальция.
Пример расчета:
Даже при раствории в воде кристаллогидрата – соли, в полученном растворе кристаллогидрата нет. Массовую долю расчитывают для безводного хлорида кальция по формуле ω (CaCl2) = m (CaCl2) / m (раствора);
Предварительно расчитывая массу раствора и массу раствора, и массу безводного хлорида кальция в кристаллогидрате: m (раствора) = m(Н2О) + m(CaCl2 х 6Н2О) = 1000 + 219 = 1219 грамм;
ν( CaCl2 х 6Н2О) = ν( CaCl2 ) = 1 моль;
m CaCl2 = 111г. Следовательно массовая доля CaCl2 = 111/1219 = 0,091 (или 9,1%)
Задание 4. Для приготовления раствора с массовой долей NaCl 6% к 200 граммам раствора с массовой долей NaCl 30% - сколько необходимо прилить воды?

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 |




