С помощью генетического конструирования создан «супермикроб», способный утилизировать большинство основных углеводородов нефти (рис. 7). Многие природные штаммы Pseudomonas putida несут катаболические плазмиды, каждая из которых кодирует фермент для расщепления одного класса углеводородов – плазмида OCT обуславливает расщепление октана, гексана, декана; XYL – ксилола и толуола; CAM – камфары, NAH – нафталина. Плазмиды CAM и NAH сами способствуют своему переносу, стимулируя спаривание бактерий.
В результате последовательных скрещиваний был получен «суперштамм», несущий плазмиды XYL и NAH и гибридную плазмиду, содержащую части плазмид OCT и CAM. Такая мультиплазмидная бактерия растет, утилизируя неочищенную нефть. Однако возможность эффективного применения такого организма в естественных условиях
требует доказательства.
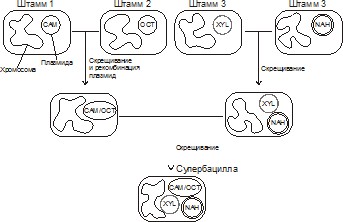
Рис. 7. Суперштамм, полученный на основе последовательных скрещиваний
четырех штаммов Pseudomonas putida (по Д. Хопвуду, 1984).
Использование методов генетического конструирования микробных штаммов-деструкторов ксенобиотиков для практического применения находится на ранней стадии. Одна из основных проблем при конструировании микроорганизмов на основе природных катаболических плазмид – стабильность. Стабильность систем «хозяин-вектор» особенно важна при интродукции штаммов в естественную среду. При возвращении микроорганизма с новой катаболической функцией в исходную природную среду ему приходится конкурировать с хорошо адаптированной к данным условиям среды естественной микрофлорой, сталкиваться с огромным разнообразием источников углерода, в том числе высокотоксичных. При этом совершенно неясны перспективы сохранения стабильности новой катаболической функции и, следовательно, самого штамма.
Пока существует большой разрыв между достижениями, полученными в конструировании микроорганизмов, и возможностями их практического применения. Вероятно, в будущем наиболее перспективными для детоксикации ксенобиотиков будут биологические системы, состоящие из микробиологической консорции индивидуальных организмов и микробных сообществ, полученных методами клеточной и генетической инженерии.
Рекомендуемая литература:
, , Методы интенсификации процесса биологической очистки сточных вод. – М., 1987. Микроорганизмы очистных сооружений. – Л., 2008. , Сбраживание осадков городских сточных вод в метанотенках. – М., 1986. , Анаэробная очистка концентрированных сточных вод. – М., 1989. Экологическая биотехнология. / под ред. К. Ферстера и Д. Вейза. –Л., 1990. , Биологические фильтры. – М., 2002. Bellmany W. D. The use of microbiological agents in upgrading waste for feed and food. –London, 2003.Контрольные задания для СРС [1,4], [2, 3]
Чем вызвана необходимость генетического конструирования «супермикробов» Принципиальные отличия химических показателей в составе нефтяных загрязнений Меры реализации современных методов утилизации нефтяных загрязнений
Практические занятия
Практическая работа №1
Тема: Исторические факты развития экологической биотехнологии
Одной из характерных особенностей роста микроорганизмов являются часто наблюдаемые эффекты его ингибирования избытком субстрата. Удельная скорость роста культур микроорганизмов на начальном участке зависимости растет с увеличением концентрации субстрата, выходит на насыщение, а затем при высоких концентрациях субстрата начинает уменьшаться. В силу этого активный рост популяции становится возможным лишь в узком диапазоне концентраций субстрата.
При анализе экспериментальных данных, если есть основания считать, что процесс может ингибироваться избытком субстрата необходимо исследовать зависимость накопления клеток или продуктов реакции в экспоненциальной фазе при различных начальных концентрациях субстрата с определением удельной скорости роста м. Если зависимость м от S0 обнаружит экстремальный характер, это будет однозначно свидетельствовать в пользу процесса с ингибированием избытком субстрата.
Кроме того, информацию о том, что рост микроорганизма связан с ингибированием избытком субстрата, можно получить из анализа одной кинетической кривой роста. Если использовать линеаризацию экспериментальных данных в координатах уравнений
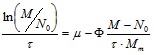 (4.1)
(4.1)
или
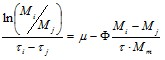
![]() (4.2)
(4.2)
до степени конверсии 0,4-0,6, то можно определить значения м и Ц. В том случае, если найденное Ц отрицательно, можно с уверенностью говорить, что процесс протекает с ингибированием избытком субстрата.
Цель работы: Изучить влияние концентрации субстрата на рост микроорганизмов.
З а д а ч и:
приготовить питательную среду с известной концентрацией субстрата S0, приготовить посевной материал с известным титром клеток, произвести засев питательной среды, рассчитать количество клеток N0 в единице объема среды, производить подсчет количества клеток в культуральной жидкости каждые 30 минут, произвести окончательный подсчет количества клеток через 24 часа после начала процесса культивирования, рассчитать удельную скорость роста м, на основании своих данных и данных полученными другими группами построить график зависимости м от S0, на основании своих данных с использованием уравнений 4.1 и 4.2 определить параметр Ф, сделать соответствующие выводы.М а т е р и а л ы и о б о р у д о в а н и е: дрожжи прессованные, сахар, сульфат аммония, фосфорнокислый калий одно - или двухзамещенный, камера Горяева, колбы конические на 250 см3, пробки ватно-марлевые.
Х о д р а б о т ы:
1) Каждая группа готовит питательную среду с определенной концентрацией сахара по заданию преподавателя в количестве не менее 150 см3.
2) В среду вносятся минеральные источники азота и фосфора. Сульфат аммония – 1% и фосфорнокислый калий – 0,5% от массы среды.
3) Готовится посевной материал на все группы. В 100 см3 теплой воды разводится 5 г прессованных дрожжей и в камере Горяева подсчитывается титр дрожжевых клеток.
4) В питательную среду вносится посевной материал в количестве 5% об.
5) Засеянная питательная среда разливается в 3 конические колбы по 50 см3. Колбы закрываются пробками и ставятся на качалку.
6) Через каждые 30 минут из колб с культуральной жидкостью отбираются пробы для подсчета титра клеток.
7) Культивирование прекращают через 24 часа после начала процесса.
8) В дальнейшем выполняют пункты 7, 8, 9, 10 задач лабораторной работы.
Вопросы на защиту лабораторной работы:
Сделайте вывод интегрального уравнения Моно. Как можно выявить механизм ингибирования роста микроорганизмов? В каких случаях используются уравнения 4.1 и 4.2? Раскройте сущность параметра Ф. В каких случаях используются параметры Ф и ц?Рекомендуемая литература:
М. Н.,, и тд. «Микобиологическое производство биологически активных веществ и препаратов"».-Москва.- «Высшая школа».-1987. , «Современные методы создания промышленных штаммов микроорганизмов».- Москва.- «Высшая школа».-1988. , и тд. «Производство белковых веществ».- Москва.- «Высшая школа».-1987. Maehara N., Komatsu H., Shimoda K. et al. Enhance of production of virus - inhibiting factor (interferon) in human diploid cells by ultraviolet irradiation and temperature shift-down after stimulation with Newcastle disease virus // Microbiol. Immunol. – 1980. – Vol. 24. – P.907-914. Schleicher J. B., Multisurface tacked plate propagation //Tissue culture: Methods and applications. – New York, Acad. Press, 1973. – P.333.Практическая работа №2
Тема. Определение скорости разбавления
Порядок выполнения работы:
При непрерывном культивировании микроорганизмов в режиме хемостата одним из основных параметров процесса является скорость разбавления D. При достижении в хемостате стационарного состояния удельная скорость роста микроорганизмов равна скорости разбавления (м=D).
Скорость разбавления можно определить как отношение объемной скорости истечения среды из ферментера к ее объему (5.1)
![]() , (5.1)
, (5.1)
где v – объемная скорость (см3/мин), V - объем среды (см3).
Так же скорость разбавления можно определить по скорости вымывания определенного вещества. Скорость вымывания вещества А можно выразить следующим образом
![]() , (5.2)
, (5.2)
где А – концентрация вещества, k – удельная скорость вымывания вещества. Знак « - « говорит о том, что концентрация вещества со временем убывает.
Приведя уравнение 5.2 к разделяющимся переменным получим
![]() . (5.3)
. (5.3)
Интегрируя 5.3 с учетом того, что при t=0 A=A0 получаем
![]() (5.4)
(5.4)
где А0 – начальная концентрация вещества.
Построив график зависимости lnA/A0 от времени t по тангенсу угла наклона линейной зависимости мы можем определить удельную скорость вымывания k или скорость разбавления D.
Цель работы: определить скорость разбавления в проточном реакторе полного смешения.
Задачи:
определить скорость разбавления по скорости вымывания вещества; определить скорость разбавления по объемной скорости истечения жидкости.Материалы и оборудование: вода, краситель метиленовый синий, фотоэлектроколориметр, модель проточного реактора полного смешения.
Ход работы:
В сосуд 3 заливается вода чуть выше уровня трубки 4 при закрытом зажиме 5. Сосуд устанавливается на магнитную мешалку 6. В сосуд 3 с водой добавляют несколько капель красителя и включают мешалку. После полного перемешивания красителя с водой открывают зажим 5 и излишек подкрашенной воды самотеком сливается в стакан 7. В полученной пробе измеряется оптическая плотность на фотоэлектроколориметре (А0). К сосуду 3 присоединяется сосуд 1 как показано на рис. 5.1. Открывается зажим 2 таким образом, чтобы вода из сосуда 1 поступала в сосуд 3 по каплям. Затем каждые 5 минут производится отбор пробы жидкости вытекающей из сосуда 3, пробы колориметрируются и результаты записываются. Отбор проб проводится до тех пор, пока показания колориметра не станут одинаковыми. По полученным данным строят график зависимости логарифма отношения оптической плотности в начальный момент времени к оптической плотности в момент времени t от времени t. По тангенсу угла наклона линейной зависимости находят скорость вымывания (скорость разбавления) При помощи мерного цилиндра определяется объемная скорость истечения жидкости v из сосуда 3 (см3/мин). Зажим 2 закрывается и сосуд 1 отсоединяется от сосуда 3. При помощи мерного цилиндра измеряется объем жидкости V в сосуде 3. По формуле 5.1 вычисляется скорость разбавления.Вопросы на защиту:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 |




