Спектроскопия PELDOR: структура каналов, формируемых антибиотиками в биологических мембранах
Общая формулировка проблемы. Молекулярные механизмы действия антибиотиков на клетки бактерий до сих пор во многом пока неясны. Для антибиотиков класса пептидов грибкового происхождения можно считать более или менее определенным, что их воздействие на клетки бактерий состоит в нарушении целостности клеточных мембран. Считается, что к такому нарушению приводит формирование пептидами каналов в мембранах. Однако надежных данных о надмолекулярной структуре этих каналов в литературе нет. Сложность задачи исследования состоит в том, что необходимо применять методы, чувствительные к измерениям расстояний в нанометровом диапазоне.
Формулировка конкретной задачи. Исследование методом импульсного двойного электрон-электронного резонанса (PELDOR) надмолекулярной структуры каналов, формируемых в модельной биологической мембране (из липидов еРС) молекулами спин-меченого пептида-антибиотика аламетицина.
Авторы исследования, лаборатория. , , в сотрудничестве с Я. Раапом (Лейденский университет, Нидерланды), С. Тониоло и его сотр. (университет г. Падова, Италия). Лаборатория химии и физики свободных радикалов (зав. лаб. ).
Используемый подход. Пептид-антибиотик аламетицин, спин-меченый в разных положениях (синтезирован С. Тониоло и сотр.), изучался с помощью развитой авторами ( и ) метода PELDOR. Метод PELDOR сейчас активно используется во многих лабораториях мира, он позволяет получать данные о расстояниях между спиновыми метками в нанометровом диапазоне и на основе этого делать выводы о конформации биомолекул и их самоассоциации (агрегации).
Полученные результаты. На рис. 1 показана найденная конформация аламетицина в модельной биологической мембране еРС (пептид содержит две нитроксильные спиновые метки ТОАС в положениях 1 и 16 аминокислотной последовательности). Из данных для однократно меченых пептидов (в положениях 1, 8 или 16) получены межмолекулярные функции распределения в нанометровой шкале расстояний и данные о числе молекул пептида в агрегатах. Это число оказалось близким к 4 (т. е. образуются тетрамеры). Определена относительная глубина погружения разных меток внутрь мембраны. Полученная совокупность данных позволила построить геометрическую модель надмолекулярной структуры агрегатов, которые формируют каналы в мембранах – см. рис. 2.
Подробно изложено в статьях:
1. , , Марьясов двойной электрон-электронный резонанс (PELDOR) - спектроскопия ЭПР в нанометровом диапазоне расстояний, Успехи химии, 6, 515-551, 2008
2. Milov A. D., Samoilova R. I., Tsvetkov Yu. D., DeZotti M., Formaggio F., Toniolo C., Handgraaf J.-W., Raap J. Structure of self-aggregated alamethicin in ePC membranes detected by pulsed electron-electron double resonance and electron spin echo envelope modulation spectroscopies // Biophys. J., 96, 3197-3].
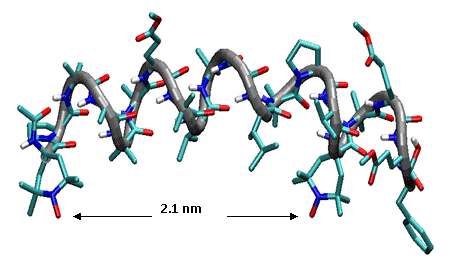

Рис. 1. Структура и конформация пептида-антибиотика аламетицина. В данном случае изучался аламетицин, спин-меченый в двух положениях (показано расстояние между метками)
 |
Рис. 2. Надмолекулярная структура образованных тетрамерами молекул пептида аламетицина каналов в модельной биологической мембране еРС. (А) – вид вдоль мембраны, на выноске сверху приводится часть структуры. (В) и (С) – два разных изображения тетрамера, если смотреть вдоль нормали к мембране, в первом случае явно показаны структуры спиралей пептида, во втором приводится срез электронной плотности в середине тетрамера



