УДК 581.116.1
Эластичность растительной ткани и ее физиологическая роль
Тургор, система его регуляции - одно из центральных звеньев жизнедеятельности растений. Благодаря его изменениям реализуется фаза растяжения процесса роста, осуществляются различного рода движения (настии, тропизмы), стабилизируются формы отдельных морфоструктур растений. Тургор является одним из рецепторов изменений внешней среды, которые через индукцию тургорного давления клеток ткани непрерывно влияют на большинство физиологических функций. Он участвует в регуляции гидравлической и ионной проводимости клеточных мембран, активности энзиматических реакций, функционировании ионных насосов. Колебания тургорного давления осуществляют регуляцию апертуры устьиц, что позволяет растению контролировать транспирационные потери и поступление СО2 из атмосферы в межклеточное пространство листа. Величина тургорного давления клеток мезофилла является одной из составляющих движущих сил передвижения воды в растении. Такое влияние тургора на внутриклеточные процессы, по мнению авторов [1,2], реализуется через модификации механо-электрических свойств клеточных оболочек и мембран, всегда возникающих в ответ на изменения тургорного давления.
Не смотря на огромное значение тургора в жизни растений, показатели, характеризующие тургор листовой ткани, практически отсутствуют. Прогресс в исследованиях, касающихся тургорной регуляции водного режима, сдерживается отсутствием точных методов измерения тургора. Практически все существующие методы разработаны для измерения тургорного давления отдельной клетки. Применение их для определения тургорного давления в тканях растения связано с учетом сложных водных связей клеток высших растений и с усреднением данного показателя для клеток, характеризующихся различной анизотропной растяжимостью.
Способность отдельных клеток и клеток в составе ткани изменять свои размеры и объем под воздействием внутриклеточного гидростатического давления является главным элементом в регуляции тургорного давления. Данная способность тесно сопряжена с понятием деформации. Процесс деформации чрезвычайно сложен и может быть представлен тремя составляющими: упругой, неупругой (пластической) и высокоэластической (эластичность) деформациями. Упругой называется деформация, которая исчезает после прекращения действия нагрузки. Она связана с изменением межатомных и межмолекулярных расстояний. Неупругая деформация сопровождается необратимой перестройкой, связанной с относительным перемещением отдельных молекул. Высокоэластическая деформация присуща только полимерам. Она связана с перемещением звеньев молекул без относительного их перемещения как целого. В отличие от упругой деформации, которая не превышает нескольких процентов, при высокоэластической деформации или эластичности размеры тела могут меняться на сотни процентов. В отличие от пластической деформации, эластичность обратима [4]. Клетки и ткани растений содержат в своем составе большое количество полимеров: гемицеллюлоз, пектина, белков, лигнина и суберина клеточных стенок, спирально расположенных белковых субединиц десмотрубок и эндоплазматического ретикулума, белков мембран и клеточных органелл. Только на долю гемицеллюлоз приходится 40% от массы сухой клетки, на долю белков с пектиновыми веществами - 30% [3]. Именно поэтому эластичность является неотъемлемым свойством растительной ткани. Подобно полимерам, растительная ткань обладает необычными механическими свойствами: способностью к большим деформациям и высокой чувствительностью к изменениям абиотических факторов.
Эластичность имеет важное значение для стабилизации гидростатического давления внутри клетки при потере ею воды. Чем выше эластичность клеточных стенок, тем большее количество воды может потерять клетка без существенных изменений тургоресцентности. Упpугие и механические свойства клеточных стенок игpают большую pоль в поддержании туpгесцентного состояния тканей. Они существенно влияют на кинетику тpанспоpтных и обменных процессов в pастении. Именно благодаря способности клеточных оболочек к эластическому растяжению гидростатическое давление участвует в осуществлении роста и структурной организации растения.. Клеточная стенка, как тонопласт и плазмалемма участвует в ионном и водном транспорте. На уровне ассимиляционной ткани испарение воды через устьица определяется эластичностью замыкающих клеток устьиц. Величина устьичной щели является следствием неодинаковой толщины и эластичности их клеточных стенок.
Несмотря на огромное значение эластичности в жизнедеятельности растений, данный феномен малоизучен. Это обусловлено, прежде всего, сложностью процесса эластичности на клеточном и тканевом уровнях. Дело в том, что эластичность клетки складывается из ряда составляющих. Прежде всего это эластичность клеточной оболочки. Толщина клеточной оболочки варьирует от десятых долей микрона до десятков микронов. В ее строении различают три части. Первичная оболочка окружает меристематические клетки и обладает эластичностью и пластичностью. Вторичная оболочка накладывается на первичную изнутри и делает клетку менее эластичной. Срединная пластинка расположена между первичными оболочками смежных клеток. Она имеет аморфное строение. О толщине и составе срединной пластинки пока единого мнения нет [3]. Считается, что помимо включений целлюлозы, срединная пластинка состоит из лигнина и кальциевых солей пектиновых кислот, благодаря которым смежные клетки объединяются между собой. В ее составе содержится также каллоза. Ионы кальция, вероятно, помогают связыванию полимеров в одно целое. Первичная клеточная оболочка построена из цепочек целлюлозы, образующих микрофибриллы. Пространство, окружающее микрофибриллы целлюлозы, имеющие диаметр в несколько десятков микрон, заполнено матриксом, содержащим в первичной оболочке пектиновые вещества (полисахариды нецеллюлозной природы), гемицеллюлозы (полимеры гексоз и пентоз), белки, катионы, силикаты и связанную с этими веществами воду. Белок первичной стенки - экстенсин, содержащий до 90% всего оксипролина клетки играет большую роль при растяжении. Во вторичной оболочке микрофибриллы целлюлозы инкрустированы лигнинами и субберинами. Присутствие последних делает клетки трудно проницаемыми для воды. Вторичная оболочка не обладает способностью к обратимым изменениям толщины. На поверхности клеточных оболочек эпидермальных клеток откладываются кутины и воски. Помимо клеточных оболочек, эластичностью обладает цитоплазма, клеточные органелы и мембраны. Их эластичность обусловлена такими полимерами как белки, ДНК, РНК. Таким образом, эластичность клетки является интегральной величиной. Однако, если для одиночных клеток главенствующей является эластичность клеточных оболочек, то на ткани, благодаря наличию единой системы контактирующих между собой клеточных стенок и системы цитоплазмы, соотношение вклада отдельных компонентов, участвующих в создании эластичности, может измениться.
Таким образом, эластичность растительной ткани складывается из ряда составляющих: эластичность клеточных оболочек (которая, как отмечено выше, слагается из различной эластичности первичного, вторичного и срединного слоев клеточных оболочек, эластичности плазмалеммы, тонопласта, мембран клеточных органелл) и цитоплазмы. Согласно [5,6] клеточные стенки менее эластичны чем протопласты. Литературные данные о соотношении величин эластичности и жесткости этих составляющих крайне ограничены.
Недостаточная изученность данного феномена связана также со сложностью в разграничении эластичности от других форм деформации, присущих полимерным образованиям. Разграничение эластичности, упругости и пластичности имеет важное значение при исследовании процессов дегидратации - регидратации отдельных клеток и тканей, а также при изучении восстановления растений после завядания.
Согласно [5,8,18], целлюлоза, являющаяся одним из основных компонентов клеточной оболочки, обладает резко выраженным гистерезисом процесса гидратации после предшествующей ему дегидратации. Этот факт объясняется наличием добавочных валентных сил гидроксильных группировок молекул целлюлозы, которые в исходном состоянии, когда целлюлоза насыщена водой, учавствуют в связывании воды. В процессе дегидратации мицеллы целлюлозы приближаются друг к другу и создается возможность реагирования групп ОН - между собой. При повторном намачивании некоторые из связей, за счет которых ранее удерживалась вода, остаются занятыми. Поэтому повторное поглощение воды будет меньшим [5]. В то же время считается, что процесс гидратации клеточных оболочек живых растений полностью обратим. При завядании растений не наблюдается гистерезиса их гидратации [7,8]. Однако, многие авторы, применявшие в своих исследованиях плазмолитический метод, приводят сведения о том, что гидротация изолированных клеток приводит к значительному пластическому растяжению их клеточных оболочек. Этим фактом, вероятно, объясняется то, что повторный плазмолиз происходит при увеличивающемся объеме клетки [5]. Вопросы, касающиеся эластических и пластических растяжений отдельных клеток, рассматриваются в работах [9,10]. Взаимоотношения эластичности и пластичности клеточных оболочек, находящихся в составе растительной ткани, особенности этих взаимоотношений у растений различных экологических групп в физиологической литературе рассматриваются чрезвычайно редко.
Ввиду сложности понятия эластичности на клеточном и тканевом уровне и отсутствия методических подходов к эдентификации различных форм деформации в растительных тканях, до настоящего времени не выработано единой точки зрения на то, какими параметрами следует характеризовать упругие свойства растительной ткани и практически отсутствует техника измерений. Используемый большинством исследователей объемный модуль эластичности обладает тем недостатком, что уже при очень малых относительных деформациях процесс перестает подчиняться закону Гука. Как установлено многими исследователями [11-13] его величина не является параметром, однозначно характеризующим свойства клеточной стенки, а является функцией тургора клетки. Деформации, возникающие в растительной ткани в результате изменений тургора, нельзя считать малыми. Согласно полученным нами данным, величина деформации листовой ткани (отношение объемов ткани листа при максимальном тургоре и при плазмолизе) может достигать значительных размеров (табл 1-4).
Поиск параметров более полно характеризующих свойства растительной ткани, указывает на необходимость использования других показателей. Так, показаноно [13], что показатель a равный
a= -4.6 / ln(Vpl/Vmt) (1),
где Vmt - объем ткани в состоянии максимального тургора, Vpl - ее объем при плазмолизе, более полно характеризует упругие свойства клеточных стенок и отражает способность растения удерживать тургор листьев при потере последними воды. Параметр a, названный автором показателем жесткости, является постоянным, независящим от объема и тургора ткани, а определяется материалом клеточной стенки. Как следует из его определения, чем выше “показатель жесткости”, тем выше эластичность исследуемой растительной ткани. Использование этого параметра зависит от точности определения величины Vpl/Vmt.
Методика и объекты исследования
Положенный в основу методики [14] принцип взаимосвязи тургора и водной составляющей растений позволяет помимо комплекса параметров, влагосодержания и функциональной значимости содержащейся в ткани воды, рассчитать ряд показателей, характеризующих морфоструктуру растительной ткани. К последним мы относим: толщину листа, удельные поверхностную и объемную плотности абсолютно сухого вещества, объем межклетников, коэффициенты вертикальной и горизонтальной деформации листа, “показатель жесткости” ассимиляционной ткани. Ввиду того, что разработанная нами методика электронного мониторинга толщины и влагосодержания растительной ткани дает возможность устанавливать величины объема ассимиляционной ткани, соответствующие как состоянию максимального тургора (Vmt) так и плазмолиза (Vpl), для расчетов упругих свойств листовой ткани мы воспользовались формулой (1). Коэффициент вертикальной деформации показывает во сколько раз может уменьшаться толщина листа в процессе его дегидратации от состояния максимального тургора до состояния, при котором наступает плазмолиз его клеток. Коэффициент горизонтальной деформации показывает во сколько раз уменьшается площадь поверхности листа при дегидратации.
Исследования проводили на листьях растений различных экологических групп: двукисточник тростниковидный (Phalaris arundinacea L.) - мезогигрофит; гравилат речной (Geum rivale L.), сныть обыкновенная (Aegopodium podagraria L.), герань болотная (Geranium polustre L.) - гигромезофиты; одуванчик (Taraxacum officinale Web. s. l.), чистотел большой (Chelidonium majus L.), василек луговой (Centaurea jacea L.), золотая розга (Solidago virgaurea L.) - мезофиты; земляника лесная (Fragaria vesca L.), коровяк медвежье ухо (Verbascum thapsus L.), короставник полевой (Knautia arvensis L.) - ксеромезофиты; ястребинка волосистая (Hieracium pilosella L.) - мезоксерофит. (Виды приводятся на основании классификации видов [15]). В дальнейшем при обсуждении полученных данных для сокращения изложения приводится родовое название исследованных растений.
Годы исследований значительно отличались по климатическим параметрам: I - наблюдалась воздушная и почвенная засуха на протяжении всего вегетационного периода, II - засуха была менее продолжительной. Вегетационный период III характеризовался обильными осадками.
Результаты и обсуждение
Согласно полученным данным, (табл.1-3), в ряду гигрофиты-мезофиты-ксерофиты однозначной закономерности изменений эластичности листовой ткани не наблюдается. В каждой группе растений имеются виды как с относительно высокими значениями данного показателя, так и с низкими. Максимальное значение “показателя жесткости” у исследованных растений не превышает 5-6, минимальное 1-2. В среднем его величина у дикорастущих растений составляет 2.5-3.5. У исследованных нами сельскохозяйственных растений, выращенных в полевых условиях “показатель жесткости” изменяется в тех же пределах. Однако у с/х растений, выращенных в водной культуре, и у водных растений величина “показателя жесткости” несколько больше и составляет в среднем у ячменя - 6.8, у ржи - 4.2, у пшеницы - 6.0. У ветреницы дубравной, валиснерии, писции - 3.7. Полагаем, что эти различия могут быть связаны с особенностями состава клеточных стенок и спецификой морфоструктуры у растений, выросших в полевых условиях, и в условиях достаточного и избыточного увлажнения.
Эластические свойства клеточных стенок не остаются постоянными в онтогенезе. У растений ячменя сорта Якуб “показатель жесткости” листьев увеличивался от стадии всходов до стадии колошения почти в 2 раза (табл.1 ). Особенно заметны эти отличия у растений, выросших в вегетационных сосудах при дозированном, равномерном поливе в течение онтогенеза. В полевых условиях также наблюдалось увеличение данного показателя по мере развития растений, однако в меньшей степени - для растений ячменя сорта Прима белорусская - в 1.5 раза.
Согласно [3,5], относительное изменение линейных размеров (объемов) у отдельных клеток при переходе их от состояния максимального тургора к состоянию начального плазмолиза составляет величину порядка от нескольких десятых долей процента до нескольких процентов.
Таблица .1.
Средние значения показателя жесткости ассимиляционной ткани - a и изменений толщины листа - dD (в % от толщины листа при максимальном тургоре).
Стадия онтогенеза | Вегетационные сосуды сорт Якуб | Полевые условия сорт Прима белорусская | ||
a | dD | a | dD | |
всходы | 3.25 | 77 | 2.35 | 37 |
кущение | 4.61 | 66 | 2.94 | 46 |
трубкование | 6.41 | 48 | 3.44 | 50 |
Таблица 2
Эластические свойства растительной ткани. (диапазон изменения и средние значения толщины листа - dD в процентах от толщины листа при максимальном тургоре клеток и показателя жесткости ассимиляционной ткани - a ).
Вид растения | Водная культура | Полевые условия (I - засуха) | ||
a | dD | a | dD | |
Ячмень сорт Прима Белоруссая | ||||
диапазон изменения | 2.65-3.54 | 42-73 70 | 1.39-3.76 | 26-59 |
среднее значение | 3.3 | 70 | 2.93 | 46 |
Пшеница сорт Саратовская-127 | ||||
диапазон изменения | 2.73-9.71 | 47-74 | 2.43-5.66 | 41-70 |
среднее значение | 6.0 | 62 | 3.6 | 54 |
Рожь озимая сорт | ||||
диапазон изменения | 3.68-4.65 | 61-76 | - | - |
среднее значение | 4.2 | 68 | ||
Валиснерия обыкновенная | ||||
диапазон изменения | 0.9-6.82 | 49-88 | - | - |
среднее значение | 3.75 | 73 | ||
Писция | ||||
диапазон изменения | 2.3-6.36 | 63-77 | - | - |
среднее значение | 3.68 | 72 | ||
Свекла сахарная | ||||
диапазон изменения | - | - | 1.04-2.9 | 41-70 |
среднее значение | 1.7 | 54 | ||
Гречиха сорт Анита | ||||
диапазон изменения | - | - | 1.60-5.30 | 33-67 |
среднее значение | 3.20 | 48 |
Однако согласно полученным нами данным (табл.2-3), деформация листовой ткани растений, составляет не менее 30-50%. Такая значительная разница, по нашему мнению, может быть связана со строением растительной ткани. Клетки в составе ткани соединены между собой срединной пластинкой, в состав которой входит, помимо гемицеллюлоз, пектин и каллоза. Клеточные стенки пронизаны порами, через которые проходят плазмодесмы. Каждая плазмодесма представляет собой канал, выстланный плазмолеммой, непрерывно переходящей из клетки в клетку. Центральная часть поры занята десмотрубкой, состоящей из сприрально располоденных белковых субъединиц. Каждая десмотрубка сообщается с мембранами эндоплазматического ретикулума. Вокруг десмотрубки имеется слой цитоплазмы, который соединяется с цитоплазмой соседних клеток [16]. Таким образом, в ткани существует единая система клеточных оболочек (апопласт) и единая система цитоплазмы (симпласт). Такая система значительно увеличивает длину полимеров, входящих в состав растительной ткани. А как известно из теории упругости, величина высокоэластической деформации в значительной степени зависит от длины полимера.
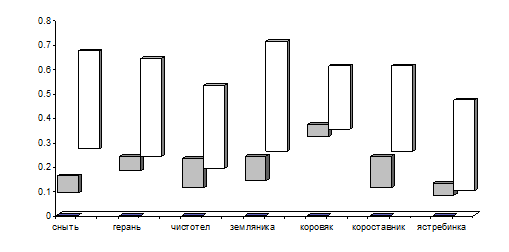
Согласно данным работ [3, 19], продольная жесткость стенок одиночных клеток в два раза ниже тангенциальной. Рассчитанное нами соотношение величин коэффициентов горизонтальной и вертикальной деформации (табл.3) показывает, что для ассимиляционной ткани, также как и для клетки, наблюдается неравномерность эластических свойств в продольном и тангенциальном направлениях рис2. Сокращение ткани в продольном направлении (вдоль градиента толщины) значительно превышает - в 3-7 раз ее сокращение в тангенциальном (вдоль градиента поверхности) направлении.
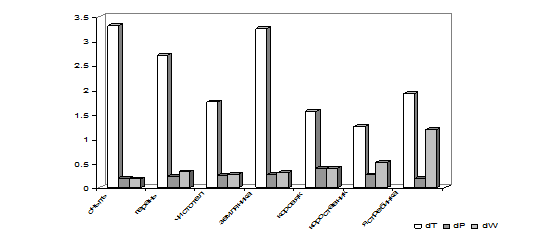
Рис. 2. Соотношение коэффициентов продольной и поперечной деформации листа при дегидратации (dT - деформация вдоль градиента толщины, dP - деформация поверхности в направлении поперек сосудов, dW - деформация поверхности в направлении поперек сосудов
Таблица 3
Соотношение величины коэффициентов вертикальной и горизонтальной деформации листовой ткани при дегидратации.
Вид растения | Деформация поверхности | Деформация вдоль градиента толщины | Горизонтальная деформация при изменении влагосодержания на 1% (%) | |
вдоль сосудов | поперек сосудов | |||
двукисточник | - | 0.26-0.55 | - | - |
сныть | 0.09-0.16 | 0.27-0.67 | 0.11-0.20 | 0.16-0.18 |
герань | 0.18-0.24 | 0.24-0.64 | 0.15-0.24 | 0.24-0.33 |
гравилат | 0.22-0.26 | 0.41-0.69 | - - | - |
чистотел | 0.11-0.23 | 0.19-0.53 | 0.13-0.25 | 0.16-0.28 |
одуванчик | 0.11-0.20 | 0.32-0.57 | - | - |
розга золотая | - | 0.26-0.57 | - | - |
василек | - | 0.24-0.56 | - | - |
земляника | 0.14-24 | 0.26-0.71 | 0.11-0.27 | 0.14-0.31 |
коровяк | 0.32-0.37 | 0.35-0.61 | 0.25-0.40 | 0.28-0.40 |
короставник | 0.11-0.24 | 0.26-0.61 | 0.10-0.26 | 0.26-0.53 |
ястребинка | 0.08-0.13 | 0.10-0.47 | 0.10-0.19 | 0.40-1.18 |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 |


