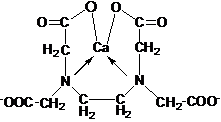Министерство образования и науки Российской Федерации
ГОУ ВПО «Кемеровский государственный университет»
,
,
ОСНОВЫ АНАЛИТИЧЕСКОЙ ХИМИИ
Часть 2. КОЛИЧЕСТВЕННЫЙ АНАЛИЗ
Учебно-методическое пособие
Кемерово 2008
Составители:
доценты кафедры аналитической химии к. х.н. Шрайбман Г. Н., к. п.н. , к. х.н. ,
Основы аналитической химии. Часть 2. Количественный анализ: учебно-метод. пособие / , , ; ГОУ ВПО «Кемеровский госуниверситет» – Кемерово: участок оперативной полиграфии, 2008.– 68 с.
Учебно-методическое пособие составлено на основе Государственного образовательного стандарта высшего профессионального образования по специальности «Химия» и соответствует программе по аналитической химии химических и биологических факультетов университетов. В каждом разделе пособия дано краткое теоретическое введение, методика решения типовых задач по основным разделам аналитической химии: химическому равновесию в гомогенных и гетерогенных системах, титриметрическому анализу. В пособии приведены лабораторные работы по качественному и количественному анализу, физико-химическим методам анализа, рекомендуемые для выполнения в подкрепление изучаемого теоретического материала. Пособие предназначено для студентов биологического факультета, изучающих общий курс аналитической химии.
Утверждено на заседании кафедры аналитической химии 3 октября 2007 г. ___________________ Зав. кафедрой АХ, д. х.н., проф. | Утверждено методической комиссией химического факультета 18 октября 2007 г. ___________________ Председатель методкомиссии, к. х.н., доцент |
Содержание
1. Количественный Химический анализ. 4
1.1.Титриметрический метод анализа. 4
1.2. Метод кислотно-основного титрования. 12
Лабораторная работа №1. Определение NaOH в контрольной задаче методом ацидиметрии. 12
1.3. Метод комплексонометрического титрования. 15
Лабораторная работа №2. Определение общей жесткости природной воды 16
1.4. Методы окислительно-восстановительного титрования. 19
1.4.1. Перманганатометрия. 20
Лабораторная работа №3. Определение Fe2+ в контрольном растворе соли Мора. 20
1.4.2. Иодометрия. 22
Лабораторная работа №4. Определение содержания аскорбиновой кислоты во фруктовых соках. 23
Лабораторная работа №5.Определение содержания остаточного хлора в питьевой воде. 25
1.5. Обработка результатов анализа. 28
1.6. СОДЕРЖАНИЕ КОЛЛОКВИУМА 2. 35
2. Физико-химические методы анализа.. 37
2.1. Потенциометрия. 37
Лабораторная работа № 6.
Потенциометрическое титрование HCl. 43
2.2.Фотометрический анализ. 45
Лабораторная работа № 7. Фотометрическое определение железа в виде тиоцианатных комплексов. 51
Лабораторная работа № 8.Фотометрическое определение железа с сульфосалициловой кислотой. 54
2.3. Эмиссионный спектральный анализ. 57
Лабораторная работа № 9. Пламенно-фотометрическое определение натрия в водопроводной воде. 62
2.4. СОДЕРЖАНИЕ КОЛЛОКВИУМА 3. 63
Примерные темы рефератов. 64
ЛИТЕРАТУРА.. 67
1. Количественный химический анализ
1.1.Титриметрический метод анализа
Титриметрия или титриметрические методы количественного анализа основаны на точном измерении объема раствора реактива, израсходованного на реакцию с определяемым веществом. Раствор реактива (титрант, рабочий раствор) должен при этом иметь точную концентрацию, обеспеченную условиями приготовления раствора (рабочий раствор с приготовленным титром) или установленную по другому раствору с точно известной концентрацией (рабочий раствор с установленным титром).
Титр - способ выражения концентрации раствора, определивший название метода, и показывающий массу растворенного вещества в граммах в 1 см3 (или 1 мл) раствора. Процесс постепенного добавления титранта к раствору определяемого вещества называют титрованием. При титровании наступает момент, когда рабочий раствор В и определяемое вещество А прореагируют между собой в эквивалентных количествах, т. е. в строгом соответствии со стехиометрией реакции. В таком случае справедлив закон эквивалентов, составляющий основу расчетов в титриметрии:
n(A) = n(B)
При титровании важно зафиксировать конец реакции, называемый точкой стехиометричности или точкой эквивалентности (ТЭ). Для экспериментального установления конечной точки титрования (КТТ), по возможности наиболее близкой к теоретической ТЭ, используют изменение окраски индикатора или какого-либо физического свойства раствора.
К химической реакции титрования предъявляются следующие требования: 1) строгая стехиометричность, отсутствие побочных реакций; 2) высокая скорость; 3) практическая необратимость (Кр ³ 107), обеспечивающая количественное превращение реагирующих веществ в продукты реакции; 4) наличие подходящего индикатора или другого способа фиксирования ТЭ.
В титриметрии используют точную мерную посуду: мерные колбы - для приготовления растворов; пипетки - для точного измерения определенного объема раствора при перенесении в другой сосуд и бюретки - для измерения объема титранта
Титриметрические методы характеризуются быстротой анализа, простотой оборудования, возможностью автоматизации определения. Чувствительность индикаторных методов титриметрии составляет 10–3 –10–4 моль/л, относительная погрешность более 0,1 %.
Классификация титриметрических методов анализа
Методы титрования. В титриметрии используют реакции всех типов - с переносом протона, электрона, электронной пары, процессы осаждения. В соответствии с типом реакции (видом химического равновесия) титриметрические методы разделяют на 4 группы, в каждой из которых выделяют отдельные группы по названию применяемых титрантов (табл.1).
Приемы титрования. Различают прямое, обратное и титрование заместителя. При прямом титровании титрант В непосредственно добавляют из бюретки к титруемому веществу А. Прием используют только при выполнении требований к реакции титрования. В случае их невыполнения или в практических целях используют прием обратного титрования, для осуществления которого необходимы два рабочих раствора титрант В1 и титрант В2. Первый добавляется к определяемому веществу А в избытке для доведения реакции до конца, а остаток В1 оттитровывается титрантом В2 для определения непрореагировавшего титранта В1. В этом случае n(А) рассчитывается по разности эквивалентных количеств двух рабочих растворов:
n(А) = n(B1) - n(B2)
Пример. Ион NH4+, являющийся в воде очень слабой (Ка=5,68×10-10) кислотой, нельзя оттитровать рабочим раствором NaOH приемом прямого титрования из-за высокой обратимости реакции. Поэтому, к пробе, содержащей соль аммония, добавляют определенный объем титрованного раствора NaOH (В1), обеспечивающий избыточное количество щелочи по отношению к ионам аммония, после чего удаляют аммиак и избыток NaOH титруют рабочим раствором НСl (B2), т. е. последовательно выполняются две реакции:
1) NH4Cl + NaOH = NH3+ NaCl + H2O;
2) NaOH + НСl = NaCl + H2O.
Тогда: n(NH4Cl) = n(NH4+) = n(N) = n(NаОН) - n(НCl)
Титрование заместителя используют при отсутствии подходящего индикатора, при несоблюдении стехиометричности, при медленном протекании реакции и др. В этом случае к определенному объему А добавляют избыток вспомогательного реагента, стехиометрически взаимодействующего с веществом А, а получающийся в эквивалентном количестве продукт реакции оттитровывают рабочим раствором В. Закон эквивалентов при титровании заместителя имеет выражение, как при прямом титровании:
n(А) = n(B)
Например, для определения соли аммония проводят реакцию с формальдегидом:
4NH4+ + 6СН2О = (СН2)6N4 + 4H+ + 6Н2O
Выделившееся эквивалентное количество ионов H+ (заместителей NH4+) оттитровывают рабочим раствором NaOH.
Н+ + OH– = H2O n(NH4+) = n(NaOH)
Способы титрования. При проведении параллельных определений, используют способ отдельных навесок или способ пипетирования (аликвот). В способе пипетирования пробу (навеску или объем), содержащую определяемое вещество А, переводят в мерную колбу вместимостью Vм. к., а на титрование отбирают пипеткой равные объемы Vп - аликвоты. В способе отдельных навесок пробу помещают в колбу для титрования (навеску растворяют) и проводят титрование, точно измеряя при этом объем израсходованного титранта Vв. Способ пипетирования является более экспрессным и менее трудоемким, но и менее точным, чем метод отдельных навесок. Расчетные формулы для разных приемов и способов титрования приведены в табл. 2.
Способы выражения концентрации растворов
в титриметрии
Все расчеты в титриметрии связаны с законом эквивалентов и понятием эквивалент. Эквивалентом называют реальную или условную частицу вещества, которая в данной реакции равноценна (эквивалентна) одному иону водорода или одному электрону. Например, эквивалент NaOH, НСl, NaCl - реальная частица, соответствующая молекуле этих веществ. Эквивалент Н3PO4 , в зависимости от числа участвующих в реакции протонов, может представлять
реальную молекулу Н3PO4 и условную часть молекулы: 1/2Н3PO4 или 1/3Н3PO4. Дробь, показывающую, какая часть молекулы или иона является эквивалентом, называют фактором эквивалентности fэкв. Фактор эквивалентности рассчитывают на основе стехиометрии реакции. Число, показывающее, сколько эквивалентов содержится в молекуле, называют числом эквивалентности и обозначают z*: fэкв = 1/z*. Молярная масса эквивалента вещества - это масса одного моля эквивалента этого вещества, равная произведению фактора эквивалентности на молярную массу вещества. Например, для вещества В:
М(fэквВ) = fэкв(В) × М(В) = 1/z*(В)×М(В)
Молярная масса эквивалента вещества может быть различной, в зависимости от протекающей реакции с его участием.
Условные обозначения и размерности концентрации. В титриметрии обычно используют следующие способы выражения концентрации:
с(В) - молярная концентрация раствора вещества В, моль/л (или моль/дм3);
с(fэквВ) - молярная концентрация эквивалента вещества В, моль/л. с(fэквВ) = n(fэквВ)/V(B),
где V(B) - объем раствора (л), содержащего n молей эквивалентов B. Соответствует старому названию «нормальная концентрация».
с(В) = fэкв ×с(fэквВ)
Не рекомендуется использовать термины «молярность» и «нормальность» раствора. Разрешаются сокращенные обозначения, например 0,025 М H2SO4 - 0,025 молярный раствор H2SO4, т. е. в одном литре раствора содержится 0,025 моль вещества H2SO4. Можно представлять концентрацию и таким образом: 0,050 н. H2SO4 - 0,050 нормальный раствор H2SO4, т. е. в одном литре раствора содержится 0,050 моль эквивалента вещества H2SO4.
Т(В) - титр раствора вещества В, г/мл (г/см3) – показывает массу вещества В в одном миллилитре раствора:
Т(В) = m(B) /V(B)
Т(В/A) - титр рабочего раствора В по определяемому веществу А, г/мл – показывает, какая масса вещества А эквивалентна одному миллилитру рабочего раствора В. Например, Т(KMnO4/Fe) = = 0,001396 г/мл означает, что 1 мл такого раствора KMnO4 эквивалентен (оттитровывает) 0,001396 г Fe.
Такой способ выражения концентрации удобен при серийных анализах, поскольку:
m(А) = V(B)×Т(В/A).
От одного способа выражения концентрации можно перейти к другому:
с(fэквВ) = Т(В)×1000/М(fэквВ)
с(В) = Т(В)×1000/М(В)
Т(В/A) = Т(В)× М(fэквА)/М(fэквВ)
с(fэквВ) = Т(В/A)×1000/М(fэквА).
Пример. Из 2,500 г Na2CO3 приготовлено в мерной колбе 500 мл раствора. Вычислить для этого раствора: а) Т(Na2CO3), б) молярную концентрацию, в) молярную концентрацию эквивалента Na2CO3, если предполагается титрование приготовленного раствора рабочим раствором НСl с индикатором метиловым оранжевым, г) определить молярную концентрацию НСl и Т(НСl/Na2CO3), если на титрование 25,00 мл раствора соды израсходовано 23,35 мл раствора НСl.
Решение.
а) Т(Na2CO3) = m(Na2CO3)/V = 2,500/500 = 0,005000 г/мл
б) с(Na2CO3) = Т(Na2CO3)×1000/М(Na2CO3)= 0,005000×1000/106,0 =
= 0,04717моль/л
в) реакция Na2CO3 с HCl при титровании с метиловым оранжевым протекает до Н2CO3, т. е. с участием двух эквивалентов карбоната натрия:
Na2CO3 + 2НСl = Н2CO3 + 2NaСl
Тогда: fэкв(Na2CO3) = 1/2; М(1/2Na2CO3) = 53,002 г/моль;
с(1/2Na2CO3) = Т(Na2CO3)×1000/М(1/2Na2CO3) =
= 0,005×1000/53,002 = 0,09434 моль/л.
г)с(НСl) = с(1/2Na2CO3) ×V(Na2CO3)/V(НСl) = 0,09434·25,00/23,35=
= 0,1010 моль/л.
Поскольку с(fэквВ) = Т(В/A)×1000/М(fэкв(А)А),
Т(НСl/Na2CO3) = с(НСl)·М(1/2Na2CO3)/1000 = = 0,1010×53,00/1000 =0,005353 г/мл
В анализе чаще всего пользуются рабочими растворами с концентрациями 0,005 – 0,1 моль/л. Не применяются 1 М растворы, так как в этом случае велика капельная ошибка титрования, т. е. ошибка при добавлении одной лишней капли титранта. Удобство использования в титриметрии с(fэквВ) - связано с тем, что при одинаковых концентрациях растворов веществ А и В реакции идут между равными их объемами согласно закону эквивалентов
n(A) = n(B)
или: с(fэквВ)×V(B) = с(fэквА)×V(А).
Выражение закона в устаревших обозначениях:
(N×V)A = (N×V)B.
УКАЗАНИЯ К ОФОРМЛЕНИЮ РАБОТ
Отчет по лабораторной работе должен содержать:
1) дату, название работы;
2) краткое описание метода, приема и способа титрования;
3) сущность методики с обязательным приведением всех уравнений реакций и указанием условий анализа;
4) цифровой материал для расчетов (привести используемые объемы мерных колб, пипеток; навески веществ, необходимые значения молярных масс или молярных масс эквивалентов; полученные экспериментальные данные параллельных измерений объемов титранта);
5) расчетные формулы и результаты расчетов согласно заданию лабораторной работы;
6) результаты расчетов абсолютной и относительной погрешностей при анализе контрольных образцов;
7) оценку воспроизводимости (сходимости) результата выборочной совокупности и границ доверительного интервала.
1.2. Метод кислотно-основного титрования
(нейтрализации)
Метод кислотно-основного титрования основан на реакции нейтрализации. Он позволяет определять содержание кислот или оснований в растворе, причем роль таких кислот и оснований могут играть гидролизующиеся соли и амфолиты (см. табл. 1). Основными рабочими растворами, применяемыми в методе нейтрализации, являются растворы сильных кислот (соляной, серной и др.) и щелочей. В качестве индикаторов наиболее часто используются (в скобках указан интервал рН перехода окраски индикатора): метилоранж (3,1 ‑ 4,4), бромкрезоловый зеленый (3,9 – 5,4), метиловый красный (4,4 – 6,2), бромтимоловый синий (6,0 – 7,6), тимоловый синий (тимолфенолфталеин) (8,0 – 9,6), фенолфталеин (8,2 – 9.8). Метод ацидиметрии - метод титрования растворами сильных кислот. В методе алкалиметрии используют рабочие растворы щелочей.
Лабораторная работа №1
Определение NaOH в контрольной задаче
методом ацидиметрии
Приготовление ~0,1 М рабочего раствора НСl. Разбавленный раствор НСl (вторичный стандартный раствор или рабочий раствор с установленным титром) готовят из концентрированного раствора с плотностью r~1,18 г/см3 или 1,18 г/мл ( массовая доля w = 36,2 %) путем его разбавления до заданного объема Vмк. Необходимый объем концентрированного раствора V(НСl) рассчитывается по формуле:
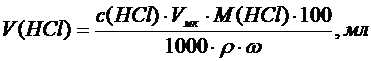
Рассчитанное количество НСl отмеряют мерным цилиндром и переносят в мерную колбу объемом Vмк, доводят до метки дистиллированной водой и тщательно перемешивают.
Стандартизация рабочего раствора НСl по раствору буры. При растворении в воде тетраборат натрия дает щелочную реакцию среды вследствие гидролиза. Образующуюся щелочь оттитровывают раствором НСl.
Na2B4O7 + 7H2O = 2NaOH + 4H3BO3
____2NаОН + 2НСl = 2NаСl + 2Н2О____
Na2B4O7 + 2НСl + 5H2O = 2NaCl + 4H3BO3
Для выполнения определения бюретку заполняют рабочим раствором НСl, пипеткой отбирают аликвоту приготовленного раствора буры (Vп = 15,00 мл или другой) и переносят в коническую колбу для титрования, добавляют туда же 1-2 капли индикатора метилоранжа и титруют до перехода желтой окраски в оранжевую. Расход кислоты отмечают по бюретке с точностью до 0,01 мл. Титрование повторяют не менее трех раз, и, если расхождение объема НСl не превышает 0,1 мл (~ двух капель), вычисляют (НСl) и рассчитывают молярную концентрацию раствора НСl по формуле из закона эквивалентов:
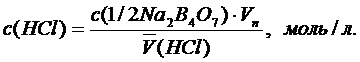
При титровании с метиловым оранжевым удобно пользоваться свидетелем, т. е. раствором, который имеет окраску, до которой следует титровать исследуемый раствор. Для приготовления свидетеля в коническую колбу для титрования вносят мерным цилиндром 40 мл дистиллированной воды, 1 – 2 капли индикатора метилового оранжевого и 1 – 2 капли титранта (HCl) – до появления оранжевой окраски.
Ход анализа. Полученный для анализа контрольный раствор щелочи разбавляют дистиллированной водой до метки в мерной колбе на 100,0 мл и тщательно перемешивают. Отбирают пипеткой. 15,00 мл в коническую колбу для титрования и титруют приготовленным рабочим раствором НСl в присутствии 1-2 капель индикатора метилоранжа (или фенолфталеина). Титрование повторяют не менее трех раз и вычисляют (НСl). Содержание щелочи в контрольной задаче рассчитывают по формуле:
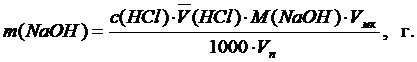
Контрольные вопросы
Общие сведения о титриметрии. Метод нейтрализации
1. Какие принципы положены в основу классификации титриметрических методов?
2. Какие требования предъявляют к реакциям прямого титрования в титриметрии?
3. Перечислите способы выражения концентрации растворов. Что такое химический эквивалент, эквивалентная масса?
4. Как изменяется выражение закона эквивалентов для разных приемов титрования?
5. Как связаны между собой титр и молярная концентрация эквивалентов?
6. Дайте определение первичного и вторичного стандарта. Перечислите требования, предъявляемые к первичным стандартам. Что такое фиксанал?
7. Изложите сущность метода пипетирования и метода отдельных навесок. Как рассчитать результаты титрования в этих методах?
8. Что такое титр по определяемому веществу? В каких случаях им удобно пользоваться?
9. Что такое точка эквивалентности, конечная точка титрования?
10. На основании чего проводится выбор индикаторов?
11. Дайте краткую характеристику метода нейтрализации.
12. Приведите примеры использования разных приемов титрования в методе нейтрализации.
13. Укажите рабочие растворы метода нейтрализации и способы их приготовления.
14. Какие вещества используют для приготовления первичных стандартных растворов в методе нейтрализации.
15. Каковы предельные значения кислотности (основности), при которых возможно прямое титрование (наблюдается скачок титрования)? Покажите их на примерах.
16. Дайте характеристику индикаторов метилового оранжевого и фенолфталеина (формулу, интервал перехода окраски, цвет, показатель титрования).
1.3. Метод комплексонометрического титрования
Комплексонометрический метод определения основан на способности ионов металлов Ме2+- Ме4+ образовывать устойчивые комплексные соединения (хелаты) с ЭДТА (этилендиаминтетрауксусная кислота) или ее двунатриевой солью (комплексон III, трилон Б). Этот кристаллогидрат – условно Na2H2Y×2Н2О – хорошо растворим в воде. В таких реакциях ЭДТА проявляет себя как шестидентатный лиганд и образует бесцветные октаэдрические комплексы состава МеY(n–4)+, т. е. реагирует с ионами металлов в молярном соотношении 1:1. Например, в случае Са2+ образуется комплекс СаY2–:
|
|
Индикаторами в комплексонометрии служат красители: кислотный хром темно-синий, хромоген черный специальный ЕТ-00, (эриохром черный Т), мурексид и др. Они обладают свойствами металлохромных индикаторов – способных изменять окраску при комплексообразовании с ионами металлов (типа MeInd). При правильно выбранном значении рН буферного раствора, в присутствии которого проводят титрование, комплекс MeInd должен иметь окраску, резко отличающуюся от окраски свободного индикатора, а его прочность должна быть значительно меньше прочности комплекса МеY(n-4)+. В частности, эриохром черный Т имеет синюю окраску (при рН от 7 до 10), а с катионами металлов образует комплексы винно-красного цвета, поэтому в точке эквивалентности вследствие перехода ионов металла из комплекса с индикатором в комплекс с ЭДТА появляется синяя окраска свободного индикатора.
На полноту протекания реакции комплексообразования ЭДТА с ионами металлов, помимо побочной реакции протонирования лиганда Y4–, которой управляют с помощью буферных растворов, оказывают влияние побочные реакции комплексообразования титруемого иона металла с другими лигандами в растворе, что следует учитывать при выборе условий титрования.
Лабораторная работа №2
Определение общей жесткости природной воды
Природная вода содержит различные количества растворенных солей и газов. Свойство природной воды, зависящее от наличия в ней преимущественно солей кальция и магния, называется жесткостью. Суммарное содержание этих солей в воде называют общей жесткостью. Общая жесткость подразделяется на карбонатную, обусловленную концентрацией гидрокарбонатов (и карбонатов при рН >8,3) кальция и магния, и некарбонатную – концентрацией в воде кальциевых и магниевых солей сильных кислот. Карбонатная жесткость составляет до 70-80 % от общей жесткости. При кипячении воды гидрокарбонаты переходят в карбонаты, выпадающие в осадок.
Ca(HCO3)2 = CaCO3¯ + H2O + CO2
Mg(HCO3)2 = MgCO3¯ + H2O + CO2
Поэтому карбонатную жесткость отождествляют с временной или устранимой. Остающаяся после кипячения жесткость - постоянная. Жесткость воды измеряется в миллимолях эквивалентов Са и Mg в 1 литре (ммоль/л), и изменяется в широких пределах: мягкая вода – меньше 4, средней жесткости – 4 ÷ 8, жесткая – 8 ÷ 12, очень жесткая – выше 12.
Жесткость относится к обобщенным показателям качества природной и питьевой воды. Согласно санитарным нормам, она не должна превышать 7,0 ммоль/л. Вода для паровых котлов должна быть более мягкой, остаточная жесткость её после умягчения £ 0,3 ммоль/л. Это необходимо для предотвращения образования накипи в паровых котлах, отопительных приборах и предотвращения перегрева металлических поверхностей. Использование жесткой воды затрудняет стирку, ухудшает качество тканей вследствие осаждения солей высших жирных кислот. В жесткой воде плохо развариваются мясо и овощи, поскольку соли кальция образуют с белками нерастворимые соединения. Магниевая жесткость придает воде горечь и оказывает послабляющее действие на кишечник. Поэтому одной из стадий водоподготовки является умягчение воды с использованием химических реагентов (Na2CO3, Na3PO4 и др.) и ионообменных смол.
Для определения временной жесткости часто используют результаты кислотно-основного титрования при определении карбонатной щелочности с индикатором метиловым оранжевым до рН ~ 4. Общую жесткость определяют комплексонометрическим титрованием с индикатором типа эриохром черный Т при рН 9,3–9,5 в присутствии аммиачного буферного раствора.
При определении Са2+ и Mg2+ в воде последовательность протекающих реакций можно представить на примере Са2+ следующими уравнениями:
Са2+ + Нind2– ↔ СаInd– + Н+
синий красный
Са2+ + H2Y2– ↔ СаY2– + 2Н+
СаInd– + H2Y2– + 2ОН– ↔ СаY2– + Нind2– + 2Н2О
красный синий
Стандартизация рабочего раствора трилона Б
по стандартному раствору сульфата магния
Ход анализа. Отбирают пипеткой 15,00 мл (Vп) стандартного 0,05000 М раствора соли MgSO4×7H2O, в колбу для титрования, разбавляют дистиллированной водой примерно до 50 мл. Затем добавляют 5 мл аммиачной буферной смеси, щепотку сухого, смешанного с NaCl индикатора эриохром черный Т до хорошо заметной, но не очень темной винно-красной окраски, и титруют из бюретки рабочим раствором трилона Б (~0,05 М) до перехода окраски раствора в синюю (без красноватого оттенка). Определение повторяют не менее трех раз и рассчитывают концентрацию трилона Б:
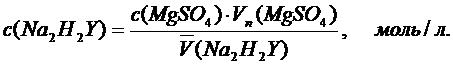
Определение общей жесткости природной воды
Предлагаемая методика применима при отсутствии в воде заметных количеств ионов Zn2+, Cu2+, Mn2+. Их мешающее влияние устраняют с помощью реагентов.
Ход анализа. Отбирают пипеткой 50,00 мл (V) пробы водопроводной (или другой анализируемой воды) воды в колбу для титрования, добавляют 5 мл аммиачного буферного раствора, щепотку индикатора до винно-красной окраски и титруют стандартизованным рабочим раствором комплексона III (трилона Б) до перехода красной окраски раствора в синюю. В конце титрования добавляют рабочий раствор по каплям и тщательно перемешивая. Титрование повторяют 2–3 раза и из сходящихся результатов вычисляют средний объем . Общую жесткость воды (ммоль эквивалентов Са2+ и Mg2+) вычисляют по формуле:
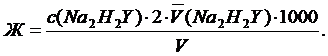
Контрольные вопросы
(Метод комплексонометрии)
1. Перечислите основные требования к реакциям, применяемым в методе комплексометрического титрования?
2. Почему в комплексометрическом титровании редко используют неорганические реагенты?
3. Назовите способы обнаружения конечной точки титрования.
4. Изложите сущность метода комплексонометрии.
5. Объясните сущность прямого, обратного, вытеснительного и косвенного приемов комплексонометрического титрования. В каких случаях применяется каждый из названных приемов?
6. Что такое металлохромные индикаторы? Напишите равновесие в растворе металлохромного индикатора.
7. Назовите важнейшие металлохромные индикаторы. Каким требованиям они должны удовлетворять?
8. Как повысить селективность комплексонометрического титрования? Приведите примеры.
9. Приведите графическую формулу ЭДТА. Какова дентатность ЭДТА?
10.Какова стехиометрия комплексов ЭДТА? Приведите графическую формулу комплексов двух - и трехзарядных ионов металлов с ЭДТА.
11. Какие вещества пригодны для стандартизации раствора ЭДТА?
12. В каких условиях проводят титрование ионов кальция раствором ЭДТА или ее солями?
13. Как проводят комплексонометрическое определение кальция и магния при совместном присутствии?
14. Почему следует удалить аммонийные соли при титровании кальция в присутствии магния?
15. Какие приемы используют в комплексонометрии при медленном протекании реакции с ЭДТА?
16. Какие ионы определяют общую жесткость воды и каковы условия ее определения? Какова роль ЭДТА в определении и устранении общей жесткости воды?
1.4. Методы окислительно-восстановительного титрования
(редоксиметрии)
Классификация наиболее широко используемых методов редоксиметрии приведена в табл. 1. Методы редоксиметрии основаны на изменении потенциала окислительно-восстановительной системы в ходе титрования вследствие изменения концентрации окисленной и восстановленной форм реагирующих веществ. Полнота протекания реакции зависит от разности стандартных (или формальных) потенциалов окислительно-восстановительных пар.
1.4.1. Перманганатометрия
Перманганатометрия – это метод титрования рабочим раствором KMnO4. Чаще всего реакцию титрования проводят в сильнокислой среде, создаваемой H2SO4:
MnO4– + 8H+ + 5ē = Mn2+ + 4H2O
Для пары MnO4–/Mn2+ Е0 = 1,51 В, что позволяет определять многие восстановители прямым титрованием.
Перманганатометрическое определение окислителей проводят, используя приемы: а) обратного титрования, применяя в качестве второго рабочего раствора либо сульфат железа(II), либо щавелевую кислоту H2C2O4; б) прямое титрование восстановленной формы анализируемого компонента.
Метод перманганатометрии можно использовать и для определения веществ, не проявляющих окислительно-восстановитель-ных свойств, в частности, ионов Са2+, реагирующих с H2C2O4 (при анализе на содержание Са почвы, минералов, биологических материалов и др.). В этих случаях применяют обратное или заместительное титрование.
Для фиксирования Т. Э. в методе используют свойство KMnO4 окрашивать раствор в розовый цвет от одной избыточной капли (титрование без индикатора).
Лабораторная работа №3
Определение Fe2+ в контрольном растворе соли Мора
Стандартизация рабочего раствора KMnO4 по щавелевой кислоте (установление концентрации рабочего раствора KMnO4.). Рабочий раствор KMnO4 готовится в лаборатории заранее путем растворения рассчитанной навески KMnO4 в определенном объеме свежей дистиллированной воды (~3,2 г на 1 литр для 0,1 н. раствора). Полученный раствор переливают в емкость из темного стекла и выдерживают 7-10 дней, после чего фильтруют через стеклянный фильтр с пористой пластинкой и хранят в сосуде из темного стекла, закрытом стеклянной пробкой. При хранении раствора его концентрация изменяется под влиянием имеющихся в воде восстановителей, аммиака, органических веществ, попадающих с пылью и др. Поэтому концентрацию рабочего раствора KMnO4 устанавливают и периодически проверяют по стандартному раствору щавелевой кислоты. При титровании протекает реакция:
2KMnO4 + 5Н2С2О4 + 3H2SO4 = 2MnSO4 + 10СО2 + К2SO4 + 8H2О
Ход работы. Бюретку ополаскивают рабочим раствором перманганата и заполняют им непосредственно перед титрованием. После окончания титрования раствор сливается в емкость с KMnO4, а бюретка и резиновая трубка с бусинкой тщательно промываются водой для предотвращения реакции разложения, протекающей на свету:
4KMnO4 + 6H2O = 4MnО(ОН)2¯ + 4КОН + 3О2
Пипеткой отбирают аликвоту Vп приготовленного раствора щавелевой кислоты (15,00 мл), переносят в колбу для титрования, добавляют 15 мл 1 М H2SO4, нагревают раствор до 70–80 0С для ускорения реакции и титруют, добавляя при непрерывном перемешивании раствор KMnO4 из бюретки до появления неисчезающей в течение 30 секунд бледно-розовой окраски. Вначале реакция протекает медленно, но накапливающиеся ионы Mn2+ оказывают каталитическое действие (автокатализ). Титрование повторяют не менее трех раз, находят (KMnO4) и рассчитывают концентрацию раствора KMnO4:
Определение Fe2+ основано на реакции прямого титрования:
2KMnO4 + 10FeSO4 + 8H2SO4 = 2MnSO4 + 5Fe2(SO4)3 + К2SO4 + 8H2О
Ход анализа. Полученный раствор соли Мора в мерной колбе на 100,0 мл разбавляют дистиллированной водой до метки, закрывают пробкой и тщательно перемешивают. Затем отбирают подготовленной пипеткой по 15,00 мл в конические колбы, прибавляют туда же по 15 мл 1 М H2SO4 и титруют из бюретки рабочим раствором KMnO4 (концентрация установлена в работе №5) до неисчезающей в течение 30 сек. бледно-розовой окраски. Титрование повторяют не менее трех раз, вычисляют (KMnO4) и массу Fe в анализируемом растворе.
1.4.2. Иодометрия
Иодометрическое титрование основано на реакциях восстановления иода до иодид-ионов и окисления иодид-ионов до иода:
I2 + 2e– ↔ 2I–
Раствор иода готовят путем растворения очищенного возгонкой иода в иодиде калия. При этом образуется растворимый комплексный ион I3–. Редокс-потенциал пары I3–/3I– Е0 = 0,54 В. Благодаря этому возможно иодометрическое определение как окислителей, так и восстановителей. В качестве второго рабочего раствора в иодометрии используют раствор тиосульфата натрия, количественно реагирующего с иодом в среде от слабокислой до слабощелочной.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |