На правах рукописи
ПАВЛОВА ТАТЬЯНА НИКОЛАЕВНА
КЕРАТОПЛАСТИКА В ВЕТЕРИНАРНОЙ ОФТАЛЬМОЛОГИИ
Специальность 06.02.01- диагностика болезней и терапия животных, патология, онкология и морфология животных
Автореферат
Диссертации на соискание ученой степени
кандидата ветеринарных наук
Москва 2013
Работа выполнена на кафедре «Незаразные болезни» ФГБОУ ВПО "Московский государственный университет пищевых производств" Министерства образования и науки РФ.
Научный руководитель: | – доктор ветеринарных наук, профессор, академик РАСХН
|
Официальные оппоненты: | – , доктор ветеринарных наук, профессор, ФГБОУ ВПО «Российский университет дружбы народов», заведующий кафедрой «Клиническая ветеринария» |
– , кандидат ветеринарных наук, ветеринарной офтальмологии доктора », ветеринарный врач | |
Ведущая организация: | ФГБОУ ВПО «Московская государственная академия ветеринарной медицины и биотехнологии им. » |
Защита состоится «27» июня 2013 года в 14.00 часов на заседании диссертационного совета Д 212.148.09. ФГБОУ ВПО "Московский государственный университет пищевых производств" по адресу: Россия, , ауд. 290.
С диссертацией можно ознакомиться в библиотеке ФГБОУ ВПО "Московский государственный университет пищевых производств"
Автореферат разослан « » 2013г.
Автореферат размещен на сайте Министерства образования и науки РФ http://vak. *****/ « » 2013 г.
Ученый секретарь диссертационного совета,
доктор ветеринарных наук, профессор
1. ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. В последние годы в нашей стране предложено много новых способов консервативного лечения заболеваний роговой оболочки: различные новые лекарственные средства, физиотерапевтические методы, из передовых методов - плазма обогащенная тромбоцитами и др.. Однако в клинической практике встречается немало животных с поражением роговицы, у которых, несмотря на применение комплекса средств консервативной терапии, заболевание не поддается лечению и прогрессирует. Это приводит к значительному снижению зрения и риску потери глазного яблока. В этих случаях единственным методом радикального лечения, в зависимости от тяжести заболевания, является послойная или сквозная кератопластика.
При многих заболеваниях роговицы, таких как проникающие ранения глаза с дефицитом ткани роговицы, ожоги глазного яблока, язвы роговицы, осложненные десцеметоцеле и перфорации ее при инфекционных, трофических, аллергических и других кератитах, необходимо ургентное хирургическое вмешательство на роговой оболочке. (, , 2012;, , 1988) Основной целью лечебной кератопластики является сохранение глазного яблока путём удаления патологического участка роговицы и замещения её дефекта.
Ранее с целью коррекции дефектов роговицы нами применялись различные материалы трансплантатов: конъюнктивальный лоскут «на ножке», аллоплант проф. Мулдашева (г. Уфа), биотрансплантат компании «Cook» (США), свежая донорская роговица. Все они имеют существенные недостатки в связи с невозможностью применения при сквозной кератопластике и тотальной послойной пересадке роговицы.
В гуманитарной офтальмологии при ургентных пересадках роговицы в качестве донорского трансплантата используется роговица высушенная над силикагелем. В отечественной и зарубежной литературе мы не нашли данных о применении роговицы высушенной над силикагелем у мелких домашних животных. Отсутствует методика консервации роговицы для животных, не разработана технология операции сквозной и послойной кератопластики с использованием данного материала, не описаны результаты клинического применения обезвоженной роговицы, не определены показания и противопоказания к хирургическому вмешательству.
Цели и задачи исследования.Разработка и внедрение в клиническую практику методики применения обезвоженной над силикагелем роговицы при операциях по сквозной и послойной кератопластике у мелких домашних животных.
Исходя из поставленной цели, были сформулированы следующие задачи:
1. подобрать наиболее доступный способ консервации донорской роговицы для собак и кошек;
2. провести гистологические анализ обезвоженной роговицы с целью определения морфологического состояния трансплантата на разных этапах консервации.
3. выполнить микробиологические исследования обезвоженной роговицы на предмет определения стерильности в процессе консервации и на различных сроках хранения.
4. разработать технологические этапы операции сквозной и послойной кератопластики в зависимости от тяжести патологии и исходного состояния роговицы;
5. определить показания и противопоказания к операции;
6. оценить непосредственные и отдаленные результаты хирургического лечения, проанализировать количество и характеринтра - и послеоперационных осложнений.
Научная новизна.
1. Впервые была разработана методика консервации обезвоженной донорской роговицы над силикагелем для применения в ветеринарной офтальмологии.
2. Впервые внедрена в клиническую практику операция сквозной и послойной кератопластики с использованием обезвоженной роговицы у мелких домашних животных.
3. Проведена оценка эффективности результатов вмешательства и состояния трансплантата в непосредственном и отдаленном послеоперационном периоде сроком до 3-х лет. Проанализирован характер и частота интра - и послеоперационных осложнений. Определены показания и противопоказания к кератопластике.
4. Проведенные исследования гистологического строения роговой оболочки показывают, что обезвоженная роговица сохраняет нормальную морфологическую структуру независимо от срока консервации.
5. На основе микробиологических исследований выявлено, что роговица при длительной консервации методом обезвоживания над силикагелем сохраняет свою стерильность. В консервированном материале отсутствует бактериальная микрофлора.
Теоретическая и практическая значимость.
1. Разработанная, апробированная и внедренная в практику система микрохирургических и лечебных мероприятий позволяет добиться высоких клинических результатов послойной и сквозной кератопластики с применением обезвоженной донорской роговицы, что является свидетельством практического решения проблемы.
2. Отработанные варианты радикальных реконструктивных вмешательств на роговице позволяют сохранить глаз как орган и в дальнейшем частично восстановить оптические функции.
3. Нами была улучшена и упрощена методика по обезвоживанию трупной роговицы над силикагелем. Данная модификация позволяет использовать этот метод консервации кадаверной роговицы широкому кругу ветеринарных офтальмологов.
Апробация работы. Основные положения работы доложены на:
- I Всероссийская межвузовская конференция ветеринарной хирургии (Москва, 2010);
- IX Международная научная конференция студентов и молодых ученых «Живые системы и биологическая безопасность населения»( Москва, 2011);
- II Всероссийская межвузовская конференция ветеринарной хирургии (Москва, 2011);
- XIX Московский международный конгресс ( Москва, 2011);
- XX Международная научная конференция студентов и молодых ученых «Живые системы и биологическая безопасность населения» (Москва, 2012);
- XX Московский международный конгресс ( Москва, 2012).
Внедрение результатов исследования.Результаты исследований внедрены в практическую работу «Центра ветеринарной офтальмологии доктора », а так же в учебный процесс и научно-исследовательскую работу по курсу частной хирургии кафедры «Незаразных болезней» ФГБОУ ВПО «Московский государственный университет пищевых производств».
Публикация результатов исследований.По теме диссертации опубликовано 7 работ, в том числе 3 из них в изданиях рецензируемых ВАК РФ: «Ветеринария» №10, Москва 2012; «Актуальные вопросы ветеринарной биологии»№3 (15), Санкт-Петербург 2012; «Актуальные вопросы ветеринарной биологии»№4 (16), Санкт-Петербург 2012;
Основные положения выносимые на защиту:
- Методика обезвоживания роговицы;
- Гистологическое доказательство сохранения морфологической структуры обезвоженной роговицы при длительной её консервации;
- Микробиологическое доказательство стерильности обезвоженной роговицы;
- Техника микрохирургичекой операции сквозной и послойной кератопластики с применением обезвоженной донорской роговицы;
- Оценка непосредственных и отдаленных результатов сквозной и послойной кератопластики при различных патологиях роговицы, интро - и послеоперационные осложнения.
Объем и структура диссертации.Диссертация изложена на 150 страницах компьютерного текста и включает введение, обзор литературы, материалы и методы исследования, результаты собственных исследований, обсуждение результатов исследований, выводы, библиографический список включает наименования работ, из них - 63 зарубежных авторов. Диссертация иллюстрирована рисунками и фотографиями.
2. СОБСТВЕННЫЕ ИССЛЕДОВАНИЯ
2.1 Материалы исследований.
Работа выполнялась на кафедре незаразных болезней ФГБОУ ВПО «Московский государственный университет пищевых производств». Экспериментальная часть выполнялась на базе «Центра ветеринарной офтальмологии доктора », в лаборатории «Веттест» и в НИИ глазных болезней РАМН.
На этапе морфологического исследования обезвоженной и регидратированной роговицы в разные сроки консервации эксперимент проводился на 10 роговицах кроликов. Данное исследование проводилось в течение 2-х лет.
На этапе бактериологического исследования глаз донора и влияния обезвоживания на микрофлору эксперимент проводился в два этапа. На первом этапе исследовали степень загрязненности трупных глаз бактериальной флорой и воздействие на неё дезинфицирующих средств и антибиотиков. Данное исследование проводилось на 67 кадаверных глазах. На втором этапе изучали влияние обезвоживания силикагелем на выживаемость золотистого стафилококка, нанесенного на роговицу до её обезвоживания. Для постановки данного эксперимента мы провели 50 опытов на роговицах кадаверных глаз, 25 опытов с силикагелем и столько же без силикагеля.
На этапе клинических исследований приживления обезвоженной донорской роговицы мы провели эксперимент на 52 кроликах (самцы). В клинической практике произведено 120 операций по послойной кератопластике и 68 операций по сквозной кератопластике на 150 животных (кошки и собаки).
Хирургическому лечению были подвергнуты животные с обширными глубокими язвами роговицы из них послойная кератопластика на 120 глазах (64%) и сквозная кератопластика на 15 глазах (8%) и корнеальными секвестрами на всю глубину роговицы 53 глаза (28%) сквозная кератопластика. В соответствии с этим выделено 2 клинические группы наблюдения.
Все операции производились с лечебной целью (100%). В 48 случаях пересаженная роговица имела 6-6,5 мм в диаметре; в 76 случаях – 7-7,5 мм; в 38 глазах – 8,0 мм; в 21 глазу – 10 мм. В 5 случаях пересаженные роговичные диски 13 мм выполняли роль биологической повязки.
Оперированные нами больные (кошки и собаки) имели крайне разнообразные клинические проявления роговичной патологии. Кроме того, они отличались друг от друга по возрасту, соматическому статусу и способам предшествовавшего консервативного лечения, этиологии заболевания и другим факторам. Ведущими отличительными признаками на наш взгляд являлись этиология и тяжесть поражения роговой оболочки. В таблице 1 показано общее количество больных, операций и оперированных глаз в разных группах наблюдения.
Таблица 1
Общая характеристика клинического материала
Группа больных по этиологическому фактору поражения роговицы | Количество больных | Количество прооперованных животных всего | Количество глаз | |
собаки | кошки | |||
Не перфарирующие язвы роговицы | 59 | 42 | 101 | 120 |
Перфарирующие язвы роговицы | 7 | 6 | 13 | 15 |
Корнеальный секвестр на всю глубину роговицы | - | 36 | 36 | 53 |
Возрастная характеристика больных к моменту заболевания и ко времени операции представлены в таблице 2. Операции у котят и щенков составили, животные старше 12 лет. Основная часть оперированных животных представлена в возрасте от 5 до 8 лет.
Таблица 2
Возраст животных к моменту операции
Группа больных по этиологическому фактору поражения роговицы | Собаки | Кошки | ||||||
До 1 г | От 1 до 5лет | От 5 до 8 лет | Старше 12 лет | До 1 года | От 1до 5лет | От 5 до 8лет | Старше 12 лет | |
Не перфарирующие язвы роговицы | 10 (16%) | 5 (7,5%) | 36 (54,5%) | 8 (12%) | 4 (5%) | 3 (3,5%) | 28 (33%) | 7 (8%) |
Перфарирующие язвы роговицы | - | 1(1%) | 4(6%) | 2 (3%) | 2 (3%) | 1 (1%) | 2 | 1 (1%) |
Корнеальный секвестр на всю глубину роговицы | - | - | - | - | 6 (7%) | 3 (3,5%) | 23 (27%) | 4 (5%) |
Всего | 10 | 6 | 40 | 10 | 12 | 7 | 53 | 12 |
Показаниями к трансплантации обезвоженной донорской роговицы послужили:
1.перфорирующие и не перфорирующие септические язвы роговицы;
2.тотальные и субтотальные корнеальные секвестры с поражением всех слоев роговицы, включая эндотелий.
Противопоказаниями к пересадке роговицы с применением обезвоженной роговицы в качестве материала для пересадки являются:
1. первичная и вторичная глаукома;
2. панофтальмит;
3. атрофия глазного яблока.
Трансплантационный материал. В качестве трансплантационного материала были использованы консервированная методом обезвоживания над силикагелем донорская роговица кошек и собак. Доноры подбирались без инфекционных и онкологических заболеваний в анамнезе. Причина смерти донора – различные травмы, почечная и сердечно-сосудистая недостаточность. Подбор материала для операции осуществлялся строго с учетом видовой принадлежности донора и реципиента.
2.2 Методы исследований.
Клинические исследования. Клинический статус животного определяли по общепринятым в ветеринарной медицине методикам ( , , , 1969; с соавт., 1985).
Морфологические исследования. Данный метод исследования применялся для изучения морфологического строения обезвоженной и регидратированной роговой оболочки в разные сроки консервации от 1 месяца до 2 лет. Гистологическое исследование проводили по общепринятым в ветеринарии методам(, , 1969) Всего было изучено 10 роговиц в следующие сроки хранения: до 3-х месяцев – 2 роговицы, до 6-ти месяцев– 1, до 8 месяцев – 1, до 10 месяцев – 2, до 1 года – 1, до 1,5 лет – 1, до 2-х лет - 2 роговицы.
Также морфологические исследование проводились для изучения процесса врастания роговицы донора в роговицу реципиента в эксперименте на кроликах после проведения сквозной и послойной кератопластики.
Метахроматическое окрашивание. Данный метод морфологического исследования применялся для определения наличия кислых мукополисахаридов. Они в значительной мере определяют физические и биологические свойства стромы роговицы. Метахроматическое окрашивание проводилось по общепринятым методикам (Лизон 1935)В норме строма роговицы окрашивается в лилово-розовый цвет, а кератоциты, эпителий и эндотелий – в сине-фиолетовый. Окраска эта нестойкая, в связи с чем мы сразу производили микрофотосъемку.
Микробиологическое исследование. Методика посева содержимого конъюнктивального мешка трупных глаз на сахарный и солевой бульоны, с целью определения загрязненности трупных глаз бактериальной флорой и воздействие на неё дезинфицирующих средств и антибиотиков. Посев на сахарный и солевой бульон выполняли по общепринятой методике (,, 2002;, 1992)
Методика посева золотистого стафилококка, нанесенного на роговицу до её обезвоживания, с целью определения выживаемости золотистого стафилококка в процессе консервации роговицы методом обезвоживания.
Опыты производились на роговице изолированных глаз следующим образом. Глаз кролика тщательно промывался раствором пенициллина, к которому выбранный штамм стафилококка был нечувствителен, затем физиологическим раствором, после чего иссекался роговично-склеральный лоскут. Последний освобождался от сосудистого тракта глаза и для определения бактериальной флоры, сохранившейся после промывания пенициллином, проводился посев на сахарный бульон. После этого роговично-склеральный лоскут укладывался на блок, имеющий кривизну нормальной роговицы, и помещался в бюксу, окруженную силикагелем, точно таким образом, как это мы делаем в клинике при засушивании донорской роговицы. В контрольном опыте блок укладывался в бюксу без силикагеля.
Далее, на поверхность роговицы наносилось 2 капли односуточной культуры патогенного золотистого стафилококка, содержащего 1000 микробных тел в 1 мл. То же делалось в контроле, но без силикагеля. Обе бюксы наглухо заливались парафином и оставлялись при комнатной температуре.
Комплексное предоперационное офтальмологическое обследование
осуществлялось методом биомикроскопии с помощью налобного бинокулярного микроскопа и щелевой лампы «SHIN-NIPPON» с использованием всех вариантов освещения (, 1974). Этот метод является незаменимыми при постановке диагноза, выборе правильной оперативной тактики, при оценке хода послеоперацилнного заживления и назначения необходимого лечения. Локализация травматического дефекта проводилась с использованием раствора флюоресцина и последующим исследованием в ультрафиолетовом освещении щелевой лампы.
Состояние тонуса обоих глаз определяли методом тонометрии по Маклакову и тонометром Tonovet. При многих патологических состояниях, изменяющих величину, сферичность или упругость роговой оболочки внутри глазное давление более достоверное значение дает исследование тонометром Tonovet.
У всех животных проводили ультразвуковое исследование глазного яблока на один из самых современных сканов MedisonSonoace X6.
Выполнялось комплексное предоперационное обследование животного, включающее биохимический и общий клинический анализ крови, рентген грудной клетки, ЭКГ и УЗИ сердца, для выявления степени анестезиологического риска.
2.3Результаты исследований
2.3.1. Метод консервации донорской роговицы с помощью обезвоживания над силикагелем
После осмотра роговицы методом бокового освещения и на щелевой лампе для изучения её прозрачности, глаз окунается в раствор антибиотика. Далее выкраивается роговично-склеральный лоскут, который освобождается от сосудистого тракта. Лоскут тот помещается на пластиковую подставку с овальной поверхностью, повторяющей кривизну роговицы и устанавливается в бюксу с силикагелем. Когда роговично-склеральный лоскут укладывается на поверхность подставки, сама роговица вмещается на овальной поверхности подставки, имеющей диаметр роговицы. Бюкса хранится при комнатной температуре. Высушивание происходит со стороны эпителия. При таком способе наилучшим образом сохраняется форма и кривизна роговицы. Силикагель до высушивания рассыпается в чашки Петри и прокаливается при температуре 120ºС в течение 1 часа для повышения его адсорбционной способности. В таких бюксах роговица окруженная силикагелем, сохраняется длительный срок – до 1-3-х лети более при комнатной температуре. Роговица даже в высушенном состоянии кажется прозрачной.
2.3.2 Результат морфологических исследований обезвоженной и регидратированной роговицы в разные сроки консервации.
Были проведены морфологические исследования обезвоженной и регидратированной роговицы в период хранения от 1 месяца до 2-х лет.
При микроскопии препаратов трупной обезвоженной роговицы до регидратации было установлено, что толщена её значительно уменьшена по сравнению со свежей, все слои как бы сжаты и густо окрашиваются гематоксилин-эозином.
Приводим описание гистологической структуры обезвоженной регидратированной роговицы кролика со сроком хранения 2 месяца (Рис. 1 А). Эпителий многослойный, плоский с нерезкими контурами клеток, что зависит от интенсивности окраски гематоксилином не только ядер, но и протоплазмы. Эпителиальный слой хорошо сохранен – все эпителиальные клетки как базального, так и среднего слоев имеют нормальную форму. Собственное вещество роговицы сохраняет пластическую структуру и нормально окрашивается эозином в светло розовый цвет. Ядра кератоцитов в одних местах имеют нормальную палочковидную форму, в других несколько извилистую. Десцеметова оболочка нормальной толщины, на задней её поверхности лежат эндотелиальные клетки.


А) Б)
Рис.1.А)Микрофотография обезвоженной, регидратированной роговицы кролика. Срок хранения 2 месяца.
Б) Микрофотография обезвоженной, регидратированной роговицы кролика. Срок хранения 18 месяцев
При гистологическом исследовании роговиц с более длительным сроком консервации морфологическая структура их не отличалась от вышеописанной (Рис. 1 Б).
Одним из показателей качества консервации является содержание в строме кислых мукополисахаридов, которым придается большое биологическое значение. Кислыемукополисахариды, как известно, относятся к углеводным соединениям. Являясь главным компонентом основного вещества соединительной ткани, они в значительной мере определяют физические и биологические свойства стромы роговицы. Для определения мукополисахаридов производили окрашивание толлуидиновым синим и сравнивали степень окрашивания на разных сроках консервации.
При окраске толлуидиновымсиним обезвоженных, а затем регидратированных роговиц, хранившихся в сроки от 1 месяца до 2 лет, интенсивность окраски не отличается от свежих, что указывает на отсутствие нарушения химизма роговицы при длительном её хранении. В этом отношении консервация обезвоживанием, при которой морфологическая структура роговицы наиболее приближается к норме, выгодно отличается от лиофилизации роговицы, приводящей к нарушению структуры мукополисахаридов.
Сохранение морфологической структуры и химизма роговицы на протяжении около 3-х лет свидетельствует о том, что использование обезвоженной роговицы практически не ограничено сроком, что имеет большое значение в практике. Это легло в основу применения нами в эксперименте и клинической работе роговиц с длительным сроком консервации.
2.3.3. Результаты бактериологического исследования глаз донора и влияние обезвоживания на микрофлору.
2.3.3.1. Результат определения бактериальной флоры трупных глаз и воздействие на неё дезинфицирующих средств.
Таблица 3
Бактериальная флора конъюнктивального мешка трупных глаз
Непатогенный белый стафилококк | 11 |
Патогенный белый стафилококк (плазмокоагуляция +, гемолиз+) | 1 |
Непатогенный золотистый стафилококк (плазмокоагуляция -,гемолиз -) | 6 |
Золотистый стафилококк (плазмокоагуляция+, гемолиз +) | 2 |
Гемолитический стрептококк | 1 |
Негемолитический стрептококк | 3 |
Зеленящий стрептококк | 1 |
Энтерококк | 1 |
Кишечная палочка | 3 |
Синегнойная палочка | 3 |
Смешенная кокковая флора | 4 |
Прочая ( плесень и др.) | 5 |
Роста нет | 17 |
Всего | 67 |
Из табл. 3 видно, что на 67 глазах была обнаружена бактериальная флора, преимущественно кокковая, из них золотистый ствафилококк - на 8 глазах.
Мы для стерилизации конъюнктивального мешка применили антибиотик широкого спектра действия – неомицин, к которому, по данным (1965), бактериальная флора конъюнктивального мешка наиболее чувствительна. Неомицин разводился физиологическим раствором непосредственно перед применением из расчета 30 ед. в 1 мл. Одна бутылочка раствора использовалась для дезинфекции двух глаз. Посев содержимого конъюнктивального мешка производился до и после обильного промывания глаза раствором неомицина.
Таблица 4
Рост бактериальной флоры до и после
обработки конъюнктивального мешка неомицином.
Количество исследованных глаз | До обработки | После обработки неомицином | Чувствительность к антибиотикам | |||||
Нет роста | Есть рост | Нет рост | Есть рост | Пениц. | Стреп. | Неомиц. | Не исслед. | |
40 | 22 | 18 | 38 | 2 | 11 | 10 | 15 | 4 |
Рост бактериальной флоры после обработки глаз неомицином бывает значительно реже, что объясняется высокой чувствительностью бактериальной флоры к неомицину.
Однако видно, что, несмотря на промывание глаз неомицином, в отдельных случаях (в 2 из 18) микробная флора оставалась на поверхности глаза после его промывания.
2.3.3.2. Результат определения выживаемости золотистого стафилококка, нанесенного на роговицу до её обезвоживания в процессе обезвоживания.
Таблица 5
Выживаемость золотистого стафилококка в опыте и контроле
(сводные данные)
С силикагелем (опыт) | Без силикагеля ( контроль) | |
Отсутствие роста | 10 | 0 |
1-115 колоний | 15 | 2 |
Сплошной рост золотистого стафилококка | 0 | 10 |
Плесень + другая флора | 0 | 8 |
Золотисты стафилококк + другая флора | 0 | 5 |
Всего | 25 | 25 |
Из таблицы 3 видно, что из 25 контрольных опытов без силикагеля в 10 наблюдался сплошной рост золотистого стафилококка, в то время как опыт с силикагелем это не имело места ни в одном случае. С другой стороны, в 10 опытах с силикагелем не наблюдалось роста, в то время как в контроле отсутствия роста не было ни в одном случае, за исключением случаев роста плесени, которая, надо полагать, вытеснила стафилококка в силу антагонизма микробов.
Таблица 6
Выживаемость золотистого стафилококка в опыте и контроле в разные сроки
Опыт | Контроль | ||||||||
Сроки | Число опытов | Отсутствие роста | Одиночные колонии | Сплошной рост зол. стаф. | Отсутствие роста | Одиночные колонии | Сплошной рост зол. стаф | Зол. стаф + другая флора | Плесень + другая флора |
До 1 месяца | 9 | 1 | 8 | 0 | 0 | 1 | 2 | 0 | 4 |
От 1 до 2-х мес | 8 | 2 | 6 | 0 | 0 | 0 | 5 | 4 | 1 |
От2 до 4 мес. | 2 | 1 | 1 | 0 | 0 | 1 | 1 | 0 | 1 |
От 4 до 7 мес | 1 | 1 | 0 | 0 | 0 | 0 | 1 | 0 | 1 |
От 7 до 10 мес | 5 | 5 | 0 | 0 | 0 | 0 | 1 | 1 | 1 |
Всего | 25 | 10 | 15 | 0 | 0 | 2 | 10 | 5 | 8 |
На основании 25 опытов по искусственному заражению роговицы патогенной культурой золотистого стафилококка до её обезвоживания мы пришли к определенному выводу, что обезвоживание роговицы силикагелем не только не способствует сохранению бактериальной флоры на её поверхности, но, наоборот, вызывает торможение роста как золотистого стафилококка, так и других микробных тел, в том числе и плесени. При хранении свыше 5 месяцев роговица практически стерильны.
Торможение роста бактериальной флоры мы объясняем резким обезвоживанием микробных тел, которое происходит одновременно с обезвоживанием роговицы под влиянием силикагеля. Поэтому при длительной консервации обезвоженной роговицы нет оснований опасаться сохранения как обычной бактериальной флоры, так и опасного для глаза патогенного золотистого стафилококка, что является весьма важным для профилактики инфекции.
2.3.4. Техника послойной и сквозной кератопластики в ветеринарной офтальмологии
1.Регидратация обезвоженной роговицы. Пребывание обезвоженной донорской роговицы в физиологическом растворе с антибиотиком (гентамицин) в соотношении 1:10 в течение 15 минут.
2. Техника выкраивания трансплантата. Предварительно регидратированный роговично-склеральный лоскут помещали на силиконовый глазной протез и закрепляли в глазном фиксаторе. С поверхности роговицы скребцом снимали весь пласт эпителия, так как он содержит большое количество водорастворимых белков, несущих иммунную информацию.
Трепан нужного размера ставили строго вертикально на центральный отдел роговицы. Выкраивание трансплантата для сквозной кератопластики старались полностью совершить трепаном, чтобы края роговичного диска оставались идеально ровными. Выкроенный трансплантат осматривали под микроскопом и укладывали в раневое отверстие роговицы пациента.
Для послойной кератопластики во время иссечения трансплантата использовали трепан модели ФМ-5. Данный трепан дает возможность получить диск роговицы определенной толщины, который удаляется или отодвигается. Для расслоения роговицы использовали нож-шпатель с заостренными краями. Благодаря использованию данной методики удается выкроить трансплантат необходимой толщины, имеющий безукоризненную поверхность и края.
Если трансплантат нужен не круглой формы, то выкраивание производили с помощью роговичных ножниц.
3. Иссечение пораженных слоев роговицы больного. Трепаном нужного размера (6,0; 6,5; 7,0; 8,0; 9,0;10,0; 11,0) с таким расчетом, чтобы по возможности были захвачены все пораженные участки роговицы. При вращательных движениях трепан должен сохранять вертикальную установку, чтобы получить ровный срез без выступов. Насечку поврежденной ткани производили осторожно, чтобы не повредить радужку и хрусталик.
При послойной кератопластике патологически измененная ткань роговицы реципиента последовательно иссекалась на максимальную глубину, но не до десцеметовой оболочки (, 1960). Насечка производилась трепаном модели ФМ-5 на необходимую глубину, а затем до необходимой глубины производилось расслаивание роговицы с помощью одноразового тупоконечного ножа - расслаивателя.
При сквозной кератопластике трепаном производится насечка максимальной глубины. Затем алмазным микролезвием делаем перворацию роговицы в зоне насечки, а дорезание роговицы по насечке производим тупоконечным алмазным микролезвием типа «Саха». Такой метод позволяет избежать травматизации радужки или хрусталика и край иссеченного ложе будет ровный, гладкий, без зазубрин, что ускорит срок приживления и качество.
При язвах роговицы в передней камере глаза очень часто встречается гипопион или синехии. На этом этапе операции производится удаление гипопиона из передней камеры и тупое рассечение синехий между радужкой и роговицей, освобождение зрачковой диафрагмы.
4. Фиксация трансплантата.Уложенный в отверстие роговицы реципиента прозрачный диск фиксировали сначала узловыми провизорными швами атравматичной иглой с пролиновой нитью 8-0. Игла проводилась на расстоянии 1 мм от края раны, через толщину роговицы, не захватывая внутренний эндотелиальный слой. Накладывали четыре шва соответственно на 3, 6, 9 и 12 часов. Разметка меридианов помогает правильно уложить трансплантата. Затем между ними накладывали одиночные узловые фиксационные швы в количестве 4-8-12 швов в зависимости от диаметра трансплантата на расстоянии 1-1,5 мм друг от друга.
Переднюю камеру наполняли физиологическим раствором или воздухом для восстановления тургора глаза и предотвращения образования синехий. Производили субконъюнктивальную блокаду антибиотика при язвах роговицы и зашивали веки. Открывали глаз через 2-4 недели. Снятие внутренних швов производили через 4-6 недель.
2.3.5. Непосредственные и отдаленные результаты реконструктивных операций выполненных на основе послойной и сквозной кератопластики с использование донорской роговицы консервированной методом высушивания над силикагелем при разных видах патологии роговицы.
После проведения экспериментальных сквозных и послойных кератопластик на кроликах мы получили отторжение трансплантата в 5%, в 95% приживление. При проведение сквозных кератопластик трансплантат помутнел, при проведении послойных пересадок роговицы трансплантата помутнел незначительно. По результатам гистологического исследования роговиц кроликов (рис. 2) проводимых через 28 – 35 дней после операций, мы отмечали отсутствие воспалительной реакции, как в тканях донора, так и реципиента. Освоение донорской роговицы происходило по типу свой - чужой, без выраженных цитотоксических реакций. В межпластинчатом пространстве наблюдали клеточную дорожку, представляющую собой пролиферативные клетки врастающих капилляров. В области рубца определялись овальные отверстия, представляющие собой канал от шовного материала.
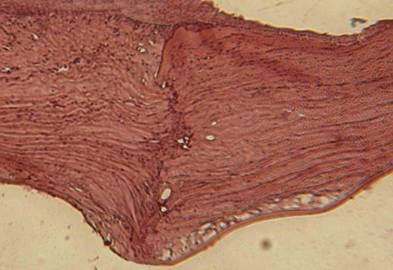
Рис. 2.Гистология роговицы кролика после проведения сквозной кератопластики через 30 дней после операции
Результаты клинических исследований показали сохранение прозрачности в области дефекта у 20% животных с небольшим диаметром трансплантата (менее 8мм) при передней послойной кератопластике. Помутнение трансплантата различной степени интенсивности мы наблюдали у 80% животных (43% незначительное помутнение; 37% оптически непрозрачная роговица) после проведения сквозных кератопластик, носящих органосохраняющий характер.
Общее количество осложнений, включающие интраоперационные и послеоперационные при сроке наблюдения до двух лет, в проведенных нами клинических исследованиях составило 15%. Интраоперационные перфорации десцеметоцеле (n=2 - 1%) корректировались сопоставлением краев дефекта десцеметовой мембраны с последующей фиксацией донорской роговицы или проведением сквозной кератопластики в условиях гипотонии.
Все послеоперационные осложнения показаны в таблице 7 и разделены на 3 группы%). Осложнения, связанные с дефектами укрепления трансплантата 8 (4%), изменения в донорской роговице 15(8%) и прочие осложнения, которые обычно сопровождают послеопеоперационный период при любых полостных операциях 4(2%)
Таблица 7
Сравнительные данные о количестве послеоперационных осложнений в разных группах наблюдения
Группы и виды осложнений | Послойная кератопластика | Сквозная кератопластика | |
Связанные с дифектом фиксации трансплантата | Несостоятельность шва | 1 (0,5%) | 2 (1%) |
Фильтрация из раны | - | 1 (0,5%) | |
Передние синехии | - | 4 (2%) | |
Изменения в трансплантате | Эрозия | 3 (1,5%) | 1 (0,5%) |
Отек | 7 (4%) | 4 (2%) | |
Прочие | Вторичная глаукома | - | 1 (0,5%) |
Панофтальмит | 1 (0,5%) | 1 (0,5%) | |
Атрофия глаза | - | 1 (0,5%) |
Послеоперационные осложнения (14%): несостоятельность швов встречалась у собак (n = 3 ) в 1.5% случаев и кошек ( n= 5) в 2.5% случаев, «болезнь трансплантата» (отмечалась с 7-го дня) являлась следствием ответа иммунной системы организма на чужеродную ткань. Проявлялось данное осложнение стойкой и интенсивной гиперемией конъюнктивы, помутнением донорской роговицы, дислокацией и отеком трансплантата, отторжения швов при сквозных кератопластиках (n = 11) в 6 % случаев у кошек (n=4) в 2% случаев. Послеоперационный панофтальмит наблюдали на 10 день у кошек(n=2) в 1% случаев, образование вторичной глаукомы после 21 дня от операции у собаки(n=1) в 0,5 % случаев.
Большое количество осложнений можно объяснить тяжестью патологии, поздними сроками обращения владельцев животных за специализированной помощью. За последние 2 года мы отметили снижение количества поcлеоперационных осложнений трансплантации донорской роговицы на 5 %.
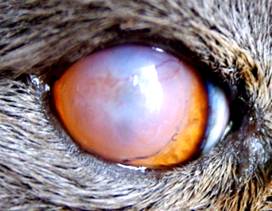
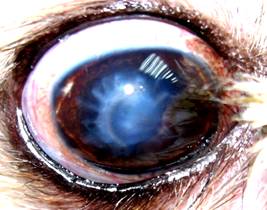
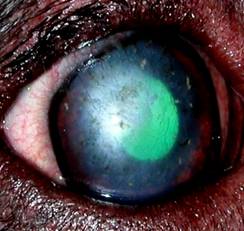
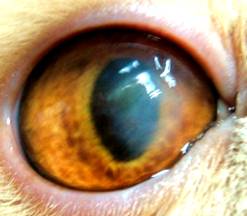
После проведенных операций у 85% животных удалось сохранить глаз как орган (рис. 3). У 63% животных удалось сохранить не только глаз, но и его частично оптические функции (рис. 4,5,6).Из недостатков метода можно отметить встречающееся непрозрачное приживление донорской роговицы.
|
|
Рис. 3 Субтатальная сквозная кератопластика через 2 месяца | Рис. 4 Состояние роговицы после сквозной кератопластики через 2 месяца |
|
|
Рис.5 Послойная субтотальная кератопластика через 3 месяца | Рис. 6 Состояние роговицы после послойной кератопластики через 3 месяца |
Заключение
Таким образом, консервация роговицы методом обезвоживания над силикагелем является простым, доступным и безопасным методом. Операции сквозной и послойной кератопластики у мелких домашних животных с применением обезвоженного трансплантата обладают высокой эффективностью, малым количеством осложнений и стабильностью функциональных результатов в непосредственном и отдаленном послеоперационном периоде. Высокие клинические результаты, физиологичность и доступность метода позволяет рекомендовать использование обезвоженной донорской роговицы в качестве материала для пересадки роговицы у мелких домашних животных для применения широкому кругу ветеринарных офтальмологов.
ВЫВОДЫ
1. Обезвоженная донорская роговица над силикагелем обладает высокой эффективностью в качестве трансплантата при сквозной и послойной кератопластике у собак и кошек.
2. Разработанная нами методика обезвоживания роговицы силикагелем предельно проста. Она обеспечивает сохранение формы и прозрачности роговицы, которая при этом не отличается от свежей. Данная модификация метода позволяет использовать данный материал широкому кругу ветеринарных офтальмологов.
3. Морфологические исследования на 10 обезвоженных и регидратированных трупных кроличьих роговицах показали, что гистологическая структура и химизм роговицы хорошо сохраняется не только в короткие сроки консервации до 2 мес., но и при весьма длительном хранении до 2-х лет. Это выгодно отличает метод обезвоживания силикагелем от других методов продолжительной консервации роговицы, при которых наблюдаются дегенеративные изменения в отдельных её слоях.
4. Бактериологические исследования по изучению выживаемости патогенной культуры золотистого стафилококка, искусственно нанесенного на роговицу (67 опытов), позволяют сделать заключение, что высушивание роговицы силикагелем не только не способствует сохранению бактериальной флоры на её поверхности, но, наоборот, вызывает торможение роста, как золотистого стафилококка, так и других микробных тел, в том числе и плесени.
5. В клинике было произведено 188 операций. Из них 120 послойных кератопластик и 68 сквозных кератопластик. Все операции производились с лечебной целью. В 85% случаях обезвоженная донорская роговица обладала высокой степенью приживления и значительной межпородной совместимостью.
6. При тяжелых язвах роговицы было произведено 120 послойных кератопластик. При перфорации роговицы, в следствие язвенного поражения и при корнеальных секвестра на всю глубину роговицы у кошек было произведено 68 сквозных кератопластик. Операции по послойной кератопластики оказались эффективны в 94,5% случаях, а при сквозной кератопластике - в 76% случаях.
7. Общие результаты всех произведенных операций послойной и сквозной пересадки высушенной роговицы таковы: 85 % благоприятный исход 15% осложнения. Прозрачное приживление трансплантата в 20% случаях; полупрозрачное в 43% и оптически не прозрачное в 37%.
ПРАКТИЧЕСКИЕ ПРЕДЛОЖЕНИЯ
1. Припроведение сквозных кератопластик диаметром более 4 мм и послойных кератопластик диаметром более 6мм рекомендуем использовать обезвоженный донорский трансплантат в качестве материала для пересадки.
2. Рекомендуем консервировать донорский материал методом обезвоживания над силикагелем по нашей методике. Данный метод прост и доступен. Донорская роговица консервированная методом обезвоживания над силикагелем сохраняется до 3-х лет не теряя своих свойств.
3. Предлагаем использовать разработанные методические указания «Сквозная и послойная пересадка роговицы с применением обезвоженной донорской роговицы у мелких домашних животных» для проведения сквозных и послойных пересадок роговицы в ветеринарной офтальмологии.
СПИСОК НАУЧНЫХ РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ
1. Павлова лиофилизированной донорской роговицы мелким домашним животным. Ветеринария.- М., 2012.-№10.- С.50-53
2. Павлова и послойная кератопластика с применением лиофилизированного донорского трансплантата у мелких домашних животных. Актуальные вопросы ветеринарной биологии.-.С-П.,2012.-№ 3.-С.68-71
3. Павлова анализ используемых материалов для пересадки роговицы в ветеринарной офтальмологии, преимущества и недостатки. Актуальные вопросы ветеринарной биологии.-.С-П.,2012.-№ 4.-С.47-50
4. Павлова и послойная кератопластика с применением лиофилизированного донорского трансплантата в ветеринарной офтальмологии/ , , научный консультант академик , доцент // Тезисы II всероссийской межвузовской конференции по ветеринарной хирургии-М.,2011.- С.111-117
5. Павлова и недостатки всех доступных материалов для кератопластики в ветеринарной офтальмологии на сегодняшний день / , , научный консультант академик , доцент // Тезисы II всероссийской межвузовской конференции по ветеринарнойхирургии – М.,2011.- С.125-129
6. Павлова терапевтического и хирургического лечения хронических поверхностных эрозий роговицы/ , научный консультант доцент // Труды XX московского международного конгресса/- М.,2012. –С. 161-166 7. Павлова материала для пересадки роговицы./ , научный консультант доцент // Труды XX московского международного конгресса/- М.2012. –С.166-170 |