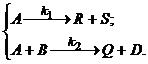 |
(3.2)
Реакция (3.1) является простой необратимой, реакция (3.2) – параллельной. В обоих случаях целевым продуктом является компонент R. Для определения технологических критериев необходимо составить уравнения математического описания всех указанных типов реакторов с учетом кинетики реакции. Рассмотрим модели непрерывных реакторов для проведения реакции (3.1).
3.3.1 Реактор идеального вытеснения (РИВ)
Для изотермического реактора математическое описание представляет собой систему уравнений материального баланса по компонентам:
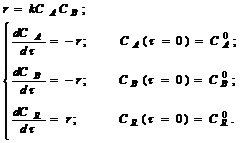 |
(3.3)
3.3.2 Реактор идеального смешения (РИС)
Уравнения материального баланса в стационарных условиях представляют собой систему вида:
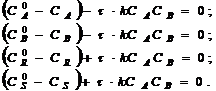
(3.4)
3.3.3 Каскад реакторов идеального смешения (РИС - m)
Параметром этой модели является число ячеек m. Система уравнений материального баланса по компонентам для j-ячейки имеет вид:
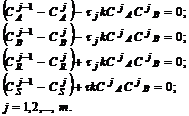 (3.5)
(3.5)
В системы уравнений (3.3), (3.4), (3.5) входят: ![]() – время пребывания в реакторе, c;
– время пребывания в реакторе, c;![]() – время пребывания в j-й ячейке, с;
– время пребывания в j-й ячейке, с; ![]() начальные концентрации компонентов, моль/м3; Са, Св, CR, CS – текущие значения концентраций, моль/м3; k – константа скорости реакции, м3 /(моль с).
начальные концентрации компонентов, моль/м3; Са, Св, CR, CS – текущие значения концентраций, моль/м3; k – константа скорости реакции, м3 /(моль с).
В результате решения систем уравнений (3.3)-(3.5) можно рассчитать концентрации всех компонентов, а затем и технологические критерии (программа № 4, Приложение А).
Ниже приведены системы уравнений материального баланса по компонентам для РИВ и РИС соответственно применительно для реакции (3.2).
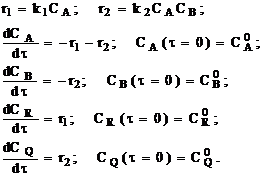 (3.6)
(3.6)
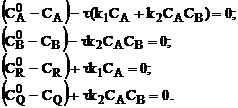 (3.7)
(3.7)
В результате численного решения систем уравнений (3.6), (3.7) (программа № 5, Приложение А) получают значения концентраций компонентов на выходе из реактора и значения технологических критериев.
3.4 Задание
3.4.1 Определить изменение концентрации компонентов А и В во времени для реакции (3.1) при проведении ее в реакторах различного типа: РИВ, РИС и каскад РИС, используя программу № 4 (Приложение А) и исходные данные, приведенные ниже. Построить зависимость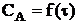 для РИВ с теоретическим значением константы скорости реакции и с экспериментально полученной, приведенной в таблице. Сравнить данные расчетов. Определить степень превращения ХА и выход целевого продукта ФR, используя теоретическое значение константы скорости реакции. Сравнить эффективность работы реакторов и предложить тип реактора для проведения данной реакции. Обосновать выводы.
для РИВ с теоретическим значением константы скорости реакции и с экспериментально полученной, приведенной в таблице. Сравнить данные расчетов. Определить степень превращения ХА и выход целевого продукта ФR, используя теоретическое значение константы скорости реакции. Сравнить эффективность работы реакторов и предложить тип реактора для проведения данной реакции. Обосновать выводы.
Исходные данные:
- константа реакции k = 0,08 л/(моль с);
- время пребывания ![]() = 600 с;
= 600 с;
- объем реактора V=l л;
- объемный расход реакционного потока 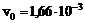 л/с;
л/с;
- начальные концентрации определяются по формулам: ![]() и
и ![]() , что соответствует различному отношению объемов компонентов А и В (1: N-1). Параметр N выбрать из таблицы 3.1 согласно номеру варианта.
, что соответствует различному отношению объемов компонентов А и В (1: N-1). Параметр N выбрать из таблицы 3.1 согласно номеру варианта.
Таблица 3.1 – Варианты заданий
Номер варианта | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
N | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
k экспер | 0,085 | 0,090 | 0,083 | 0,075 | 0,078 | 0,086 | 0,091 | 0,084 | 0,077 |
| 100 | 110 | 120 | 130 | 140 | 150 | 160 | 180 | 200 |
3.4.2 По графику CA=f(![]() ) определить время пребывания, при котором достигается такая же степень превращения, как и в РИС при
) определить время пребывания, при котором достигается такая же степень превращения, как и в РИС при ![]() =600. Сравнить объемы реакторов VРИВ/VРИС. Сделать необходимые выводы.
=600. Сравнить объемы реакторов VРИВ/VРИС. Сделать необходимые выводы.
3.4.3 Рассчитать реакторы идеального смешения и идеального вытеснения для параллельной реакции (3.2), используя программу № 5 (Приложение А) и исходные данные:
k1 =l,692.10-4 1/с;
k2= 1,708.10-41/с; ![]() моль/л;
моль/л;
объемный расход реакционного потока v0=0,005 л/с.
Время пребывания указано в таблице согласно номеру варианта.
Определить степень превращения ХА, выход продукта ФR в различных реакторах при заданном времени пребывания. Сравнить эффективность реакторов по этим технологическим критериям. Определить время пребывания и выход целевого продукта в различных реакторах при достижении одинаковых степеней превращения. По заданному расходу потока вычислить объемы реакторов, сравнить полученные данные, сделать необходимые выводы.
3.5 Контрольные вопросы
1. Какие реакторы идеального типа вы знаете? Чем они характеризуются?
2. Сформулируйте основные допущения модели каскада реакторов идеального смешения.
3. Назовите основные технологические критерии реакционных процессов.
4. В каких случаях применяется такой показатель, как селективность?
5. Назовите область применения идеальных моделей для расчета химических реакторов.
6. Какую роль играет кинетика химического процесса при выборе типа реактора?
7. Укажите основные недостатки и достоинства реакторов периодического действия. В каких производствах чаще всего встречаются такие реакторы?
ЛАБОРАТОРНАЯ РАБОТА № 4.
ИССЛЕДОВАНИЕ ВЛИЯНИЯ УСЛОВИЙ ПРОВЕДЕНИЯ
ГАЗОФАЗНОЙ РЕАКЦИИ НА ОБЪЕМ РЕАКТОРА
4.1 Цель работы
Изучить влияние температуры и давления на степень превращения в реакции окисления оксида азота и оценить объем реактора вытеснения при различных условиях.
4.2 Краткие теоретические сведения
Процесс получения разбавленной азотной кислоты из аммиака осуществляют либо при атмосферном давлении, либо при повышенном давлении; причем химическая и принципиальная схемы этих процессов не отличаются друг от друга.
Химическая схема производства включает три основные реакции:
– контактное окисление аммиака до окиси азота:
4NH3 + 5O2 = 4NO + 6H2O;
– окисление окиси азота до двуокиси азота: 2NO + O2 = 2NO2;
– абсорбция двуокиси азота водой с образованием азотной кислоты и окиси азота (которая возвращается в процесс):
3NO2 + H2O = 2HNO3 + NO.
Суммарная реакция образования азотной кислоты из аммиака выражается в виде уравнения
NH3 + 2O2 = HNO3 + H2O.
Принципиальная схема производства азотной кислоты из аммиака включает шесть основных операций (рисунок 4.1).


1 – очистка воздуха и аммиака; 2 – окисление аммиака на
катализаторе; 3, 4 – охлаждение нитрозных газов с использованием тепла в холодильнике; 5 – окисление окислов азота и образование азотной кислоты; 6 – очистка отходных газов
Рисунок 4.1 – Принципиальная схема производства
азотной кислоты
Окисление оксида азота до диоксида азота осуществляется по схеме
2NO +О2 = 2NO2+Q . (4.1)
Эта реакция является гомогенной газовой реакцией, фактически необратимой, наблюдаемый порядок которой соответствует молекулярности. Она протекает с уменьшением объема и сопровождается выделением теплоты. Снижение температуры и повышение давления способствуют смещению равновесия реакции вправо. Окисление оксида азота – самая медленная стадия производства азотной кислоты, она и определяет скорость всего процесса.
Газ, выходящий из реактора окисления аммиака, быстро охлаждается до температуры окружающего воздуха для конденсации из него водяных паров. До поступления в абсорбционные колонны, где получается азотная кислота, газ подвергается окислению в реакторе вытеснения до тех пор, пока отношение NO2/NO не будет равно 5/1. Состав газа на входе в реактор:
NO – 9 мол.%; NO2 – 1 мол. %; О2 – 8 мол.%; N2 – 82 мол.%.
Хвостовые газы производства азотной кислоты содержат после абсорбции колонн от 0,05 до 0,2 % оксидов азота, которые по санитарным требованиям без дополнительной очистки запрещено выбрасывать в атмосферу.
Хвостовые газы отправляют:
– в башни щелочной абсорбции, орошаемые водным раствором соды, где окислы азота (NO и NO2) абсорбируются содовым раствором с образованием солей
NO + NO2 + Na2CO3 = 2NaNO2 + CO2;
2NO2 + NaCO3 = NaNO2 + NaNO3 +CO2;
– на каталитическое восстановление оксидов азота горючими газами (водородом, природным газом, аммиаком). Восстановление оксидов азота снижает их содержание в очищенном газе до 0,001–0,005 %.
Схема установки каталитической очистки газов от оксидов азота приведена на рисунке 4.2.
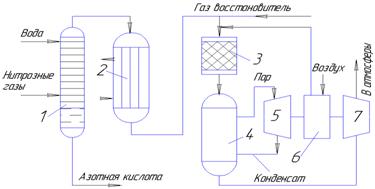
1 – абсорбционная колонна; 2 – подогреватель; 3 – контактный
аппарат; 4 – котел-утилизатор; 5 – паровая турбина; 6 – воздушный компрессор; 7 – газовая турбина
Рисунок 4.2 – Установка каталитической очистки газов
от оксидов азота
4.3 Математическое описание кинетики процесса
Скорость реакции можно выразить следующим образом:
(4.2)
Характеристическое уравнение реактора вытеснения имеет вид:
![]() (4.3)
(4.3)
Показать, что с учетом изменения объема уравнение (4.3) может быть преобразовано к виду:
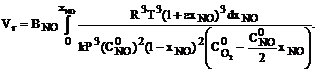 (4.4)
(4.4)
где k – константа скорости реакции;
Р – давление, атм.;
Т – температура, К;
xno – степень превращения NO;
R – газовая постоянная идеального газа, R=0,08205 л атм. град-1 моль-1 ;
BNO – мольный расход реагента NО, моль/с;
– начальные концентрации компонентов, моль/л;
![]() – коэффициент, учитывающий изменение объема газа.
– коэффициент, учитывающий изменение объема газа.
Значение коэффициента определяется по формуле
![]() . (4.5)
. (4.5)
Связь между объемным и мольным расходом реагентов:
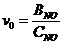 . (4.6)
. (4.6)
Формула (4.4) позволяет определять объем реактора при различных условиях проведения процесса: температуре и давлении.
4.4 Задание
4.4.1 Считая, что охлаждение реактора является эффективным и в нем поддерживается постоянная температура, вычислить по программе № 6 (Приложение А) объем изотермического реактора вытеснения при различных степенях превращения (0,1<х<хзад).
Исходные данные:
Т=293 К; Р = 1 атм.; k = 1,4.104 л2.моль-2.с-1 (при температуре 20 °С); ![]() = -0,45.
= -0,45.
Определить начальные концентрации компонентов и заданную степень превращения, если известно, что расход газа на входе в реактор равен v0 (при температуре 0 °С и давлении 1 атм.). Значение v0 взять из таблицы 4.1 согласно номеру варианта.
Таблица 4.1 – Варианты заданий
Номер варианта | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
v0 10-4, м3/ч | 0,6 | 0,7 | 0,8 | 0,9 | 1,0 | 1,1 | 1,2 | 1,3 | 1,4 |
4.4.2 Рассчитать объем реактора при заданной степени превращения, пренебрегая изменением объема реакционной смеси. Сопоставить объемы, дать объяснение.
4.4.3 Считая газовую смесь идеальной, определить объем реактора при проведении процесса под давлением 5 атм. Дать объяснение.
4.4.4 Рассчитать объем реактора при температуре 60 °С, если константа скорости при этой температуре равна 1,л2 моль-2..с-1.
4.4.5 Рассчитать объем реактора, работающего в адиабатическом режиме для достижения той же глубины превращения. Температура на входе в реактор Т=273 К. Для выполнения расчета внести изменения в программу. Конечная температура в любом сечении реактора с учетом изменения теплоемкости по степени превращения описывается следующим уравнением:
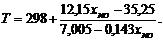 (4.7)
(4.7)
Зависимость константы скорости от температуры:
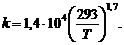 (4.8)
(4.8)
Сделать выводы о влиянии температурного режима в реакторе на его объем.
4.5 Контрольные вопросы
1. От каких факторов зависит скорость реакции окисления оксида азота? При каких условиях скорость реакции увеличивается?
2. Назовите основные стадии производства азотной кислоты.
3. Какие методы очистки хвостовых газов от оксидов азота применяются в промышленном производстве азотной кислоты?
ЛАБОРАТОРНАЯ РАБОТА № 5.
РАСЧЕТ НЕИЗОТЕРМИЧЕСКИХ РЕАКТОРОВ
5.1 Цель работы
5.1.1 Изучение тепловых режимов химических реакторов.
5.1.2 Моделирование политропического реактора идеального вытеснения.
5.1.3 Исследование влияния тепловой нагрузки на степень превращения при обеспечении температуры реакции в заданном диапазоне.
5.2 Краткие теоретические сведения
Химические реакции, как правило, сопровождаются выделением или поглощением тепла, что приводит к изменению температуры реакционной массы. От температуры зависят состояние химического равновесия и предельно достижимая степень превращения реагентов, скорость реакции, селективность и ряд других факторов. Для регулирования процесса в нужном направлении необходимо обеспечить тот или иной температурный режим.
Химические реакторы по способу организации температурного режима делятся на следующие типы:
• изотермические (температура реакции постоянна);
• адиабатические (отсутствие теплообмена с окружающей средой);
• политропические (частичный подвод или отвод тепла).
Для контроля над ходом реакции нужно регулировать температуру в пределах заданного диапазона. Этого можно достичь осуществлением соответствующего теплообмена. В промышленных аппаратах не всегда целесообразно поддерживать действительно изотермические условия. Процесс можно вести в промежуточном режиме (политропический процесс), организуя теплообмен с внешним источником тепла через поверхность теплообмена. Одним из способов управления температурой является изменение скорости теплопередачи путем регулирования расхода теплоносителя или изменения температуры конденсации его паров.
Учет тепловых явлений осуществляется при составлении теплового баланса химического реактора. При расчете неизотермического реактора необходимо совместно решать систему уравнений материального и теплового балансов, из которых первое учитывает изменение количества вещества, а второе – изменение количества теплоты при протекании химического процесса.
Рассмотрим необратимую реакцию первого порядка А ![]() S, проводимую в реакторе идеального вытеснения с тепловым эффектом
S, проводимую в реакторе идеального вытеснения с тепловым эффектом ![]() Н. В реакционной смеси содержится инертное вещество с концентрацией CR. Чтобы избежать образования побочных продуктов, для регулирования температуры в рубашку кожухотрубного реактора подают противотоком воду. Составим уравнения математического описания этого процесса.
Н. В реакционной смеси содержится инертное вещество с концентрацией CR. Чтобы избежать образования побочных продуктов, для регулирования температуры в рубашку кожухотрубного реактора подают противотоком воду. Составим уравнения математического описания этого процесса.
Уравнения материального баланса для РИВ в стационарных условиях имеют вид:
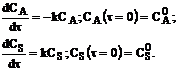 (5.1)
(5.1)
Уравнения теплового баланса для реакционного потока и теплоносителя:
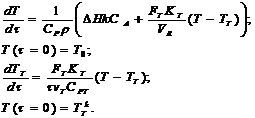 (5.2)
(5.2)
Зависимость константы скорости реакции от температуры описывается уравнением
![]() (5.3)
(5.3)
Теплоемкость смеси можно определить по правилу аддитивности:
СР = СРАСА +CPSCS +CPRCR. (5.4)
В уравнения (5.1)–(5.4) входят величины:
СА, Cs – концентрации исходного вещества и продукта соответственно, моль/м3;
CR – концентрация инертного компонента, моль/м3;
СРА, СРS, CPR – теплоемкости компонентов, Дж/(кг·К);
СР – теплоемкость реакционной смеси, Дж/(кг·К);
Т, ТT – температуры соответственно реакционного потока и теплоносителя, К;
k – константа скорости реакции, м3/(моль·с);
k0 – предэкспоненциальный множитель;
Е – энергия активации, Дж/моль;
R – газовая постоянная, Дж/(кмоль ·К) ;
FT – поверхность теплообмена, м2;
КT – коэффициент теплопередачи, Вт/(м2·К);
VR – объем реактора, м3;
– среднее время пребывания в реакторе, с;
vT – массовый расход теплоносителя, кг/с;
СRT – теплоемкость теплоносителя, Дж/кг·К.
Система уравнений (5.1)–(5.4) полностью описывает процесс химического превращения в реакторе идеального вытеснения и может быть решена любым численным методом относительно требуемых величин.
5.3 Задание
Реализуя численный эксперимент с помощью математической модели, определить концентрационный и температурный профиль по длине аппарата. Определить расход теплоносителя, обеспечивающий заданные начальные и конечные температуры теплоносителя. Определить степень превращения реагента А. Исследовать влияние начальной температуры реакционного потока и расхода теплоносителя на степень превращения исходного реагента. Сделать необходимые выводы.
Исходные данные:
CR = 10,8 кмоль/м3; ![]() Cpa = Cps = 62 кДж/(кмольК);
Cpa = Cps = 62 кДж/(кмольК);
CPR = 53 кДж/(кмоль К); ![]() Н = - 448.104 кДж/(кмоль);
Н = - 448.104 кДж/(кмоль);
k0 =1,8; Е = - 44900 Дж/моль; 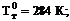 Ттк = 293 К;
Ттк = 293 К;
Кт = 0,320 кВт/(м2·К); Ft = 14,16 м2 ; СРТ = 4,190 кДж/(кг·К);
VR = 0,283 м3; ![]() = - 3600 с ; L = 5,9 м; =103 кг/кмоль.
= - 3600 с ; L = 5,9 м; =103 кг/кмоль.
Начальную концентрацию реагента А выбрать из таблицы 5.1 согласно номеру варианта.
Таблица 5.1 – Варианты заданий
Номерварианта | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 1,5 | 1,6 | 1,7 | 1,8 | 2,0 | 2,2 | 2,4 | 2,6 | 2,8 |
Поиск расхода теплоносителя в интервале 0,1< vT <3,0 осуществляется с помощью итерационной процедуры в моделирующем алгоритме.
Исследования по влиянию начальной температуры реакционного потока на степень превращения выполнить при 296 К< Т <306 К. По полученным данным построить графики в координатах СА, Т = f(![]() ) при одном значении Т0 и XA=f ( vT, T0).
) при одном значении Т0 и XA=f ( vT, T0).
5.4 Контрольные вопросы
1. Принцип составления уравнения теплового баланса адиабатического реактора.
2. В каких случаях применяются адиабатические реакторы для проведения химических процессов, в каких политропические?

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



