ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
Государственное образовательное учреждение
высшего профессионального образования
«Алтайский государственный технический университет
имени »
Бийский технологический институт (филиал)
, ,
ОБЩАЯ ХИМИЧЕСКАЯ ТЕХНОЛОГИЯ
Методические рекомендации по выполнению лабораторных работ
для студентов специальностей 240901
очной и очно-заочной форм обучения
Бийск 2007
УДК 66.01
Багров, химическая технология: методические рекомендации по выполнению лабораторных работ для студентов специальностей 240901 очной и очно-заочной форм обучения / , , .
Алт. гос. техн. ун-т, БТИ. – Бийск:
Изд-во Алт. гос. техн. ун-та, 2007. – 59 с.
Методические рекомендации содержат указания к выполнению лабораторных работ с обработкой данных на ЭВМ, краткие теоретические сведения по отдельным темам курса, индивидуальные задания и пакет программ для выполнения расчетов.
Рассмотрены и одобрены на заседании кафедры
«Процессы и аппараты химической технологии».
Протокол № 2 от 01.01.2001 г.
Рецензент: доцент, к. т.н. (БПГУ, Бийск)
© , , 2007
© БТИ АлтГТУ, 2007
СОДЕРЖАНИЕ
ВВЕДЕНИЕ…………………………………………………………. | 5 |
ЛАБОРАТОРНАЯ РАБОТА № 1. ИССЛЕДОВАНИЕ ПРОЦЕССА ОКИСЛЕНИЯ СЕРНИСТОГО АНГИДРИДА НА ВАНАДИЕВОМ КАТАЛИЗАТОРЕ В ПРОТОЧНОМ ТРУБЧАТОМ РЕАКТОРЕ…………………………………………. | 6 |
1.1 Цель работы……………………………………………………… | 6 |
1.2 Краткие теоретические сведения……………………………… 1.3 Математическое описание процесса………………………….. 1.4 Алгоритм решения……………………………………………… | 6 8 9 |
1.5 Задание………………………………………………………….. | 9 |
1.6 Контрольные вопросы …………………………………………. | 11 |
ЛАБОРАТОРНАЯ РАБОТА № 2. ИССЛЕДОВАНИЕ ПРОЦЕССА ВОССТАНОВЛЕНИЯ ДВУОКИСИ УГЛЕРОДА УГЛЕМ............................................................................................... | 12 |
2.1 Цель работы……………………………………………………… | 12 |
2.2 Краткие теоретические сведения………………………………. | 12 |
2.3 Описание кинетики процесса…………………………………… | 13 |
2.4 Задание…………………………………………………………… | 15 |
2.5 Контрольные вопросы………………………………………….. | 16 |
ЛАБОРАТОРНАЯ РАБОТА № 3. СРАВНЕНИЕ | |
ЭФФЕКТИВНОСТИ РАБОТЫ ИЗОТЕРМИЧЕСКИХ | |
РЕАКТОРОВ…………………………………………………………. | 17 |
3.1 Цель работы……………………………………………………… | 17 |
3.2 Краткие теоретические сведения……………………………….. | 17 |
3.3 Математическое описание изотермических реакторов……….. | 18 |
3.4 Задание…………………………………………………………… | 20 |
3.5 Контрольные вопросы…………………………………………… | 21 |
Лабораторная работа № 4. ИССЛЕДОВАНИЕ | |
ВЛИЯНИЯ УСЛОВИЙ ПРОВЕДЕНИЯ ГАЗОФАЗНОЙ | |
РЕАКЦИИ НА ОБЪЕМ РЕАКТОРА……………………………….. | 22 |
4.1 Цель работы……………………………………………………… | 22 |
4.2 Краткие теоретические сведения………………………………. | 22 |
4.3 Математическое описание кинетики процесса………………… | 24 |
4.4 Задание…………………………………………………………… | 25 |
4.5 Контрольные вопросы…………………………………………… | 26 |
ЛАБОРАТОРНАЯ РАБОТА № 5. РАСЧЕТ НЕИЗОТЕРМИЧЕСКИХ РЕАКТОРОВ……………………………. | 27 |
5.1 Цель работы……………………………………………………… | 27 |
5.2 Краткие теоретические сведения……………………………….. | 27 |
5.3 Задание…………………………………………………………… | 29 |
5.4 Контрольные вопросы ………………………………………….. 30
ЛАБОРАТОРНАЯ РАБОТА № 6. РЕАКТОРЫ С НЕИДЕАЛЬНОЙ СТРУКТУРОЙ ПОТОКА……………………. | 31 |
6.1 Цель работы……………………………………………………… | 31 |
6.2 Краткие теоретические сведения………………………………. | 31 |
6.3 Задание…………………………………………………………… | 32 |
6.4 Контрольные вопросы…………………………………………... | 35 |
Лабораторная работа № 7. Обогащение минерального сырья. Флотация………………………… | 36 |
7.1 Цель работы……………………………………………………... | 36 |
7.2 Краткие теоретические сведения………………………………. | 36 |
7.3 Описание лабораторной установки……………………………. | 39 |
7.4 Методика проведения работы………………………………...... | 39 |
7.5 Обработка данных………………………………………………. | 40 |
7.6 Контрольные вопросы…………………………………………... | 40 |
Лабораторная работа № 8. Жесткость воды и ее | |
определение. Методы снижения жесткости воды………………………………………………………………… | 42 |
8.1 Цель работы……………………………………………………… | 42 |
8.2 Краткие теоретические сведения………………………………. | 42 |
8.3 Описание лабораторной установки……………………………. | 44 |
8.4 Определение жесткости воды………………………………….. | 45 |
8.5 Обработка данных………………………………………………. | 46 |
8.6 Контрольные вопросы………………………………………….. | 46 |
Литература………………………………………………………. | 47 |
ПРИЛОЖЕНИЯ А Пакет программ на алгоритмическом языке | |
Turbo Pascal к лабораторным работам……………………………... | 48 |
ВВЕДЕНИЕ
Одной из основных задач инженерного исследования химических процессов является установление закономерностей их протекания, необходимых для разработки и проектирования новых и анализа работы существующих технологий с целью их совершенствования.
Закономерности химических процессов могут быть установлены экспериментально либо расчетным путем. И в том, и в другом случае определяется влияние параметров процесса на его эффективность.
При обработке экспериментальных данных чрезвычайно важно получение количественных соотношений между параметрами процесса, т. е. математической модели процесса, включающей в себя уравнения кинетики, гидродинамики, распределение концентраций, температурных полей и т. д.
Подобная модель может быть использована для практических целей. Однако применение математических моделей химико-технологических процессов в большинстве случаев связано с использованием вычислительных машин.
В данном лабораторном практикуме по курсу общей химической технологии используются персональные компьютеры (ПК). В каждой лабораторной работе формулируется ее цель, приводится математическое описание процесса, метод решения и задания, предлагаемые студентам для выполнения.
Использование ПК в расчетных занятиях по курсу ОХТ расширяет класс решаемых задач, позволяя дать оперативный ответ на вопрос о том, что произойдет с реактором или процессом в целом при тех или других изменениях параметров.
ЛАБОРАТОРНАЯ РАБОТА №1.
ИССЛЕДОВАНИЕ ПРОЦЕССА ОКИСЛЕНИЯ
СЕРНИСТОГО АНГИДРИДА НА ВАНАДИЕВОМ
КАТАЛИЗАТОРЕ В ПРОТОЧНОМ ТРУБЧАТОМ
РЕАКТОРЕ (4 часа)
1.1 Цель работы
Целью настоящей работы является анализ кинетических закономерностей процесса окисления сернистого ангидрида для установления технологических параметров его осуществления в промышленных реакторах.
1.2 Краткие теоретические сведения
Получение серной кислоты из колчедана и серы контактным способом по открытой (нециклической) схеме можно разделить на четыре крупные стадии (рисунки 1.1, 1.2):
- получение обжигового газа, содержащего диоксид серы;
- подготовку обжигового газа к контактному окислению;
- каталитическое окисление диоксида серы;
- абсорбцию триоксида серы.
При различном технологическом оформлении некоторые детали этих стадий, особенно второй, будут отличаться, однако принципиальный подход к их осуществлению и выбору технологического решения зависит от тех задач, которые решаются на рассматриваемом этапе, и в разных конкретных процессах получения серной кислоты будет одинаковым.
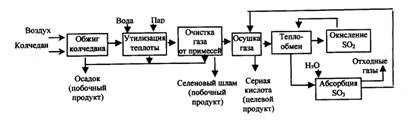
Рисунок 1.1 – Функциональная схема производства серной
кислоты методом одинарного контактирования
|
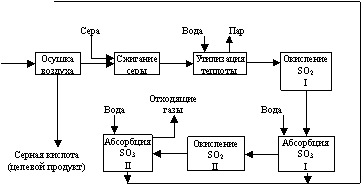

Рисунок 1.2 – Функциональная схема производства серной
кислоты из серы методом двойного контактирования
Процесс окисления сернистого ангидрида на ванадиевой контактной массе – важнейшая составная часть промышленного способа получения серной кислоты. Суть его состоит в осуществлении реакции SO2 + 1/2 О2 ![]() SO3.
SO3.
Это гетерогенно-каталитический, экзотермический, обратимый процесс, протекающий с уменьшением объема, без побочных реакций. Скорость реакции зависит от степени приближения к равновесию и, как функция температуры, проходит через максимум (с ростом температуры растет константа скорости прямой реакции и уменьшаются константа равновесия и равновесная степень превращения). Скорость реакции повышается с ростом концентрации кислорода, поэтому процесс в промышленности проводят при избытке кислорода.
Обратимые экзотермические реакции необходимо проводить в соответствии с линией оптимальных температур (ЛОТ), т. е. понижая температуру в контактном аппарате по мере роста степени превращения реагентов.
Чаще всего в промышленности используют полочные контактные аппараты с наружным теплообменом. Схема теплообмена предполагает максимальное использование тепла реакции для подогрева исходного газа и одновременное охлаждение газа между полками.
1.3 Математическое описание процесса
Кинетическое уравнение описывает скорость изменения концентрации реагентов по мере протекания реакции окисления сернистого ангидрида. Оно позволяет определять необходимые для расчета реактора технологические параметры.
Кинетика данного процесса с достаточной степенью точности описывается уравнением Иванова-Борескова [8]:
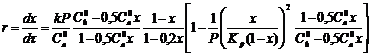 , (1.1)
, (1.1)
где r – скорость реакции, с-1;
![]() , – начальные концентрации SO2 и О2 соответственно доли;
, – начальные концентрации SO2 и О2 соответственно доли;
Р – давление, атм.;
х – степень превращения, доли;
Кр – константа равновесия реакции, атм.-0,5;
k – константа скорости, с-1атм.-0,5.
В случае, когда исходная газовая смесь состоит из SO2 и воздуха, величина находится по формуле:
![]() = 0,21(1-
= 0,21(1-
Значения Кр рассчитываются по уравнению:
. (1.3)
Величины констант скоростей для ванадиевого катализатора с размером гранул от 2 до 3 мм рассчитываются в зависимости от температуры по следующим формулам:
![]() при Т<673К; (1.4)
при Т<673К; (1.4)
![]() при 673 К < Т< 806 К; (1.5)
при 673 К < Т< 806 К; (1.5)
![]() = 1,361 при Т>806 К. (1.6)
= 1,361 при Т>806 К. (1.6)
Обозначив правую часть уравнения (1.1) за f(x), можем представить это уравнение для нахождения условного времени пребывания при заданных х:
![]() . (1.7)
. (1.7)
При расчете следует иметь в виду, что степень превращения не может превышать равновесную степень превращения для той температуры, при которой велся расчет. Значение хр может быть получено по соотношению:
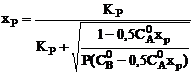 . (1.8)
. (1.8)
1.4 Алгоритм решения
Для определения условного времени пребывания при заданной степени превращения согласно уравнению (1.7) необходимо применить численные методы для вычисления определенного интеграла и метод решения трансцендентного уравнения (1.8). Программа решения задачи приведена в
1.5 Задание
1.5.1 Построение зависимостей x=F(![]() ) и r=F(x)
) и r=F(x)
Эти зависимости в случае изотермического процесса позволяют определить большинство технологических параметров и размеры реактора, необходимые для достижения заданной степени превращения. В соответствии с номером варианта принять заданное значение начальной концентрации сернистого ангидрида ![]()
![]() и при температуре Т=773 К выполнить расчеты на компьютере. Предел допустимой точности решения определяется по равновесной степени превращения Хр, которая также рассчитывается в программе на основании уравнения (1.8). По полученным данным строят график в координатах "х -
и при температуре Т=773 К выполнить расчеты на компьютере. Предел допустимой точности решения определяется по равновесной степени превращения Хр, которая также рассчитывается в программе на основании уравнения (1.8). По полученным данным строят график в координатах "х - ![]() " или "r -
" или "r - ![]() ". На графике "х -
". На графике "х - ![]() " проводят линию, параллельную оси
" проводят линию, параллельную оси ![]() , соответствующую значениям Хр. Решение справедливо до значения
, соответствующую значениям Хр. Решение справедливо до значения ![]() , соответствующего пересечению этой линии с кривой "х -
, соответствующего пересечению этой линии с кривой "х - ![]() ".
".
1.5.2 Построение линии оптимальных температур (ЛОТ)
Для определения оптимальных условий работы промышленного реактора используется линия оптимальных температур (ЛОТ). Она может быть получена с помощью графика "х - ![]() " или "r -
" или "r - ![]() ". Для серии температур в интервале 693 К < Т < 893 К получают кривые r=F(t) (рисунок 1.3) по результатам расчета с помощью программы № 1. Далее рассматривают сечения полученного семейства кривых линиями
". Для серии температур в интервале 693 К < Т < 893 К получают кривые r=F(t) (рисунок 1.3) по результатам расчета с помощью программы № 1. Далее рассматривают сечения полученного семейства кривых линиями ![]() =const. Исходя из этих сечений, строят график в координатах r=F(T) при
=const. Исходя из этих сечений, строят график в координатах r=F(T) при ![]() =const (рисунок 1.4). Линия, соединяющая максимумы полученных кривых, называется линией оптимальных температур.
=const (рисунок 1.4). Линия, соединяющая максимумы полученных кривых, называется линией оптимальных температур.
1.5.3 Построить профиль концентрации CА=f(l) по высоте трубчатого реактора при температуре Т=853 К и начальной концентрации![]() , заданной в таблице 1.1, согласно номеру варианта.
, заданной в таблице 1.1, согласно номеру варианта.
Таблица 1.1 – Варианты заданий
Номер варианта | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 0,05 | 0,07 | 0,1 | 0,15 | 0,2 | 0,25 | 0,3 |
При этом заданы:
объем аппарата Vr = 3,14 10-3 м3;
диаметр аппарата d = 0,l м;
длина аппарата L = 0,4 м;
объемный расход газа v = 7,84 10-3 м3/с.
При расчетах воспользоваться программой № 2.
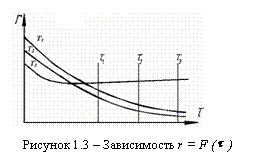

ростой необратимой.___Рисунок 1.4 – Построение ЛОТ по зависимости r = F (![]() )
)
1.6 Контрольные вопросы
1. Каковы основные стадии получения серной кислоты в промышленных условиях?
2. Особенности стадии окисления SO2 в SO3.
3. Какие аппараты и катализаторы применяются в промышленности для этой стадии?
4. Какими путями можно достичь повышения степени превращения SO2?
5. Что такое линия оптимальных температур?
6. Назовите способы осуществления оптимального температурного режима.
ЛАБОРАТОРНАЯ РАБОТА № 2.
ИССЛЕДОВАНИЕ ПРОЦЕССА ВОССТАНОВЛЕНИЯ
ДВУОКИСИ УГЛЕРОДА УГЛЕМ
2.1 Цель работы
Целью данной работы является определение области протекания гетерогенного процесса восстановления двуокиси углерода на угле.
2.2 Краткие теоретические сведения
Газификация производится для получения из малоценного твердого топлива генераторных газов, которые являются беззольным, транспортабельным топливом и сырьем для химических синтезов.
Различают:
- газификацию при помощи воздуха CО2 + C ![]() 2CO - Q;
2CO - Q;
- газификацию водяным паром С + H2O(пар)![]() CO + H2 – Q.
CO + H2 – Q.
Этот обратимый, эндотермический, гетерогенный процесс может быть осложнён как внешним, так и внутридиффузионным торможением. Для правильного выбора технологического режима этого процесса необходимо знать, какая стадия определяет скорость процесса –химическая кинетика или подвод реагентов к поверхности раздела фаз. При низких и средних температурах процесс газификации идет в кинетической области, т. е. лимитируется скоростью химических реакций. При увеличении температуры коэффициент скорости химической реакции возрастает в несколько раз быстрее, чем коэффициент диффузии, поэтому при определенной для данных условий температуре (примерно 900 оС) скорость реакции уравнивается со скоростью диффузии (а при более высоких температурах превышает последнюю). При температуре выше 1000 оС процесс протекает в диффузионной области.
Поэтому так же, как и в ряде других случаев взаимодействия газа с твердым материалом, скорость газификации зависит в основном от поверхности газификации, диффузии активного газового компонента (углекислого газа, водяного пара) к углероду топлива и от интенсивности перемешивания фаз.
Задача определения области протекания процесса может быть облегчена, если известны его кинетические закономерности. В этом случае результаты эксперимента необходимо сопоставить с теоретическими расчетами, проведенными по уравнению, описывающему химическую кинетику процесса.
2.3 Описание кинетики процесса
Уравнение химической кинетики восстановления двуокиси углерода, найденное на основании представлений о механизме реакции при отсутствии диффузионных торможений и с учетом неоднородности поверхности, имеет вид:
![]()
(2.1)
где т – число молей СО2, поступающих в реактор за время t;
![]() – удельная поверхность угля, м2/кг;
– удельная поверхность угля, м2/кг;
g – масса угля, кг;
t – время, ч;
![]() – степень превращения С02;
– степень превращения С02;
![]() , – парциальные давления СО2 и СО, атм.
, – парциальные давления СО2 и СО, атм.
Константы прямой и обратной скоростей реакции зависят от температуры процесса и определяются по уравнениям:
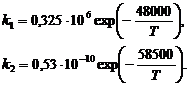
(2.2)
Уравнение кинетики дает возможность рассчитать скорость реакции восстановления двуокиси углерода при заданной температуре опыта в интервале парциальных давлений СО2:
|
Для численного решения уравнения (2.1) преобразуем его таким образом, чтобы в него была введена независимая переменная – время пребывания.
Подставим в уравнение (2.1) выражение для dg:
dg= dV, (2.3)
где ![]() – насыпная масса угля, кг/м3;
– насыпная масса угля, кг/м3;
dV – изменение объема массы g угля в процессе реакции, м3.
Объем реакционной массы связан с временем пребывания в реакционной зоне следующим соотношением:
dV=vo d![]() , (2.4)
, (2.4)
где v0 – объемный расход газа через слой угля, м3/ч.
Таким образом, изменение массы угля как функции времени выразится зависимостью:
dg=![]() vo d
vo d![]() . (2.5)
. (2.5)
После подстановки выражения (2.5) в уравнение (2.1) получим:
![]() (2.6)
(2.6)
![]() Учитывая, что величины m, t,
Учитывая, что величины m, t, ![]() ,
,![]() ,v0 постоянны для выбранных условий опыта, обозначим
,v0 постоянны для выбранных условий опыта, обозначим ![]() . Если в уравнении (2.6) выразить концентрации компонентов газовой смеси через степень превращения
. Если в уравнении (2.6) выразить концентрации компонентов газовой смеси через степень превращения
(2.7)
то получим:
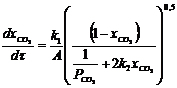 . (2.8)
. (2.8)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



