Материал: вода водоема.
Ход работы
100 мл исследуемой осветленной или предварительно разбавленной воды (чтобы в ней содержалось до 0,004 мг азота) помещают в колбу или стакан, приливают 5 мл реактива Грисса и перемешивают. Окраска появляется через 40 мин и сохраняется неизменной в течение 3 часов. Через 40 мин растворы фотометрируют в кюветах толщиной 5 см с зеленым светофильтром (X = 530 нм) по отношению к дистиллированной воде с добавлением реактива
Грисса.
Содержание нитритов находят по калибровочному графику или визуальным сравнением интенсивности окраски пробы и шкалы
стандартных растворов.
При очень малом содержании нитритов, когда окраска в исследуемой пробе не проявляется в течение 30 мин, пробу воды и стандарты следует подогревать в течение 10 мин до 70°С (в одинаковых условиях), охладить и фотометрировать с этими стандартами.
Построение калибровочного графика В ряд мерных колб вносят рабочий стандартный раствор в количестве 0,1; 0,2; 0,4; 0,8; 1,2; 1,6; 1,0; 1,5; 2,0 мл, что соответствует содержанию 0,2; 0,4; 0,8; 1,2; 1,6; 2; 3; 4 мкг азота нитритов. В колбу доливают дистиллированную воду до метки и прибавляют 5 мл 10%-ного раствора реактива Грисса, перемешивают и через 40 мин фотометрируют. Калибровочный график строят в координатах: оптическая плотность - содержание азота нитритов (мкг). Целесообразно строить два калибровочных графика, для содержания азота нитритов от 0 до 4 мкг и от 0 до 1,6 мкг.
Содержание азота нитритов (мг/л) рассчитывают но формуле:
![]()
где:
А - количество азота нитритов, найденное по калибровочному
графику (мкг);
V - объем пробы, взятой для анализа (мл).
Лабораторная работа № 9
Определение нитратного азота
Предельно допустимая концентрация нитратов в воде водоемов -
10 мг/л (по азоту).
Метод основан на реакции между нитратами и фенолдисуль-фокислотой с образованием нитропроизводных фенола, которые со щелочами образуют окрашенные в желтый цвет соединения.
Определению мешают хлориды в концентрациях более 10 мг/л, их влияние устраняется в ходе анализа добавлением сульфата серебра. Определению мешают цветность воды более 20-25°С; в этом случае к 150 мл исследуемой воды добавляют 3 мл суспензии гидроксида аммония, пробу тщательно перемешивают и после отстаивания в течение нескольких минут осадок отфильтровывают, выбрасывая первую порцию фильтра.
Чувствительность метода 0,1 мг/л азота нитратов.
Оборудование, реактивы, материалы
1) фотоколориметр; 2) водяная баня; 3) обратный холодильник; 4) фарфоровые чашки; 5) стеклянные палочки; 6) мерные колбы на 100 мл, 1000 мл; 7) пипетки на 1 мл, 5 мл с делениями и на 1 мл, 5 мл без делений; 8) колбы на 100 мл; 9) фенолдисульфокислота. 25 г кристаллического бесцветного фенола (если препарат окрашен, то его необходимо очистить перегонкой) растворяют в 150 мл серной кислоты пл. 1,84 г/ см3 и нагревают в течение 6 час на водяной кипящей бане в колбе с обратным холодильником. Раствор хранят в склянке из темного стекла с притертой пробкой; 10) сульфат серебра, раствор. 4,4 г Аg2SО4 растворяют в дистиллированной воде и доводят объем до 1 л в мерной колбе. 1 мл раствора эквивалентен приблизительно 1 мг хлор-иона. Раствор хранят в склянке из темного стекла с притертой пробкой; 11) гидроксид аммония, суспензия для коагуляции; 12) аммиак, 25 %-ный раствор; 13) стандартный раствор нитрата калия KNO3: 0,7216 г KNO3, высушенного при 105°С до постоянной массы, растворяют в дистиллированной воде в мерной колбе и доводят объем до 1 л. Для консервации прибавляют 1 мл хлороформа. В 1 мл раствора содержится 0,1 мг нитратного азота.
Материал: вода водоема.
Ход работы
Для анализа отбирают 100 мл (или менее) прозрачной воды или фильтрата, добавляют раствор Ag2SO4 в количестве, эквивалентном содержанию хлор-иона в пробе. Выпаривают в фарфоровой чашке на кипящей водяной бане досуха (осадок AgCI отфильтровывают в том случае, если содержание хлоридов превышает 15 мг в исследуемом объеме). После охлаждения сухого остатка добавляют в чашку 1 мл фенолдисульфокислоты и сразу же растирают стеклянной палочкой до полного смешения с сухим остатком. Добавляют 15-20 мл дистиллированной воды и через 10-15 мин - 5 мл концентрированного аммиака до максимального развития окраски. Раствор переносят в
мерную колбу на 100 мл, ополаскивают чашку небольшими порциями дистиллированной воды и сливают их в колбу, доводят до метки дистиллированной водой.
Оптическую плотность определяют на фотоколориметре с синим светофильтром (X, = 480 нм) в кюветах с толщиной 2 см по отношению к дистиллированной воде с добавлением всех реактивов.
Содержание азота нитратного определяют по калибровочному графику. Можно проводить визуальное определение, сравнивая интенсивность окраски пробы и шкалы стандартных растворов.
Построение калибровочного графика
0,2; 0,5; 1,0; 2,0 мл стандартного раствора выпаривают в фарфоровых чашках досуха и продолжают, как при анализе пробы.
Получают шкалу растворов с содержанием 0,02; 0,05; 0,10; 0,15; 0,20 мг азота нитратов. Фотометрируют и строят калибровочный график в координатах: оптическая плотность - содержание азота
нитратов (мг).
Содержание азота нитратов (мг/л) рассчитывают по формуле:
![]()
где:
А - количество азота нитратов, найденное по калибровочному
графику или по шкале стандартных растворов (мг);
V - объем пробы, взятой для анализа (мл).
Лабораторная работа № 10
Определение растворенного кислорода по Винклеру
Количество кислорода, растворенного в воде имеет большое значение для оценки состояния водоема. Его снижение указывает на резкое изменение биологических процессов в водоемах, а также на загрязнение водоемов веществами, биохимически интенсивно окисляющимися.
Концентрация растворенного кислорода в воде зависит, кроме того, от природных факторов - атмосферного давления, температуры воды, содержания растворенных солей. Концентрация кислорода в воде для питьевого и бытового использования должна быть не менее 4 мг/л в любой период года.
Принцип метода определения основан на использовании растворенного кислорода, содержащегося в определенном объеме воды, для окисления гидроксида марганца (II) в гидроксид марганца (III):
MnSO4 + 2NaOH = Мп(ОН)г + Na2SO4
4Мп(ОН)г + О2 + Н2О = 4Мп(ОН)3
Гидроксид марганца (III), в свою очередь, окисляет в кислой среде KI:
2Мп(ОН)3 + 3H2SO4 + 2KI = 2MnSO4 + K2SO4 + I2 + 6НгО
Iг + 2Na2S2O3 = 2NaI + Na2S4O6
Предел обнаружения растворенного кислорода по этому методу составляет 0,05 мг/л.
Оборудование, реактивы, материалы
1) склянки с притертой пробкой на 120 мл; 2) пипетки на 1 мл, 2 мл; 3) конические колбы на 250-300 мл; 4) бюретка для титрования; 5) мерные колбы на 50 мл, 500 мл; 6) сульфат или хлорид марганца (II) раствор. Растворяют 200 г MnSO4 • 2Н2О (или 240 г MnSO4 • 4НгО или 182 г MnSO4 • Н2О или 212, 5 г МпС1г • 4Н2О) в дистиллированной воде и доводят объем до 1/2 л. Фильтруют через бумажный фильтр. Разбавленный раствор в кислой среде при добавлении KI не должен выделять свободного йода; 7) щелочной раствор KI: а) растворяют 75г КI в 50 мл дистиллированной воды. При подкис - лении разбавленный раствор не должен выделять йод; б) растворяют 250 г NaOH или 350 г КОН в 250 мл дистиллированной прокипяченой воды (для удаления СО2). Оба раствора смешивают и доводят объем до 1/2 л; 8) серная кислота пл. 1,84 г/мл, разбавленный раствор 1:1; 9) тиосульфат натрия Nа2S2О3 • 5Н2О, 0,01 н; 10) крахмал, 1 %-ный раствор.
Материал: вода водоема.
Ход работы
Пробы воды отбирают в прокалиброванные стеклянные емкости с притертой пробкой вместимостью 120 мл. Склянки опускают на глубину 0,5 м, вынимают и сразу закрывают пробкой, чтобы под пробкой не образовались пузырьки воздуха. После этого сразу же на месте отбора фиксируют кислород, для чего в склянки при помощи пипетки на 1 мл, погружая ее до дна, вносят 1 мл раствора MnSO4 или МпС12. Другой такой пипеткой в верхнюю часть склянки вносят 1 мл щелочного раствора KI. Склянку осторожно закрывают пробкой, при этом из склянки выливают 2 мл исследуемой воды, т. е. столько, сколько налили реактивов. Затем жидкость перемешивают перевертыванием. В таком состоянии оставить пробу для транспортировки.
Перед титрованием (осадок должен хорошо осесть) приливают 2 мл H2SO4 (1:1). Раствор H2SO4 вносят пипеткой в нижнюю часть склянки, при этом часть жидкости переливается через крап. Закрывают склянку пробкой по тем же правилам и перемешиваю! до растворения осадка Мп(ОН)3.
После этого всю пробу переливают в коническую колбу для титрования вместимостью мл и быстро титруют 0,01 н раствором тиосульфата натрия при непрерывном помешивании до слабо-желтого цвета, после чего прибавляют I мл раствора крахмала и продолжают титровать до исчезновения синей окраски.
Расчет содержания растворенного кислорода в воде X (мг/л) производится по формуле:
![]()
где:
А - объем тиосульфата натрия, пошедшего на титрование, мл;
Н - нормальность Nа2S2О3 с учетом поправки;
V1 - объем пробы в склянке, мл (120 мл);
V2 - объем реактивов, добавленный до образования Мп(ОН)2, (2 мл);
1000 - пересчет на 1 л;
8 - эквивалентная масса кислорода, соответствующая 1 мл 1 н раствора Na2S2O3.
![]()
где:
К - поправочный коэффициент.
Лабораторная работа № 11
Определение запыленности воздуха
Пыль является аэрозолем. Аэрозоли представляют собой частицы вещества (твердые или жидкие) во взвешенном состоянии. Они распространены в приземном слое, тропосфере и стратосфере. Время жизни их различно: от нескольких часов до многих лет. В тропосфере различают 3 типа распределения частиц: фоновое, океаническое и континентальное. Частицы попадают в атмосферу с Земли в готовом виде, но значительная их часть образуется в результате химических реакций между газообразными, жидкими и твердыми веществами, включая пары воды.
Большое количество аэрозолей образуется в результате естественных природных процессов, но немалая их доля имеет антропогенное происхождение. По самым осторожным оценкам количество частиц ежегодно попадающих в воздушный бассейн Земли в результате деятельности человека - около 1 миллиарда тонн в год. Химический состав частиц различен, это диоксид кремния - песок, токсичные металлы, пестициды, углеводороды и др. Максимальный антропогенный вклад приходится на сульфаты. Аэрозоли в стратосфере менее разнообразны, чем в тропосфере. Основным твердым компонентом стратосферы является сульфат аммония.
Основной источник антропогенных аэрозолей - процесс горения. Энергетика и транспорт дают 2/3 общего количества антропогенных аэрозолей. Среди прочих источников аэрозолей - металлургические предприятия, производство строительных материалов, химические производства.
Аэрозоли способны изменять климат Земли, осаждаясь в альвеолах легких, они вызывают тяжелое заболевание у людей - пневмо-кониозы. Частицы аэрозоли могут нести на себе радиоактивность, вирусы, микробы, грибки, вызывать смоги и кислые дожди, то есть создавать угрозу не только живым существам, но и машинам, механизмам, приборам, качеству чистых материалов. Кроме того, пыль уносит с выбросами ценные материалы и может стать причиной разрушительных взрывов.
Для количественной характеристики запыленности воздуха в настоящее время используется преимущественно весовой метод (гравиметрия). Кроме того существует счетный метод. Весовые показатели определяют массу пыли в единице объема воздуха. Это прямые методы измерения запыленности. Существует также группа косвенных методов измерения запыленности. Под косвенными понимают методы измерения как с выделением пыли из воздуха, так и без выделения, основанные на определении ее массы путем использования различных физических явлений (интенсивности излучения, электрического поля, оптической плотности и т. д.).
Наиболее распространенным является гравиметрический метод определения весовой концентрации пыли. Через аналитический фильтр просасывают определенный объем запыленного воздуха. Массу всей витающей пыли без разделения на фракции рассчитывают по увеличению массы фильтра. Лучшими являются фильтры из ткани ФПП. Метод применяется для определения разовых и среднесуточных концентраций пыли в воздухе населенных пунктов и санитарно-защитных зон в диапазоне 0,04-10 мг/м3.
Оборудование, реактивы, материалы
1) улавливающее устройство: фильтродержатель, фильтр из ткани ФПП, аспиратор для отбора проб, стакан-насадка на фильтродержатель, металлический, разборный, конусовидный - для регулирования пропускаемого воздуха с учетом скорости ветра; 2) аналитические весы; 3) эксикатор; 4) пинцет с пластмассовыми наконечниками; 5) чашки стеклянные диаметром 10 см; 6) барометр; 7) психрометр; 8) анемометр.
Материал: воздух населенного пункта.
Работа рассчитана на 2 учебных часа.
Ход работы
Фильтр из ткани ФПП выдерживают в течение 40-60 мин в весовой комнате, взвешивают, помещают в пакет и доставляют на место отбора, где его вкладывают в фильтродержатель, который крепко завинчивают. Перед отбором проб проверяют герметичность фильтродержателя, для чего его входное отверстие закрывают пробкой и включают прибор: при герметичном присоединении расходомер воздуха показывает ноль.
Отбор проб проводят со скоростью 250-400 л/мин, чтобы навеска пыли на фильтре была не менее 4 мг. Отбор ведется не более 30 мин. После протягивания воздуха фильтр пинцетом извлекают из держателя, складывают вчетверо запыленной поверхностью внутрь и помещают в тот же пакет, из которого он был взят. В лаборатории фильтр выдерживают в течение 40-60 мин при комнатной температуре и доводят до постоянной массы. Если отбор проводился при относительной влажности, близкой к 100%, то фильтр помещают в стеклянной чашке в эксикатор с плавленым хлористым кальцием на 30-50 мин, а затем уже выдерживают при комнатной температуре 40-50 мин.
Обработка результатов
Концентрацию пыли С мг/м:) вычисляют по формуле:
C=M/V0,
где:
М - масса пыли на фильтре, равна разности масс запыленного и
чистого фильтра, мг;
V0 - объем аспирированного воздуха, приведенный к нормальным условиям, м3.
Под нормальными условиями подразумевается температура 0°С и атмосферное давление 1013 гПа (760 мм рт. ст.):
![]()
где:
Vt - объем аспирированного воздуха при температуре t и атмосферном давлении Р гПа, м3;
273 - коэффициент расширения газов;
1013 - нормальное давление, ГПа.
Лабораторная работа № 12
Определение диоксида серы
Соединения серы попадают в атмосферу как естественным путем, так и в результате антропогенной деятельности. В роли естественного источника выступает поверхность суши и океана. Соединения серы образуются в процессе разрушения органических веществ с помощью анаэробных микроорганизмов. Предполагается, что выделение серы биологическим путем не превышает 30-40 млн. т/год, что составляет 1/3 всего выделяемого количества серы. При извержении вулканов в атмосферу наряду с большим количеством диоксида серы попадают сероводород, сульфаты и элементарная сера (2%). Поступает сера в атмосферу и с поверхности океанов в виде сульфатов.
В результате антропогенной деятельности в атмосферу попадает значительное количество серы, главным образом в виде диоксида (59-69%).
Среди источников этого соединения на первом месте стоит сжигание угля (70% антропогенных выбросов). В процессе горения сера превращается в сернистый газ, а часть серы остается в золе в твердом состоянии. При сгорании нефтепродуктов сернистого газа образуется гораздо меньше. Основными источниками образования ЗОг наряду с сжиганием ископаемого топлива является металлургическая промышленность (переработка сульфидных руд свинца, меди и цинка), а также предприятия по производству серной кислоты и переработке нефти.
Диоксид серы - наиболее вредный газ из распространенных загрязнителей воздуха. Он вызывает заболевания дыхательных путей, ведет к возникновению хронического бронхита.
В атмосфере SO2 под действием кислорода окисляется до SO3, последний растворяется в капельках влаги с образованием серной кислоты. Это приводит к выпадению кислотных дождей. Если в атмосфере содержится аммиак, то идет образование сульфата аммония. В своем большинстве твердые аэрозольные частицы представляют собой сульфаты и туманообразную H^SO4. Содержание таких частиц в городах достигает 10 мг/м3. Предельно допустимая концентрация максимально разовая для SO2 - 0,5 мг/м3, среднесуточная - 0,05 мг/м3, класс опасности SO2 - 3.
Метод определения основан на окислении SO2 в процессе его улавливания из воздуха раствором перекиси водорода с последующим количественным определением осадка, образующегося при взаимодействии сульфат-иона с хлоридом бария. Влияние сульфатов и серной кислоты устраняют улавливанием их на фильтр АФА, который помещают перед поглотительным прибором в пластмассовом фильтродержателе. Метод рекомендуется для определения разовых концентраций. Чувствительность определения 5 мкг f в анализируемом объеме пробы. Диапазон измеряемых концент-> раций 0,08-1,5 мг/м3 при отборе пробы объемом 80 л.
Оборудование, реактивы, материалы
1) улавливающее устройство: аспиратор для отбора проб, поглотительный прибор Рихтера, пластмассовый фильтродержатель с фильтром АФА; 2) аналитические весы; 3) барометр; 4) термометр; 5) фотоколориметр; 6) глицерин (х. ч.) или этиленгликоль (х. ч.); 7) соляная кислота, конц. (пл. 1,19 х. ч.); 8) спирт этиловый, ректификат; 9) перекись водорода (Н2О2), х. ч.; 10) калий сернокислый, безводный (х. ч.), K2 SO4; 11) поглотительный раствор: 10 мл 30%-ной Hf>2 растворяют в 1 л воды, 0,3%-ный раствор НгО2 хранят в темной склянке не более недели; 12) барий хлористый, составной реактив: 5,85 г кристаллического хлористого бария (ВаСl2 • 2Н2О) растворяют в 50 мл воды. Затем приливают 150 мл этилового спирта и 150 мл глицерина или этиленгликоля. Величину рН смеси доводят до 2,5-2,8 конц. соляной кислотой HCI. Раствор оставляют на 48 часов и в случае появления осадка фильтруют через фильтр «синяя лента». Срок хранения 2 месяца; 13) исходный стандартный раствор. Безводный сернокислый калий мелко растирают и сушат при температуре 120-150 "С в течение 2 часов. Навеску 0,2720 г растворяют в 100 мл воды. Этот раствор соответствует содержанию 8Ог 1000 мкг/мл; 14) рабочий стандартный раствор. Готовят 10-кратным разбавлением исходного стандартного раствора поглотительным раствором. Полученный раствор соответствует содержанию SO2 100 мкг/мл.
Материал: воздух населенного пункта.
Работа рассчитана на 4 часа.
Ход работы
Для определения разовой концентрации исследуемый воздух со скоростью 4 л/мин протягивают в течение 20 мин через поглотительный прибор Рихтера, содержащий 6 мл поглотительного раствора. Для очистки воздуха от аэрозолей сульфатов и серной кислоты, мешающих определению, перед поглотительным прибором помещают пластмассовый фильтродержатель с фильтром АФА, присоединенный встык. Металлический фильтродержатель применять нельзя.
В лаборатории уровень раствора в поглотительном приборе доводят до 6 мл дистиллированной водой. Для анализа 5 мл раствора пробы переносят в пробирку и добавляют 1 мл раствора BaCl2.
Содержимое пробирки тщательно встряхивают и через 10 мин определяют оптическую плотность раствора в кювете толщиной 10 мм при длине волны 400 нм относительно нулевой пробы.
Время от добавления последнего реактива До измерения оптической плотности для всех проб должно быть одинаковым. Одновременно проводят измерение нулевой пробы, для чего 5 мл поглотительного раствора анализируют аналогично. Оптическая плотность нулевой пробы должна быть не более 0,01. Количество SO2 в пробах находят с помощью калибровочного графика. Анализ проб можно проводить и визуально.
Расчет концентрации С мг/м3 в атмосферном воздухе проводят по формуле:
![]()
где:
а - общий объем пробы в поглотительном приборе (6 мл);
b - объем пробы для анализа (5 мл);
т - количество SO2 в пробе, найденное по калибровочному графику, мкг;
V0 - объем протянутого воздуха, приведенный к нормальным условиям, л.
Построение калибровочного графика
В мерные колбы на 100 мл наливают 1, 2, 4, 6, 8, 12, 16, 20 мл рабочего стандартного раствора (100 мкг/мл). Разбавляют до метки поглотительным раствором. Концентрация SO2 в 5 мл стандартного раствора в мерных колбах составляет соответственно 5,10, 20, 30, 40, 60, 80, 100 мкг. Для приготовления шкалы стандартов отбирают в пробирки по 5 мл каждого стандарта и проводят операции по методике, описанной выше.
Лабораторная работа № 13
Определение диоксида азота
Азот образует смесь различных оксидов, но лишь NO и NO2 имеют значение как атмосферные загрязнители. Обычно суммарные концентрации NO и NO2 в атмосфере обозначаются как NOX.
Оксиды азота играют основную роль в образовании фотохимического «смога», влияют они и на разрушение озонового слоя, ведут также к образованию кислых дождей. Загрязнение атмосферы оксидами азота в целом сравнительно невелико. Но в районах с развитой химической промышленностью имеются локальные зоны повышенного содержания NO и NO2 в воздухе.
Монооксид азота NO - бесцветный газ, образующийся в больших количествах в цилиндрах двигателей внутреннего сгорания при взаимодействии Ог с N? В дальнейшем он окисляется кислородом до двуокиси азота NO2.
Диоксид азота представляет собой коричнево-бурый газ, ядовитый, с неприятным запахом. При растворении NO2 в воде образуется азотная кислота. В отличии от серной азотная кислота может долгое время оставаться в атмосфере в газообразном состоянии, так как она плохо конденсируется. Пары азотной кислоты поглощаются в атмосфере каплями облаков или частицами аэрозоля.
Образование оксидов азота в процессах сжигания связано с окислением атмосферного азота и, в меньшей степени, с окислением органических соединений азота, содержащихся в топливе. С повышением температуры количество оксидов азота значительно увеличивается. Основным источником выбросов NОХ, не связанных с сжиганием топлива, является производство азотной кислоты. Оксиды азота образуются в природе и как результат превращений органического азота. Энергетика и транспорт выбрасывают в атмосферу 36% из почти 60 млн. т ежегодных выбросов оксидов азота, т. е. в масштабах, сравнимых с естественным выделением соединений азота. Газообразный NО2 токсичен (2 класс опасности), является также сильным коррозионно-активным агентом. Предельно допустимая концентрация максимально разовая составляет 0,085 мг/м3, среднесуточная 0,04 мг/м3.
Метод определения содержания диоксида азота в воздухе с реактивом Грисса-Илосвая основан на взаимодействии двуокиси азота и сульфаниловой кислоты с образованием диазосоединения, которое, реагируя с a-нафтиламином, дает азокраситель. Последний окрашивает раствор от бледно-розового до красно-фиолетового цвета. По интенсивности окраски раствора определяют количество NO2. Озон в концентрации, не превышающей концентрацию NO2 в 3 раза, не мешает определению. Чувствительность определения ОД мкг в анализируемом объеме пробы. Диапазон измеряемых концентраций составляет 0,03-0,64 мг/м3 при отборе пробы воздуха 5 л.
Оборудование, реактивы, материалы 1) улавливающее устройство: аспиратор для отбора проб, поглотительный прибор Рихтера; 2) аналитические весы; 3) барометр; 4) термометр; 5) фотоколориметр; 6) калий йодистый, х. ч,; 7) натрий азотистокислый, х. ч.; 8) поглотительный раствор: 20 г KI растворяют в 250 мл воды. Полученный раствор должен быть бесцветным и храниться в банке из темного стекла. Срок хранения 2 недели; 9) натрий сернистокислый, х. ч., 0,06%-ный раствор. 0,03 г /Va^SOg растворяют в 50 мл воды. Раствор готовят перед анализом; 10) уксусная кислота, х. ч., 12%-ный раствор. 64 мл концентрированной кислоты помещают в мерную посуду на 500 мл и доводят до метки водой; 11) сульфаниловая кислота, ч. д. а., 5 г сульфаниловой кислоты растворяют в 150 мл 12%-ного раствора уксусной кислоты. Хранят раствор в плотно закрытой склянке из темного стекла; 12) а-нафтиламин, ч. д. а. 0,2 г а-нафтиламина растворяют в 20 мл воды при нагревании на водяной бане до образования лиловых капель на дне колбы. Раствор осторожно сливают в темную склянку, оставляя осадок в колбе, и приливают к раствору 150 мл 12%-ного раствора уксусной кислоты; 13) составной реактив (реактив Грисса-Илосвая). Перед анализом смешивают растворы а-нафтиламина и сульфаниловой кислоты в отношении 1:1; 14) исходный стандартный раствор: 2-3 г азотистокислого натрия растирают и сушат при температуре 50-60°С в течение 2 часов. Навеску NaNO2 0,1500 г растворяют в мерной колбе емкостью 100 мл. 1 мл полученного раствора соответствует 1000 мкг Л/О2; 15) раствор, 1 мл которого соответствует 10 мкг Л/О^ готовят разведением стандартного раствора поглотительным раствором в 100 раз; 16) рабочий стандартный раствор. Готовят 10-кратным разбавлением раствора, содержащего 10 мкг/мл NO2 поглотительным раствором. 1 мл рабочего раствора соответствует 1 мкг NO2. Исходный стандартный раствор сохраняется в течение 2 недель в склянке из темного стекла. Рабочий стандартный раствор готовят перед анализом. Материал: воздух населенного пункта. Работа рассчитана на 4 часа.
Ход работы
Для определения разовой концентрации NО2 исследуемый воздух протягивают через поглотитель Рихтера, наполненный 6 мл поглотительного раствора, со скоростью 0,25 л/мин в течение 20 мин. Во время отбора пробы следует избегать освещения поглотительного прибора солнечными лучами. Срок хранения отобранных проб не более 2 суток.
В лаборатории уровень раствора в поглотительном приборе доводят до метки 6 мл дистиллированной водой. Для анализа 5 мл раствора из каждой пробы переносят в пробирку и добавляют по 0,5 мл составного реактива.
Содержимое пробирок тщательно встряхивают и через 20 мин (непосредственно перед измерением) в пробирки приливают по 15 капель 0,06%-ного раствора Na^SO3 и еще раз встряхивают. Оптическую плотность измеряют в кюветах толщиной 10 мм при I длине волны 540 нм относительно воды. Время от добавления составного реактива до измерения оптической плотности всех проб должно быть одинаковым.
Количество NO2 в пробах находят по калибровочному графику. Одновременно проводят измерение оптической плотности нулевой пробы.
Расчет концентраций диоксида азота в воздухе проводят по формуле:
![]()
где:
а - общий объем пробы в поглотительном приборе (6 мл);
b - объем пробы для анализа (5 мл); т - количество NO2 в пробе, найденное по калибровочному графику, мкг;
V0 - объем протянутого воздуха, приведенный к нормальным
условиям, л.
Построение калибровочного графика
В мерные колбы на 50 мл наливают 1,2,4,6,8,10,20 мл рабочего стандартного раствора (1 мкг/мл). Разбавляют до метки поглотительным раствором. Концентрация ЫОг в 5 мл стандартного раствора в мерных колбах составляет соответственно 0,1; 0,2; 0,4; 0,6; 0,8; 1,0; 2,0 мкг.
Для приготовления шкалы стандартов отбирают в пробирки по 5 мл каждого стандарта и проводят операции по методике, описанной выше.
Лабораторная работа № 14
Определение аэрозоля серной кислоты и растворимых сульфатов
Максимальный антропогенный «вклад» в загрязнение атмосферы взвешенными частицами приходится на сульфаты и серную кислоту.
Метод определения аэрозоля серной кислоты и растворимых сульфатов основан на взаимодействии сульфатов с хлористым барием. Количество сульфатов определяется по интенсивности помутнения растворов. Определению мешают нерастворимые аэрозоли; их влияние устраняют фильтрованием.
ПДКП1аХ. р. для серной кислоты - 0,3 мг/м3, ПДКс. с. - 0,1 мг/м3.
Метод рекомендуется для определения разовых концентраций. Чувствительность определения 4 мкг в анализируемом объеме пробы. Диапазон измеряемых концентраций составляет 0,005-0,100 мг/м3 при отборе пробы воздуха объемом 2 м3.
Оборудование, реактивы, материалы
1) улавливающее устройство: аспиратор для отбора проб, фильтродержатель пластмассовый с фильтром АФА-ХП-18; 2) стеклянный фильтр с пористой пластиной; 3) фотоколориметр; 4) барометр; 5) термометр; 6) реактивы и материалы те же, что и для определения SO2.
Работа рассчитана на 3 часа.
Ход работы
Исследуемый воздух протягивают через фильтр АФА со скоростью 40 л/мин в течение 20 мин. После отбора фильтр переносят пинцетом в стаканчик на 25 мл, смачивают 0,2 мл этилового спирта и приливают 10 мл горячей воды. Содержимое стаканчика перемешивают стеклянной палочкой в течение 10 мин. Нерастворившуюся часть аэрозоля отфильтровывают через стеклянный фильтр с пористой пластинкой.
Для определения сульфат-ионов из пробы отбирают 4 мл фильтрата, добавляют 1 мл раствора ВаС12. Одновременно готовят нулевой раствор, для чего чистый фильтр обрабатывают аналогично пробе. Через 15 мин, предварительно встряхнув, определяют оптическую плотность раствора в кювете толщиной 10 мм при длине волны 400 нм относительно дистиллированной воды. Время от добавления раствора ВаС12 до измерения оптической плотности растворов для всех проб должно быть одинаковым.
Значение оптической плотности нулевого раствора должно быть не более 0,01. Если она превышает это значение, необходимо проверить чистоту посуды и измерительных кювет, качество приготовленных растворов. Количество аэрозоля серной кислоты и растворимых сульфатов в пробе определяют с помощью калибровочного графика по разности результатов измерений оптической плотности растворов пробы и нулевого раствора.
Построение калибровочного графика
В мерные колбы на 50 мл наливают 0,5; 1; 2; 3; 4 мл рабочего стандартного раствора (100 мкг/мл), 0,6; 0,8; 1 мл исходного стандартного раствора (1000 мкг/мл). Разбавляют до метки дистиллированной водой. Концентрация SO42- в 4 мл стандартного раствора составляет соответственно 4; 8; 16; 24; 32; 48; 64; 80 мкг.
Для приготовления шкалы стандартов используют по одному фильтру, предназначенному для отбора проб и проводят все операции согласно ходу анализа. Одновременно измеряют оптическую ~лотность нулевой пробы.
Расчет концентраций аэрозоля серной кислоты и растворимых сульфатов проводят по формуле:
где:
а - общий объем пробы (10 мл);
to - объем пробы для анализа (4 мл);
m - количество SO42- в пробе, найденное по калибровочному графику, мкг;
V0 - объем протянутого воздуха, приведенный к нормальным условиям.
Лабораторная работа № 15
Оценка качества воды малых рек и озер по биотическому индексу Вудивисса
О чистоте воды природного водоема можно судить по видовому разнообразию и обилию животного населения.
Чистые водоемы заселяют пресноводные моллюски, личинки веснянок, поденок, вислокрылок и ручейников. Они не выносят загрязнения и быстро исчезают из водоема. Как только в него попадают сточные воды.
Умеренно загрязненные водоемы заселяют водяные ослики. Бокоплавы, личинки мошек (мокрецов), двустворчатые моллюски-шаровики, битинии, лужанки, личинки стрекоз и пиявки.
Чрезмерно загрязненные водоемы заселяют малощетинковые кольчецы (трубочники), личинки комара-звонца (мотыли) и ильной мухи (крыска).
Для определения биотического индекса необходимо взять пробу воды из водоема с помощью водного сачка. Проба включает небольшое количество воды с илом и беспозвоночных животных, обнаруженных в сачке. Перед разбором проба промывается на сите, все обнаруженные беспозвоночные переносятся в чистую воду, налитую в чашки Петри или эмалированные ванночки. Содержимое чашек Петри тщательно разбирается и определяется по видам и группам видов беспозвоночных животных.
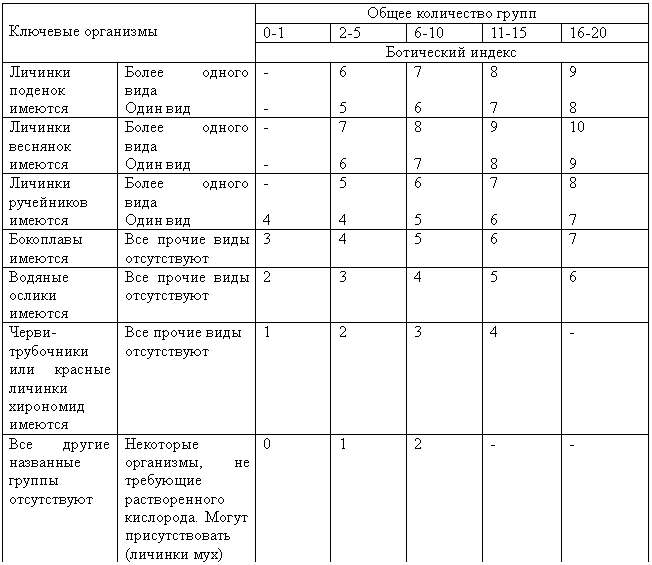
В исследуемой пробе определяют ключевые виды (табл. 2) и группы сопутствующих видов. Под группой сопутствующих видов в одних случаях понимают род, или семейство, или класс беспозвоночных, в других – каждый вид. Определив количество групп и число ключевых видов, находим в ( табл.1 ) вертикальный столбец и горизонтальную графу и на их пересечении и определяем биотический индекс.
Если водоём получает от 0 до 2 баллов — он сильно загрязнён, относится к полисапробной зоне, водное сообщество находится в сильно угнетённом состоянии. Оценка 3–5 баллов говорит о средней степени загрязнённости (альфа-мезосапробный), а 6–7 баллов — о незначительном загрязнении водоёма (бета-мезосапробный). Чистые (олигосапробные) реки обычно получают оценку 8–10 баллов, а особенно богатые водными обитателями участки могут быть оценены и более высокими значениями индекса.
Таблица 1
Определение биотического индекса пресноводных экосистем по донным беспозвоночным
Лабораторная работа № 16
Оценка состояния древостоя с использованием простейшей шкалы
Оценка состояния древостоя производится для установления вредного влияния антропогенных факторов. Оценка производится следующим образом.
1. Внутри ключевого участка закладывается пробная площадка 100 м2.
2. Определяются виды деревьев, растущих на пробной площадке.
3. С помощью шкалы визуальной оценки деревьев по внешним признакам (табл. 1) определяются баллы состояния отдельных деревьев каждого вида – b1, b2, b3 и т. д.
4. Вычисляется средний балл состояния для каждого вида деревьев но формуле:
![]() , где:
, где:
Кj - коэффициент состояния i-ro вида деревьев;
bi - баллы состояния отдельных деревьев;
Ni - общее число учтенных деревьев i-ro вида;
∑ - сумма.
5. Коэффициент состояния лесного древостоя в целом (К) определялся как среднее арифметическое средних баллов состояния различных деревьев на пробной площадке:
Таблица 1. Шкала визуальной оценки деревьев по внешним признакам
![]() , где
, где
Кi - коэффициент состояния i-ro вида;
R - число видов деревьев.
6. Состояние древостоя оценивается по следующим критериям:
К < 1,5 - здоровый древостой (I)
К = 1,6-2,5 - ослабленный древостой (II)
К = 2,6-3,5 - сильно ослабленный лес (III)
К = 3,6-4,5 - усыхающий лес (IV)
К > 4,6 - погибший лес (V)
Таблица 1. Шкала визуальной оценки деревьев по внешним признакам
Балл | Характеристика состояния |
1 | Здоровые деревья, без внешних признаков повреждения, величина прироста соответствует норме |
2 | Ослабленные деревья. Крона слабо ажурная, отдельные ветви усохли. Листья и хвоя часто с желтым оттенком. У хвойных деревьев на стволе сильное смолотечение и отмирание коры на отдельных участках |
3 | Сильно ослабленные деревья. Крона изрежена, со значительным усыханием ветвей, сухая вершина. Листья светло-зеленые, хвоя с бурым оттенком и держится 1-2 года. Листья мелкие, но бывают и увеличены. Прирост уменьшен или отсутствует. Смолотечение сильное. Значительные участки коры отмерли |
4 | Усыхающие деревья. Усыхание ветвей по всей кроне. Листья мелкие, недоразвитые, бледно-зеленые с желтым оттенком, отмечается ранний листопад. Хвоя повреждена на 60 % от общего количества. Прирост отсутствует. На стволах признаки заселения короедами, усачами, златками (буровая муха, отверстие на коре и древесине) |
5 | Сухие деревья. Крона сухая. Листьев нет, хвоя желтая или бурая, осыпается или осыпалась. Кора на стволах отслаивается или полностью опала. Стволы заселены ксилофагами (потребители древесины). |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



