Химия углеводов и биологически важных азотсодержащих соединений
ХИМИЯ
УГЛЕВОДОВ И БИОЛОГИЧЕСКИ
ВАЖНЫХ АЗОТСОДЕРЖАЩИХ СОЕДИНЕНИЙ
(контрольно-измерительные материалы)
Учебное пособие включает теоретический материал по химии углеводов и биологически важных азотсодержащих соединений (гетероциклических соединений, нуклеиновых кислот). В пособии представлены контрольно-измерительные материалы (КИМы) Единого государственного экзамена по химии, вступительных экзаменов, разного уровня олимпиад по вышеуказанным темам, примеры решения задач. Оно предназначено для школьников старших классов, абитуриентов и учителей, работающих в профильных химико-биологических классах общеобразовательных учреждений.
Введение
В развитии современной медицины и биологии важная роль отводится химии, изучающей биологически значимые вещества. Связь между биологией, медициной и химией устанавливалась на протяжении многовековой истории развития естествознания. Глубокое взаимопроникновение этих наук приводит к появлению новых научных направлений, изучающих молекулярную природу отдельных физиологических процессов, молекулярные основы патогенеза болезней, молекулярные аспекты фармакологии, биотехнологии и т. д. Поэтому профилирующим экзаменом для абитуриентов, поступающих в некоторые вузы, является экзамен по химии, требования к уровню знаний по которому возрастают с каждым годом.
Учебное пособие составлено с учетом Обязательного минимума содержания среднего (полного) общего образования по химии (Приказ Минобразования № 56 от 30.06.99 г.), обязательного минимума содержания основного общего образования по химии (приказ Минобразования № 000 от 19.05.98 г.), Федерального компонента гос. стандарта общего образования (приказ № 000 Минобразования РФ от 5 марта 2004 г.), типовой программы по химии для поступающих в вузы, программы для вступительных испытаний в медицинские вузы, утвержденной МЗ и МП РФ (Москва, 1995), примерных программ вступительных экзаменов в вузы РФ (Москва, 2000), материалов для подготовки к Единому государственному экзамену и включает в себя теоретический материал, необходимый будущим врачам и биологам для успешного освоения комплекса различных дисциплин, изучение которых базируется на знании основ биоорганической химии.
Учебное пособие предназначено для школьников старших классов, абитуриентов и учителей, работающих в профильных химико-биологических классах общеобразовательных учреждений.
4
УГЛЕВОДЫ
Углеводы - это природные органические вещества, имеющие общую формулу Cm(H2O)n (где m, n > 3), содержащие карбонильную группу и несколько гидроксильных групп. По способности к гидролизу углеводы подразделяются на моно-, ди-, олиго - (от греческого oliges – немного) и полисахариды. Ди-, олиго - и полисахариды при гидролизе расщепляются до моносахаридов.
Моносахариды
Моносахаридами, или простыми углеводами, называются углеводы, которые не подвергаются гидролизу. Моносахаридами являются рибоза, глюкоза, фруктоза, галактоза и другие. Они представляют собой сладкие на вкус, хорошо растворимые в воде белые кристаллические вещества.
Моносахариды, содержащие альдегидную группу называются альдозами, содержащие кетоногруппу – кетозами, например:

глюкоза фруктоза
(альдоза) (кетоза)
По числу атомов углерода в цепи моносахариды делятся на тетрозы (четыре атома углерода С4Н8О4), пентозы (пять атомов углерода С5Н10О5), гексозы (шесть атомов углерода С6Н12О6), гептозы (семь атомов углерода С7Н14О7) и т. д. В природе чаще всего встречаются пентозы и гексозы. Окончание –оза указывает на принадлежность соединения к классу углеводов, например:
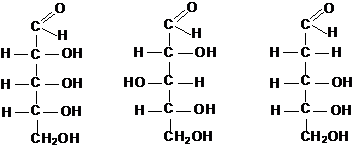
рибоза ксилоза дезоксирибоза
5

глюкоза галактоза фруктоза
Изображенные структуры получили название проекционных формул 3Фишера.
Для моносахаридов характерно явление цикло-цепной таутомерии. Таутомерия – это способность вещества существовать в виде нескольких структурных форм, которые называются таутомерами. Молекулы моносахаридов в водных растворах могут существовать не только в виде открытых форм, но и в виде циклических форм. Циклическая форма образуется при переходе атома водорода от гидроксильной группы при 4-ом или 5-ом углероде к кислороду карбонильной группы, например:
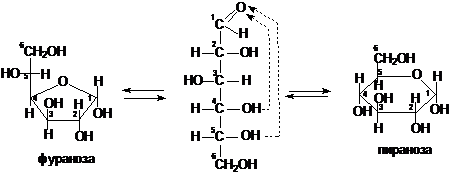
В результате образуются термодинамически более устойчивые пяти - или шестичленные таутомеры данного моносахарида. Пятичленные циклические таутомеры называются фуранозами, а шестичленные – пиранозами. Для изображения циклических форм моносахаридов используют формулы Хеуорса.
6
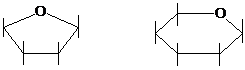
фуранозный цикл пиранозный цикл
В циклических формах моносахаридов нет карбонильной группы. Атом углерода С-1 в циклическом таутомере называют аномерным, а гидроксильную группу связанный с первым углеродным атомом – полуацетальной или гликозидной. В зависимости от расположения гликозидной гидроксильной группы в пространстве различают α- и β-аномеры. В α-аномерах гликозидный гидроксил расположен под плоскостью цикла, а в β-аномерах – над плоскостью цикла.
Ниже представлены цикло-цепная таутомерии некоторых моносахридов.
Цикло-цепная таутомерия глюкозы:

7
Цикло-цепная таутомерия фруктозы:

Цикло-цепная таутомерия рибозы:

8
Молекула моносахарида содержит несколько асимметрических (хиральных) атомов углерода, поэтому для моносахаридов характерно явление оптической изомерии. Например, в открытой форме молекулы глюкозы имеется 4 асимметричных атома углерода. Исходя из правила N = 2n, число стереоизомеров для нее равно 16, т. е. 8 пар оптических изомеров (энантиомеров). Энантиомеры отличают друг от друга, относя их к D - или L-ряду. Принадлежность к D - или L-ряду для моносахаридов определяется по пространственному расположению атома H и ОН-группы у последнего асимметрического атома углерода, сравнивая его с глицериновым альдегидом:
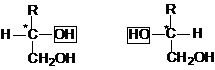
моносахарид моносахарид
D-ряда L-ряда
Углеводы D - и L-ряда являются зеркальными отражениями друг друга. Большинство природных моносахаридов принадлежит к D-ряду.
Получение моносахаридов
1. Глюкоза в растениях образуется в процессе фотосинтеза из углекислого газа и воды:
СО2 + 6Н2О hv® С6Н12О6 + 6О2 – 2920 кДж.
2. При гидролизе ди - и полисахаридов в кислой или щелочной среде (в зависимости от строения дисахарида) могут быть получены два одинаковых или два разных моносахарида. Например, в промышленности глюкозу получают гидролизом крахмала или целлюлозы:
(С6Н10О5)n + nН2О H+® nС6Н12О6
Фруктозу получают гидролизом сахарозы: С12Н22О11 + Н2О ® С6Н12О6 + С6Н12О6
глюкоза фруктоза
3. Неполное окисление многоатомных спиртов:
НОСН2-(НСОН)4-СН2ОН [O]® НОС-(НСОН)4-СН2ОН
Химические свойства моносахаридов
Для моносахаридов характерны реакции как многоатомных спиртов, так и карбонильных соединений.
Реакции со спиртамиДанные реакции протекают в кислой среде (катализатор) по гликозидному гидроксилу:
9
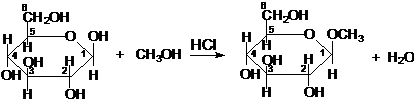
β-глюкопираноза β-метилглюкопиранозид
Образующийся в ходе реакции гликозид может подвергаться кислотному гидролизу с образованием исходных реагентов:
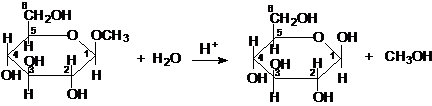
β-метилглюкопиранозид β-глюкопираноза
Реакции с алкилгалогенидамиЭти реакции протекают в щелочной среде по всем гидроксильным группам молекулы моносахарида:
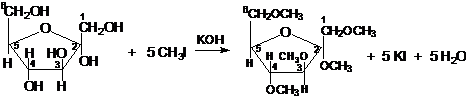
α-фруктофураноза α-метил-1,3,4,6-тетраметил-
фруктофуранозид
Реакции с фосфорной кислотойРеакция с фосфорной кислотой может протекать по гликозидному гидроксилу и по первичноспиртовым группам (-СН2ОН):
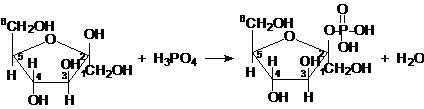
β-фруктофураноза 2-фосфат-β-фруктофуранозы
10
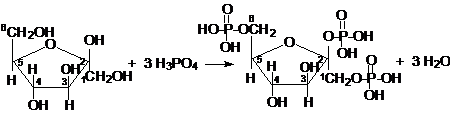
β-фруктофураноза 1,2,6-трифосфат-β-фруктофуранозы
Реакции с галогенангидридами карбоновых кислотТакие реакции протекают по всем гидроксильным группам моносахаридов:
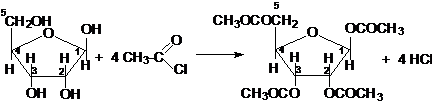
β-рибофураноза 1,2,3,5-тетраацетилрибофураноза
Реакции восстановленияРеакции восстановления протекают у моносахаридов в открытой форме, при этом альдегидная группа восстанавливается в спиртовую группу:

глюкоза сорбит
(альдегидо-спирт) (шестиатомный спирт)
Реакции с гидроксидом меди (II)В состав молекул моносахаридов входят несколько гидроксильных групп, поэтому без нагревания они реагируют с гидроксидом меди (II) как многоатомные спирты, образуя комплексное соединение ярко-синего цвета:
11

глюкоза комплекс меди (II)
Реакции окисления (на примере глюкозы)В зависимости от окислителя и условий реакции, окислению подвергаются как альдегидная группа моносахаридов, так и спиртовые гидроксильные группы.
а) окисление в щелочной среде
Окисление глюкозы в щелочной среде приводит к образованию солей глюконовой кислоты. Глюконовая кислота в щелочной среде неустойчива и подвергается деструкции углеродного скелета.
В качестве окислителей в реакцию вступают аммиачный раствор оксида серебра или гидроксид меди (II), реакции протекают при нагревании:

12

б) окисление в нейтральной среде
Мягкие окислители, такие как бромная вода, окисляют глюкозу до глюконовой кислоты (рибозу до рибоновой кислоты, а галактозу до галактоновой кислоты):

глюкоза глюконовая кислота
в) Окисление в кислой среде
Сильный окислитель – разбавленная азотная кислота окисляет моносахариды до двухосновных кислот. Глюкоза окисляется в глюкаровую (сахарную) кислоту, рибоза окисляется в рибаровую кислоту, галактоза окисляется в галактаровую кислоту:
13

глюкоза глюкаровая кислота
Реакции брожения глюкозыБрожение – процесс разложения глюкозы под действием микроорганизмов или ферментов. Различают следующие виды брожения глюкозы.
а) Спиртовое брожение глюкозы:
С6Н12О6 ![]() 2С2Н5ОН + 2 СО2 + 70 кДж
2С2Н5ОН + 2 СО2 + 70 кДж
б) молочнокислое брожение глюкозы:
С6Н12О6 ![]() 2 СН3- СН-СООН
2 СН3- СН-СООН
½
СН3
в) маслянокислое брожение гдюкозы:
С6Н12О6 ![]() СН3-СН2-СН2-СООН + 2СО2 + 2Н2
СН3-СН2-СН2-СООН + 2СО2 + 2Н2
г) лимоннокислое брожение глюкозы:
С6Н12О6 +3[O] 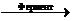 НООС-СН2-С(ОН)-СН2-СООН + 2Н2О
НООС-СН2-С(ОН)-СН2-СООН + 2Н2О
½
СООН
д) в живых организмах происходит окисление глюкозы по действием кислорода
воздуха по реакции:
С6Н12О6 + 6О2 ®СО2 + 6Н2О + 2920 кДж
При этом выделяется энергия, которая используется организмом. Поэтому глюкоза является основным источником энергии организма.
Фруктоза (кетоноспирт), являясь изомером глюкозы, вступает во все реакции многоатомных спиртов, но в отличие от глюкозы (альдегидоспирта), не обладает восстанавливающими свойствами: не реагирует с аммиачным раствором оксида серебра, не окисляется Cu(OH)2.
14
Дисахариды
Дисахариды состоят из остатков двух моносахаридов одинаковой или разной природы и имеют формулу С12Н22О11. К ним относят сахарозу, мальтозу, целлобиозу и лактозу. Все эти вещества представляют собой хорошо растворимые в воде бесцветные кристаллы сладкого вкуса.
Мальтоза состоит из двух остатков молекул глюкопиранозы, связанных между собой α-1,4-гликозидной связью (через 1-ый и 4-ый атомы углерода):
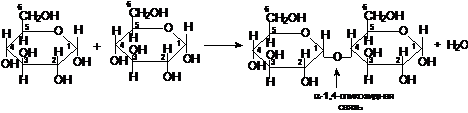 α-глюкопираноза α-глюкопираноза α-мальтоза
α-глюкопираноза α-глюкопираноза α-мальтоза
Целлобиоза состоит из двух остатков молекул глюкопиранозы, связанных между собой β-1,4-гликозидной связью (один остаток фиксировано находится в β -форме):
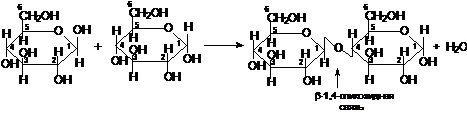 β-глюкопираноза α-глюкопираноза α-целлобиоза
β-глюкопираноза α-глюкопираноза α-целлобиоза
Лактоза образована из остатков β-галактопиранозы и a-глюкопиранозы, связанных между собой β-1,4-гликозидной связью:
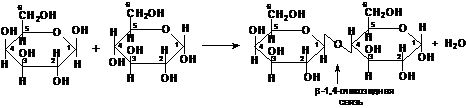
β-галактопираноза α-глюкопираноза α-лактоза
15
Сахароза образована из остатка α-глюкопиранозы и остатка β-фруктофуранозы, связанных между собой α-1,2-гликозидной связью:
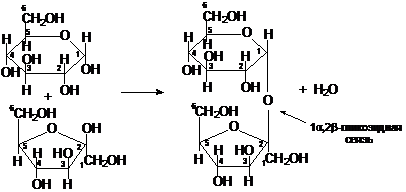
α-глюкопираноза + β-фруктофураноза сахароза
Получение дисахаридов
Наиболее распространенным дисахаридом является сахароза (тростниковый сахар). Его получают экстракцией из сахарной свеклы или сахарного тростника. Сахароза является важным источником углеводов в пище человека.
Лактоза (молочный сахар) содержится в молоке%) и получается из молочной сыворотки.
Мальтоза (солодовый сахар) содержится в проросшенных семенах хлебных злаков и образуется при неполном гидролизе крахмала под действием ферментов.
Целлобиоза получается при неполном гидролизе целлюлозы.
Химические свойства дисахаридов
Дисахариды подразделяются на два типа: восстанавливающие и невосстанавливающие. К восстанавливающим дисахаридам относят мальтозу, лактозу и целлобиозу. В молекулах мальтозы, лактозы, целлобиозы один полуацетальный (гликозидный) гидроксил остается свободным и поэтому дисахариды существуют в двух таутомерных формах, одна из которых – альдегидная. Эти дисахариды могут участвовать в реакции серебряного зеркала и восстанавливать свежеосажденный Cu (OH)2 до Cu2O, например:
C12H22O11 + Ag2O ![]() C12H22O12 + 2 Ag¯
C12H22O12 + 2 Ag¯
C12H22O11 + 2Cu(OH)2 ® C12H22O12 + Cu2O¯ + 2H2O
16
В молекуле сахарозы свободный гликозидный гидроксил отсутствует. В связи с этим сахароза не может раскрываться и переходить в альдегидную форму и поэтому она не обладает восстанавливающими свойствами. Поэтому сахароза невосстанавливающий дисахарид.
Дисахариды вступают во многие реакции, характерные для моносахаридов: реакции со спиртами, алкилгалогенидами, фосфорной кислотой, с галогенангидридами кислот.
Полисахариды
Углеводы, содержащие в молекуле более 10 остатков моносахаридов, называются полисахаридами. Общая формула полисахаридов (С6Н10О5)n. Молекулярная масса природных полисахаридов, важнейшими из которых являются крахмал и целлюлоза, может быть от нескольких тысяч до нескольких миллионов.
Крахмал – природный полимер, образованный остатками a-глюкозы. Крахмал представляет собой смесь полисахаридов амилопектина и амилозы. Амилоза – растворимый в воде линейный полисахарид, в котором остатки a-глюкозы связаны между собой α-1,4-гликозидной связью:
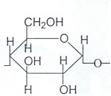
Линейная полимерная цепь амилозы свернута в спираль, внутри которой имеется тонкий (0,5 нм) канал, в который могут проникать некоторые молекулы. Например, при обработке крахмала йодом, туда проникают молекулы йода и окрашивают полимер в синий цвет. Эта реакция с йодом является качественной реакцией на крахмал.
Амилопектин – нерастворимый в воде полимер с разветвленным строением. В его молекуле остатки a-глюкозы связаны a-1,4- и a-1,6- гликозидными связями:
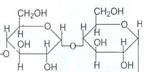
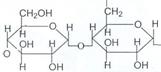
17
Химические свойства крахмала
Крахмал не растворяется в холодной воде. В горячей воде образует коллоидный раствор (клейстер). При нагревании в кислой среде крахмал гидролизуется с разрывом связей между остатками a-глюкозы. При этом образуется ряд промежуточных продуктов (декстрины, затем мальтоза). Конечным продуктом гидролиза крахмала является a-глюкоза:
(С6Н10О5)n + n H2O ® n С6Н12О6
Крахмал – ценный питательный продукт. Он входит в состав хлеба (в муке 75-80%), картофеля (25%), круп и является важнейшим источником углеводов в человеческом организме. Используется в производстве глюкозы, этанола, молочной кислоты, в пищевой промышленности, в медицине.
Другим распространенным в природе полисахаридом является целлюлоза (или клетчатка). Он представляет собой твердое, нерастворимое в воде волок-нистое вещество. Является основным веществом растительных клеток. Например, 50% древесины, 95-98% хлопка и льна состоят из целлюлозы. Состав его такой же, как у крахмала -(С6Н10О5)n. В отличие от крахмала молекулы целлюлозы имеют линейное строение, причем цепи располо-жены параллельно друг к другу и соединены между собой водородными связями, в так называемые волокна. Остатки b-глюкозы в целлюлозе соединены между собой b-1,4-гликозидной связью:
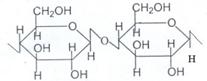
Химические свойства целлюлозы
При нагревании в кислой среде целлюлоза гидролизуется до b-глюкозы по схеме: целлюлоза®амилоид ®целлобиоза®b-глюкоза.
Целлюлоза растворяется а аммиачном растворе Cu(OH)2 (реактив Швейцера).
Для целлюлозы характерна способность к образованию сложных эфиров. Так, при взаимодействии с азотной или уксусной кислотами в присутствии концен-трированной серной кислоты образуются соответствующие сложные эфиры:
[C6H7O2(OH)3]n + 3nHNO3 ® [C6H7O2(ONO2)3]n + 3nH2O
[C6H7O2(OH)3]n + 3nCH3COOH ®[C6H7O2(OCOCH3)3]n + 3nH2O
Полный нитрат целлюлозы (пироксилин) – взрывчатое вещество, его используют для приготовления бездымного пороха. Из ацетата целлюлозы изготавливают ацетатное волокно, лаки и кинопленки.
18
Примеры решения задач
1. При полном гидролизе 78,84 г олигосахарида образовался только один продукт – глюкоза, при спиртовом брожении которой выделилось 29,57 г СО2. Установите число остатков глюкозы в молекуле олигосахарида (степень полимеризации) и рассчитайте массу воды, необходимой для гидролиза, если выход реакции брожения составил 70%.
Дано: m(олигосахарида) = 78,84 г m(СО2) = 29,97 г h = 70%
n(олигосахарида) - ? m(H2О) - ? | Решение: Запишем уравнение гидролиза олигосахарида и спиртового брожения глюкозы: (С6Н10О5)n + (n-1)H2O ® nС6Н12О6 С6Н12О6 ферменты® 2С2Н5ОН + 2 СО2 Определяем количество олигосахарида, углекислого газа и глюкозы: |
v((С6Н10О5)n) = 78,84/162 = 0,487 моль.
v(СО2) = 29,57/44 = 0,672 моль
v(С6Н12О6) = 0,5 v(СО2) = 0,336 моль; с учетом выхода реакции брожения v(С6Н12О6) = 0,48 моль. m(С6Н12О6) = 0,48. 180 = 86,4 г. Масса воды, необходимой для гидролиза рассчитывается как разность масс глюкозы и олигосахарида: m(H2О) = m(С6Н12О6) - m((С6Н10О5)n) = 86,4 – 78,84 = 7,56 г. v(Н2О) = 7,56/18 = 0,42 моль. Из соотношения количеств глюкозы и воды определяем степень полимеризации, т. е число остатков глюкозы:
![]() ,
,
откуда n = 8.
Ответ: n = 8; m(H2О) = 7,56 г.
2. Образец дисахарида массой 7,8 г подвергли гидролизу в кислой среде. К полученному раствору добавили избыток аммиачного раствора оксида серебра и получили осадок массой 10,8 г. Определите молекулярные формулы дисахарида и продуктов его гидролиза. Напишите возможные формулы продуктов гидролиза (в линейной форме).
Дано: m(дисахарида) = 7,8 г m(осадка) = 10,8 г
Формула дигосахарида - ? | Решение: Запишем уравнение гидролиза дисахарида: Cm+n(H2O)x+y-1 + H2O ® Cm(H2O)x + Cn(H2O)y Допустим, что количество дисахарида а моль. Тогда количества моносахаридов тоже будет по а моль. Они реагируя с аммиачным раствором оксида серебра |
образуют по 2а моль серебра:
Cm(H2O)x + Ag2O ® 2Ag¯
Cn(H2O)y + Ag2O®2Ag¯
4a = 10,8/108 = 0,1, т. е. а = 0,025 моль Тогда молярная масса дисахарида: М(Cm+n(H2O)x+y-1) = 7,8/ 0,025 = 312 г/моль. Подбирая, находим искомую формулу дисахарида: С11Н20О10. Уравнение гидролиза дисахарида:
19
С11Н20О10+ H2O ® C6(H2O)6 + C5(H2O)5
глюкоза рибоза
Ответ: С11Н20О10.
3. При нагревании 3 г кислородсодержащего органического вещества природ-ного происхождения с избытком свежеприготовленного гидроксида меди (II) получено 2,88 г осадка красного цвета. При сжигании образца этого вещества в атмосфере озона суммарное количество углекислого газа и воды в три раза превысило количество озона, необходимого для полного сгорания образца. Определите формулу исходного вещества и приведите структурные формулы его изомеров в линейной форме.
Дано: m(соединения) = 3 г m(осадка) = 2,88 г v(СО2+H2О)/v(О3)=3
Формула соединения - ? | Решение: со свежеприготовленным гидроксидом меди (II) с образованием осадка красного цвета могут реагировать соединения, содержащие альдегидную группу: CnHxOzCHO + 2Cu(OH)2 t® CnHxOzCOOH + Cu2O¯ + H2O Определяем количество осадка: v(Cu2O) = 2,88/144 = 0,02 моль. Из уравнения реакции видно, что количество органического соединения тоже 0,02 моль. Тогда его молярная масса составит: |
M(CnHxOzCHO)= 3/0,02 = 150 г/моль. Отсюда 12n + x +16z + (12 + 16 +1) = 150 или 12n + x +16z = 121.
Напишем уравнение сгорания соединения в озоне:
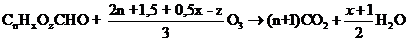
По условию задачи:
![]()
Решая уравнение, находим, что n = z. Далее, решая систему уравнений:
12n + x +16z = 121
n = z
находим 28n + х = 121.
Поскольку, n и х – целые числа, то анализ уравнения 28n + х = 121 показывает, что значения n, равные 1,2,3 бессмысленны (в этих случаях не соблюдается валентности углерода и водорода). При n =z = 4 х = 9. Таким образом, искомая формула С4Н9О4СНО – рибоза.
Ответ: С4Н9О4СНО – рибоза.
20
Задачи и упражнения для самостоятельной работы
по теме: УГЛЕВОДЫ
Часть А
К каждому заданию части А дано четыре ответа, из которых только один верный. В ответе укажите цифру, соответствующую выбранному Вами ответу.
А1.Общая формула углеводов:
1) (С6Н12О6)n 2) Сn(Н2О)m 3) СxНyОz 4) (СН2О)n
А2. На какие группы подразделяют углеводы по типу функциональных групп?
1) альдозы и кетозы 2) моносахариды и дисахариды
3) глюкозы и фруктозы 4) пентозы и гексозы
А3. Какое из веществ относится к олигосахаридам?
1) глюкоза 2) сахароза 3) крахмал 4) клетчатка
А4. В организме животных и человека глюкоза:
1) является источником энергии
2) выполняет запасающую функцию
3) участвует в процессе фотосинтеза
4) является катализатором
А3. В состав дезоксирибонуклеиновой кислоты (ДНК) входят остатки:
1) дезоксирибозы, фосфорной кислоты, азотистых оснований
2) аминокислоты, фосфорной кислоты, рибозы
3) фосфорной кислоты, рибозы, азотистого основания
4) дезоксирибозы, аминокислоты, азотистого основания
А4. Какой углевод в организме человека играет центральную роль в энергетическом обмене?
1) фруктоза 2) сахароза 3) крахмал 4) глюкоза
А5. Комплементарными основаниями в макромолекулах нуклеиновых кислот являются:
1) тимин и аденин, цитозин и гуанин
2) тимин и гуанин, аденин и цитозин
3) тимин и цитозин, аденин и гуанин
4) цитозин и аденин, гуанин и тимин
А6. Глюкозу от фруктозы можно отличить с помощью:
1) хлорида железа (III)
2) реакции «серебряного зеркала»
3) раскаленной медной проволоки
4) бромной воды
А7. Содержание какого вещества повышается в крови при заболевании сахарным
диабетом?
1) мальтозы 2) глюкозы 3) фруктозы 4) рибозы
А8. Картофель используется в промышленности для получения:
1) жиров 2) белка 3) целлюлозы 4) крахмала
21
А9. Высокомолекулярное соединение:
1) сахароза 2) клетчатка 3) жир 4) стеариновая кислота
А10. Укажите, растворы каких из ниже перечисленных веществ при нагревании
со свежеприготовленным Cu(OH)2 образуют осадок красного цвета:
1) глицерин
2) глюкоза
3) сахароза
4) уксусная кислота
А11. Укажите функциональные группы, входящие в состав молекул изомера
глюкозы, если известно, что данное вещество образуется при гидролизе
сахарозы:
1) карбонильная 2) карбоксильная 3) аминогруппа 4) метильная
А12. Полисахаридом является:
1) крахмал 2) сахароза 3) глюкоза 4) фруктоза
А13. Дисахаридом является углевод, название которого:
1) крахмал 2) сахароза 3) глюкоза 4) целлюлоза
А14. Гидролизу не подвергается углевод:
1) крахмал 2) целлюлоза 3) сахароза 4) фруктоза
А15. Побочным продуктом спиртового брожения глюкозы является:
1) H2O 2) CO2 3) H2 4) CH3COCH3
А20. Шестиатомный спирт (сорбит) образуется в результате восстановления:
1) гексановой кислоты
2) рибозы
3) бензилового спирта
4) глюкозы
А21. Углеводом, не усваивающимся в организме человека, является:
1) крахмал 2) целлюлоза 3) сахароза 4) фруктоза
А23. Глюкозу можно отнести к двум классам органических соединений:
1) спирт, кетон
2) спирт, альдегид
3) альдегид, кислота
4) амин, кислота
А24. Продуктом полного гидролиза крахмала является:
1) a-глюкоза 2) b-глюкоза 3) фруктоза 4) сахароза
А25. К моносахаридам относятся:
1) мальтоза, глюкоза, целлюлоза
2) глюкоза, сахароза, крахмал
3) фруктоза, мальтоза, целлюлоза
4) глюкоза, фруктоза, рибоза
А26. К полисахарам относятся:
1) мальтоза, глюкоза
2) крахмал, целлюлоза
3) галактоза, фруктоза
4) крахмал, сахароза
22
А27. К углеводам относятся:
1) глюкоза, крахмал, сахароза
2) все сладкие на вкус вещества
3) сахароза, глицин, угольная кислота
4) целлюлоза, гидролаза, фруктоза
А28. В результате гидролиза сахарозы образуются:
1) гидролаза и сахарин
2) уксусная кислота и этанол
3) галактоза и глицин
4) глюкоза и фруктоза
А29. В процессе фотосинтеза в растениях из углекислого газа и воды образуется:
1) глюкоза 2) сахароза 3) крахмал 4) угольная кислота
А30. В каком ряду соединений указаны только вещества, относящиеся к
углеводам?
1) целлюлоза, полипептид, галактоза
2) сахароза, крахмал, гидролаза
3) глюкоза, фруктоза, целлюлоза
4) рибоза, крахмал, глицерин
А31. Качественная реакция на обнаружение глюкозы:
1) обесцвечивание бромной воды
2) реакция «серебряного зеркала»
3) взаимодействие с металлическим натрием
4) взаимодействие с раствором хлорида железа (III)
А32. Продукт окисления глюкозы:
1) сорбит 2) глюконовая кислота 3) фруктоза 4) целлюлоза
А33. Глюкоза и фруктоза:
1) гомологи 2) полисахариды
3) структурные изомеры 4) геометрические изомеры
А35. a-глюкоза и b-глюкоза – это:
1) оптические изомеры 2) структурные изомеры
3) олигосахариды 4) геометрические изомеры
А36. Оптическая изомерия углеводов связана с существованием в их молекулах:
1) нескольких гидроксильных групп
2) асимметричных атомов углерода
3) карбонильной группы
4) хиральных (асимметричных) центров
А34. Образование полисахаридов из моносахаридов – это реакция:
1) полимеризации 2) поликонденсации
3) этерификации 4) гидролиза
А35. Основной углеводный компонент древесины:
1) крахмал 2) глюкоза 3) сахароза 4) целлюлоза
А36. Какой материал получают из целлюлозы?
1) поливинилацетат 2) лавсан (полиэтилентерефталат)
3) капрон (поликапроамид) 4) ацетатное волокно
23
А37. Какой процесс с участием углеводов приводит к выделению наибольшего количества энергии?
1) окисление кислородом воздуха 2) восстановление
3) брожение 4) поликонденсация
А38. Сколько групп - ОН содержит молекула глюкозы?
1 6
А39. Из 200 г 15%-ного раствора сахарозы выпарили 50 г воды. Массовая доля
сахарозы в оставшемся растворе:
1) 11,25% 2) 12%% 4) 25%
А40. Глюкозу получают:
1) гидролизом крахмала или целлюлозы
2) восстановлением глюконовой кислоты
3) гидролизом фруктозы
4) брожением этанола
А41. Сахароза, в отличие от глюкозы, не обладает восстановительными
свойствами. Причина этого:
1) в том, что сахароза – дисахарид
2) в отсутствии у сахарозы альдегидной группы
3) в наличии у сахарозы гидроксильных групп
4) в том, что глюкоза является многоатомным спиртом
А42. При молочнокислотном брожении глюкозы массой 200 г получили 160 г молочной кислоты. Практический выход составил:
1) 80% 2) 50% 3) 70% 4) 90%
А43. При спиртовом брожении глюкозы выделилось 4,48 л газа (н. у.) и образовался этанол массой:
1) 8,5 г 2) 9,2 г 3) 10,2 г 4) 11,3 г.
А44. Гидролизу подвергается:
1) глюкоза 2) сахароза 3) фруктоза 4) рибоза
А45. Формула вещества, образующегося при восстановлении глюкозы:
1) С6Н12О7 2) С6Н10О5 3) С6Н12О6 4) С6Н14О6
Часть В
В заданиях части ответом является набор букв или число
В заданиях на соответствия ответ дать в виде таблицы с указанием букв, соответствующих заданию.
В1. Установите соответствие между веществами и их физическими свойствами.
Вещество Физическое свойство
1) хлорид натрия А) низкая температура кипения
2) кислород Б) электропроводность в растворе
3) графит В) электропроводность
4) глюкоза Г) неэлектропроводность в растворе
1 | 2 | 3 | 4 |
24
В2. Голубой осадок гидроксида меди (II) в избытке щелочи при нагревании становится оранжевым при взаимодействии с:
А) глюкозой
Б) фруктозой
В) сахарозой
Г) ацетальдегидом
Д) ацетоном
Е) формальдегидом
(Ответ запишите в виде букв в алфавитном порядке без запятой)-----
В3. Среди перечисленных веществ укажите те, которые можно получить брожением глюкозы:
А) фруктоза
Б) CH3OH
В) C2H5OH
Г) CН3СН(OН)СООН
Д) сахароза
Е) CO2
(Ответ запишите в виде букв в алфавитном порядке без запятой)
В4. Среди перечисленных укажите те, которые реагируют с глюкозой:
А) фруктоза
Б) CH3OH
В) Cu(OH)2
Г) H2O
Д) H2
Е) Ag(NH3)2OH
(Ответ запишите в виде букв в алфавитном порядке без запятой)
Часть С
Запишите полное решение. Ответ запишите четко и разборчиво
1. Приведите уравнения реакций, с помощью которых можно осуществить следующие превращения:
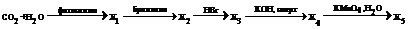
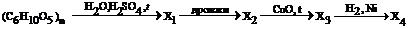
Крахмал ®сахароза®глюкоза®глюконовая кислота
Целлюлоза ®глюкоза®пентаацетат глюкозы
25
2. Полученное из глюкозы соединение состава С3Н6О3 в реакции с натрием образует соединение состава C3H4O3Na2, с карбонатом кальция C6H10O6Ca, с этанолом в присутствии серной кислоты С5Н10О3. Назовите это соединение и напишите уравнения реакций.
3. Вычислите массу 10%-ного раствора глюкозы, подвергшегося брожению, если известно, что при этом выделилось столько же газа, сколько его образуется при полном сгорании 35 мл этанола (плотность 0,8 г/мл).
4. Массовая доля крахмала в картофеле составляет 20%. Какую массу глюкозы можно получить из 2 т картофеля, если выход продукта составляет 80% от теоретического.
5. Определите массу сахарозы, если при гидролизе ее получилось 270 г смеси глюкозы и фруктозы.
6. Соединение «А» - белый нерастворимый в воде порошок, набухающий в горячей воде с образованием клейстера. Конечным продуктом гидролиза является вещество «В», которое под воздействием фермента молочнокислых бактерий образует соединение «С» с двойственной химической функцией, накапливающееся при скисании молока. Приведите формулы веществ «А», «В» и «С» и уравнения реакций.
7. Соединение «А» - твердое волокнистое вещество, не растворяющееся в воде. Под действием азотной кислоты в присутствии концентрированной серной кислоты «А» переходит в сложный эфир «В», а под действием уксусного ангидрида – в сложный эфир «С». Приведите формулы веществ «А», «В» и «С» и уравнения реакций.
8. Какие из перечисленных ниже веществ могут попарно вступать в реакции: сахароза, муравьиная кислота, вода, гидроксид меди (II). Напишите уравнения реакций с указанием условий их протекания.
9. Определите строение кислородсодержащего органического соединения, 18 г которого могут прореагировать с 23,2 г аммиачного раствора оксида серебра, а объем кислорода, необходимый для сжигания такого же количества этого вещества, равен объему образующегося при его сгорании углекислого газа.
10. Смесь ацетальдегида и глюкозы, массой 2,68 г, растворили в воде и к нему добавили аммиачный раствор оксида серебра, приготовленный из 50,218 г 34%-ного раствора нитрата серебра. Выпавший при легком нагревании осадок отфильтровали, фильтрат нейтрализовали азотной кислотой. При этом выпало 5,74 г осадка. Рассчитайте массовые доли веществ в исходной смеси.
11. При окислении некоторого кислородсодержащего органического вещества массой 1,8 г аммиачным раствором оксида серебра (I) получили серебро массой 5,4 г. Какое органическое вещество подвергнуто окислению?
12. При полном гидролизе 49,5 г олигосахарида образовался только один продукт – глюкоза, при спиртовом брожении которой получено 22,08 г этанола. Установите число остатков глюкозы в молекуле олигосахарида (степень полимерии-зации) и рассчитайте массу воды, необходимой для гидролиза, если выход реакции брожения составил 80%.
26
13. При полном гидролизе 105,12 г олигосахарида образовался только один продукт – глюкоза, при спиртовом брожении которой выделилось 42,24 г СО2. Установите число остатков глюкозы в молекуле олигосахарида (степень полимеризации) и рассчитайте массу воды, необходимой для гидролиза, если выход реакции брожения составил 75%.
14. При полном гидролизе 57,6 г олигосахарида образовался только один продукт – глюкоза, при спиртовом брожении которой получено 19,32 г этанола. Установите число остатков глюкозы в молекуле олигосахарида (степень полимеризации) и рассчитайте массу воды, необходимой для гидролиза, если выход реакции брожения составил 60%.
15. Образец дисахарида массой 10,26 г подвергли гидролизу в кислой среде. К полученному раствору добавили избыток аммиачного раствора оксида серебра и получили осадок массой 6,48 г. Определите молекулярные формулы дисахарида и продуктов его гидролиза. Напишите возможные формулы продуктов гидролиза (в линейной форме).
16. Образец дисахарида массой 4,68 г подвергли гидролизу в кислой среде. К полученному раствору добавили избыток аммиачного раствора оксида серебра и получили осадок массой 3,24 г. Определите молекулярные формулы дисахарида и продуктов его гидролиза. Напишите возможные формулы продуктов гидролиза (в линейной форме).
17. Образец дисахарида массой 10,92 г подвергли гидролизу в кислой среде. К полученному раствору добавили избыток аммиачного раствора оксида серебра и получили осадок массой 15,12 г. Определите молекулярные формулы дисахарида и продуктов его гидролиза. Напишите возможные формулы продуктов гидролиза (в линейной форме).
18. При нагревании 6 г кислородсодержащего органического вещества природ-ного происхождения с избытком аммиачного раствора оксида серебра получено 10,8 г осадка. При сжигании образца этого вещества в кислороде суммарное количество углекислого газа и воды в 2 раза превысило количество кислорода, необходимого для полного сгорания образца. Определите формулу исходного вещества и приведите структурные формулы его изомеров в линейной форме.
19. При нагревании 4,5 г кислородсодержащего органического вещества природ-ного происхождения с избытком свежеприготовленного гидроксида меди (II) получено 7,2 г осадка красного цвета. При сжигании образца этого вещества в кислороде суммарное количество углекислого газа и воды в 2 раза превысило количество кислорода, необходимого для полного сгорания образца. Определите формулу исходного вещества и приведите структурные формулы его изоме-ров в линейной форме.
20. При нагревании 6,7 г кислородсодержащего органического вещества природ-ного происхождения с избытком аммиачного раствора оксида серебра получено 10,8 г осадка. Для сжигания образца этого вещества потребовалось кислород объемом, в 1,1 раза превышающий объем углекислого газа, выделяющегося при сгорания образца. Определите формулу исходного
27
вещества и приведите структурные формулы его изомеров в линейной форме.
21. Сколько (в г) глюкозы было подвергнуто спиртовому брожению, если при этом выделилось столько же газа, сколько его образуется при полном сгорании 16 г метанола?
БИОЛОГИЧЕСКИ ВАЖНЫЕ АЗОТСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
Гетероциклические соединения – это органические соединения, в циклах которых, кроме атомов углерода, содержатся атомы азота, серы, кислорода и других элементов, называемые гетероатомами. Размер цикла может быть различным. По числу гетероатомов гетероциклические соединения делятся на одноатомные (пиррол, фуран, тиофен, пиридин) и двухатомные (пиримидин, имидазол, пиразол). В них атомы углерода и азота находятся в sр2-гибридном состоянии. Наибольшее распространение в природе имеют пяти - и шестичленные циклы. Их можно получить из каменноугольной смолы или синтетическим путем.
Гетероциклические соединения с одним гетероатомом
Пятичленные гетероциклы
Представителями пятичленных гетероциклов с одним гетероатомом являются пиррол, фуран и тиофен:
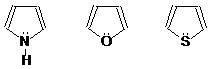
пиррол фуран тиофен
Эти соединения обладают ароматическим характером, т. к. в них образуется сопряженная система из 4 π-электронов атома углерода и 2 р-электронов гетероатома (рπ-сопряжение).
Наиболее важное биологическое значение имеют азотсодержащие гетероциклические соединения.
Эти циклы образуются наиболее легко и отличаются большой прочностью.
Химические свойства пиррола
Пиррол – бесцветная жидкость с характерным запахом, плохо растворимая в воде, быстро темнеющая на воздухе.
28
Реакции ароматического характераВ реакциях электрофильного замещения водород замещается в α-положении.
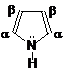
Так как пиррол является «ацидофобным» (боящийся кислот), т. е. в присутствии кислот полимеризуется, то в реакциях электрофильного замещения используют специфические реагенты, не содержащие протонов (Н+):
а) Реакция нитрования:
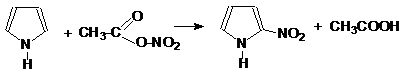
пиррол 2-нитропиррол
б) реакция сульфирования:

пиррол 2-сульфопиррол
в) реакция галогенирования:
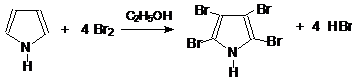
пиррол 2,3,4,5-тетрабромпиррол
Реакции присоединения (гидрирования):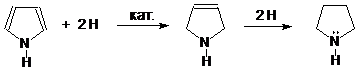
пиррол пирролин пирролидин
29
В ряду пиррол–пирролин–пирролидин основные свойства усиливаются.
Реакции со щелочными металламиПиррол обладает кислотными свойствами, т. к. неподеленная электронная пара атома азота участвует в образовании единой сопряженной системы. Например, он реагирует щелочными металлами:
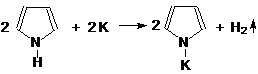
пиррол пиррол-калий
Шестичленные гетероциклы с одним гетероатомом
Важным представителем шестичленных гетероциклов с одним гетероатомом является пиридин (бесцветная жидкость, с характерным запахом):

В молекуле пиридина (как и в бензоле) имеется общее π-электронное облако из шести электронов, пять из которых предоставляют атомы углерода и один электрон дает атом азота. Но ароматические свойства пиридина выражены слабее, чем у бензола. Это связано с влиянием электроотрицательного атома азота.
Химические свойства пиридина
Пиридин является более слабым основанием, чем алифатические амины. С водой он смешивается в любых соотношениях. Водный его раствор окрашивает лакмус в синий цвет.
1. Реакции электрофильного замещения
Реакции электрофильного замещения в пиридине протекают преимущественно в β-положении.
а) Реакции нитрования:
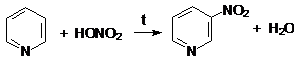
пиридин 3-нитропиридин
30
б) Реакции галогенирования:
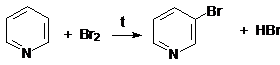
пиридин 3-бромпиридин
в) Реакции алкилирования
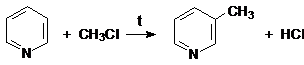
пиридин 3-метилпиридин
2. Реакции нуклеофильного замещения:
Пиридин вступает в реакции нуклеофильного замещения, которые протекают в α-положении, например:
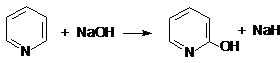
пиридин 2-оксипиридин
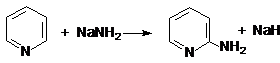
пиридин 2-аминопиридин
3. Пиридин проявляет основные свойства за счет азота аминогруппы

пиридин хлорид пиридиния
31
4. Реакции восстановления:
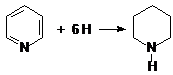
пиридин пиперидин
Пиперидин – циклический вторичный амин, более сильное основание, чем пиридин.
5. Реакции окисления:
Пиридин устойчив к окислению, но его гомологи ведут себя как гомологи бензола: они легко окисляются, например:
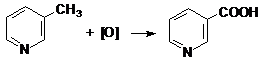
3-метилпиридин пиридинкарбоновая кислота
(никотиновая кислота)
Гетероциклические соединения с двумя гетероатомами
Пятичленные гетероциклы
Представителями пятичленных гетероциклов с двумя гетероатомами являются пиразол и имидазол:
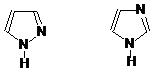
пиразол имидазол
Пиразол и имидазол представляют собой сопряженные системы. Вследствие влияния второго атома азота пиразол и имидазол более стабильны, чем пиррол.
32
Химические свойства
Реакции с кислотами и щелочными металлами
Имидазол и пиразол являются амфотерными соединениями – слабыми NH-кислотами и основаниями. Они реагируют с кислотами и щелочными металлами:

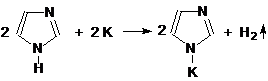
Реакции электрофильного замещения протекают в положении 4 или 5.
а) Реакции нитрования:
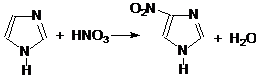
имидазол 4-нитроимидазол
б) Реакции галогенирования:
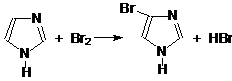
имидазол 4-бромимидазол
в) Реакции алкилирования:
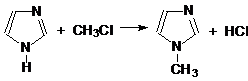
33
Шестичленные гетероциклы
Представителями шестичленных гетероциклов с двумя гетероатомами являются пиримидин, пиридазин и пиразин:
ИНСТИТУТ РАЗВИТИЯ ОБРАЗОВАНИЯ РЕСПУБЛИКИ ТАТАРСТАН
(кафедра методики преподавания естественнонаучных дисциплин)
ХИМИЯ
УГЛЕВОДОВ И БИОЛОГИЧЕСКИ
ВАЖНЫХ АЗОТСОДЕРЖАЩИХ СОЕДИНЕНИЙ
(Теория и контрольно-измерительные материалы)
Казань 2008
ББК 24.23
УДК 547.002
Печатаетося п решению Учебно-методического совета Института развития обраования Республики Татарстан
Составители:
, , , ,
Рецензенты:
доцент кафедры общей и органической химии КГМУ, к. х.н. ;
доцент кафедры общей химии КГАСУ, к. б.н.
Химия углеводов и биолгически важных азотсодержащих соединений (теория и контрольно-измерительные материалы)/, , , – Казань: ИРО РТ, КГМУ, 2007. – 43 с.
Учебное пособие включает теоретический материал по химии углеводов и биологически важных азотсодержащих соединений (гетероциклических соединений, нуклеиновых кислот). В пособии представлены контрольно-измерительные материалы (КИМы) Единого государственного экзамена по химии, вступительных экзаменов по вышеуказанным темам, примеры решения задач. Оно предназначено для школьников старших классов, абитуриентов и учителей.
© Казанский государственный медицинский университет, 2007
© Институт развития образования Республики Татарстан, 2007
Введение
В развитии современной медицины и биологии важная роль отводится химии, изучающей биологически значимые вещества. Связь между биологией, медициной и химией устанавливалась на протяжении многовековой истории развития естествознания. Глубокое взаимопроникновение этих наук приводит к появлению новых научных направлений, изучающих молекулярную природу отдельных физиологических процессов, молекулярные основы патогенеза болезней, молекулярные аспекты фармакологии, биотехнологии и т. д. Поэтому профилирующим экзаменом для абитуриентов, поступающих в некоторые вузы, является экзамен по химии, требования к уровню знаний по которому возрастают с каждым годом.
Учебное пособие составлено с учетом Обязательного минимума содержания среднего (полного) общего образования по химии (Приказ Минобразования № 56 от 30.06.99 г.), обязательного минимума содержания основного общего образования по химии (приказ Минобразования № 000 от 19.05.98 г.), Федерального компонента гос. стандарта общего образования (приказ № 000 Минобразования РФ от 5 марта 2004 г.), типовой программы по химии для поступающих в вузы, программы для вступительных испытаний в медицинские вузы, утвержденной МЗ и МП РФ (Москва, 1995), примерных программ вступительных экзаменов в вузы РФ (Москва, 2000), материалов для подготовки к Единому государственному экзамену и включает в себя теоретический материал, необходимый будущим врачам и биологам для успешного освоения комплекса различных дисциплин, изучение которых базируется на знании основ биоорганической химии.




