9. Образовательные технологии и методические рекомендации по организации изучения дисциплины
Чтение лекций по данной дисциплине проводится с использованием мультимедийных презентаций. Презентация позволяет преподавателю четко структурировать материал лекции, экономить время, затрачиваемое на рисование на доске схем, написание формул и других сложных объектов, что дает возможность увеличить объем излагаемого материала. Кроме того, презентация позволяет очень хорошо иллюстрировать лекцию не только схемами и рисунками которые есть в учебном пособии, но и полноцветными фотографиями, рисунками, портретами ученых и т. д. Электронная презентация позволяет отобразить физические и химические процессы в динамике, что позволяет улучшить восприятие материала.
При работе в малоконтингентной группе, сформированной из достаточно успешных студентов, целесообразно использовать диалоговую форму ведения лекций с использованием элементов практических занятий, постановкой и решением проблемных задач и т. д.
При проведении практических занятий преподавателю рекомендуется не менее 1 часа из двух (50% времени) отводить на самостоятельное решение задач. Практические занятия целесообразно строить следующим образом:
1. Вводная преподавателя (цели занятия, основные вопросы, которые должны быть рассмотрены).
2. Беглый опрос.
3. Решение 1-2 типовых задач у доски.
4. Самостоятельное решение задач.
5. Разбор типовых ошибок при решении (в конце текущего занятия или в начале следующего).
Для проведения занятий необходимо иметь большой банк заданий и задач для самостоятельного решения, причем эти задания могут быть дифференцированы по степени сложности. В зависимости от дисциплины или от ее раздела можно использовать два пути:
1. Давать определенное количество задач для самостоятельного решения, равных по трудности, а оценку ставить за количество решенных за определенное время задач.
2. Выдавать задания с задачами разной трудности и оценку ставить за трудность решенной задачи.
По результатам самостоятельного решения задач следует выставлять по каждому занятию оценку. Оценка предварительной подготовки студента к практическому занятию может быть сделана путем экспресс-тестирования (тестовые задания закрытой формы) в течение 5, максимум - 10 минут. Таким образом, при интенсивной работе можно на каждом занятии каждому студенту поставить по крайней мере две оценки.
По материалам модуля или раздела целесообразно выдавать студенту домашнее задание и на последнем практическом занятии по разделу или модулю подвести итоги его изучения (например, провести контрольную работу в целом по модулю), обсудить оценки каждого студента, выдать дополнительные задания тем студентам, которые хотят повысить оценку за текущую работу.
При проведении лабораторного практикума необходимо создать условия для максимально самостоятельного выполнения лабораторных работ. Поэтому при проведении лабораторного занятия преподавателю рекомендуется:
1. Провести экспресс-опрос в устной форме по теоретическому материалу, необходимому для выполнения работы (с оценкой).
2. Проверить планы выполнения лабораторных работ, подготовленных студентом дома (с оценкой).
3. Оценить работу студента в лаборатории и полученные им данные (оценка).
4. Оценить степень теоретической подготовленности студента (тестирование или контрольная работа, с оценкой).
5. Разобрать задания контрольных работ.
6. Проверить и выставить оценку за отчет.
Любая лабораторная работа должна включать глубокую самостоятельную проработку теоретического материала, изучение методик проведения эксперимента, обработку и интерпретацию экспериментальных данных. В ряд работ целесообразно включить разделы с дополнительными элементами научных исследований, которые потребуют углубленной самостоятельной проработки теоретического материала.
При организации внеаудиторной самостоятельной работы по данной дисциплине преподавателю рекомендуется использовать следующие ее формы:
· подготовка и написание рефератов, докладов, очерков и других письменных работ на заданные темы.
· выполнение домашних заданий разнообразного характера. Это - решение задач; подбор и изучение литературных источников; подбор иллюстративного и описательного материала по отдельным разделам курса в сети Интернет.
· выполнение индивидуальных заданий, направленных на развитие у студентов самостоятельности и инициативы. Индивидуальное задание получает каждый студент.
10. Оценочные средства для текущего контроля успеваемости, промежуточной
аттестации по итогам освоения дисциплины и учебно-методическое обеспечение
самостоятельной работы студентов
Всего по текущей работе в течение каждого семестра студент может набрать 50 баллов, в том числе:
3 семестр
- лабораторный практикум - 12 баллов;
- контрольные работы – всего 26 баллов;
- выполнение индивидуальных домашних заданий «Строение, номенклатура, природа химических связей в молекулах углеводородов» и «Получение и химические свойства углеводородов» – до 12 баллов;
4 семестр
- лабораторные работы - 18 баллов;
- контрольные работы – всего 32 балла;
5 семестр
- лабораторные работы - 15 баллов;
- контрольные работы – всего 23 балла;
- выполнение индивидуальных домашних заданий «Разработка оптимальных способов синтеза органического вещества» и «Расшифровка строения органических соединений по данным об их химических и спектральных свойствах» – до 12 баллов;.
Зачет проставляется автоматически, если студент набрал по текущей работе не менее 26 баллов. Минимальное количество баллов по каждому из видов текущей работы составляет половину от максимального.
Для самостоятельной работы используются задания и задачи, приведенные в перечисленных ниже учебных пособиях:
1. , , Голубчиков органических соединений. Учеб. пособие для химических вузов. / Под ред. . 3-е изд., испр. СПб: НИИ химии СПбГУ, 20с.
2. Практикум по органической химии. Синтез и идентификация органических соединений. / Под ред. и .- Москва: Высшая школа, 19с.
3. Строение и свойства углеводородов: метод. указания по органической химии для студентов заочного отделения / , ; Иван. гос. хим.-технол. ун-т. Иваново, 2с.
4. , Серкова и упражнения по органической химии. / Под ред. .- Москва: Высшая школа, 19с.
5. Вопросы для подготовки к контрольным работам по теме «Кислородсодержащие органические соединения»: Метод. указания. / , , ёв; ГОУ ВПО Иван. гос. хим-технол. ун-т. Иваново, 20с.
6. Азотсодержащие производные углеводородов: Методические указания / , , ; Иван. гос. хим.-технол. ун-т. - Иваново, 2с.
7. , Янковский в органической химии. Сборник задач. – Москва: Химия, 1985, 230 с.
8. Установление строения органических соединений по их химическим и физико-химическим свойствам. Методические указания. Составители: , , - Иваново: ИХТИ. 1991, 48 с.
Индивидуальные домашние задания
I. Строение, номенклатура, природа химических связей в молекулах углеводородов
1. Напишите структурную формулу предложенного углеводорода. Какой общей формуле соответствует ваше соединение и к какому гомологическому ряду оно относится?
2. Напишите структурные формулы 3-5 изомеров исходного соединения, относящихся к одинаковому с ним гомологическому ряду. Дайте им название, пользуясь рациональной номенклатурой и номенклатурой ИЮПАК. Сделайте то же самое для 3-5 изомеров в каждом из нескольких других гомологических рядов, имеющих ту же общую формулу СnН2n±x, что и исходный углеводород.
3. Выделите в молекуле максимальное число простых фрагментов – одно - и двухвалентных радикалов – и назовите их.
4. Укажите типы гибридизации всех углеродных атомов в исходном углеводороде. Каждый sp3-атом углерода отнесите к определенному типу: первичный, вторичный, третичный или четвертичный.
5. Изобразите схему перекрывания АО при образовании всех типов s-связей в молекуле предложенного углеводорода (sp3-s, sp2-s, sp-s, sp3-sp3, sp3-sp2, sp2-sp2, sp3-sp, sp2-sp, sp-sp). Выделите в молекуле плоские, тетраэдрические и линейные участки, если таковые есть.
6. Выделите ароматическую систему в молекуле, если она имеется. Какие типы p-связывания имеются в молекуле с кратными p-связями (изолированная, кумулированная или сопряженная система p-связей)? Изобразите схему перекрывания р - атомных орбиталей при образовании всех p- связей в предложенном соединении.
7. Распределите все связи С-Н в вашем соединении по группам в зависимости от гибридного состояния атома углерода, с которым связан водород, и расположите их в порядке увеличения прочности к гомолитическому разрыву.
8. Напишите формулы всех свободных радикалов, которые могут образовываться при отрыве одного атома водорода от молекулы углеводорода. Радикалы расположите в порядке увеличения их устойчивости, т. е. по легкости образования.
9. Укажите вид стереоизомерии, который характерен для предложенного углеводорода (цис-транс-, зеркальная) или одного из его изомеров. Изобразите проекционные формулы геометрических и зеркальных стереоизомеров.
10. При помощи справочных данных охарактеризуйте физические свойства предложенного вам углеводорода или близкого ему по строению изомера.
11. Рассчитайте тепловой эффект сгорания предложенного углеводорода, сравните полученную величину с табличным значением.
12. Изобразите проекционные формулы Ньюмена заслоненных и заторможенных конформаций, возникающих при вращении одной части молекулы вашего углеводорода относительно другой ее части вокруг оси s-связи RCH2-CH2R.
II. Способы получения и химические свойства углеводородов
1. Напишите реакции, отражающие способы получения предложенного насыщенного углеводорода из различных органических соединений с таким же строением углеродного скелета.
2. Получите свой алкан по реакции Вюрца. Образуются ли при этом побочные продукты?
3. Подействуйте на алкан 1 моль хлора на свету или при t = 300°С и напишите все возможные продукты монозамещения исходного соединения. На основании механизма реакции определите основной продукт реакции. Рассчитайте состав смеси монохлор - и монобромзамещенных соединений (% первичных, % вторичных, % третичных).
4. Напишите реакции термического крекинга, а также каталитической циклизации насыщенного углеводорода.
5. Напишите реакции нитрования, сульфохлорирования и сульфоокисления предложенного алкана, укажите их особенности.
6. Получите предложенный алкен из спиртов, моно - и дигалогенопроизводных.
7. Напишите реакции алкена с HBr, H2SO4, H2O в присутствии кислот, HClO, Br2. На конкретном примере реакции электрофильного присоединения объясните действие правила Марковникова. Как будет происходить присоединение НBr в присутствии перекисей?
8. Осуществите гидрирование и полимеризацию предложенного алкена.
9. Окислите алкен водным раствором перманганата, озоном с последующим гидролизом, хромовой кислотой.
10. Получите предложенный алкин из дигалогенпроизводных с различным расположением атомов галогена.
11. Осуществите: а) последовательное гидрирование, б) последовательное действие HCl на алкин, в) реакцию присоединения воды в присутствии солей ртути(II), а также схемы г) циклотримеризации и д) цепной полимеризации алкина, е) реакцию с металлическим натрием, а затем с любым первичным галогенпроизводным.
12. На основе углеродного скелета алкана напишите структурные формулы изомерных диенов (с изолированными, кумулированными и сопряженными p-связями), назовите их. С представителем каждого типа диенов проведите реакции : а) гидрирования 1 моль водорода на катализаторе и в момент выделения (атомарный), б) электрофильного присоединения 1 и 2 моль HBr, в) взаимодействия с 1 моль HBr. Какие особенности реакционной способности сопряженных диенов можно наблюдать?
13. Осуществите полимеризацию сопряженного диена и реакцию циклоприсоединения с его участием.
14. Напишите следующие реакции электрофильнгого замещения в ароматической p-системе предложенных аренов: а) хлорирование, нитрование и сульфирование до монопроизводных, б) моно - и диалкилирование, в) ацилирование, а затем – нитрование. На примере любого процесса объясните механизм реакции и ориентацию электрофильной частицы. Расположите все предложенные арены в порядке увеличения реакционной способности в SE2-реакциях..
15. Для аренов, имеющих алкильные заместители, проведите реакции: а) хлорирования 1 моль реагента на свету, б) нитрования разбавленной азотной кислотой, в) окисления боковых цепей. Каковы основные продукты реакций с точки зрения устойчивости промежуточных радикальных частиц.
III. Разработка оптимальных способов синтеза органического вещества
1. Области практического применения синтезируемого продукта и краткий обзор способов его получения.
2. Подбор методик синтеза и выбор наиболее оптимальной из них.
3. Анализ химизма процессов. Уравнения всех реакций, применяемых в ходе синтеза. Сведения об их механизмах и побочных продуктах.
4. Характеристики свойств веществ, применяемых в процессе синтеза, а также конечного продукта.
5. Пересчет количеств реагентов с целью получения заданного количества продукта.
6. Схемы аппаратурного оформления, отражающие последовательность операций синтеза, выделения и очистки продуктов.
7. Оценка возможностей использования различий в физико-химических свойствах исходных веществ и продуктов реакции для слежения за ходом процесса, определения конца реакции и чистоты полученных веществ.
IV. Расшифровка строения органических соединений по данным об их химических и спектральных свойствах
1. Установите по характеру УФ-спектра соединения наличие или отсутствие в его молекуле сопряженных или ароматических хромофорных систем.
2. Установите по величинам химических сдвигов и мультиплетностям сигналов протонов в ПМР-спектре соединения:
А) тип протонов, находящихся в составе различных групп атомов;
Б) соотношения между числами протонов различных типов по интенсивности сигналов;
В) с учетом сведений об элементном составе, молярной массе или брутто-формуле соединения и данных по интенсивности, химическому сдвигу и мультиплетности резонансных сигналов протонов сделайте заключение о структуре соединения.
3. Используя данные по характеристическим частотам функциональных групп в ИК-спектре, уточните строение молекулы неизвестного соединения.
4. Используйте данные по химическим и физическим свойствам соединения для уточнения и окончательного доказательства структуры неизвестного соединения.
5. Для установленной структуры соединения изобразите спектры 13С ЯМР, DEPT, а также двумерных методик COSY, NOESY и HETCOR.
Комплект контрольно-измерительных материалов для текущего, промежуточного и итогового контроля
Контроль промежуточных знаний студентов осуществляется путем тестирования. Комплект тестовых заданий по дисциплине состоит из 50 заданий: модуль 1 – 15 вопросов, модуль 2 – 25 вопросов, модуль 3 – 10 вопросов. В тестах предлагается использовать задания различных форм: с выбором ответа (форма А), с кратким свободным ответом (форма В), с полным развернутым ответом (дать определение понятия или термина, написать схему реакции, написать последовательность превращений – форма С). Время проведения тестирования рассчитывается исходя из двух минут на одно задание. Примеры контрольных тестов по каждому модулю приведены ниже.
Модуль 1-2 ” Теоретические основы органической химии. Химия углеводородов ”
1. Какое строение имеет углеводород, при бромировании которого на свету получается только одно третичное бромпроизводное, а сам углеводород можно получить по реакции Вюрца из первичного галогеналкана в качестве единственного продукта?
Ответ: 1) 2,4-диметилгексан; 2) 2,3-диметилгексан;
3) 3,4-диметилгексан; 4)2,5-диметилгексан.
2. Назовите соединение по номенклатуре ИЮПАК:
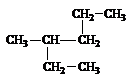
Ответ: 1) 1,2-диэтилпропан; 2) 3-метил-4-этилбутан;
3) 2-этилпентан; 4) 3-метилгексан.
3. В какой реакции преимущественно образуется 1-бутен?
|
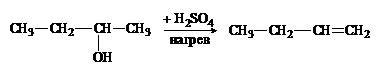
|
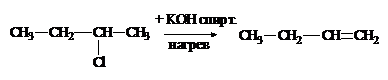
|
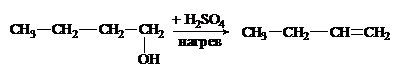
|

4. Что получится в результате следующей цепи превращений:
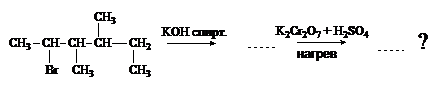
|
|
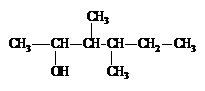
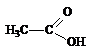 и
и 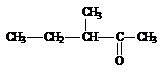
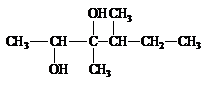
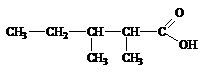
|
3) СО2 + Н2О +
5. Какое соединение образуется в результате реакции 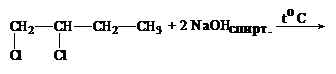
Ответ: 1) 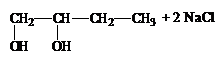 ; 2)
; 2) ![]() ;
;
3) ![]() ; 4)
; 4) ![]() .
.
6. Какова формула конечного продукта в следующей цепи превращений:
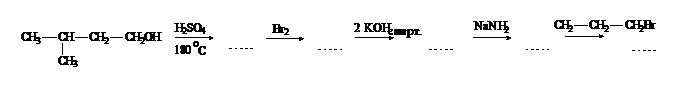
Ответ: 1) 2-метил-3-гептин; 2) 2,5-диметил-3-гексин;
3) 3,3-диметил-1-гексин.
7. Какова структурная формула углеводорода С5Н8, при озонолизе которого образуется малоновый альдегид
( 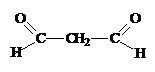 ) и формальдегид (
) и формальдегид (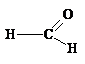 )?
)?
Ответ: 1) СН2=СН-СН2-СН=СН2; 2) СН3-СН=С=СН-СН3; 3) 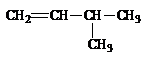 .
.
8. Что получится в качестве конечного продукта в следующей схеме синтеза?
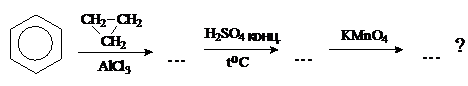
Ответ: 1) 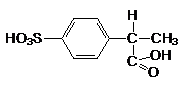 ; 2)
; 2) 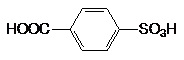 ;
;
3) 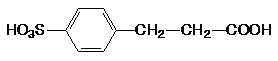 .
.
9. Какое вещество (или смесь веществ) преимущественно образуется при нитровании м-нитрохлорбензола?
Ответ: 1) 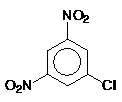 ; 2)
; 2) 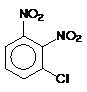 ;
;
3) 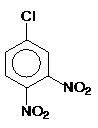 и
и 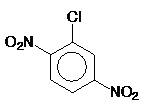 .
.
10. Какое соединение образуется при взаимодействии СCl4 и толуола, взятых в мольном соотношении 1:3 в присутствии AlCl3?
Ответ: 1)  ;
;
2)  ; 3)
; 3) 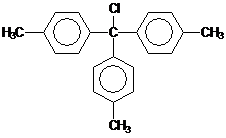 .
.
Модуль 3 “Химия монофункциональных производных углеводородов”
Галогенопроизводные углеводородов
1. Расположите следующие соединения в ряд по уменьшению скорости реакции нуклеофильного замещения:
а) бромбензол;
б) бензилбромид;
в) третбутилбромид;
г) изопропилбромид
Ответ: 1) а>б>в>г; 2) б>в>г>а; 3) б>г>в>а; 4) г>в>б>а; 5) в>г>б>а.
2. По какому механизму протекает реакция взаимодействия бензилхлорида с водным раствором КОН:
Ответ: 1) бимолекулярное нуклеофильное замещение;
2) мономолекулярное нуклеофильное замещение;
3) нуклеофильное элиминирование.
3. При помощи каких реагентов можно осуществить следующие превращения:
Бутан ® 2-хлорбутан ® 2-бутен ® 2,3-дибромбутан.
Ответ _______ .
4. Запишите схему получения бензилбромида из бензола.
Кислородсодержащие производные углеводородов
1. Какой спирт может быть получен при взаимодействии ацетона с третбутилмагнийбромидом?
1) 2,3,3-диметил-2-бутанол;
2) 1-бутанол;
3) 2-бутанол;
4) 1-гептанол.
2. 
3. 
Ответ: а) ___________________
б) __________________
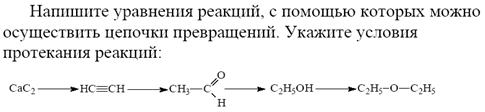
4. 
5. Окислением какого спирта может быть получен изобутаналь?
Ответ: 1) 1-бутанол;
2) 2-бутанол;
3) 2-метил-1-пропанол;
4) 2-метил-2-пропанол.
6. Какие соединения образуются в ходе следующей цепочки превращений:

Ответ: ___________________ .
7. Запишите схему получения орто-хлорбензальдегида из бензола.
8. Сравните кислотные свойства уксусной и трифторуксусной кислот:
1) трифторуксусная кислота сильнее уксусной, т. к. является ароматической;
2) трифторуксусная кислота сильнее уксусной, т. к. содержит электроноакцепторные заместители в углеводородном фрагменте;
3) уксусная кислота сильнее трифторуксусной, т. к. не содержит электроноакцепторных заместителей в углеводородном фрагменте;
4) кислоты не различаются по силе.
9. Какие соединения являются промежуточными и конечным продуктом в следующей цепи превращений:
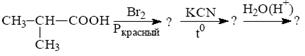
Ответ: ___________________ .
10. Запишите схему синтеза масляной кислоты из 1-пропанола.
Азотсодержащие соединения.
1. Какое соединение образуется при нитровании кумола (изопропилбензола) 15%-ной HNO3 при t = 150ºC под давлением?
1) 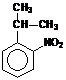 2)
2) 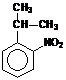 +
+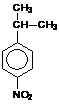 3)
3) 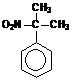 4)
4) 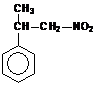
2. Какие реагенты необходимо использовать для проведения следующей цепи превращений:
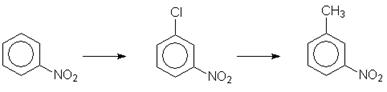
Ответ: ___________________ .
3. Запишите схему синтеза a-нитроэтилбензола из ацетилена.
4. Первичные ароматические амины при взаимодействии с азотистой кислотой на холоду образуют
1) нитрозосоединения;
2) нитросоединения;
3) диазасоединения;
4) соли азотистой кислоты.
5. Расположите следующие амины в ряд по уменьшению основности в газовой фазе:
1) CH3NH2; 2) (CH3-CH2)2NH; 3) (CH3)3N
Ответ: ___________________ .
6. Запишите схему синтеза пара-нитроанилина из бензола.
7. Какое соединение является конечным продуктом в следующей цепочке превращений:
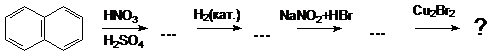
а) 2-нитро-3-бромнафталин; б) b-бромнафталин;
в) a-бромнафталин; г) 1-нитро-2-бромнафталин.
8. Какой реагент необходимо использовать, чтобы провести реакцию замещения:
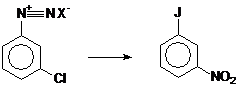
Ответ: ___________________ .
9. Какие соединения необходимо взять в качестве азо - и диазосоставляющих для получения красителя «метилового красного» 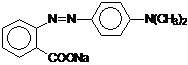 ? Запишите уравнение реакции.
? Запишите уравнение реакции.
Металлоорганические соединения.
1. Какие соединения получаются при действии на эфирный раствор н-бутиллития А) формальдегида; Б) воды; В) диоксида углерода; Г) ацетона? Продукты реакций гидролиза соединений назовите;
2. Какие из приведенных соединений (назовите их) относятся к классу металлоорганических? Почему? Ответ поясните. А) СH3CH2ONa; Б) СH3C≡CNa; B) CH3COOK; Г) (СH3)3B; Д) C2H5ZnCl;
3. Осуществите превращения, соединения назовите:
CH3-C≡CH ![]() A
A ![]() B
B ![]() C
C ![]() D
D ![]() E
E ![]() F
F ![]() G
G
Гетероциклические соединения.
1. Синтезируйте из пиридина a-аминопиридин и β-аминопиридин;
2. Синтезируйте из слизевой кислоты фуран и напишите для него реакции нитрования, ацилирования, гидрирования и диенового синтеза с малеиновым ангидридом;
3. Путем химических превращений из фурана получите 2-метилпиррол.
Модуль 4 “Химия би - и полифункциональных производных углеводородов”
1. Из ацетилена синтезируйте a-оксипропионовую кислоту. Что получится при действии на нее водуотнимающих средств при нагревании? Напишите уравнения реакций.
2. Напишите схемы взаимодействия глиоксиловой кислоты с А) бисульфитом натрия; Б) синильной кислотой; В) гидроксиламином; Г) аммиачным раствором окиси серебра. Что получится при действии на нее водного раствора щелочи (реакция Канницаро)?
3. Для ацетоуксусного эфира напишите реакции со следующими веществами: А) синильной кислотой; Б) гидросульфитом натрия; В) гидроксиламином; Г) пятихлористым фосфором; Д) хлористым ацетилом; Е) аммиаком; Ж) йодистым метилмагнием.
Гидроксикислоты.
1. Ацилирование салициловой кислоты по группе –ОН уксусным ангидридом приводит к образованию:
1) лактида;
2) лактона;
3) аспирина.
2. Какие из представленных гидроксикислот способны образовывать лактоны:
1) салициловая;
2) лимонная;
3) молочная;
4) яблочная.
Ответ: ___________________ .
3. Изобразите стереоизомеры винной кислоты.
Оксокислоты.
1. Синтез с использованием ацетоуксусного эфира приводит к образованию
а) карбоновой кислоты и кетона;
б) карбоновой кислоты и спирта;
в) кетона и альдегида;
г) альдегида и муравьиной кислоты.
2. Какие соединения являются продуктами в следующей цепи превращений:
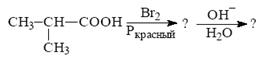
Ответ: ___________________ .
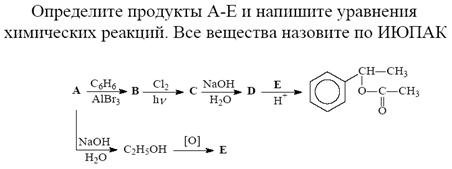
3. 
Углеводы.
1. Глюкоза относится к:
1) альдогексозам;
2) альдопентозам;
3) кетогексозам;
4) кетопентозам.
2. Какие из перечисленных углеводов являются восстанавливающими?
1) мальтоза,
2) целлобиоза,
3) сахароза,
4) лактоза.
Ответ: ___________________ .
3. Напишите схему взаимодействия фруктозы с фенилгидразином.
Аминокислоты, пептиды и белки.
1. Сколько аминокислот состава С4H9O2N имеют оптически активные изомеры?
1) 5
2) 4
3) 3
4) 2
2. Какие реагенты необходимо использовать для проведения следующего синтеза:
Ацетилен ® акрилонитрил ® нитрил β-аминопропионовой кислоты ® β-аминопропионовая кислота
Ответ: ___________________ .
3. Из бензола синтезировать мета-аминобензойную кислоту.
Модуль 5 “ Спектральная идентификация органических соединений ”
1. В спектре ПМР смеси циклогексана, тетраметилсилана, хлороформа и бензола содержится 4 пика при d = 0; 1,4; 7,2; и 7,4 м. д. (соотношение площадей 2/1/3,5/2,5). Какой сигнал относится к какому веществу? Определите количественный состав смеси.
2. Соединение С10Н13Br при окислении перманганатом калия превращается в бензойную кислоту и имеет в спектре ПМР три синглета при d = 1,7; 3,1 и 7,3 м. д. с соотношением интегральных интенсивностей 6/2/5. Какова его структура?
3. Изобутилен обработан HBr. Данные спектра ПМР продукта реакции: 1,0 (дублет); 2,1 (мультиплет); 3,2 (дублет); с соотношением интенсивностей 6/1/2. Прошла реакция по правилу Марковникова или против него? Ответ аргументируйте.
ЭКЗАМЕНАЦИОННЫЕ ВОПРОСЫ
3 семестр
ВОПРОС 1.
1. Предмет органической химии. Классификация органических соединений. Типы углеводородных фрагментов и функциональных групп в составе органической молекулы.
2. Особенности строения атома углерода. Катенация.
3. Понятие и типы изомерии. Структурная изомерия (скелетная, изомерия положения ФГ).
4. Понятие и типы изомерии. Пространственная изомерия (цис-транс-, оптическая).
5. Валентные состояния атома углерода. Условия и типы гибридизации (пространственное расположение орбиталей и валентные углы).
6. Типы химических связей в молекулах органических соединений. Простые и делокализованные связи.
7. Понятие ароматичности. Ароматическая p-связь. Признаки ароматических систем.
8. Электронные и пространственные эффекты в органической химии. Индукционный электронный эффект.
9. Электронные и пространственные эффекты в органической химии. Эффект сопряжения.
10. Электронные и пространственные эффекты в органической химии. Пространственные эффекты. Конформации молекул.
11. Типы заместителей в органических соединениях. Электронные доноры и электронные акцепторы, их электронные эффекты.
12. Особенности физико-химических свойств органических соединений. Полярность, растворимость, хромофорные свойства (окраска).
13. Классификация реакций и реагентов в органической химии. Реакционные центры молекул органических соединений.
14. Обратимые реакции в органической химии и их характеристики. Константа равновесия. Реакции комплексообразования и кислотно-основного взаимодействия. Кислоты и основания в органической химии.
15. Необратимые реакции в органической химии и их характеристики. Константа скорости реакции. Понятие механизма реакции.
16. Гомолитический и гетеролитический способы разрыва химической связи в органической химии.
17. Описание молекул органических соединений в методе валентных связей (ВС) и методе молекулярных орбиталей (МО). Ограничения метода ВС. Связывающая, разрыхляющая и несвязывающие орбитали. Порядок связи в молекулах ОС.
18. Хромофорные свойства органических соединений. Понятие хромофора и ауксохрома. Метод электронной спектроскопии. Электронные спектры поглощения и их применение в идентификации органических соединений.
19. Метод инфра-красной (ИК) спектроскопии и его применение в идентификации органических соединений. Взаимосвязь прочности химической связи и частоты ее колебаний.
20. Метод ядерного магнитного резонанса (ЯМР). Взаимосвязь природы атомов водорода и величины сдвига их сигнала в ПМР-спектре.
21. Механизм реакции радикального замещения (SR) на примере реакции хлорирования изобутана. Характеристика устойчивости возможных промежуточных частиц.
22. Механизм реакции электрофильного присоединения (AdE) на примере присоединения НСl к 2-метилбутену-2. Усточивость промежуточных частиц.
23. Особенности механизма электрофильного присоединения (AdE) на примере 2-метилбутадиена-1,3. 1,2- и 1,4- присоединение.
24. Механизм реакции электрофильного замещения (SE2) на примере реакции нитрования бензойной кислоты. Ориентирующее и активирующее действие заместителей в бензольном кольце.
ВОПРОС 2.
1. Пропан. Строение, свойства и способы получения.
2. Пропилен. Строение, свойства и способы получения.
3. Бутин-1. Строение, свойства и способы получения.
4. Этилбензол. Строение, свойства и способы получения.
5. Изопрен. Строение и свойства.
6. Метилаллен. Строение и свойства.
7. Пентадиен-1,4. Строение и свойства.
8. Нафталин. Строение и свойства.
9. Дифенил. Строение и свойства.
10. Реакции окисления алкенов.
11. Реакция озонолиза в алкенах, алкинах, диенах и аренах.
12. Реакции полимеризации алкенов и сопряженных диенов. Типы полимеризации.
13. Определить совместное и несовместное ориентирующее действие следующих функциональных групп в молекуле бензола:
14. Какими электронными эффектами обладают следующие заместители:
15. Реакции образования двойной связи. Правило Зайцева.
16. Из каких исходных соединений можно получить по реакции Вюрца следующие углеводороды:
17. Кислотные свойства углеводородов.
18. Реакции окисления ароматических углеводородов (на примере бензола).
19. Расположить радикальные частицы в порядке увеличения их устойчивости. Ответ аргументировать.
20. Крэкинг. Приведите пример реакции.
21. В каком ряду производных бензола облегчается протекание реакции электрофильного замещения (SE2):
22. Реакции алкилпроизводных бензола в боковой цепи.
4 семестр
вопрос 1.
1. a-Иодтолуол. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
2. 2-Бутанол. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
3. Бензиловый спирт. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
4. b-Нафтол. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
5. Многоатомные спирты (этиленгликоль, глицерин, гидрохинон). Взаимное влияние функциональных групп и химические свойства.
6. п-Br-Фенол. Электронное строение и электронные эффекты ОН-группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
7. Этилсульфид. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
8. Метилэтиловый эфир. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
9. Бензолсульфокислота. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
10. Бензиламин. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
11. м-Нитроанилин. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
12. Фенилнитрометан. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
13. Бензальдегид. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
14. 2,2-Диметил-3-пентанон. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
15. Малоновая кислота. Электронное строение и электронные эффекты функциональной группы. Взаимное влияние групп химические свойства молекул. Получение.
16. п-Br-Бензойная кислота. Электронное строение и электронные эффекты СООН-группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
17. Масляная кислота. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
18. b-Метилмасляный альдегид. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
19. Метилэтиламин. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
20. п-Толуидин. Электронное строение и электронные эффекты функциональной группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
21. п-Диазобензолсульфонат. Электронное строение и электронные эффекты диазо-группы. Реакционные центры молекулы и ее химические свойства. Способы получения.
22. Диальдегиды и дикетоны. Хиноны. Строение и химические свойства ненасыщенных альдегидов и кетонов.
23. Фосфорорганические соединения. Фосфины, фосфоновые кислоты, фосфиноксиды. Сходство и различие с аминами в строении и свойствах.
24. Простые металлоорганические соединения. Li-, Mg- и Hg - органические соединения.
25. Бор- и алюминий - органические соединения.
26. Кремний-органические соединения и соединения на основе углерода. Сходство и различия в строении и свойствах.
27. Металлоорганические соединения с делокализованной связью.
Вопрос 2.
1. Механизм взаимодействия 2-метилбутана с азотной кислотой.
2. Механизм взаимодействия хлорбензола с азотной кислотой.
3. Механизм взаимодействия хлористого бензила с водным раствором щелочи. Влияние различных факторов на протекание реакции.
4. Механизм взаимодействия хлористого пропила с амидом натрия. Влияние различных факторов на протекание реакции.
5. Механизмы взаимодействия галогенпроизводных со спиртовым раствором щелочи.
6. Механизм нуклеофильного замещения в ряду функциональных производных бензола.
7. Механизм взаимодействия п-нитроанилина с азотистой кислотой.
8. Механизм реакции нуклеофильного присоединения к альдегидам и кетонам. Примеры реакций.
9. Механизм взаимодействия изо-бутилового спирта и масляной кислоты.
10. Объясните характер взаимодействия альдегидов и кетонов при альдольной и кротоновой конденсации.
11. Реакционная способность a-положений у некоторых функциональных производных углеводородов и ее причины (альдегиды, карбоновые кислоты, нитросоединения и т. д.).
12. Из ацетоуксусного эфира получите метилэтилкетон. Протекающие реакции объясните.
13. Из ацетоуксусного эфира получите изо-масляную кислоту. Протекающие реакции объясните.
14. Из малонового эфира получите 2-метилпентановую кислоту. Протекающие реакции объясните.
15. Механизмы кислотного и щелочного гидролиза изо-пропилацетата.
16. Схемы восстановления нитросоединений. Роль рН среды. Бензидиновая перегруппировка.
17. Синтез спиртов на основе реактивов Гриньяра. Примеры реакций.
18. Взаимодействие нитросоединений со щелочами. Реакции нитросоединений с участием a-углеродного атома.
19. Характер превращений а) фенилуксусного альдегида и б) бензальдегида в щелочной среде.
20. Основные свойства аминов. Зависимость от строения амина и природы заместителей.
21. Кислотные свойства спиртов и карбоновых кислот. Зависимость от строения углеродного фрагмента и природы заместителей.
22. Син-анти-изомерия оксимов. Перегруппировка Бэкмана.
23. Механизм и условия реакции азосочетания. Роль рН среды. Побочные процессы.
24. Реакции диазосоединений с выделением азота.
25. Схема окисления спиртов и фенолов.
26. Перегруппировка амидов карбоновых кислот по Гофману.
27. Реакции алифатических и ароматических аминов с азотистой кислотой.
3 вопрос.
1. Из бензола получите азокраситель.
2. Из бензола получите N-метил-п-Br-анилин.
3. Из бензола получите азокраситель.
4. Из бензола получите м-Br-фенол.
5. Из ацетилена получите резорцин.
6. Из бензола получите п-аминобензойную кислоту.
7. Из этана получите пропилацетат.
8. Из бензола получите м-дибромбензол.
9. Из бензола получите п-фенилендиамин.
10. Из бутанона получите N-метиламид пропионовой кислоты.
11. Из хлорэтана получите янтарную кислоту.
12. Из этана получите амид пропионовой кислоты.
13. Из ацетоуксусного эфира получите пентанон-2.
14. Из малонового эфира получите 3-метилвалериановую кислоту.
15. Из бензола получите бензиловый эфир бензойной кислоты.
16. Из этана получите янтарную кислоту.
17. Из ацетилена получите 2-метил-2-бутанол.
18. С помощью озонолиза получите 3-метилбутаналь и подвергните его кротоновой конденсации.
19. Из толуола получите амид фенилуксусной кислоты.
20. Сравните кислотные свойства следующих карбоновых кислот и объясните изменение свойств: уксусная, трихлоруксусная, фенилуксусная, изомасляная, бензойная, п-гидроксибензойная, м-гидроксибензойная.
21. Сравните основные свойства следующих аминов и объясните изменение свойств: метиламин, метилэтиламин, диметилэтиламин, анилин, бензиламин, п-нитроанилин, м-нитроанилин.
22. Из бензола получите хлорангидрид п-Br-бензолсульфокислоты.
23. Из этилена получите хлорангидрид пропионовой кислоты.
24. Из бензола получите азокраситель.
25. Из этилена получите 2-бутанол.
26. Из бензола получить п-нитрофениловый эфир бензойной кислоты.
Окислением алкена получите пропаналь и напишите для него реакцию альдольной конденсации.
5 семестр
Вопрос 1.
1. Сравнительная характеристика строения реакционных центров и реакционной способности углеводородов (алканы, алкены, диены, алкины, арены).
2. Сравнительная характеристика строения реакционных центров и реакционной способности галогенпроизводных и спиртов.
3. Сравнительная характеристика строения реакционных центров и реакционной способности альдегидов (кетонов) и карбоновых кислот.
4. Сравнительная характеристика строения реакционных центров и реакционной способности аминов и нитросоединений.
5. Сравнительная характеристика валентных состояний углерода и кремния в органических соединениях и их отражение на реакционной способности.
6. Сравнительная характеристика валентных состояний азота и фосфора в органических соединениях и их отражение на реакционной способности.
7. Сравнительная характеристика валентных состояний серы и кислорода в органических соединениях и их отражение на реакционной способности.
8. Особенности химических свойств бифункциональных производных углеводородов. Галогено-, окси - и кетокарбоновые кислоты.
9. Особенности химических свойств бифункциональных производных углеводородов. Производные угольной кислоты. Строение и свойства.
10. Углеводы. Моносахариды. Химические свойства линейной и циклической форм альдоз и кетоз. Оптическая изомерия углеводов.
11. Углеводы. Дисахариды. Строение и свойства. Восстанавливающие и невосстанавливающие сахара.
12. Углеводы. Олиго - и полисахариды. Целлюлоза и ее реакционная способность.
13. Аминокислоты. Классификация, физико-химические свойства и реакционная способность. Отношение a-, b - и g-аминокислот к нагреванию.
14. Пептиды и полипептиды. Структура и основные биологические функции белков.
15. Пятичленные гетероциклы с одним гетероатомом. Пиррол, фуран и тиофен. Электронная и геометрическая структура. Ароматичность. Реакционная способность.
16. Конденсированные пятичленные гетероциклы с одним гетероатомом. Индол. Электронная и геометрическая структура. Ароматичность. Реакционная способность.
17. Пятичленные гетероциклы с двумя или более гетероатомами. Строение и реакционная способность.
18. Шестичленные ароматические гетероциклы. Пиридин и его гомологи. Электронная и геометрическая структура. Ароматичность. Реакционная способность.
19. Шестичленные гетероциклы с двумя или более гетероатомами. Строение и свойства. Пиримидиновые и пуриновые основания.
20. Нуклеиновые кислоты. Строение и биофункции.
Вопрос 2.
1. Электронная спектроскопия поглощения. Принцип метода. Электронный спектр поглощения (ЭСП) и его основные характеристики. Типы электронных переходов.
2. Светопоглощающие свойства органических соединений. Понятие хромофора и ауксохрома. Сильные и слабые хромофоры, связь силы хромофора с ЭСП. Сольватохромный эффект.
3. Электронная спектроскопия испускания (ЭСИ). Флуоресценция и фосфоресценция. Принцип и применение метода. Свойства возбужденных состояний органических соединений.
4. Спектрополяриметрия. Спектры кругового дихроизма (КД) и дисперсия оптического вращения (ДОВ) оптически активных молекул.
5. Метод инфракрасной (ИК) спектроскопии. Типы колебаний химических связей. Характеристические колебания в ИК-спектре. Взаимосвязь прочности химической связи и частоты ее колебаний.
6. Зависимость положения полос в ИК-спектрах от строения молекул и других факторов. Применение ИК-спектроскопии для идентификации и исследования структуры молекул органических соединений..
7. Спектроскопия комбинационного рассеяния (КР). Принцип и применение метода. Сравнительная характеристика ИК - и КР-спектров.
8. Ядерный магнитный резонанс (ЯМР). Условия возникновения. Химический сдвиг. Спин-спиновое взаимодействие ядер и его характеристика. ПМР.
9. Зависимость химического сдвига и других параметров спектра ПМР от природы органического соединения.
10. Спектроскопия ядерного магнитного резонанса на ядрах 13С. Простой 13С ЯМР-спектр и спектр DEPT. Связь со строением органической молекулы.
11. Динамический ЯМР-эксперимент. Изучение быстрых процессов (вращение, инверсия, изомеризация, таутомерия и т. д.) при варьировании температурного режима.
12. Двумерный ЯМР-эксперимент. Гомо - (1Н – 1Н) и гетеро - (13С – 1Н) ядерный COSY. Принцип и применимость метода.
13. Двумерный ЯМР. Гомо - (1Н – 1Н) ядерный NOESY. Принцип и применимость метода.
14. Спектроскопия электронного парамагнитного резонанса (ЭПР). Условия возникновения спектра ЭПР. Тонкая структура ЭПР-спектра, ее связь со строением молекулы.
15. Масс-спектрометрия. Принцип и различные модификации метода. Применение метода в идентификации органических соединений.
16. Фотоэлектронная спектроскопия (ФЭС). Принцип и использование метода (сравнительно с методом электронной спектроскопии поглощения).
17. Хроматография. Принцип и модификации метода (газовая, жидкостная и т. д.). Применение комбинированной масс-спектро-хроматографии для идентификации реакционных смесей.
18. Принцип линейности свободных энергий (ПЛСЭ). Константы Гаммета как количественные характеристики реакционной способности органических соединений.
19. Фотохимия органических соединений. Фотолиз, фотоизомеризация, фотоперенос электрона, фотопротолитические реакции.
20. Элементы электрохимии органических соединений. Реакции электроокисления (спирты и фенолы, амины, карбоновые кислоты) и электровосстановления (углеводороды, нитросоединения, карбонильные соединения).
11. Учебно-методическое и информационное обеспечение дисциплины:
а) основная литература________________________________________________________ Основная:
1. Нейланд химия.- М.: Высшая школа. 1990, 751с.
2. Органическая химия. - М.: Мир. 1974, 1132 с.
3. , Курц химия. - Изд. МГУ. 1999, Т. 1-4.
4. , Березин современной органической химии. - М.: Высшая школа. 1999.
5. Механизмы реакций углеводородов. Методические указания. Составитель: - Иваново: ИГХТА. 1995, 48 с.
6. Органическая химия. Карбонилпроизводные углеводородов. Учебное пособие. Составители: , , Хелевина : ИГХТА. 1995, 88 с.
7. Спектроскопия ЯМР. Методические указания. Составитель: - Иваново: ИХТИ. 1991.
8. Инфракрасные спектры органических соединений. Методические указания. Составитель: , - Иваново: ИХТИ. 1988, 32с.
9. Установление строения органических соединений по их химическим и физико-химическим свойствам. Методические указания. Составители: , , - Иваново: ИХТИ. 1991, 48 с.
10. Количественная оценка реакционной способности сопряженных и ароматических углеводородов с применением метода возмущений молекулярных орбиталей. Методические указания. Составители: , - Иваново: ИХТИ. 1990, 36 с.
11. Методы работы в лабораторном практикуме по органической химии. Методические указания. Составители: , - Иваново: ИГХТА. 1995, 40 с.
12. Многостадийные синтезы в лабораторном практикуме по органической химии. Методические указания. Составители: , , - Иваново: ИГХТА. 1995, 88 с.
13. Синтезы органических соединений. Методические указания. Составители: , - Иваново: ИХТИ. 1989, 86 с.
14. , Кувшинова пособие «Органическая химия. Синтез гетероциклических соединений». Иван. гос. хим.-технол. ун-т. Иваново. 2004. 91с.
15. Семейкин пособие «Органическая химия. Синтез и реакции элементорганических соединений». Иван. гос. хим.-технол. ун-т. Иваново. 2004. 68с.
____________________________________________________________________________
б) дополнительная литература______________________________________________
1. Современная органическая химия. М.: Мир, 1981. T. I и 2.
2. , Несмеянов органической химии. М.: Химия. 1974. T. I и 2.
3. , Темникова основы органической химии. М: Химия. 19с.
____________________________________________________________________________
- в) программное обеспечение СИСТЕМНЫЕ ПРОГРАММНЫЕ СРЕДСТВА: Microsoft Windows XP, Microsoft Vista
- ПРИКЛАДНЫЕ ПРОГРАММНЫЕ СРЕДСТВА: Microsoft Office 2007 Pro, Opera
- СПЕЦИАЛИЗИРОВАННОЕ ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ: Origin Pro 8.1, КОМПАС, Mathcad
- Электронные учебные ресурсы:
– контрольные тесты по каждому модулю;
– текст лекций с контрольными вопросами для самопроверки;
– слайд-конспект лекционного курса.
г) базы данных, информационно-справочные и поисковые системы:
12. Материально-техническое обеспечение дисциплины (модуля)
Лекции по дисциплине проводятся в аудитории, оснащенной видеопроектором.
При проведении лабораторного практикума используется лаборатория кафедры органической химии (кв. м.)
Программа составлена в соответствии с требованиями ФГОС ВПО с учетом рекомендаций и ПрООП ВПО по направлению и профилю подготовки____________ .
Автор (ы) _____________ (подпись, ФИО)
Заведующий кафедрой______ (кафедра-разработчик программы) (подпись, ФИО)
Рецензент (ы)______________ (подпись, ФИО)
Программа одобрена на заседании научно-методического совета факультета органической химии и технологии ФГБОУ ВПО «ИГХТУ» от «___» __________ 2011 г., протокол № ____
Председатель НМС ___________________ ФИО

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



