Графическим отображением уравнения Аррениуса является прямая линия в координатах lg k - 1/T (аррениусовская зависимость). Эта зависимость лежит в основе определения сроков годности лекарств в растворах методом ускоренного старения. Метод заключается в том, что определяется несколько констант скорости реакции разложения лекарственного вещества при высоких температурах (когда в соответствии с правилом Вант-Гоффа скорость разложения резко возрастает) и затем с помощью экстраполяции находится k при температуре хранения. Исходя из её значения рассчитывается срок годности.
Вопросы для самоподготовки
1. Предмет химической кинетики. Её значение для фармации, медицины, биологии.
2. Скорость химической реакции. Размерность скорости. Истинная (мгновенная) и средняя скорость.
3. Кинетическая классификация химических реакций. Молекулярность и порядок реакции (по данному веществу и общий).
4. Способы определения порядка реакции.
5. Зависимость скорости реакции от концентрации реагентов. Закон действующих масс. Константа скорости.
6. Реакции 1-го порядка. Вывод кинетического уравнения. Время полупревращения.
7. Расчет сроков годности лекарственных препаратов. Метод ускоренного старения.
8. Реакции 2-го порядка. Кинетические уравнения: а) для случая равных и б) для случая неравных концентраций реагентов. Время полупревращения.
9. Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Температурный коэффициент скорости.
10. Основные положения теории активных столкновений. Энергия активации реакции. Лимитирующая стадия.
11. Уравнение Аррениуса (вывод). Расчет энергии активации. Расчет констант скорости реакции при различных температурах.
12. Основные положения теории переходного состояния. Активированный комплекс. Энергетический профиль реакции.
13. Сложные реакции (последовательные, цепные, параллельные, сопряжённые). Примеры сложных реакций.
14. Особенности протекания гетерогенных реакций. Примеры. Реакции с диффузионным и кинетическим контролем.
15. Фотохимия. Фотохимические реакции (примеры). Основные законы фотохимии (закон Гротгуса - Дрейпера, закон Бунзена - Роско, закон Штарка - Эйнштейна). Фотохимические реакции в фармации.
16. Световая и темновая стадии фотохимических реакций. Фотосенсибилизация. Квантовый выход реакций.
17. Катализ. Значение катализа в фармации и биологии. Виды катализа (гомогенный и гетерогенный). Катализаторы, ингибиторы, промоторы, каталитические яды.
18. Механизм действия катализатора. Его влияние на энергию активации реакции. Примеры гомогенного катализа. Кислотно-основный катализ в фармации и биологии.
19. Гетерогенный катализ. Активные центры. Мультиплетная теория Баландина.
20. Катализ на носителях. Теория активных ансамблей Кобозева.
21. Ферментативный катализ. Ферменты.
Решение типовых задач.
Задача 1. При гидролизе этилхлорида, содержащегося в фармпрепарате “Хлористый этил”, в 80%-ном водном растворе этанола концентрация его меняется во времени следующим образом:
Время t, час | 0 | 4 | 10 | 27 | 67 |
Концентрация С, моль/л | 0,3115 | 0,258 | 0,194 | 0,085 | 0,013 |
Определите порядок реакции, константу скорости и время полупревращения.
Решение: Для определения порядка реакции рассчитаем значения константы скорости для различных промежутков времени. Исходя из предположения о наиболее простом случае, расчет проведем по кинетическому уравнению для реакции 1-го порядка:
1 C0 k = ¾ ln ¾¾ . t Ct |
Подставляем значения для каждого времени:
k1 = (1/4) ln (0,3115/0,258) = 0,04711 час-1;
k2 = (1/10) ln (0,3115/0,194) = 0,04735 час-1;
k3 = (1/27) ln (0,3115/0,085) = 0,04810 час-1 ;
k4 = (1/67) ln (0,3115/0,013) = 0,04741 час-1.
Поскольку значения k мало отличаются, примем, что порядок реакции первый (если бы значения k отличались значительно, расчет следовало бы провести по кинетическому уравнению 2-го порядка).
Константу скорости рассчитаем как среднее арифметическое из полученных значений:
k = (0,04711 + 0,04735 + 0,04810 + 0,04741) /4 = 0,04749 час-1.
Время полупревращения t1/2 можно рассчитать по кинетическому уравнению, заменяя Сt на соответствующее ему значение С0/2:
1 C0 ln2 0,693 t1/2 = ¾ ln ¾¾¾ = ¾¾ = ¾¾¾ . k С0/2 k k |
Подставляем значения:
t1/2 = 0,693/0,04749 = 14,592 час = 14 час 36 мин.
Задача 2. Вычислите время разложения на 10% инъекционного раствора, если константа скорости разложения лекарственного вещества в нём при 60оС равна 1,64´10-6 с-1 , а при 90оС – 4,2´10-6 с-1.
k2 Е* (T2 - T1) ln ¾ = ¾ ¾¾¾, k1 R T1T2 |
Решение: Для расчета срока годности нужно знать константу скорости разложения вещества при 20оС. Воспользуемся для её нахождения уравнением Аррениуса:
где k1 и k2 - константы скорости соответственно при температурах T1 и T2 (в К); E¹ - энергия активации реакции; R - универсальная газовая постоянная.
R ln(k2/k1) T1T2 8,314 ln(4,2´10-6/1,64´10-6)´333´363 E¹ = ¾¾¾¾¾¾¾¾ = ¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾ = T2 - T1 = 31502,69 Дж/моль = 31,5 кДж/моль. |
Сначала найдем значение энергии активации:
Зная E¹ , можно определить константу скорости при 20оС k20 (принимая, что k1 = k90) по этому же уравнению:
k90 31502,69 ln ¾¾ = ¾¾¾¾¾ ´ ¾¾¾¾¾ = 2,494; k20 8,´ 363 |
k90/k20 = e2,494 = 12,107;
отсюда k20 = k90 /12,107 = 4,2´10-6/12,107 = 3,47´10-7 c-1.
Считая, что разложение препарата идет по кинетике первого порядка, рассчитаем срок годности t1/10 как время разложения на 10%:
1 100 1,1111 0,1054 t1/10 = ¾ ln ¾¾¾¾ = ln ¾¾¾ = ¾¾¾¾—— = 303740 c » 3,5 сут. k k 3,47´10-7 |
Задача 3. Содержание изотопа 14С в бивне мамонта составляет 5,25% от его содержания в живых тканях растительности на месте находки. Сколько времени прошло после гибели мамонта? Период полураспада данного изотопа 5600 лет.
Решение: Считая, что изотоп 14С распадается по кинетике 1 порядка, рассчитаем время по соответствующему уравнению (см. Задачу 1). Сначала найдем константу скорости распада 14С:
0,693 0,693 k = ¾¾¾ = ¾¾¾ = 1,2375´10-4 год-1. t1/2 5600 |
1 100 t = ¾¾¾¾¾¾ ln ¾¾¾ » 23814 лет. 1,2375´10-4 5,25 |
Зная k, определим искомое время:
Задача 4. Реакция между веществами А и В выражается уравнением 2А + В = C. Начальная концентрация А равна 3,2 моль/л, а В - 1,6 моль/л. Константа скорости равна 0,75 мин-1.Какова скорость реакции а) в начальный момент; б) по истечении некоторого времени, когда концентрация А уменьшилась на 0,5 моль/л? Как изменится начальная скорость, если концентрации увеличить в 2 раза?
Решение: Воспользуемся уравнением закона действующих масс (считая, что порядок реакции по каждому веществу соответствует его стехиометрическому коэффициенту):
v = k CA2 CB.
Тогда
а) v0 = 0,75´3,22´1,6 = 12,288 моль/(л · мин).
б) при уменьшении СА на 0,5 моль/л в соответствии с уравнением реакции CB уменьшится на 0,25 моль/л. Скорость реакции при этом будет равна
v = 0,75 (3,2-0,5)2´(1,6-0,25) = 7,38 моль/(л · мин).
При увеличении концентраций реагентов в 2 раза скорость реакции станет равной
v = k (2СА)2 (2СВ) = 8 k СА2 СВ, т. е. увеличится в 8 раз.
Задача 5. Для реакции разложения вещества в водном растворе константа скорости при 100С равна 1,080*10-4 c-1, при 600С равна 5,484*10-2 c-1. Определить температурный коэффициент скорости реакции.
Решение: Воспользуемся соотношением
kt+10=γnkt
где γ – температурный коэффициент, k – константы скорости при двух температурах, n - интервал между температурами.
n= (t2-t1)/10 = (60-10)/10 = 5
Логарифмируя выражение kt+10=γnkt получаем lg kt+10 = n lgγ + lg kt, и, если вывести lgγ = (lg kt+10 - lg kt) / n = lg (5,484*10-2) – lg (1,080*10-4) / 5 = 0,5412
Тогда γ = 100,5412= 3,48, т. е. при подъеме температуры на каждые 10 градусов скорость реакции увеличивается в 3,48 раза.
Задачи для самостоятельного решения
Задача 1. Как изменится скорость реакции, идущей по уравнению 2Н2 + О2 = 2Н2О, если давление увеличить в 3 раза?
Ответ: увеличится в 27 раз.
Задача 2. Найти среднее значение константы скорости реакции (1порядка) разложения Н2О2 в водном растворе, а также определить время полупревращения и время разложения H2O2 на 90%, если на титрование одинаковых проб раствора израсходованы следующие объёмы раствора КMnO4 (мл):
Время отбора проб t, мин. | 0 | 10 | 20 | 30 |
Объём раствора, мл | 21,6 | 12,4 | 7,2 | 4,1 |
Ответ: kср = 0,0554; 12,5 мин; 41,56 мин.
Задача 3. При гидролизе сахарозы образовались глюкоза и фруктоза. При этом произошло следующее изменение угла вращения плоскости поляризации при 25оС в присутствии 0,5 н. HCl:
t, мин | 0 | 175 | ¥ |
a, о | 25,1 | 5,4 | –8,4 |
Вычислить: 1) константу скорости реакции; 2) сколько сахарозы (в %) инвертируется в течение 250 мин.
Ответ: 1) k = 5,06´10-3; 2) 71,8%.
Задача 4. Как возрастет скорость реакции при повышении температуры от 20оС до 100оС, если температурный коэффициент скорости равен 2?
Ответ: в 256 раз.
Задача 5. Для реакции разложения HI константа скорости при 280оС равна 7,96´10-7, а при 300оС – 3,26´10-6 мин-1. Рассчитать энергию активации, константу скорости при 290оС и температурный коэффициент реакции в указанном интервале температуры.
Ответ: Е¹ =185,6 кДж/моль; k = 1,63´10-6; g = 2,02.
Задача 6. Константа скорости омыления уксусноэтилового эфира в щелочной среде – реакция 2 порядка. При 10оС её k = 2,38. Определить время (мин), необходимое для омыления 90% уксусноэтилового эфира, если смешать при 10оС 1 л 0,05 М раствора эфира с а) 1 л 0,0 5 М NaOH; б) 1 л 0,1 М NaOH.
Ответ: а) 2 часа 31 мин; б) » 28 мин.
Работа 2.1. Изучение кинетики реакции инверсии сахарозы
Цель работы: изучение кинетических характеристик реакции первого (псевдопервого) порядка.
Целевые задачи: расчет константы скорости реакции с использованием поляриметрического метода; освоение методики работы на поляриметре; расчет других кинетических характеристик реакции (константы скорости, энергии активации, времени полупревращения, времени инверсии сахарозы на 10%).
Сахароза и продукты её гидролиза являются оптически активными веществами, поэтому для контроля за ходом данной реакции возможно использование поляриметрического метода. По мере накопления продуктов гидролиза происходит изменение знака угла вращения плоскости поляризованного света с отрицательного на положительный. Это явление называется инверсией.
Реакция гидролиза сахарозы в присутствии ионов Н+:
С12Н22О11 ----> С6Н12О6 + С6Н12О6 сахароза глюкоза фруктоза |
является бимолекулярной и её скорость может быть рассчитана по уравнению
v = k CсахарозыСводы
Однако при проведении гидролиза в разбавленном растворе, когда концентрация воды в ходе процесса меняется незначительно, величину Своды можно считать постоянной и тогда уравнение закона действующих масс можно записать следующим образом:
V = k¢Cсахарозы
где k¢ = k Своды.
При этом течение гидролиза подчиняется кинетическому уравнению для реакции 1-го порядка:
1 C0 k = ¾ ln ¾¾ t C |
где С0 – начальная концентрация сахарозы; С - концентрация сахарозы, наблюдаемая ко времени t, прошедшему от начала реакции. Поэтому данную реакцию относят к псевдомономолекулярным (или реакциям псевдопервого порядка).
Устройство и принцип действия поляриметра
Монохроматический свет от источника (натриевой лампы), расположенного в отделении (1) проходит через поляризатор (2), становясь при этом поляризованным. Далее луч поляризованного света попадает в кюветное отделение (3), где располагается кювета (4) с исследуемым раствором. Если в кювете имеется оптически активное вещество, плоскость поляризации света поворачивается вправо или влево в зависимости от природы вещества. Вследствие поворота плоскости поляризации луч света может пройти через анализатор (5) и попасть в окуляр (6) только в том случае, если анализатор повернут на тот же угол и в том же направлении. Поворот анализатора осуществляется регулятором (7).
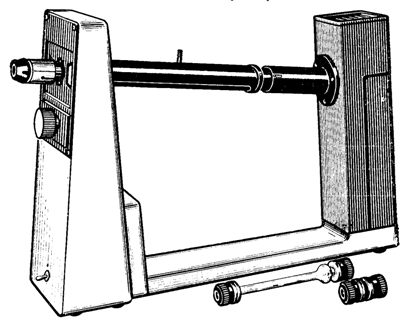
Отсчет показаний производится с помощью шкал, расположенных по обе стороны от окуляра в окошках (8). Включение и выключение прибора осуществляется тумблером (9).
Измерения с помощью поляриметра проводятся следующим образом:
1. После включения прибор прогревается около 10 мин до появления яркого желтого света в вентиляционных отверстиях отделения (1).
2. Кювета (4) заполняется без пузырьков воздуха исследуемым раствором и помещается в кюветное отделение (3), крышка кюветного отделения закрывается.
3. Вращением регулятора (10) устанавливается резкость изображения в окуляре (6). При этом на черном фоне должен быть виден желтый кружок, разделенный вертикальной линией; одна из половин кружка может быть более темной, чем другая.
4. Поворотом регулятора (7) достигается такое положение, при котором обе половины освещенного кружка приобретают одинаковую яркость и вертикальная граница полукружий исчезает.
ВНИМАНИЕ! Если при вращении регулятора (7) вокруг светового кружка вместо черного фона появляется желтое свечение, значит анализатор выведен из чувствительной области. В этом случае следует ориентируясь по шкале (8) совместить нули подвижной шкалы и неподвижного нониуса и начать измерение снова. |
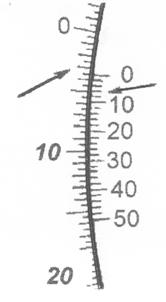
5. Угол поворота (“вращения”) плоскости поляризации светового луча определяется с помощью шкал (8). При прецизионных измерениях угол отсчитывается дважды (по левой и по правой шкале) с вычислением среднего арифметического; при учебных измерениях можно ограничиться одним отсчетом по левой шкале.
Принцип отсчета показаний приведен на рисунке ниже. Деления подвижной шкалы нанесены через каждые 0,5 градуса. Неподвижный нониус позволяет определить угол с точностью 0,02о. Сначала определяется число градусов, отделяющих нуль нониуса от нуля подвижной шкалы. Затем среди делений нониуса находится такое, которое сливается в одну линию с каким-либо делением подвижной шкалы. Это деление нониуса дает десятые и сотые доли градуса. Оба показания складывают. Так, изображение на рисунке соответствует углу 3,5 + 0,06 = 3,56О.
Оснащение рабочего места.
Поляриметр с кюветой Водяная баня
Склянка с притертой пробкой Термометр
Цилиндры на 10 мл Раствор сахарозы 20%
Растворы соляной кислоты 1н., 2н., 3н., 4н.
Проведение опыта.
1. Проверить оснащение рабочего места. Измерить и записать температуру опыта.
2. Включить водяную баню или термостат и довести температуру до 60оС. Включить поляриметр и дать ему прогреться не менее 10 мин.
3. Наполнить кювету дистиллированной водой (проверив отсутствие пузырьков воздуха), установить ее в поляриметр и убедиться, что угол вращения у оптически неактивной воды равен 00. Удалить из кюветы воду.
4. Отмерить раствор сахарозы и раствор HCl (концентрации и объёмы растворов указываются преподавателем). Слить оба раствора в склянку с притертой пробкой. В момент смешивания начать отсчет времени.
4. Полученной реакционной смесью заполнить кювету поляриметра и измерить углы вращения плоскости поляризации (at) через 5, 10, 15, 20, 30, 40 минут от начала реакции. Примечание. Сахароза и продукт её гидролиза – глюкоза вращают плоскость поляризации вправо, а фруктоза – влево, поэтому в ходе реакции угол поворота анализатора уменьшается от (примерно) -70 до 0о, а к концу реакции вращение становится положительным из-за большего удельного вращения фруктозы по сравнению с глюкозой.
5. Оставшуюся в склянке смесь поместить в водяную баню или термостат при 60оС на 30 мин. При этом реакция проходит практически до конца.
6. Смесь охладить, заполнить ею кювету и определить угол вращения, соответствующий наступлению равновесия (a¥).
7. Результаты показать преподавателю и занести в таблицу.
Концентрация раствора HCl: | |||||||||||||
Температура опыта Т = оС | |||||||||||||
№ | Время от начала опыта t, мин | 1/t | Угол вращения a, о | at-a¥ | ln(at-a¥) | a0-a¥ ln¾¾¾ at-a¥ | k, мин-1 | ||||||
1 | 0 | – | – | – | – | – | |||||||
2 | 5 | ||||||||||||
3 | 10 | ||||||||||||
··· | ··· | ||||||||||||
6 | ¥ | – | – | – | – | – | |||||||
kсредн= | |||||||||||||
8. Привести в порядок рабочее место и сдать дежурному.
9. Построить график зависимости ln(at–a¥)от времени и продлить его до
пересечения с осью ординат, как показано на рисунке:
ВНИМАНИЕ! Чтобы не потерять и не разбить покровное стекло, находящееся под завинчивающейся крышкой кюветы, раствор из неё следует осторожно выливать в кристаллизатор. |
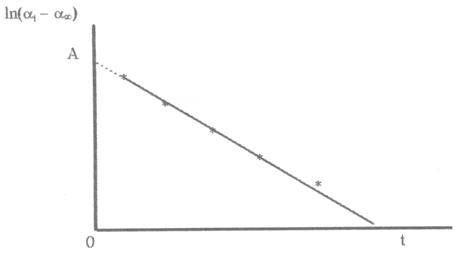
Измерить отрезок ОА, равный ln(a0–a¥), и записать его значение в

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




