На правах рукописи
разработка и стандартизация комплексного фитопрепарата для лечения синдрома хронической усталости
15.00.01 – Технология лекарств и организация фармацевтического дела
15.00.02 – Фармацевтическая химия, фармакогнозия.
Автореферат
диссертации на соискание ученой степени
кандидата фармацевтических наук
Москва-2009 г.
Диссертационная работа выполнена во Всероссийском научно-исследовательском институте лекарственных и ароматических растений (ВИЛАР) РАСХН
Научный руководитель:
Доктор фармацевтических наук, профессор | |
Доктор фармацевтических наук |
Официальные оппоненты:
Доктор фармацевтических наук, профессор | |
Кандидат фармацевтических наук |
Ведущая организация: Лабораторный центр ФГУ «НЦ ЭСМП» Росздравнадзора
Защита состоится «____» _____________2009 г. в 14 часов на заседании диссертационного совета Д 006.070.01 во Всероссийском научно-исследовательском институте лекарственных и ароматических растений (ВИЛАР) РАСХН
С диссертацией можно ознакомиться в библиотеке ВИЛАР
Автореферат разослан «___» __________ 2009 г.
Ученый секретарь диссертационного совета Д 006.070.01, доктор фармацевтических наук |
Актуальность темы
За последние десятилетия сформировалась новая патология современного мира, болезнь, встречающаяся в цивилизованных странах, связанная с особенностями и укладом жизни населения крупных городов, общей экологической ситуацией и нервно-психическим прессингом, которая включает понятие синдрома хронической усталости (СХУ).
Синдром хронической усталости – заболевание неизвестной этиологии, выраженное общей слабостью, снижением работоспособности. Наряду с этим пациенты жалуются на головные боли, миалгии, артралгии, ухудшение памяти, депрессии, расстройства сна. В некоторых случаях на субфебрильную температуру, болезненные ощущения в горле, увеличение шейных лимфоузлов. Многие клиницисты придерживаются мнения о вирусной этиологии СХУ, а психиатры придерживаются теории, что первичным в развитии СХУ являются психические заболевания с последующим изменением иммунной, эндокринной систем и развитием соответствующего симптомокомплекса.
Главным принципом лечения СХУ является комплексное лечение, включающее нормализацию режима отдыха и физической нагрузки; разгрузочно-диетическую терапию, назначение витаминных препаратов, лечебную физкультуру, аутогенную тренировку, иммунокоррекцию с выраженным адаптогенным действием, дневные транквилизаторы, ноотропные средства, энтеросорбенты и другие симптоматические препараты.
Исходя из вышеизложенного, считаем целесообразным разработку комплексного лекарственного средства для симптоматического лечения СХУ.
В настоящее время в номенклатуре лекарственных средств нет препаратов, обладающих одновременно тонизирующим, противовоспалительным и улучшающим обмен веществ действием.
Этой задаче отвечает лекарственное средство многокомпонентного состава растительного происхождения.
Растительные лекарственные препараты содержат комплекс биологически активных веществ (БАВ) в природной композиции и обладают мягким и щадящим действием.
В связи с этим, представляется актуальным и своевременным разработка и создание стандартизованного лекарственного средства растительного происхождения с целенаправленным теоретически и экспериментально обоснованным действием, направленным на предупреждение и лечение СХУ.
Цель и задачи исследования
Целью настоящего исследования является теоретическое и экспериментальное обоснование состава комплекса, разработка способов получения фитосубстанций в виде сухих экстрактов, а также лекарственной формы, и стандартизация препарата для лечения синдрома хронической усталости.
Для достижения указанной цели необходимо было решить следующие основные задачи:
· с помощью биотест-систем и фармакологических исследований теоретически и экспериментально обосновать рациональность состава многокомпонентной растительной композиции «Стабинорм»;
· изучить закономерности экстрагирования действующих веществ из лекарственного растительного сырья;
· провести качественную и количественную оценку экстрактов на присутствие и содержание основных действующих веществ;
· провести исследование по разработке рационального состава и технологии получения таблеток «Стабинорм»;
· разработать нормативные документы на сухие экстракты женьшеня, рапонтикума, крапивы, таблеток «Стабинорм» и опытно-промышленные регламенты на сухие экстракты и готовую лекарственную форму.
· провести патентный и информационный поиск для защиты разработанного лекарственного средства объектами интеллектуальной собственности, а именно: патентом РФ на изобретение и товарным знаком РФ на словесное наименование.
Научная новизна
В соответствии с результатами биохимического и фармакологического скрининга доказана возможность создания препарата «Стабинорм» для симптоматического лечения СХУ на основе пяти сухих экстрактов.
Теоретически обоснован и экспериментально подтвержден способ получения сухих экстрактов, включающий в себя основные стадии: экстрагирование, упаривание, очистку и сушку. С учетом химического состава исходного растительного сырья подобраны оптимальные параметры технологических процессов, характерные для каждого объекта. Выявлены закономерности выхода БАВ из сырья, имеющего различное анатомическое строение. Базируясь на теоретических основах сушки термолабильных веществ, экспериментально отработан щадящий режим сушки экстрактов методом распыления.
На основании данных фармакологического скрининга и литературных данных предложена рецептура и разработана технология производства таблеток.
Подтверждено присутствие БАВ в сухих экстрактах и готовой лекарственной форме с помощью современных физико-химических методов анализа. Разработаны методики сквозной стандартизации сухих экстрактов и готовой лекарственной формы таблеток «Стабинорм» из них.
С учетом вклада доминирующих БАВ разработаны методики качественного и количественного определения биологически активных веществ с помощью метода спектрофотометрии (суммы панаксозидов в пересчёте на панаксозид Rb1 в сухом экстракте женьшеня, аскорбиновой кислоты в экстракте крапивы); с помощью метода ВЭЖХ разработана методика количественного определения экдистерона в сухом экстракте рапонтикума сафлоровидного, а также БАВ в таблетках «Стабинорм».
Проведен поиск и отбор патентной документации, касающейся состава и технологии получения таблеток Стабинорма.
Оформлена и подана заявка на выдачу патента РФ на изобретение «Средство «Стабинорм» для лечения синдрома хронической усталости» (Заявка № от 01.01.2001 г.)
Проведен информационный поиск в автоматизированной базе данных товарных знаков РФ. На основании анализа полученных результатов подана заявка и получено свидетельство № 000 на товарный знак «Стабинорм».
Практическая значимость
На основании проведенных исследований разработаны:
· ФСП 42- «Экстракт женьшеня сухой»;
· ФСП 42- «Экстракт крапивы сухой»;
· ФСП 42- «Экстракт рапонтикума сафлоровидного сухой»;
· ФСП 42- «Таблетки «Стабинорм»;
· Опытно-промышленные регламенты на сухие экстракты женьшеня, крапивы, рапонтикума и таблетки «Стабинорм».
Основные положения, выносимые на защиту:
· результаты теоретических и экспериментальных исследований по обоснованию состава таблеток «Стабинорм», рекомендованных для профилактики и симптоматического лечения синдрома хронической усталости;
· результаты разработки способов получения 3-х сухих экстрактов;
· результаты исследований по определению показателей подлинности, качественного и количественного определения действующих веществ в сухих экстрактах и готовой лекарственной форме.
· результаты разработки технологии получения таблеток «Стабинорм».
Апробация работы
Материалы диссертации доложены и обсуждены на IX Международном съезде «Фитофарм» (Санкт-Петербург, 2005 г.), научно-практической конференции, посвященной 75-летию ВИЛАР (Москва, 2006 г.).
Связь задач исследования с проблемным планом.
Диссертационная работа выполнена в соответствии с тематическим планом научно-исследовательских работ ВИЛАР РАСХН по «Программе фундаментальных и приоритетных прикладных исследований по научному обеспечению развития агропромышленного комплекса РФ на гг.», задание 04, шифр 04.13 «Разработка технологий производства высокоэффективных лечебных и профилактических препаратов из растительного сырья».
Публикации
По материалам диссертации опубликовано 4 научные работы, из них 3 – в рецензируемых изданиях ВАК РФ; подана заявка на изобретение.
Объем и структура диссертации
Диссертационная работа изложена на страницах компьютерного текста, состоит из введения, обзора литературы (глава 1), трех глав экспериментальной части, выводов, списка литературы, включающего 165 источников, в том числе 53 иностранных, приложений. Работа содержит 33 рисунка и 25 таблиц.
Во введении обоснована актуальность темы, сформулированы цели и задачи исследования, представлены научная новизна и практическая значимость работы.
В первой главе на основании обзора данных литературы описаны возможные причины возникновения синдрома хронической усталости и методы их коррекции с помощью лекарственных средств. Приведены сведения о лекарственном растительном сырье (ЛРС), используемом в профилактических и лечебных целях при данной патологии. Представлена номенклатура лекарственных препаратов на основе сухих экстрактов из ЛРС, а также методы их стандартизации и нормы содержания БАВ. На основании этого в состав комплексного препарата, предназначенного для лечения и профилактики синдрома хронической усталости, включены компоненты, обладающие тонизирующей активностью, улучшающим общий обмен веществ, противовоспалительным, иммуномодулирующим, противовирусным и другими действиями.
Во второй главе приведены сведения об объектах исследований, используемые методы и приборы.
В третьей главе представлены исследования по разработке способов получения сухих экстрактов корней женьшеня, листьев крапивы двудомной и корневищ и корней рапонтикума сафлоровидного и методик их качественного и количественного анализа.
Четвертая глава посвящена обоснованию состава и технологии получения таблеток «Стабинорм». Описаны разработанные методики стандартизации данного комплексного фитопрепарата.
В пятой главе на основании проведенных патентных исследований и поиска в базе данных товарных знаков РФ представлены результаты по патентованию изобретения на оригинальное лекарственное средство для лечения синдрома хронической усталости и регистрации словесного обозначения «Стабинорм» в качестве объекта интеллектуальной собственности - товарного знака.
Основное содержание работы
2. Объекты и методы исследования
Объектом исследования служило лекарственное растительное сырье, отвечающее требованиям нормативной документации:
Корни женьшеня Panax ginseng C. A. Mey. сем. Аралиевые – Araliaceae | ГФ ХI, вып. 2, ст. 66 |
Листья крапивы двудомной Urtica dioica L. сем. Крапивные – Urticaceae | ГФ ХI, вып. 2, ст. 25 |
Корневищ с корнями рапонтикума сафлоровидного (левзеи сафлоровидной) Rhaponticum carthamoides (Willd.) Lljin (syn. Leuzea carthamoides (Willd.) DC.) сем. Астровые - Asteraceae | ФС |
На основе вышеперечисленного сырья получены сухие экстракты, используемые для получения таблеток «Стабинорм», рекомендуемых для профилактики синдрома хронической усталости.
Измельчение воздушно-сухое сырья с содержанием влаги от 9,06 до 12,00% проводили согласно ГФ ХI изд., вып.1. Отбор средней и аналитических проб проводили согласно – ГФ ХI изд., вып.1, с.267; пробы для определения подлинности, измельченности и содержание примесей – 100 г, влажности – 10 г, действующих веществ и золы – 40 г.
Определение влаги, тяжелых металлов в сухих экстрактах проводили, согласно ГФХI изд., вып.2, статья «Экстракты».
Исследование качественного состава изучаемых объектов проводили методом тонкослойной хроматографии (ТСХ) использовали хроматографические пластины «Сорбфил» и систем растворителей: хлороформ - спирт метиловый - вода в соотношении 61:32:7.
Все величины Rf обнаруженных соединений являются средними из пяти измерений. Растворители для хроматографии и реактивы для получения производных использовали марки ХЧ или ЧДА.
Спектры поглощения соединений в УФ - и видимой областях регистрировали на приборе Gelios (США) в кюветах с толщиной поглощающего слоя 10мм.
При разработке методик качественного и количественного определения биологически активных веществ были использованы хроматографически чистые вещества и стандарты.
Идентификацию веществ методом ВЭЖХ проводили на приборе фирмы «Gilson» с последующей компьютерной обработкой результатов исследования с помощью программы Мультихром для Windows. В работе применялся обращено-фазовый вариант метода, в качестве неподвижной фазы использовали металлические колонки Kromasil С18, ReproSil - Pur C-18AQ, Kromasil 100 С18, Диасорб 130 С16; подвижная фаза: ацетонитрил-0,05 % раствор кислоты фосфорной. Анализ проводили при комнатной температуре, скорость подачи элюента – 1 мл/мин. Детектирование осуществляли с помощью УФ-детектора при длине волны – 250 нм для экдистерона и 265 нм для элеутерозида В.
Статистическую обработку результатов анализа проводили согласно ГФ XI.
3. Разработка способа получения сухих экстрактов и их стандартизация
Подбор оптимальных параметров экстрагирования и разработка технологии получения сухих экстрактов
В состав лекарственного препарата «Стабинорм» входят 5 сухих экстрактов, на 3 из которых (сухие экстракты листьев крапивы, корней женьшеня и экстракт корневищ и корней рапонтикума) нами предложена технология получения, на другие 2 – сухие экстракты зверобоя и элеутерококка нормативная документация разработана и утверждена ранее.
Состав и соотношение компонентов данной растительной композиции подобран с учетом химического состава БАВ и фармакологических свойств каждого вида лекарственного растительного сырья и подтвержден биотестированием с помощью запатентованных биотест-систем и доклиническим фармакологичес-ким изучением.
Технологическая схема получения сухих экстрактов предусматривает стадии твердофазной экстракции, концентрирование полученного извлечения, очистку сепарированием и сушку концентрированного экстракта.
В ходе разработки технологии получения экстрактов учитывали факторы, влияющие на полноту экстрагирования сырья: тип и концентрация экстрагента, измельченность сырья, время достижения равновесной концентрации в системе зкстрагент-сырье, кратность экстракции.
В результате установлено, что оптимальным экстрагентом для корней женьшеня является 30% спирт, корней рапонтикума 70% спирт, для листьев крапивы 30% спирт, при трехкратной экстракции каждого сырья в течение часа при температуре 60 °С в соотношении 1:10 и измельченности сырья 1-3 мм для корней женьшеня и листьев крапивы и 3-5мм для подземных органов рапонтикума.
С помощью предложенной технологии получено по 5 опытных серий сухих экстрактов. По результатам проведенных исследований оформлены и утверждены опытно-промышленные регламенты на производство сухих экстрактов женьшеня, крапивы и рапонтикума.
Разработка методик стандартизации сухих экстрактов
Стандартизацию экстрактов проводили согласно ОФС «Экстракты» ГФ XI и разработанным нами методикам, аналогичным на исходное сырье и адаптированным к условиям анализа изучаемых субстанций.
Сухой экстракт женьшеня
Установление подлинности сухого экстракта проводили с помощью качественной реакции с реактивом Фелинга на восстанавливающие сахара и метода хроматографии в тонком слое сорбента с целью обнаружения панаксозидов после детектирования 5% спиртовым раствором кислоты фосфорномолибденовой.
Количественное определение суммы панаксозидов проводили спектрофотометрическим методом после проведения цветной реакции раствора препарата с фосфорномолибденовой кислотой при длине волны 700 нм (рис. 1).
Расчет содержания суммы панаксозидов проводили в пересчете на панаксозид Rb1, который в данных условиях проведения цветной реакции имеет максимум поглощения при данной длине волны. Удельный показатель поглощения комплекса панаксозида Rb1 с фосфорномолибденовой кислотой при длине волны 700 нм установлен нами экспериментально на стандартном образце фирмы Sigma и равен 217.
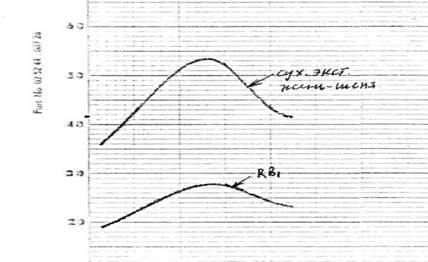
Рис.1. – УФ-спектр поглощения комплекса панаксозида Rb1, сухого экстракта женьшеня с фосфорномолибденовой кислотой.
Таблица 1
Метрологические характеристики методики количественного определения суммы панаксозидов в пересчёте на панаксозид Rb1 в сухом экстракте женьшеня
f | X | S2 | S | P,% | t(f, P) | ∆X | E, % |
9 | 15,22 | 0,3156 | 0,5617 | 95 | 2,26 | 1,2526 | ±8,23 |
Из табл. 1 видно, что ошибка единичного определения методики с 95% вероятностью составляет ±8,23%.
По результатам анализа 5 опытных серий сухого экстракта женьшеня установлена норма содержания суммы панаксозидов не менее 10%.
Сухой экстракт рапонтикума сафлоровидного
Наиболее значимыми веществами рапонтикума сафлоровидного с точки зрения биологической активности являются фитоэкдистероиды, которые определяют фармакологические эффекты данного лекарственного средства в живом организме.
Нами исследована возможность применения метода ВЭЖХ с целью определения экдистерона в экстракте по сопоставлению времени удерживания со стандартным образцом (СО) экдистерона (ТУ ) для установления подлинности и его количественной оценки.
В ходе исследования определены оптимальные условия хроматографического анализа сухого экстракта: подвижная фаза: ацетонитрил-0,05 % раствор кислоты фосфорной, колонка размером 250х4,6 мм, сорбент С-18АQ или Диасфер С18 с размером частиц 5 мкм, скорость элюирования во всех экспериментах составляла 1 мл/мин, при длине волны УФ-детектора 245 нм, время регистрации хроматограммы 30 мин; определены этапы и режимы элюирования.
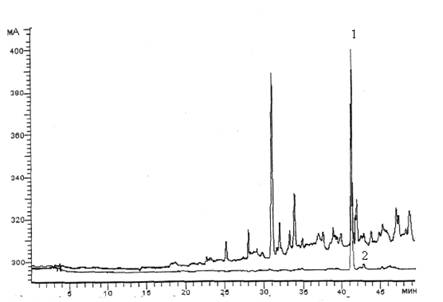
Рис. 2. – ВЭЖХ-хроматограмма экстракта левзеи (1) и СО экдистерона (2)
Метрологические характеристики разработанной методики свидетельствуют об удовлетворительной ее воспроизводимости (табл.2).
Таблица 2
Метрологические характеристики методики количественного определения экдистерона в сухом экстракте левзеи сафлоровидной
f | X | S2 | S | P,% | t (f, P) | ∆X | E, % |
5 | 0,78 | 0,0002 | 0,0141 | 95 | 2,57 | 0,0,0148 | ±3,23 |
По результатам опытов с добавками экдистерона установлено отсутствие систематической ошибки в процессе количественного определения по предлагаемой методике (табл. 3).
Содержание экдистерона в сухом экстракте рапонтикума должно быть не менее 0,7%.
Таблица 3
Результаты опыта с добавками экдистерона к навеске сухого экстракту рапонтикума
Содержание экдистерона в сырье, мг | Добавлено экдистерона, мг | Должно быть, мг | Найденомг | Относительная ошибка, % |
0,78 | 0,15 | 0,93 | 0,91 | +2,98 |
0,78 | 0,25 | 1,03 | 1,01 | +1,28 |
0,78 | 0,50 | 1,28 | 1,21 | -2,94 |
Сухой экстракт крапивы двудомной
Согласно данным литературы листья крапивы содержат аскорбиновую кислоту, витамин К1, пантотеновую кислоту, каротиноиды, гликозид уртицин, дубильные вещества, органические кислоты и др. соединения.
Для определения подлинности БАВ предлагаем включить качественные реакции:
а) с 10% раствором свинца ацетата на наличие дубильных веществ;
б) с 0,1% спиртовым раствором натрия 2,6-дихлорфенол-индофенолята на наличие аскорбиновой кислоты;
в) с раствором железа хлористого на наличие фенольных соединений.
Ввиду того, что экстракт крапивы вводится в комплексный препарат как источник БАВ с адаптогенными свойствами, нами для количественного определения выбран параметр содержания аскорбиновой кислоты и на основании этого разработан спектрофотометрический метод, основанный на получении окрашенного комплекса аскорбиновой кислоты с раствором натрия фосфорномолибдата. После проведения реакции УФ-спектр раствора препарата в области 600-900 нм имеет максимум поглощения при длине волны (700±10) нм (рис.3). Для расчета содержания аскорбиновой кислоты параллельно определяют оптическую плотность комплекса стандартного образца аскорбиновой кислоты с натрия фосфорномолибдатом, полученного в тех же условиях, что и комплекс раствора испытуемого образца с натрия фосфорно-молибдатом.
Метрологические характеристики методики рассчитаны по результатам анализа одного образца препарата в одиннадцати независимых повторностях (табл.4).
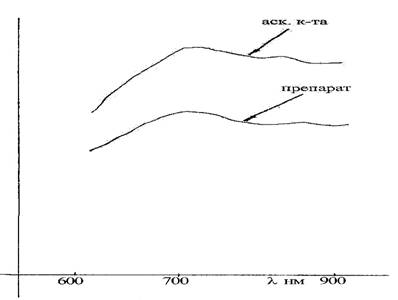
Рис. 3. – УФ-спектр поглощения кислоты аскорбиновой в сухом экстракте крапивы
Таблица 4
Метрологические характеристики методики количественного определения аскорбиновой кислоты в сухом экстракте крапивы
f | X | S2 | S | P,% | t(f, P) | ∆X | E, % |
10 | 3,77 | 0,7889 | 0,1104 | 95 | 2,23 | 0,2462 | ±6,53 |
Таким образом, ошибка единичного определения методики с 95% вероятностью составляет ±6,53%.
Опыты с добавками аскорбиновой кислоты показали на отсутствие систематической ошибки (табл. 5).
Таблица 5
Результаты опытов с добавками аскорбиновой кислоты
Найдено аскорбиновой кислоты в сырье, мг | Добавлено аскорбиновой кислоты, мг | Должно быть аскорбиновой кислоты, мг | Найдено г | Относительная ошибка, % |
3,77 | 0,75 | 4,52 | 4,61 | + 1,99 |
3,77 | 1,49 | 5,26 | 5,48 | - 4,18 |
3,77 | 2,98 | 6,75 | 6,43 | - 4,74 |
Содержание аскорбиновой кислоты в сухом экстракте должно быть не менее 2,5%.
На основании проведенных исследований оформлены и утверждены ФСП на «Женьшеня экстракт сухой», «Рапонтикума экстракт сухой» и «Крапивы экстракт сухой».
4.Разработка состава технологии получения таблеток «Стабинорм»
Наиболее распространенной лекарственной формой для фитопрепаратов являются таблетки.
Высокая производительность таблеток, точность дозирования входящих компонентов, возможность варьирования размеров, стабильность при хранении, удобство приема и др. создают возможность масштабного их производства.
В связи с этим при разработке лекарственного препарата «Стабинорм» предложена лекарственная форма таблетки.
Изучение технологических свойств сухих экстрактов и их смеси показало, что они обладают неудовлетворительными характеристиками, такими как низкая сыпучесть, гигроскопичность и др.
Для улучшения технологических свойств суммы сухих экстрактов, входящих в состав Стабинорма и получения таблеточной массы, отвечающей требованиям прессуемости и сыпучести, необходимо было введение вспомогательных веществ, улучшающих сыпучесть и уменьшающих гигроскопичность действующих веществ. В ходе исследования нами подобран состав вспомогательных веществ и их количество, предложен метод влажной грануляции (рис. 4).
Введение сахара молочного в состав таблеток целесообразно в связи тем, что лекарственное вещество гигроскопично, кроме того, молочный сахар обладает хорошими показателями прессуемости и сыпучести. Для увлажнения гранулята использовался 5% раствор крахмального клейстера. В качестве скользящего вещества предложен стеарат кальция. Оптимальный состав таблетки: суммы экстрактов сухих 0,025 г и вспомогательных веществ до получения таблетки массой 0,15 г. подобран с учетом показателей качества: прочности, распадаемости, растворения.
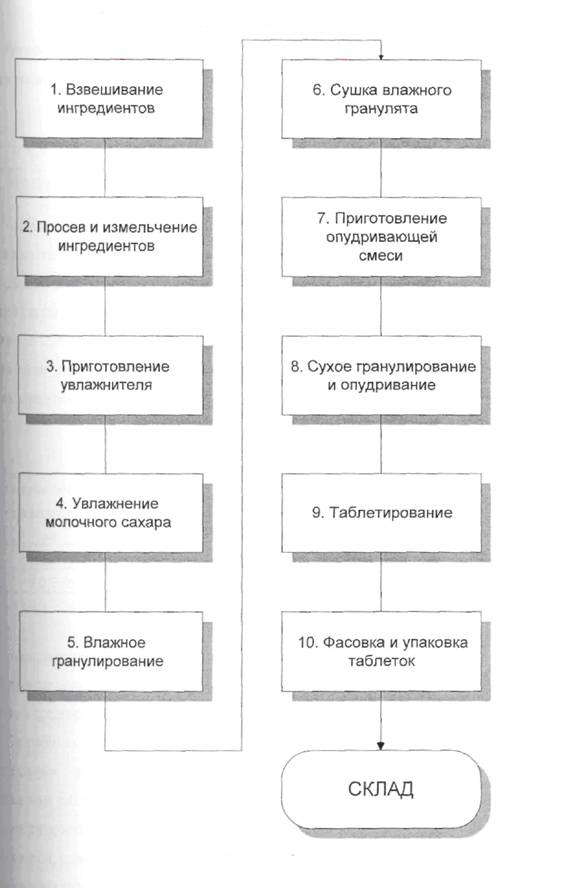
Рис. 4. – Технологическая схема получения таблеток «Стабинорм»
Таким образом, таблетки «Стабинорм» имеют следующий состав в расчете на таблетку массой 0,15 г:
Женьшеня экстракта сухого с содержанием суммы панаксозидов в пересчете на панаксозид Rb1 10% Элеутерококка экстракта сухого с содержанием элеутерозида В 0,3% Рапонтикума сафлоровидного (левзеи сафлоровидной) экстракта сухого с содержанием экдистерона 1% Крапивы экстракта сухого с содержанием аскорбиновой кислоты 2,5% Зверобоя экстракта сухого с содержанием суммы флавоноидов в пересчете на рутин 8% Лактоза (сахар молочный) Крахмал картофельный сорт «экстра» Кальция стеарат (кальций стеариновокислый) Кроскармеллоза натрия | - 0,0023 г - 0,0045 г - 0,0114 г - 0,0045 г - 0,0023 г -0,1035 -0,017 -0,0015 -0,003 |
Технология получения таблеток включает следующие основные стадии:
· Вспомогательные работы (просеивание сырья, подготовка посуды, приготовление увлажнителя).
· Получение массы для таблетирования (смешивание и увлажнение, влажное гранулирование, введение во влажные гранулы сухого экстракта, сушка влажной массы, сухое гранулирование и опудривание гранул.
· Таблетирование и обеспыливание.
Результаты проведенных балансовых загрузок положены в основу составления опытно-промышленного регламента на производство таблеток «Стабинорм».
С учетом данных о химическом составе входящих в состав препарата сухих экстрактов (гликозиды, флавоноиды, дубильные вещества, аскорбиновая кислота), нами разработаны методы идентификации и количественной оценки основных групп БАВ в таблетках «Стабинорм».
Установление подлинности Стабинорма предложено проводить с помощью качественных реакций, метода ТСХ и ВЭЖХ.
Реакция пенообразования подтверждает наличие сапонинов, цианидиновая проба – флавоноидов, реакция с хлоридом окисного железа – дубильных веществ катехиновой природы, реакция с 2,6-дихлорфенолиндофенолятом натрия – аскорбиновой кислоты.
ТСХ-анализ позволяет идентифицировать в препарате панаксозиды.
Обнаружение элеутерозида В и экдистерона проводили методом ВЭЖХ. Идентификацию осуществляли по сопоставлению с временами удерживания и по спектрам поглощения хроматографических пиков стандартных образцов этих соединений.
Выбор длины волны детектирования произведен на основании рассмотрения спектров поглощения хроматографических пиков стандартных образцов элеутерозида В и экдистерона. Максимум поглощения элеутерозида В находится при длине волны 265 нм, экдистерона – при 250 нм. Предложено проводить хроматографи-ческий анализ при одновременном детектировании на двух длинах волн: 250 и 265 нм. Допускается последовательное хроматографи-рование образцов с детектированием процесса разделения компонентов при 265 нм для определения элеутерозида В и при 250 нм для определения экдистерона (рис. 5).
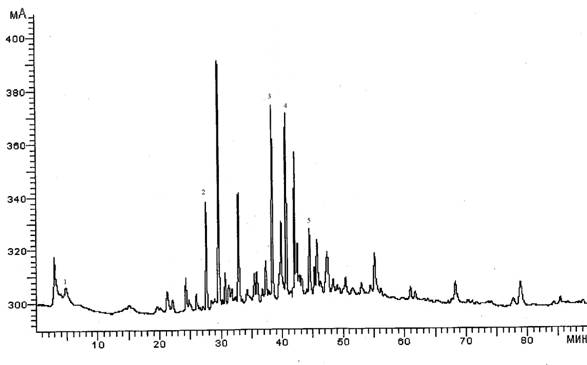
Рис. 5. – ВЭЖХ-хроматограмма извлечения из таблеток:
1-витамин С; 2-элеутерозид В; 3-экдистерон; 4-рутин; 5-гиперицин
Времена удерживания элеутерозида В и экдистерона в препарате относительно растворов стандартных образцов могут отличаться не более, чем на 3%. Необходимость введения данной качественной характеристики обусловлено требованием исключения случайной ошибки при идентификации пиков только по временам удерживания, объектом исследования является комплексный препарат, представляющая собой смесь экстрактов пяти растений.
Предложенная методика использована нами для количественного определения БАВ в таблетках «Стабинорм».
Содержание элеутерозида В в одной таблетке в пересчете на среднюю массу таблеток должно быть от 0,000010 до 0,000025 г.
Метрологические характеристики методики представлены в табл.6.
Таблица 6
Метрологические характеристики методики определения элеутерозида в таблетках «Стабинорм» методом ВЭЖХ
f | X | S2 | S | P,% | t(f, P) | ∆X | E, % |
9 | 0,01297 | 0,7889 | 0,000247 | 95 | 2,26 | 0,000558 | ±4,3 |
Данные таблицы свидетельствуют, что относительная ошибка единичного определения методики с 95% вероятностью составляет ±4,3%.
Отсутствие систематической ошибки в разработанной методике подтверждено опытами с добавками элеутерозида В к навеске препарата (табл.7).
Таблица 7
Результаты опытов с добавками элеутерозида В
Найдено элеутерозида В в навеске препарата, мг | Добавлено элеутерозида В, мг | Должно быть элеутерозида В, мг | Найдено элеутерозида В, мг | Относи-тельная ошибка, % |
0,012 | 0,010 | 0,022 | 0,021 | + 4,55 |
0,012 | 0,015 | 0,027 | 0,029 | - 7,41 |
0,012 | 0,020 | 0,032 | 0,030 | - 6.25 |
В табл. 8 представлены метрологические характеристики методики количественного определения экдистерона.
Таблица 8
Метрологические характеристики методики определения экдистерона
в таблетках «Стабинорм»
f | X | S2 | S | P,% | t(f, P) | ∆X | E, % |
9 | 0,105 | 0,105 | 0,00165 | 95 | 2,26 | 0,003729 | ±3,55 |
Из данных, представленных в табл. 8 видно, что относительная ошибка единичного определения методики с 95% вероятностью не превышает ±3,55%.
Результаты опытов с добавками экдистерона указывают на отсутствие систематической ошибки методики (табл. 9).
Таблица 9
Результаты опытов с добавками экдистерона к навеске препарата
Найдено экдистерона, г | Добавлено экдистерона, мг | Должно быть экди-стерона, мг | Найдено экдистерона, мг | Относительная ошибка, % |
0,950 | 0,10 | 1,050 | 1,090 | + 3,81 |
0,950 | 0,15 | 1,100 | 1,160 | + 5,45 |
0,950 | 0,20 | 1,150 | 1,095 | - 4,78 |
Согласно данным анализа 5 опытных серий таблеток «Стабинорм», установлена норма содержания БАВ в препарате: экдистерона в одной таблетке в пересчете на среднюю массу таблеток должно быть от 0,00006 до 0,00015 г.; элеутерозида В в одной таблетке в пересчете на среднюю массу таблеток должно быть от 0,000010 до 0,000025 г.
Наряду с этим в проект НД включена спектрофотометрическая методика количественного определения суммы гликозидов, содержание которых в одной таблетке в пересчете на панаксозид Rb1 и среднюю массу таблеток должно быть от 0,0045 до 0,0055 г.
Таблица 10
Метрологические характеристики результатов количественного определении суммы панаксозидов спектрофотометрическим методом.
f | X | S2 | S | P,% | t(f, P) | ∆X | E, % |
9 | 3,41 | 0,0228 | 0,1510 | 95 | 2,26 | 0,3367 | ±9,87 |
Данные таблицы 10 свидетельствуют, что ошибка единичного определения методики с 95% вероятностью составляет ±9,87%.
На основании проведенных исследований составлен проект ФСП «Таблетки «Стабинорм».
С помощью разработанных методик анализа БАВ установлен срок годности таблеток «Стабинорм» в упаковке, предусмотренной проектом ФСП, который составляет 2 года.
5. Патентование разработанного состава и товарного знака таблеток «Стабинорм»
Поиск и отбор патентной документации, касающейся состава и технологии получения таблеток Стабинорма проводился по фондам СССР, Российской Федерации и Евразийского патентного ведомства Всероссийской патентно-технической библиотеки Федерального института промышленной собственности (ФИПС).
Изобретений с полным составом предложенного средства не было найдено. На основании этого оформлена и подана заявка на выдачу патента РФ на изобретение «Средство «Стабинорм» для лечения синдрома хронической усталости» (Заявка № от 01.01.2001 г.)
Для защиты словесного наименования препарата проведен информационный поиск в автоматизированной базе данных товарных знаков РФ. На основании анализа полученных результатов подана заявка и получено свидетельство № 000 на товарный знак «Стабинорм».
Общие выводы
1. С помощью биотест-систем и фармакологических исследований обоснован состав многокомпонентной растительной композиции «Стабинорм».
2. На основании результатов изучения физико-химических и реологических характеристик сухих экстрактов женьшеня, элеутерококка, рапонтикума сафлоровидного, крапивы и зверобоя разработаны состав и соотношение компонентов для таблеток «Стабинорм»; рациональность выбранной рецептуры подтверждена фармакологическими исследованиями.
3. Установлены закономерности влияния технологических факторов (полярность экстрагента, его концентрация, температура, соотношение сырья и экстрагента, время экстракции) на выход суммы экстрактивных и действующих веществ из растительного сырья женьшеня, рапонтикума сафлоровидного и крапивы; разработана и предложена оптимальная схема получения сухих экстрактов для создания лекарственных и профилактических средств данного профиля.
4. Исследование качественного состава сухих экстрактов и таблеток «Стабинорм» методами ТСХ, спектрофотометрии, ВЭЖХ и качественными реакциями установило наличие следующих групп БАВ: флавоноидов, экдистероидов, панаксозидов, элеутерозидов, аскорбиновой кислоты и других.
5. Разработаны методы количественного определения аскорбиновой кислоты в сухом экстракте крапивы; суммы панаксазидов, в пересчёте на панаксозид Rb1 в сухом экстракте женьшеня, экдистерона в сухом экстракте рапонтикума. Наряду с этим разработаны методики количественного определения суммы панаксазидов, в пересчете на панаксозид Rb1, элеутерозида В, экдистерона в таблетках «Стабинорм».
6. Проведены исследования по изучению стабильности сухих экстрактов и лекарственной формы препарата. Установлено, что все контролируемые показатели качества остаются в пределах норм в течение 2 лет и 6 мес. в естественных условиях хранения.
7. Разработаны и оформлены НД на сухие экстракты женьшеня, рапонтикума, крапивы и таблетки «Стабинорм».
8. Оформлена и подана заявка на выдачу патента РФ на изобретение «Средство «Стабинорм» для лечения синдрома хронической усталости» (Заявка № от 01.01.2001 г.). Оформлена и подана заявка на регистрацию словесного наименования препарата в качестве объекта интеллектуальной собственности – товарного знака «Стабинорм». Получено свидетельство № 000 на товарный знак «Стабинорм».
Список работ, опубликованных по теме диссертации
1. Использование специфических ферментных тест-систем in vitro для разработки многокомпонентного препарата «Стабинорм» / , , и др. // Вопросы биологической, медицинской и фармацевтической химии. - № 4. – 2007. – С.25-30.
2. Анализ номенклатуры и методов стандартизации лекарственных средств на основе сухих экстрактов из лекарственного растительного сырья / , , // Вопросы биологической, медицинской и фармацевтической химии. - № 3.–2008.–С.13-17.
3. Разработка методов контроля качества таблеток «Стабинорм» / , , и др.// Вопросы биологической, медицинской и фармацевтической химии. - № 4. – 2008. (в печати).
4. Название фитопрепарата, логотип и слоган как объекты интеллектуальной собственности / , , // Материалы XI Международного съезда «Актуальные проблемы создания новых лекарственных препаратов природного происхождения» (Санкт-Петербург - 2005. - С.732-735).



