Количественная оценка НСТ-теста показала, что ингаляция биотехнологических штаммов приводила к дозозависимому повышению микробоцидной активности, т. е. характерному для микроорганизмов «метаболическому взрыву» в фагоцитах (макрофаги, нейтрофилы). При этом повышение их метаболической активности происходило путем увеличения свободных форм кислорода (свободные радикалы, супероксидного аниона и кислорода О2).
Иная реактивность клеточных элементов выявлена на воздействие грамотрицательных бактерий (Pseudomonas, Alcaligenes). При воздействии этих бактерий в концентрации 104 и 105 кл/м3 наблюдалось уменьшение общего числа клеточных элементов в лаважной жидкости респираторного тракта за счет снижения преимущественно нейтрофилов и макрофагов. Полученные данные объясняются высокими адгезивными свойствами клеточной оболочки, а также способностью грамотрицательных бактерий нарушать кислородную метаболическую активность фагоцитов [ 1986, Sorensen, 1987, Bishop, 1987].
Проведенные исследования показали, что функционально - метаболическая активность фагоцитирующих клеток респираторного тракта значимо менялась в зависимости от концентрации промышленных микроорганизмов, минимальные изменения фагоцитов были отмечены на пороговых уровнях воздействия по сенсибилизирующему эффекту.
Оценивая значимость изученных показателей (миграционная активность клеток, НСТ-тест), нужно признать целесообразность использования их в качестве интегральных при установлении порогов вредного действия штаммов при ингаляционном воздействии.
2. Оценка иммунотропных свойств промышленных микроорганизмов
Показано, что воздействие нокардиоформных актиномицетов в концентрации 106 и 107 кл/м3 не оказывало иммунотропного действия (табл.4). Воздействие штаммов рода Rhodococcus в концентрации 108 кл/м3 приводило лишь к увеличению полиморфноядерных лейкоцитов, что может свидетельствовать о развитии неспецифических воспалительных процессов в ответ на фактор высокой интенсивности.
Воздействие грамположительных бактерий в концентрациях 104 и 105 кл/м3 на организм различно. Одни бактерии (Lactobacillus, Micrococcus, B.subtilis 72, B.subtilis 103) не обладали иммунотропными свойствами. Общее содержание лимфоцитов, концентрация Т - и В-лимфоцитов, а также показатели соотношения Т/В и эозинофилии находились на уровне контрольных значений (для Т/В – 2.0-2.5; для Эо/Эк – 1.0-1.5). Эти штаммы не проявляли аллергенной активности. Ингаляция других грамположительных бактерий (B.subtilis 65, B.licheniformis 60,103) и актиномицетов (S.fradiae, S.aureofaciens) в концентрации 105 кл/м3 приводила к слабо выраженным изменениям иммунной системы.
Таблица 4
Характеристика иммунотропной и сенсибилизирующей активности промышленных микроорганизмов при ингаляционном воздействии
Концентрация, кл/м3 | Т- лимфоциты % | В-лимфоциты % | ГНТ % | ГЗТ мм |
Контроль R.erythropolis 5х107 | 44.2±1.5 39.6±2.3 | 17.8±1.5 20.2±1.4 | 4.7±1.2 5.7±1.0 | 0.142±0.007 0.151±0.010 |
B.subtilis 103 Контроль 6х104 6х105 | 46.5±0.9 44.2±1.4 42.8±1.7 | 16.8±1.0 17.2±1.2 17.6±1.5 | 3.6±0.6 4.6±1.7 9.1±2.8 | 0.13±0.013 0.20±0.007 0.29±0.022 |
B.licheniformis 60 Контроль 5х104 5х105 | 44.0±1.1 45.5±1.5 39.1±1.0* | 21.8±0.9 20.4±1.0 25.4±1.7 | 4.6±0.4 4.4±0.5 9.0±0.9** | 0.12±0.03 0.22±0.03 0.38±0.02** |
P. сaryophylii Контроль 7х103 7х104 | 43.9±2.0 40.5±2.1 33.2±1.9** | 18.4±2.3 18.9±2.1 22.5±1.7* | 4.0±0.9 6.1±1.6 12.6±2.4** | 0.139±0.021 0.233±0.064 0.403±0.034* |
P. canescens Контроль 2х103 2х104 | 41.6±0.8 39.8±0.4 36.3±1.2* | 21.1±0.8 22.2±1.8 27.0±1.4* | 3.5±0.6 4.2±±2.7** | 0.19±0.03 0.24±0.04 0.36±0.04* |
A. awamori Контроль 1.2х104 1.2х105 | 43.5±2.3 32.2±1.7** 29.6±3.5** | 21.0±1.1 24.6±0.9 30.4±1.4** | 4.4±±1.1** 24.4±2.7** | 0.188±0.018 0.138±0.028 0.306±0.044* |
C.tropicalis Контроль 3х103 3х104 | 42.2±2.6 38.7±1.7 35.5±1.7 | 19.5±1.6 25.5±1.7* 31.3±2.1** | 4.7±0.4 11.2±1.8** 20.0±3.3** | 0.201±0.045 0.436±0.061* 0.490±0.051* |
Обозначения: * Р<0.05, ** Р<0.01
Иммунотропное действие грамотрицательных бактерий (Pseudomonas, Alcaligenes) и микромицетов (Penicillium, Aspergillus, Candida) выявлялось на достаточно низких уровнях воздействия – 103-104 кл/м3. Влияние на организм характеризовалось изменением баланса иммунокомпетентных клеток и увеличением эозинофилов крови. Отмечено снижение Т-лимфоцитов и увеличение В-лимфоцитов, а также показано существенное изменение баланса Т - и В-лимфоцитов периферической крови. Показатель соотношения Т/В при ингаляции P.caryophylii снижен до 1.5 (в контроле 2.4), а показатель эозинофилии, напротив, увеличен до 1.9 (в контроле 1.0). Величина показателя Т/В при воздействии A.awamori в концентрации 105 кл/м3 снижена до 0.97 (в контроле 2.1).
При воздействии грибов на более высоком уровне в лейкограмме подопытных животных отмечались изменения многих показателей: снижение общего числа лимфоцитов, увеличение моноцитов и нейтрофилов в периферической крови, характеризующих выраженное цитотоксическое действие. При воздействии дрожжеподобного гриба Candida в концентрации 3х104 кл/м3 отмечено снижение коэффициентов массы иммунокомпетентных органов (тимус и селезенка).
Воздействие грамнегативных бактерий и микроскопических грибов вызывало у животных формирование гиперчувствительности немедленного и замедленного типа на уровне 103-104 кл/м3.
Полученные результаты свидетельствуют о том, что длительная ингаляция большинства изученных штаммов приводит к изменению баланса иммунокомпетентных клеток, эозинофилии в крови и сенсибилизации экспериментальных животных. При этом происходит формирование гиперчувствительности немедленного типа, опосредованной антителами-реагинами, а также гиперчувствительности замедленного типа, опосредованной Т-лимфоцитами. Увеличение количества эозинофилов в периферической крови служит признаком аллергеноопасности штаммов, хотя не исключено непосредственное участие эозинофилов в сенсибилизации организма, опосредованное через Fc – рецепторы этих клеток к Ig E (, , 1989, 2003, , 1999).
При этом иммунотропная, в том числе и сенсибилизирующая активность биотехнологических штаммов проявляется в зависимости от их таксономической принадлежности, а величина регистрируемого эффекта – от уровня действия микробиологического фактора.
|
|
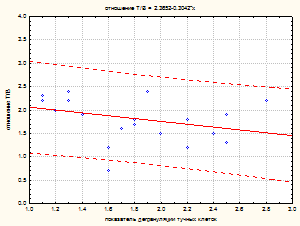
Рис.1 Связь между показателем дегрануляции тучных клеток и соотношением Т/В-лимфоцитов (а), показателем дегрануляции тучных клеток и показателем эозинофилии (б) при ингаляционном воздействии биотехнологических штаммов на минимально эффективных уровнях в зависимости от их таксономической характеристики.
Регрессионный анализ наиболее информативных и гигиенически значимых показателей иммунотропной активности 26 биотехнологических штаммов, принадлежащих к различным таксономическим группам, позволил выявить связь между показателем дегрануляции тучных клеток и соотношением Т/В-лимфоцитов, а также между показателями дегрануляции тучных клеток и эозинофилии (рис.1а, б).
Установленная зависимость, отражающая патогенетические механизмы развития сенсибилизации (ГНТ), имеет прогностическую значимость в плане регламентирования и оценки риска воздействия новых штаммов промышленных микроорганизмов.
3. Совершенствование программы исследований по гигиеническому нормированию биотехнологических штаммов
На основе анализа результатов исследований и данных информационного банка усовершенствована программа исследований по гигиеническому нормированию промышленных микроорганизмов.
Кластерный анализ, широко используемый в микробиологии (,1989, Jongman e. a.,1996), позволил сгруппировать и объединить изученные штаммы различных таксонов в зависимости от выделенных гигиенически значимых показателей: показателя дегрануляции тучных клеток, баланса Т - и В-лимфоцитов и показателя эозинофилии. Пространственное положение штаммов определялось евклидовым расстоянием, рассчитанным на основе экспериментальных данных.
Наиболее четкие группировки были получены по показателю дегрануляции тучных клеток. На рис.2 выявляются 3 группы микроорганизмов. Наиболее удаленная группа (3) представлена микроорганизмами, у которых не выражены сенсибилизирующие свойства. Центральная группа (1) представлена микроорганизмами с выраженными сенсибилизирующими свойствами. К ней примыкает группа (2) биотехнологических штаммов, у которой аллергенные свойства выражены в слабой степени.
Результаты кластерного анализа данных позволил разработать шкалу аллергенной активности промышленных микроорганизмов, которая может быть использована для тестирования новых штаммов в скрининговых исследованиях "аллерген – не аллерген". В таблице 5 приведены оценочные критерии сенсибилизирующей активности штаммов.
|
|
|
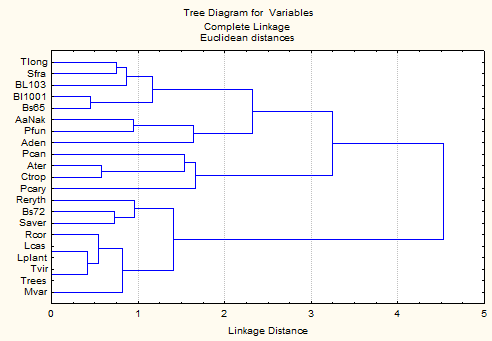
Рис.2 Дендрограмма для промышленных микроорганизмов, построенная по показателю дегрануляции перитонеальных тучных клеток при ингаляции на уровне Limch (по оси x – сходство, отн. ед., по оси y – сокращенное название штамма)
Таблица 5
Шкала аллергенной активности
промышленных микроорганизмов, выявляемой в реакции
дегрануляции тучных клеток in vitro (ГНТ)
Критерии | 1 группа | 2 группа | 3 группа |
достоверность различий (a) количества деграну-лированных ТК (%) в опытной и контрольной группах | a≤0.01 | 0.01<a≤0.05 | a> 0.05 |
величина показателя дегрануляции (ДТК) | 2.0<ДТК | 1.5≤ДТК≤2.0 | ДТК<1.5 |
частота развития сенсибилизации (Р), % | 50<Р≤100 | 20< Р≤50 | 0≤Р≤20 |
Анализ созданного информационного банка данных по обоснованию ПДК 131 биотехнологического штамма и микробиологического препарата показал, что лимитирующим критерием вредного действия подавляющей части микроорганизмов (около 80 %) являлись сенсибилизирующие свойства. С учетом таксономической характеристики биотехнологических штаммов среди бактерий аллергенными свойствами обладали 75%, среди актиномицетов – 67%, среди грибов – 80 % (рис.3).
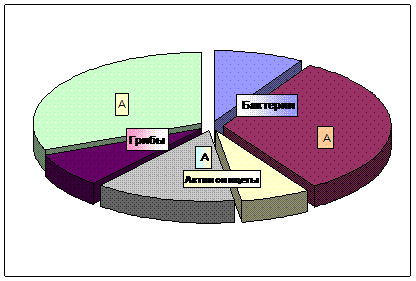
Рис.3 Структура массива промышленных микроорганизмов в зависимости от таксономического положения и лимитирующего показателя вредного действия. А – микроорганизмы, нормированные по аллергенному эффекту
Совокупность полученных данных позволила усовершенствовать научную программу исследований по гигиеническому нормированию микроорганизмов, используемых в биотехнологической промышленности, и обосновать приоритетный список микроорганизмов, наиболее опасных для развития аллергических заболеваний.
Для микроорганизмов родов Lactobacillus, Micrococcus, Rhodococcus и др., не проявляющих сенсибилизирующих и иммунотропных свойств, после исследования патогенных свойств возможно установление групповых (родовых) нормативов.
Промышленные микроорганизмы (Bacillus subtilis, Bacillus licheniformis, Streptomyces, Trichoderma), обладающие слабыми аллергенными свойствами, могут быть исследованы по укороченной программе (патогенные, иммунотропные, в том числе сенсибилизирующие свойства).
Для биотехнологических штаммов, принадлежащих к родам Pseudomonas, Alcaligenes, Penicillium, Aspergillus, Candida и обладающих выраженными сенсибилизирующими свойствами, необходимо проведение исследований по полной программе, включая изучение всех наблюдаемых эффектов (патогенность, функционально-метаболическая активность фагоцитов респираторного тракта, иммунотропный, сенсибилизирующий и дисбиотический эффекты). Микроорганизмы этих родов составляют приоритетный перечень биотехнологических штаммов в плане контроля и оценки риска их воздействия на здоровье работников.
В ходе проведения исследований были усовершенствованы подходы к определению уровней микробного загрязнения в воздухе производственных помещений и атмосферном воздухе, что позволяет осуществлять эффективный контроль за соблюдением гигиенических регламентов в условиях расширения биотехнологического производства.
Установлено, что бактериальные формы, используемые в промышленных целях, различаются своим отношением к широкому спектру антибиотиков (30 наименований), принадлежащих к различным группам в зависимости от химической структуры: β-лактамы (пенициллины, аминопенициллины, карбоксипенициллины и цефалоспорины), аминогликозиды, тетрациклины, макролиды, линкозамины, гликопептиды, рифамицины, сульфаниламиды, полимиксины, нитрофураны.
Так, грамположительные бактерии являются чувствительными к антибиотикам. Их устойчивость составляет 0-33%. Исключением, пожалуй, является B. thuringiensis, резистентность которого составляет 48% от испытанных антибиотиков. Устойчивость Rhodococcus к антибиотикам также невысока и составляет 24-30%. Наиболее резистентными штаммами являются грамотрицательные бактерии, их устойчивость к антибиотикам составляет 54-91% (рис. 4).
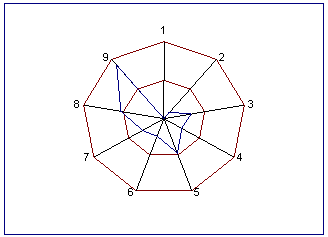

Рис.4 Диаграмма антибиотикорезистентности биотехнологических штаммов: 1 – B.subtilis 103, 2 – В. subtilis 65, 3 – В. subtilis 72, 4 – B.licheniformis 1001, 5 – B. thuringiensis var.israelensis, 6 – R. erythropolis КД, 7 – R. corallinus, 8 – A.denitrificans С-32, 9 – P.caryophylii КМ 92-102/1
Полученные экспериментальные данные были использованы для усовершенствования методов индикации и идентификации новых биотехнологических штаммов, что позволяет ускорить разработку и повысить эффективность методов контроля микробного загрязнения производственных помещений и атмосферного воздуха.
4. Разработка и апробация модели тучноклеточной популяции в токсиколого-гигиенических исследованиях
Принимая во внимание полифункциональный характер действия тучных клеток, оценка их секреторной активности является перспективным направлением при гигиеническом нормировании факторов окружающей среды [, , 1982, , 2001]. С одной стороны, тучные клетки являются клетками-мишенями для специфических IgE при реализации аллергического процесса и широко используются в этом плане. С другой стороны, дегрануляция тучных клеток может осуществляться неиммунологическим путем при действии химических веществ – либераторов гистамина [, , 1976, , 1979, и др., 1987, , 2000].
Нами разработана и апробирована модель тучноклеточной популяции при гигиеническом нормировании биологических и химических факторов. Морфо-функциональная оценка секреторной активности тучноклеточной популяции включает построение цитограммы по фазам секреторного цикла, определение индексов дегрануляции и насыщения тучных клеток, а также составление цитограммы пула дегранулированных клеток.
|
|
Рис.5 Фазы секреторного цикла тучноклеточной популяции при ингаляции промышленных микроорганизмов. По оси x: а – A.denitrificans (к – контроль, а – 4х104 , А – 4х105 кл/м3), б – плесневые грибы (к – контроль, р – P.funiculosum 104 кл/м3, а – A.awamori 2х104 кл/м3, A – A.awamori 2х105 кл/м3). 1,2, 3, 4 – фазы секреции тучных клеток. По оси y - % тучных клеток
Показано, что ингаляция микроорганизмов, обладающих сенсибилизирующими свойствами, вызывала значимые изменения секреторной активности тучноклеточной популяции в сторону увеличения числа дегранулированных форм (рис.5 а, б). Одновременно с этим изменялась и структура пула дегранулированных клеток, среди которых преобладали опустошенные, лишенные гранул клетки (рис.6 А, Б). При этом наблюдаемые изменения секреторной активности тучноклеточной популяции подчинялись зависимости концентрация – эффект, что позволило точно дифференцировать уровни воздействия вредного фактора, в том числе и минимальные, отражающие адаптивные реакции организма на клеточном уровне.
|
|
Рис.6 Цитограмма пула дегранулированных тучных клеток при ингаляции промышленных микроорганизмов. По оси x: А – (к – контроль, а – A.denitrificans 4 х104 , А – A.denitrificans 4х105 кл/м3), Б – (к – контроль, в – B.licheniformis 5х104, В – B.licheniformis 5х105, р – P.funiculosum 104, а – A.awamori 2х104 кл/м3;1 – слабо, 2 – умеренно и 3 – сильно дегранулированные формы тучных клеток. По оси y - %
Разработанная модель тучноклеточной популяции была апробирована при гигиеническом нормировании химических веществ, обладающих различным механизмом действия: мерказолил (сенсибилизация), пиракрил (гонадотропное действие).
Так, при введении пиракрила в дозе 5.0 мг/кг состояние тучноклеточной популяции характеризовалось усилением инфильтрации клеток в органы (матки и яичников) репродуктивной системы и снижением депонирующих форм тучных клеток. При этом наибольшие структурно - функциональные изменения популяции наблюдались в восстановительном периоде, которые выражались в резком снижении депонирующих форм и увеличением дегранулирующих клеток, что обусловлено высокой кумулятивной активностью препарата (рис.7).
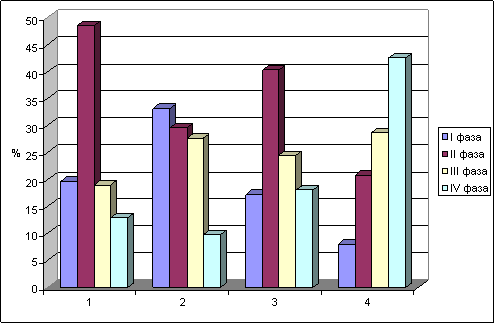

подострый период восстановительный период
Рис.8 Фазы секреторного цикла тучноклеточной популяции матки при введении пиракрила в дозе 5.0 мг/кг в течение 1 месяца (подострый период) и через 1 месяц после окончания введения (восстановительный период). 1, 3 – контроль, 2, 4 – опыт.
Вместе с тем изменения секреторной активности тучноклеточной популяции органов репродуктивной системы при воздействии пиракрила коррелировали с изменениями гормонального статуса (снижение эстрогенов), удлинением эстрального цикла и нарушением морфологической структуры репродуктивных органов (отек, расширение сосудов, лимфо - и гемостаз).
Авторы полагают, что нарушение женской репродуктивной функции при действии пиракрила осуществляется за счет местных гистамин-эстрогеновых отношений и последующего влияния на гипоталямо-гипофизарные механизмы регуляции репродукции [, 1987, , 1987, ,1988, , 1990].
Таким образом, морфофункциональная оценка тучноклеточной популяции представляет собой адекватную модель как для установления минимально эффективных уровней воздействия биологических и химических факторов окружающей среды, так для определения характера их вредного действия на организм, а наиболее информативными показателями ее являются индекс дегрануляции и насыщения, а также структура пула дегранулированных тучных клеток.
5. Оценка микроэкологии кишечника животных при гигиеническом нормировании микроорганизмов, используемых в биотехнологии
При проведении токсиколого-гигиенических исследований оценка микроэкологического баланса кишечника включала количественную и качественную характеристику реакции аутохтонной микрофлоры в ответ на воздействие штаммов в минимально эффективных концентрациях/дозах.
Показано, что ингаляция грамположительных бактерий и нокардиоформных актиномицетов в концентрациях 105, 106, 107 и 108 кл/м3 вызывали слабую ответную реакцию со стороны условно-патогенной микрофлоры, которая выражалась в изменении частоты высеваемости отдельных ее представителей (E.coli,энтерококки, Proteus).
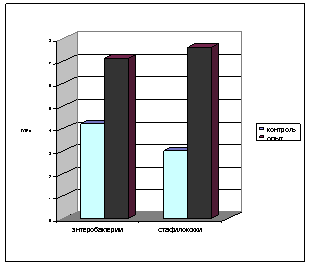
Воздействие грамотрицательных бактерий приводило к более существенным сдвигам микробного баланса в кишечнике. Менялась не только частота высеваемости представителей микрофлоры (лактозоположительные E.coli, стафилококки, клостридии, энтерококки), но и концентрация отдельных представителей условно-патогенной микрофлоры (стафилококки, энтеробактерии) (рис.8 б).
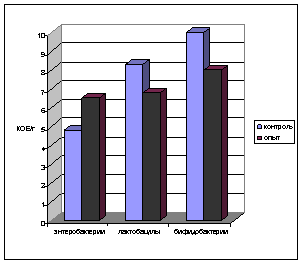
Наибольшие изменения были отмечены при воздействии плесневых грибов на уровне 104 и 105 кл/м3. Они затрагивали не только наиболее реактивную часть микробиоценоза, но и касались ее облигатной части – бифидобактерий и лактобацилл (рис.8 а). Воздействие плесневых грибов вызывало также изменение широкого спектра условно-патогенной микрофлоры, о чем свидетельствовала оценка частоты их высеваемости (рис.9).
а |
б |
Рис.8 Количественная характеристика нарушений микроэкологического баланса кишечника при ингаляции A.awamori, A.terreus, P.funiculosum (а) и энтеральном введении P.caryophylii, A.denitrificans (б)

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




 а
а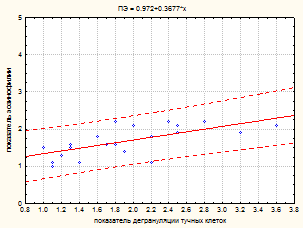 б
б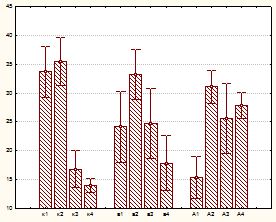 а
а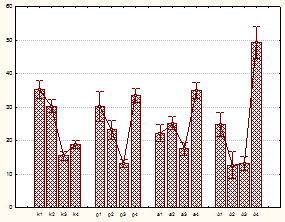 б
б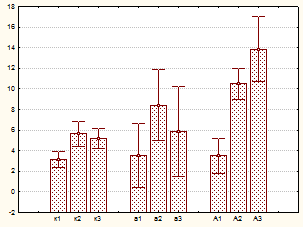 А
А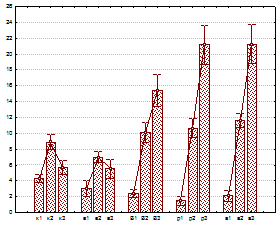 Б
Б