Таблица 12
Результаты количественного определения таблеток ладастена
(прямое прессование) методом УФ-СФМ
Номер серии | Серия 1 | Серия 2 | Серия 3 |
Содержание, г/табл | 0,05008 | 0,04897 | 0,04934 |
Метрологические характеристики (Р=95%, n=5) |
|
|
|
Таблица 13
Результаты количественного определения таблеток ладастена
(влажное гранулирование) методом УФ-СФМ
Номер серии | Серия 1 | Серия 2 | Серия 3 |
Содержание, г/табл | 0,0509 | 0,0505 | 0,0501 |
Метрологические характеристики (Р=95%, n=5) |
|
|
|
В качестве альтернативного метода определения количественного содержания ладастена в лекарственной форме был применен метод ВЭЖХ.
Исследования проведены на колонке Ultra 5 мкм C18 (250 x 4,6 мм) с предколонкой Ultra 5 мкм C18 (30 x 4,6 мм), в подвижной фазе – ацетонитрил – метанол – вода очищенная, доведенная до рН 2,50 ± 0,05 фосфорной кислотой (7:2:1); скорость потока 1,0 мл/мин; режим элюирования – изократический, аналитическая длина волны – 260 нм.
В этих условиях разделение пиков АПБФА и ПБА происходило не полностью, однако скорость проведения анализа значительно увеличивалась, по сравнению со скоростью анализа при определении посторонних примесей.
Линейная зависимость площадей пиков от концентрации растворов ладастена наблюдалась в интервале от 0,0005 до 0,015 мг/мл; коэффициент корреляции 0,9998. Рабочая концентрация растворов ладастена – 0,01 мг/мл. Предел количественного определения ладастена составлял 0,016 мкг, предел обнаружения – 0,008 мкг.
Точность и сходимость методики оценивали для обоих составов таблеток, путем анализа модельных смесей известных количеств ладастена с плацебо на уровне 80 – 120% от концентрации действующего вещества в испытуемом растворе (0,01 мг/мл). Относительная ошибка разработанной методики количественного определения содержания ладастена в модельных смесях разного состава не превышала 0,5 % (табл. 14, 15).
Содержание ладастена во всех образцах таблеток соответствовало требованиям ГФ XI издания (50 мг ± 7,5%) (см. табл. 16, 17).
Таблица 14
Результаты количественного определения ладастена методом ВЭЖХ
на модельных смесях для таблеток, полученных прямым прессованием
Взято ладастена, г | 0,0202 | 0,0213 | 0,0225 | 0,0242 | 0,0250 |
Найдено ладастена, г | 0,02024 | 0,02142 | 0,02233 | 0,02401 | 0,02501 |
Метрологические характеристики (Р=95%, n=5) |
|
|
|
|
|
Взято ладастена, г | 0,0263 | 0,0276 | 0,0290 | 0,0300 | |
Найдено ладастена, г | 0,02633 | 0,02725 | 0,02910 | 0,02963 | |
Метрологические характеристики (Р=95%, n=5) |
|
|
|
|
Таблица 15
Результаты количественного определения ладастена методом ВЭЖХ
на модельных смесях для таблеток, полученных влажным гранулированием
Взято ладастена, г | 0,0202 | 0,0213 | 0,0224 | 0,0238 | 0,0250 |
Найдено ладастена, г | 0,02023 | 0,02141 | 0,02231 | 0,02362 | 0,02501 |
Метрологические характеристики (Р=95%, n=5) |
|
|
|
|
|
Взято ладастена, г | 0,0265 | 0,0276 | 0,0288 | 0,0300 | |
Найдено ладастена, г | 0,02634 | 0,02762 | 0,02901 | 0,02985 | |
Метрологические характеристики (Р=95%, n=5) |
|
|
|
|
Подлинность таблеток ладастена обоих составов было предложено определять с помощью методов УФ-спектрофотометрии и ВЭЖХ.
Разработку теста «Растворение» таблеток ладастена проводили на приборе «Лопастная мешалка», скорость вращения – 100 об/мин, температура – 37 ± 1°С. Среда растворения – 2% водный раствор натрия додецилсульфата (NaДС). Объем среды растворения 900 мл. Количественное содержание ладастена в растворе определяли методом УФ-спектрофотометрии при 258 нм.
Из всех образцов таблеток за 300 минут в раствор высвобождалось не менее 60% ладастена. Кинетика растворения представлена на рисунке 4.
Таблица 16
Результаты количественного определения таблеток ладастена
(прямое прессование) методом УФ-спектрофотометрии
Номер серии | Серия 1 | Серия 2 | Серия 3 |
Содержание, г/табл | 0,04992 | 0,04891 | 0,04930 |
Метрологические характеристики (Р=95%, n=5) |
|
|
|
Таблица 17
Результаты количественного определения таблеток ладастена
(влажное гранулирование) методом УФ-спектрофотометрии
Номер серии | Серия 1 | Серия 2 | Серия 3 |
Содержание, г/табл | 0,05072 | 0,05015 | 0,05001 |
Метрологические характеристики (Р=95%, n=5) |
|
|
|
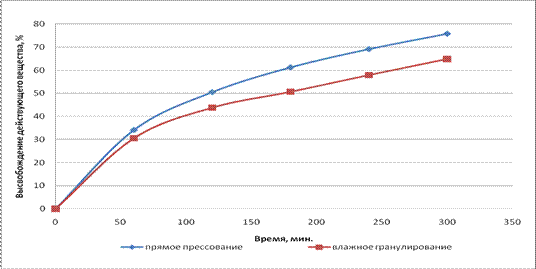
Рис. 4. Кривая зависимости высвобождения ладастена из таблеток от времени эксперимента
Установление сроков годности таблеток ладастена
Для изучения стабильности таблеток ладастена, полученных прямым прессованием, при хранении, был использован метод «ускоренного старения» при 40 ºС. Качество препарата по истечении срока хранения, эквивалентного 2 годам хранения в естественных условиях, практически не изменилось. Установлен предварительный срок годности 2 года.
Таблетки ладастена, полученные влажным гранулированием, хранили в естественных условиях, в защищенном от света месте. Качество препарата не изменилось при хранении в течение 1 года, исследования продолжаются.
На основании проведенных исследований были установлены предварительные нормы качества таблеток ладастена полученных прямым прессованием и влажным гранулированием, представленные в таблицах 18, 19.
Таблица 18
Нормы качества таблеток ладастена 50 мг, полученных прямым прессованием
Показатели | Метод испытания | Нормы |
Описание | Визуально | Таблетки белого или почти белого цвета плоскоцилиндрической формы, с риской |
Подлинность | УФ-спектрофотометрия | УФ-спектр испытуемого раствора в области от 200 до 350 нм должен иметь максимум поглощения при (258±2) нм |
ВЭЖХ | Время удерживания основного пика на хроматограмме испытуемого раствора должно совпадать со временем удерживания пика ладастена на хроматограмме раствора стандарта | |
Средняя масса | ГФ ХI, вып.2, с.154 | От 0,185 г до 0,215 г (0,2 ± 7,5%) |
Отклонение от средней массы | ГФ ХI, вып.2, с.154 | 18/20: ± 7,5%; 2/20: ± 15% |
Распадаемость | ГФ ХI, вып.2, с.154 | Не более 15 мин |
Однородность дозирования | ВЭЖХ | 1/10 ± 15 %; 0/10 ± 25 % |
Посторонние примеси | ВЭЖХ | Единичной примеси: не более 0,2%; сумма примесей: не более 0,5% |
Микробиологи-ческая чистота | ГФ ХII | Категория 3А |
Растворение | ГФ ХI, вып.2, с.154 и ОФС , СФМ | Не менее 60% за 240 минут |
Количественное определение | ВЭЖХ | От 0,04625 г до 0,05375 г (0,05 ±7,5%) |
Срок годности | 2 года |
Таблица 19
Нормы качества таблеток ладастена 50 мг, полученных влажным гранулированием
Показатели | Метод испытания | Нормы |
Описание | Визуально | Таблетки белого или почти белого цвета плоскоцилиндрической формы, без риски |
Подлинность | СФМ | УФ-спектр испытуемого раствора в области от 200 до 350 нм должен иметь максимум поглощения при длине волны (258±2) нм |
ВЭЖХ | Время удерживания основного пика на хроматограмме испытуемого раствора должно совпадать со временем удерживания пика ладастена на хроматограмме раствора стандарта | |
Средняя масса | ГФ ХI, вып.2, с.154 | От 0,09 г до 0,110 г (0,1 ± 10 %) |
Отклонение от средней массы | ГФ ХI, вып.2, с.154 | ± 10% |
Распадаемость | ГФ ХI, вып.2, с.154 | Не более 15 мин |
Однородность дозирования | СФМ | 1/10 ± 15 %; 0/10 ± 25 % |
ВЭЖХ | ||
Посторонние примеси | ТСХ | Единичной примеси: не более 0,2%; сумма примесей: не более 0,5% |
ВЭЖХ | ||
Микробиологи-ческая чистота | ГФ ХII | Категория 3А |
Растворение | ГФ ХI, вып.2, с.154 и ОФС , СФМ | Не менее 60% за 240 минут |
Количественное содержание | СФМ | от 0,04625 г до 0,05375 г (0,05 ± 7,5%) |
ВЭЖХ | ||
Срок годности | 2 года |
ОБЩИЕ ВЫВОДЫ:
1. Впервые изучены физико-химические свойства, спектральные характеристики и основные показатели качества лекарственных форм тропоксина и ладастена.
2. Проведены исследования хроматографического поведения тропоксина и ладастена в лекарственных формах, а также полупродуктов их синтеза и продуктов деструкции методами ТСХ и ВЭЖХ. Разработаны методики определения посторонних примесей в лекарственных формах тропоксина и ладастена.
3. Разработаны методики количественного определения тропоксина и ладастена в таблетках с помощью методов УФ-спектрофотометрии и ВЭЖХ.
4. Разработаны методики проведения теста «Растворение» и установлены нормы качества по этому показателю для таблеток ладастена обоих составов и таблеток тропоксина, изготовленных методом прямого прессования.
5. Изучена устойчивость лекарственных форм тропоксина и ладастена при хранении методом «ускоренного старения» и в естественных условиях, установлены предварительные сроки годности лекарственных препаратов.
6. На основании проведенных исследований установлены нормы качества лекарственных форм тропоксина и ладастена. Разработаны проекты ФСП на препараты.
По теме диссертации опубликованы следующие работы:
1. , , Коночкина (Дуденкова) М. Е., Пятин методов анализа субстанции ладастена и сиднокарба при их совместном присутствии // X Российский национальный конгресс «Человек и лекарство», тезисы докладов. Москва. 2003. с. 612.
2. , , Коночкина (Дуденкова) М. Е., , Алексеев состава и методик анализа таблеток ладастена, полученных прямым прессованием // Вестник Российского Университета Дружбы Народов. 2008. №4. С. 10-15.
3. Коночкина (Дуденкова) М. Е., , Пятин методик и норм качества таблеток ладастена, изготовленных методом прямого прессования // XVII Российский национальный конгресс «Человек и лекарство», тезисы докладов. Москва. 2010. с. 525.
4. Коночкина (Дуденкова) М. Е., , Пятин методик и норм качества таблеток тропоксина, изготовленных методом прямого прессования. // XVII Российский национальный конгресс «Человек и лекарство», тезисы докладов. Москва. 2010. с. 525.
5. Коночкина (Дуденкова) М. Е., , Пятин методики определения остаточных растворителей (ОР) в субстанции тропоксина. // 5-я Международная конференция «Биологические основы индивидуальной чувствительности к психотропным средствам». Москва. 2010. с. 53.
6. , ,, , Карбушева методики определения посторонних примесей в субстанции и таблетках тропоксина с помощью ВЭЖХ. // Химико-фармацевтический журнал. 2011. Т.45. № 12. С. 52-56.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |



