БИОФИЗИЧЕСКИЕ МЕХАНИЗМЫ ФИЗИОЛОГИЧЕСКОГО, БИОЛОГИЧЕСКОГО ДЕЙСТВИЯ КСЕНОНА (ИНЕРТНЫХ ГАЗОВ) Довгуша В.В. ФГУП НИИ промышленной и морской медицины ФМБА России.
Действие на организм инертных газов, как наркотических веществ, свидетельствует об отсутствии химических процессов или реакций. Молекулы наркотического вещества в процессе взаимодействия с нервной клеткой ничего не окисляют и не восстанавливают, сами химически не изменяются, но тем не менее, вызывают наркоз. Действительно, для протекания любой химической реакции почти наверняка требовалось бы участие ферментов, а поскольку ферменты стереоспецифичны, то левая и правая формы наркотического вещества вели бы себя при этом различно. Собственно говоря, в контексте рассматриваемого нами вопроса, они и ведут себя по-разному – одни вещества, например, левовращающий изомер морфина, обладают сильными наркотическими свойствами, а их оптические правовращающие изомеры – нет. По-видимому, определённые изомеры биологически активных веществ, в т.ч. и наркотиков, пространственно соответствуют реакционным центрам рецепторов мембран. Основную роль при этом, вероятно, играет поляризованное излучение кластеров.
Нами отмечено, что чем меньше у газов магнитная восприимчивость, тем относительная наркотическая активность больше (табл. 1).
Таблица 1
Газ | Отношение растворимости в масле к растворимости в воде | Магнитная молекулярная восприимчивость х 106 | 1/2 | Средняя поляризуемость (α- ⋅ 1024 см3) |
He | 1,7 | -1,9 | -1 | 0,202 |
Ne | 2,07 | -7,7 | -4 | 0,392 |
H2 | 2,1 | -4,0 | -2 | - |
N2 | 5,24 | -11,8 | -2 | - |
Ar | 5,3 | -19,73 | -4 | 1,629 |
Kr | 9,6 | ~ -40,0 * | -4 | 2,46 |
Xe | 20,0 | ~ -80,0 * | -4 | 4,00 |
O2 | 5,0 | +3380 | 676 | - |
CO2 | 1,6 | -18,93 | -12 | - |
* Расчётный метод.
Эта же закономерность отмечается исходя из данных магнитной поляризуемости. Поляризуемость – коэффициент, связывающий электрический момент атома (иона, молекулы) с напряжённостью электрического поля. Характерно, что отношение коэффициента растворимости масло/вода к показателю магнитной восприимчивости у всех инертных газов приблизительно одинаково – около – 4-х (у азота – 2).
Каждая молекула газа индивидуальна по своим частотным характеристикам. Любая молекула имеет свою ЭМ-характеристику, которая создаётся всей структурой молекулы, в том числе и пространственной. Одна и та же частотно-полевая характеристика возможна у различных молекул газа (например, N2O и Xe), различных по структуре, но скоординированных по частоте структурированной водой организма при нормальном давлении.
Нами отмечено, что основные линии в атомном спектре жизненно важных элементов находятся на уровне длины - 400 ± 37 нм (рис.1). Основные линии в атомном спектре инертных газов находятся на уровне ≈ 800 ± 27 нм как линии нейтральных атомов. Чем больше длина волны, тем меньше частота (рис. 2).
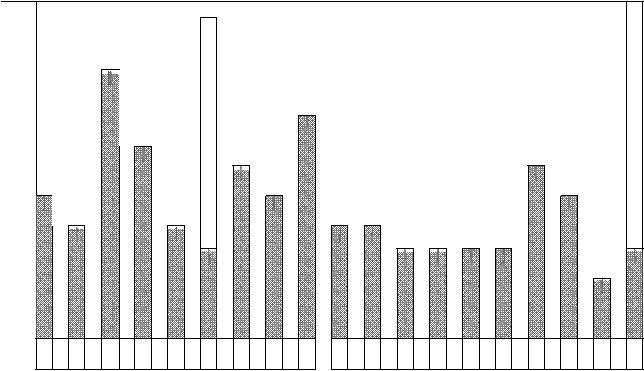 λ, нм
λ, нм
100
0
800
600
400
200
0
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() Рис. 1. Основные линии в атомном спектре жизненно важных элементов
Рис. 1. Основные линии в атомном спектре жизненно важных элементов
λ, нм
 1200
1200
1000
800
600
400
200
0
Н Не Ne Ar Kr Xe Rn N

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |




