Практическое занятие № 12
Гравиметрия
Аудиторные занятия
92. Какую навеску купороса FeSO4·7H2O требуется взять для определения в нем железа в виде оксида Fe2O3, считая, что оптимальная масса Fe2O3 равна 0,2 г?
93. Какую массу пирита, содержащего около 30% серы, нужно взять для анализа, чтобы получить 0,3 г осадка сульфата бария?
94. Для определения содержания в природном известняке карбоната кальция, анализируемый образец массой 100 г подвергли термическому разложению, а весь выделившийся при этом углекислый газ поглотили натронной известью. Масса приемника до отгонки СО2 составила 150 г, после отгонки – 176,4 г. Определите массовую долю карбоната кальция в природном известняке.
95. Для анализа производственных сточных вод на содержание сульфат-иона отобрали пробу 200,0 мл и осадили определяемый ион в виде сульфата бария BaSO4. Масса прокаленного осадка BaSO4 составила 0,04213 г. Вычислите концентрацию сульфат-ионов (в мг/л) в пробе.
96. Навеску удобрения массой 2,634 г растворили в соляной кислоте и разбавили до 250,0 см3. В 50,00 см3этого раствора осадили MgNH4PO4 и прокалили осадок до Mg2P2O7, масса которого оказалась равной 0,3062 г. Вычислить массовую долю (в %) P2O5 во влажном и абсолютно сухом удобрении, если содержание влаги в образце 8,50%.
Домашнее занятие.
97. Какую навеску смеси, состоящей из 30% Na2SO4 и 70% К2SO4, следует взять для анализа на содержание ![]() , чтобы масса прокаленного осадка была не более 0,2 г?
, чтобы масса прокаленного осадка была не более 0,2 г?
98. Какой объем раствора (NH4)2C2O4·H2O с массовой долей 3,5% (r = 1 г/см3), потребуется для осаждения оксалата кальция из навески апатита 3Сa3(PO4)3·CaF2 массой 0,15 г при стехиометрическом соотношении реагирующих веществ?
99. Для определения состава глауберовой соли общей формулы 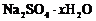 образец массой 80,5 г прокалили при 110°С до постоянной массы. При этом масса сухого остатка составила 35,5 г. Определите формулу кристаллогидрата сульфата натрия.
образец массой 80,5 г прокалили при 110°С до постоянной массы. При этом масса сухого остатка составила 35,5 г. Определите формулу кристаллогидрата сульфата натрия.
100. Из навески серебряного сплава массой 0,2466 г после соответствующей обработки был получен осадок хлорида серебра массой 0,2675 г. Вычислите массовую долю серебра в сплаве.
101. В растворе, приготовленном из железного купороса FeSO4·7H2O, железо(II) окислили азотной кислотой до железа(III), а затем осадили раствором аммиака в виде гидроксида железа(III). Масса прокаленного осадка оксида железа(III) составила 0,2662 г. Напишите уравнения всех проведенных реакций и вычислите содержание в растворе ионов железа(II) и железного купороса.
Практическое занятие № 13
Физико-химические методы анализа
102. При определении ванадия методом добавок навеску стали в 0,5000 г растворили, объем раствора довели до 50,0 см3. Затем аликвоты раствора по 20 см3 отобрали в две мерные колбы на 50 см3. В одну из них добавили навеску соли ванадия, содержащую 0,0030 г ванадия. В обе колбы добавили перекись водорода и объемы довели до метки. Вычислить процентное содержание ванадия в стали, если при фотометрировании получили следующие результаты: Ах = 0,24, Ах+ст = 0,38.
103. Для определения HF используют зависимость удельной электропроводности c от содержания кислоты в растворе:
СHF, моль/дм3 | 0,004 | 0,007 | 0,015 | 0,030 | 0,060 | 0,121 | 0,243 |
c×104, Ом–1×см–1 | 2,5 | 3,8 | 5,0 | 8,0 | 12,3 | 21,0 | 36,3 |
Постройте по этим данным градуировочный график в координатах lgc – lgСHF и с его помощью определите концентрацию фтороводородной кислоты в растворе, удельная электропроводность которого составляет 3,2×10–4 Ом–1×см–1.
104. Построить кривые потенциометрического титрования в координатах рН – V, ![]() рН/
рН/![]() V – V. Определить концентрацию соляной кислоты, если на титрование 20,00 см3 анализируемого раствора кислоты 0,1000 н. раствором NaOH получили следующие результаты:
V – V. Определить концентрацию соляной кислоты, если на титрование 20,00 см3 анализируемого раствора кислоты 0,1000 н. раствором NaOH получили следующие результаты:
VNaOH, cм3 | 10,0 | 18,0 | 19,0 | 19,9 | 20,0 | 20,1 | 21,0 | 22,0 |
рН | 1,48 | 2,28 | 2,59 | 3,60 | 7,00 | 10,60 | 11,49 | 11,68 |
105. Для определения содержания кадмия в сплаве методом добавок навеску сплава в 3,5420 г растворили и после соответствующей обработки объем раствора довели до 250,0 см3. Для снятия полярограммы взяли 18,0 см3 этого раствора. Высота полуволны оказалась 19,5 мм. После добавки 2,0 см3 0,04300 н. раствора сульфата кадмия(II) высота волны увеличилась до 21,5 мм. Определите процентное содержание кадмия в сплаве.
Домашнее занятие.
106. Навеску n-нитробензойной кислоты O2N – C6H4 – COOH массой 0,0492 г. растворили в 50,00 см3 смеси спиртов и 5,00 см3 полученного раствора оттитровали 0,0200 М раствором метилата натрия спектрофотометрическим методом. Постройте кривую титрования и рассчитайте массовую долю кислоты в навеске по следующим данным:
V (р-ра CH3ONa), см3 | 0,6 | 0,8 | 1,0 | 1,2 | 1,4 | 1,6 | 1,8 |
А | 0,255 | 0,340 | 0,420 | 0,500 | 0,565 | 0,555 | 0,545 |
107. В две мерные колбы вместимостью 100,0 см3 поместили по 10,00 см3 сточной воды. В одну колбу добавили 10,00 см3 стандартного раствора CuSO4 с Т(Cu) = 0,001000 г/см3. В обе колбы ввели растворы аммиака, рубеановодородной кислоты и разбавили водой до метки. При фотометрировании получили следующие значения оптической плотности: Ах = 0,240, Ах+ст = 0,380.
108. В стандартных растворах NaF были измерены электродные потенциалы фторидселективного электрода относительно хлорсеребряного электрода и получены следующие данные:
| 1 × 10–1 | 1 × 10–2 | 1 × 10–3 | 1 × 10–4 | 1 × 10–5 |
Е, мВ | 100 | 140 | 190 | 230 | 275 |
Исследуемый раствор, содержащий фторид-ион, объемом 10,00 см3 разбавили водой до 50,00 см3 и измерили электродный потенциал фторидселективного электрода в полученном растворе, значение которого оказалось равным 210 мВ. Определите активность фторид-иона в исследуемом растворе.
109. При полярографировании стандартных растворов свинца(II) получили следующие результаты
| 0,25 | 0,50 | 0,75 | 1,00 | 1,25 |
h, мм | 2,0 | 4,0 | 6,0 | 8,0 | 10,0 |
Навеску сплава массой 4,848 г растворили и раствор разбавили до 50,00 см3. Высота полярографической волны свинца в полученном растворе оказалось равной 7,2 мм. Вычислите массовую долю (%) свинца в образце.
Таблица 1. Константы диссоциации некоторых слабых электролитов
Формула электролита | Кi | Кd | pКd | Формула электролита | Кi | Кd | pКd |
Кислоты | H2CO3 | К1 | 4,5×10–7 | 6,35 | |||
СH3СООН | К1 | 1,74×10–5 | 4,76 | К2 | 4,8×10–11 | 10,32 | |
HСООН | К1 | 1,78×10–4 | 3,75 | HF | К1 | 6,8×10–4 | 3,17 |
HCN | К1 | 5,01×10–10 | 9,30 | H2SO3 | К1 | 1,4×10–2 | 1,85 |
HNO2 | К1 | 6,90×10–4 | 3,16 | Основания | |||
NH4OН | К1 | 1,76×10–5 | 4,75 |
Таблица 2. Термодинамические значения произведения растворимости некоторых труднорастворимых электролитов при 25°С
Формула электролита | ПР° | Формула электролита | ПР° | Формула электролита | ПР° |
AgBr | 5,3010–13 | BaSO4 | 1,10×10–10 | Hg2Cl2 | 1,32×10–18 |
AgCl | 1,78×10–10 | СаC2O4 | 2,29×10–9 | Hg2SO4 | 6,76×10–7 |
Ag2СO3 | 8,13×10–12 | Ca3(PO4)2 | 1,00×10–26 | PbCrO4 | 1,18×10–14 |
Ag2СrO4 | 1,10×10–12 | СaSO4 | 9,12×10–6 | PbSO4 | 1,60×10–8 |
Ag2S | 6,31×10–50 | CdCO3 | 5,20×10–12 |
Таблица 3. Стандартные электродные потенциалы по отношению к потенциалу стандартного водородного электрода при 25°С
Электродный процесс | Е°, В | Электродный процесс | Е°, В |
| +0,09 |
| –1,57 |
| +0,54 | Fe3+ + e ® Fe2+ | +0,77 |
| +1,51 |
| +1,33 |
| +0,94 |
| +0,60 |
Ni2+ + 2e ® Ni0 | –0,23 | Cd2+ + 2e ® Cd0 | –0,40 |
Ag+ + e ® Ag0 | +0,80 |
| +1,19 |
Таблица 4. Константы устойчивости комплексных ионов (данные приведены для температур 25-30°С)
Комплексная частица | β | lgβ | Комплексная частица | β | lgβ |
[Ag(CN)2]– | 7,08×1019 | 19,85 | [Cu(NH3)4]2+ | 1,07×1012 | 12,03 |
[Ag(S2O3)2]3– | 2,88×1013 | 13,46 | [Ni(NH3)4]2+ | 2,95×107 | 7,47 |
[Ag(NH3)2]+ | 1,74×107 | 7,24 | [Zn(NH3)4]2+ | 3,85×109 | 9,59 |
[Co(NH3)4]2+ | 1,18×105 | 5,07 |

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




