Лучевая болезнь, заболевание, возникающее от воздействия различных видов ионизирующих излучений. Человек, животные, микроорганизмы и растения постоянно подвергаются извне действию гамма-излучений земной коры, космических лучей и изнутри облучаются находящимися в организме человека в ничтожных количествах радиоактивными веществами (46K, 226Ra, 222Rn, 14C и др.). Развитие лучевой болезни. наступает лишь тогда, когда суммарная доза облучения начинает превышать естественный радиоактивный фон. Способность радиации вызывать лучевую болезнь зависит от биологического действия ионизирующих излучений; чем больше поглощённая доза излучения, тем сильнее выражено поражающее действие радиации.
У человека лучевая болезнь может быть обусловлена внешним облучением, когда источник его находится вне организма, и внутренним - при попадании радиоактивных веществ в организм с вдыхаемым воздухом, через желудочно-кишечный тракт или кожу. Лучевая болезнь может развиться при относительно равномерном облучении всего тела, какого-либо органа или участка организма. Различают острую лучевую болезнь, возникающую от однократного общего облучения в сравнительно больших дозах (сотни рад), и хроническая форму, которая может быть результатом перенесённой острой лучевой болезни либо хронического воздействия малыми дозами (единицы рад).
Общие клинические проявления лучевой болезни зависят главным образом от полученной суммарной дозы. При однократном общем облучении дозой до 100 р (порядка 1 Гр) происходят сравнительно лёгкие изменения, которые могут рассматриваться как состояние так называемой предболезни. Дозы свыше 100 р вызывают те или иные формы лучевой болезни (костно-мозговую, кишечную) разной тяжести, при которых основные проявления и исход лучевой болезни зависят главным образом от степени поражения органов кроветворения.
Дозы однократного общего облучения свыше 600 р (более 6 Гр) считают абсолютно смертельными; гибель наступает в сроки от 1 до 2 мес после облучения. При наиболее типичной форме острой лучевой болезни вначале, через несколько минут или часов, у получивших дозу больше 200 р возникают первичные реакции (тошнота, рвота, общая слабость). Через 3-4 сут симптомы стихают, наступает период мнимого благополучия. Однако тщательное клиническое обследование выявляет дальнейшее развитие болезни. Этот период продолжается от 14-15 суток до 4-5 недель.
В последующем ухудшается общее состояние, нарастает слабость, появляются кровоизлияния, повышается температура тела. Количество лейкоцитов в периферической крови после кратковременного увеличения прогрессивно уменьшается, падая (вследствие поражения кроветворных органов) до чрезвычайно низких цифр (лучевая лейкопения), что предрасполагает к развитию сепсиса и кровоизлияний. Продолжительность этого периода 2-3 недели.
Существуют и другие формы лучевой болезни. Например, при общем облучении в дозах от 1000 до 5000 р (10-50 Гр) развивается кишечная форма лучевой болезни, характеризующаяся преимущественно поражением кишечника, ведущим к нарушению водно-солевого обмена (от обильных поносов), и нарушением кровообращения. Человек при этой форме обычно погибает в течение первых суток, минуя обычные фазы развития лучевой болезни. После общего облучения в дозах свыше 5000 р (более 50 Гр) смерть наступает через 1-3 сутки или даже в момент самого облучения от повреждения тканей головного мозга (эта форма лучевой болезни называется церебральной). Другие формы лучевой болезни человека и животных в основном определяются местом облучения.
Особенности течения и степень нарушений при лучевой болезни зависят от индивидуальной и возрастной чувствительности; дети и старики менее устойчивы к облучению, поэтому тяжёлые поражения у них могут возникать от меньших доз излучения. В период эмбрионального развития ткани организма особенно чувствительны к действию радиации, поэтому облучение беременных женщин (например, применение лучевой терапии) нежелательно даже в малых дозах.
Процесс восстановления организма после облучения в умеренных дозах наступает быстро. При лёгких формах лучевой болезни выраженные клинические проявления могут отсутствовать. При более тяжёлых формах лучевой болезни период полного восстановления иногда затягивается до года и больше. Как отдалённые проявления лучевой болезни у женщин отмечается бесплодие, у мужчин - отсутствие сперматозоидов; эти изменения чаще носят временный характер. Через много месяцев и даже лет, после облучения, иногда развивается помутнение хрусталика (так называемая лучевая катаракта). После перенесённой острой лучевой болезни иногда остаются стойкие невротические проявления, очаговые нарушения кровообращения; возможно развитие склеротических изменений, злокачественных новообразований, лейкозов, появление у потомства пороков развития, наследственных заболеваний.
Характерные черты хронической лучевой болезни - длительность и волнообразность её течения. Это обусловлено проявлениями поражения, с одной стороны, и восстановительных и приспособительных реакций - с другой. При преимущественном поражении того или иного органа или ткани отмечается несоответствие между глубиной поражения поврежденных структур и слабо выраженными или поздно проявляющимися признаками общих реакций организма.
На ранних стадиях основные клинические проявления - многообразные нарушения нервной регуляции функций внутренних органов и в первую очередь сердечно-сосудистой системы. Могут возникать изменения ферментативной активности и секреторно-моторной функции желудочно-кишечного тракта; нарушения физиологической регенерации кроветворения вызывают развитие лейкопении. При продолжающемся облучении и прогрессировании заболевания все проявления усугубляются.
Лечение острой лучевой болезни направлено на нормализацию органов кроветворения (пересадка костного мозга, переливание крови, введение препаратов нуклеиновых кислот, стимуляторы кроветворения), борьбу с инфекцией (антибиотики), предупреждение возникновения кровоизлияний (витамины), уменьшение интоксикации (кровопускание, кровозамещение), воздействие на нервную систему и др. При хронической лучевой болезни. назначают питание, богатое белками и витаминами, длительное пребывание на свежем воздухе, лечебную физкультуру; симптоматические средства (сердечные, нейротропные, нормализующие функцию желудочно-кишечного тракта и тому подобное). При нарушении кроветворения - стимулирующие его препараты.
Принятые законодательно нормы предельно допустимых доз и концентраций радиоизотопов для различных производств и профессиональных групп установлены из расчёта общего облучения в дозе не более 50 мЗв/год (5 рад/год) и гарантируют безопасность работы с этими веществами. Опасность облучения может возникнуть при нарушении правил охраны труда или в аварийных ситуациях, в условиях военного времени (применение противником атомного оружия).
Атомные взрывы резко повышают загрязнение внешней среды радиоактивными продуктами деления, вследствие чего в ней увеличивается количество радиоактивного йода (111I), стронция (90Sr), цезия (137Cs), углерода (14C), плутония (239Pu) и других. Возникает угроза опасного для здоровья облучения и увеличения числа наследственных болезней. В подобных случаях решающее значение для профилактики развития лучевой болезни имеет защита от ионизирующих излучений.
2.5.1 Дозы, получаемые человеком от различных источников
Радиационные воздействия на человека отличаются значительной разнообразностью, они могут быть, в зависимости от места нахождения источников относительно организма, подвергшегося воздействию радиации:
- внешними;
- внутренними.
В зависимости от происхождения:
- естественными;
- техногенными (антропогенными).
В зависимости от физического состояния нуклидов:
- газообразными;
- жидкими;
- твердыми.
В зависимости от активности:
- высокоактивными;
- низкоактивными.
В зависимости от нахождения источника ионизирующего излучения:
- земными;
- космическими.
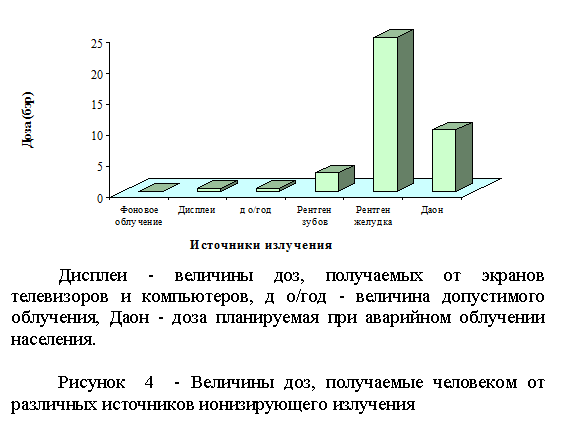
Дозы, получаемые человеком от естественных источников, могут колебаться в значительной степени в зависимости от места проживания и работы. Так жители гор и ландшафтом с повышенным радиационным фоном могут получать в дозы несколько раз превышающие годовые нагрузки жителей равнин. Летчики, альпинисты также получают дополнительные лучевые нагрузки. Допустимые пределы приведены в пункте 10 – нормы радиационной безопасности, а на диаграмме – рисунок - 4, показаны величины доз, получаемые человеком от различных источников.
На диаграмме показаны величины естественного фонового облучения, средние величины доз, получаемых от экранов телевизоров и компьютеров, величина допустимого облучения, дозы, получаемые при рентгене зубов и желудка, и, наконец, планируемая доза при аварийном облучении.

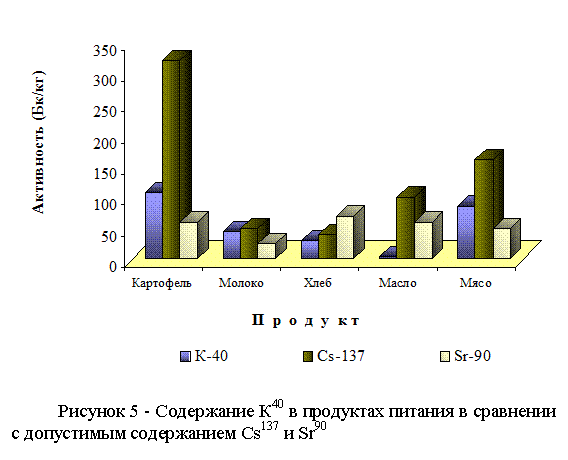
Нормируемой величиной является также содержание некоторых радионуклидов техногенного происхождения в продуктах питания. В первую очередь это относится к радионуклидам цезия-137 и стронция-90. На диаграмме – рисунок 5 - приводится содержание К-40 в продуктах питания в сравнении с допустимым содержанием Cs-137 и Sr-90.
Как следует из диаграммы, во многих продуктах питания содержание естественного радионуклида К40 составляет значительную величину по сравнению с допустимым содержанием Cs-137 и Sr-90. В почве территорий с высокими антропогенными загрязнениями цезием и стронцием, содержание калия-40, как правило, во много раз превышает средние суммарные величины Cs137 и Sr90. Вклад радиоактивного калия составляет 12,3 % от всей величины среднего фонового уровня естественного облучения костного мозга человека и дает основную долю внутреннего облучения.
Естественное облучение костного мозга человека – одного из наиболее чувствительных органов складывается из облучения космическими источниками, суммарная величина которых достигает 50 мкР/год, величина литосферных и атмосферных источников также равна 50 мкР/год.
Из элементов, находящихся в организме существенную роль играет К40, который дает 15 мкР/год, меньший вклад дают другие элементы, находящиеся внутри организма человека – рисунок 6 - радон - 222 адсорбированный в крови дает 3 мкР/год, углерод – 14 – 1,6 мкР/год, радон - 226 и радон -228 и дочерние продукты их распада суммарно дают также 1,6 мкР/год, и, наконец, полоний - 210 и дочерние продукты распада дают 0,4 мкР/год.

2.6 Сравнительные величины радиочувствительности
В таблице 2 приведены данные разных авторов по определению величины LD50 у представителей различных филогенетических групп при общем однократном облучении рентгеновскими или гамма лучами.
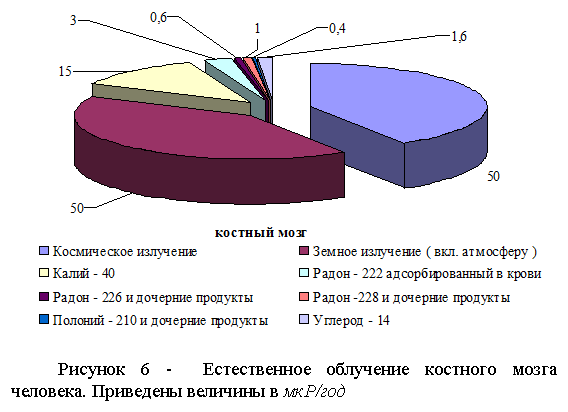

Таблица 2- Радиочувствительность разных групп организмов
Объект | LD50, Гр |
Вирусы | |
Бактерии | |
Высшие растения | 10-1500 |
Беспозвоночные | 30-7000 |
Позвоночные | 20-200 |
Как видно из таблицы, диапазон устойчивости к радиации в живой природе достаточно широк. Наиболее устойчивы к действию ионизирующих излучений микроорганизмы - дозы, способные вызвать их гибель, составляют сотни и тысячи грей. Для беспозвоночных животных диапазон летальных доз обычно на порядок ниже этих величин, а для позвоночных они составляют десятки грей, здесь наиболее чувствительны к радиационным воздействиям млекопитающие. Исходя из данных таблицы 2 можно сделать вывод, что по мере усложнения биологической организации объектов их устойчивость к радиации резко снижается.
Обычно животные, облученные в дозе Гр, живут в среднем (за некоторым исключением) от нескольких дней до нескольких недель. Лучевой синдром в этом диапазоне доз облучения назван «костномозговой» или «кроветворный», ибо решающее значение в его исходе имеет поражение кроветворной системы организма, в первую очередь костного мозга. В результате глубокого торможения процессов клеточного деления происходит опустошение костного мозга. На исход лучевой болезни существенно влияет способность кроветворных органов к восстановлению, которое зависит от количества сохранившихся стволовых клеток.
В интервале доз от 10 до 100 Гр средняя продолжительность жизни млекопитающих практически не зависит от величины поглощенной дозы и составляет в среднем 3,5 сут. Эффект независимости средней продолжительности жизни от величины дозы облучения получил название «3,5-дневный эффект», а возникающий лучевой синдром — «желудочно-кишечный». Летальный исход этого синдрома связан с поражением слизистой кишечника и желудка, высокой чувствительностью к радиации быстро делящихся эпителиальных клеток, оголением ворсинок.
Облучение в дозах, превышающих 100 Гр, приводит к гибели млекопитающих, наступающей в первые несколько дней или даже несколько часов. У гибнущих животных наблюдают явные признаки поражения центральной нервной системы, поэтому этот лучевой синдром называют «церебральный». Происходит резкое подавление жизнедеятельности нервных клеток, реакция которых на облучение принципиально отличается от реакции костного мозга и кишечника отсутствием клеточных потерь.
Если поглощенная доза достигает 1000 Гр и более, животные гибнут сразу же «под лучом». Механизм такого поражения может быть связан с тем, что возникают массовые структурные поражения макромолекул. Иногда лучевой синдром, вызванный облучением в таких высоких дозах ионизирующей радиации, называют молекулярной смертью.
В ответных реакциях организма на действие ионизирующей радиации условно можно выделить три последовательно развивающиеся во времени стадии; физические реакции, биофизические процессы и общебиологические изменения. Физическая стадия - поглощение энергии, ионизация и возбуждение атомов и молекул, образование радикалов - происходит в течение микро - и миллисекунд. Биофизические процессы - внутри - и межмолекулярный перенос энергии, взаимодействие радикалов друг с другом и с неповрежденными молекулами, внутримолекулярные изменения - происходят в течение секунд - миллисекунд. Общебиологические изменения в клетке и организме - образование стабильных измененных молекул, нарушение генетического кода, транскрипции и трансляции, биохимические, физиологические и морфологические изменения в клетках и тканях, иногда заканчивающиеся гибелью организма, могут протекать в течение минут - суток или растягиваться на годы.
Установлено, что разные органы и ткани сильно различаются по своей чувствительности к ионизирующей радиации, а также по роли в лучевой патологии и конечном исходе болезни. По морфологическим изменениям их радиочувствительность располагается (по степени убывания чувствительности) в такой последовательности:
- органы кроветворения;
- половые железы;
- слизистые оболочки, слюнные, потовые и сальные железы, волосяные сосочки, эпидермис;
- желудочно-кишечный тракт;
- печень;
- органы дыхания;
- железы внутренней секреции (надпочечники, гипофиз, щитовидная железа, островки поджелудочной железы, паращитовидная железа);
- органы выделения;
- мышечная и соединительная ткани;
- соматические костная и хрящевая ткани;
- нервная ткань.
Органы кроветворения наиболее радиочувствительны, поражение костного мозга, тимуса, селезенки, лимфатических узлов - одно из важнейших проявлений острой лучевой болезни. Значительные морфологические и функциональные нарушения наблюдаются во всех кроветворных органах, причем изменения в системе крови представляется возможным обнаружить вскоре после действия радиации и даже при относительно небольших дозах облучения.
Обычно процесс клеточного опустошения подразделяют на три стадии. Первая, длящаяся около 3 ч, характеризуется относительным постоянством содержания клеток в кроветворных тканях. Вторая стадия охватывает интервал времени от 3 до 7 ч после облучения, для нее характерно резкое и глубокое опустошение костного мозга и лимфоидных тканей (количество клеток в костномозговой ткани может снижаться более чем наполовину). В третьей стадии скорость клеточного опустошения замедляется и дальнейшее уменьшение количества клеток происходит в костном мозге в результате репродуктивной гибели, а также продолжающейся дифференцировки части клеток и миграции их в кровь. Длительность течения третьей стадии пропорциональна дозе облучения.
Лимфоидная ткань обедняется клеточными элементами раньше, чем ткань костного мозга. Число нейтрофилов при одной и той же дозе облучения снижается медленнее, чем число лимфоцитов. При лучевой патологии наблюдаются морфологические изменения белой крови, гиперсегментирование, фрагментация ядер. Лейкоциты набухают, увеличиваются их размеры и зернистость, накапливаются пигменты, структура ядра разрыхляется и т. д. Вслед за снижением числа нейтрофилов уменьшается число тромбоцитов, что приводит к увеличению времени свертывания крови. Клетки крови и ее плазма обладают сравнительно высокой устойчивостью к действию ионизирующей радиации. Биохимические сдвиги в крови облученных животных отчетливо выражены лишь в разгар лучевого поражения, оставаясь на начальных этапах поражения малозаметными. Кровь постепенно теряет способность снабжать ткани достаточным количеством кислорода, и в результате гипоксии организм погибает.
Наиболее существенное в лучевых изменениях желудочно-кишечного тракта - быстрое и глубокое опустошение тканей. Так, клеточное опустошение в кишечнике крипт уже завершается на первые-вторые сутки, а ворсинок - на третьи-четвертые сутки после облучения мышей. Если облучение производится в небольших дозах, то уже на пятые сутки можно наблюдать восстановление клеточного эпителия. Для желудочно-кишечного синдрома характерен следующий комплекс нарушений, определяющих гибель организма: поражение эпителия, деструкция крипт и ворсинок, инфекционные процессы за счет кишечной флоры, закупорка и поражение кровеносных сосудов, нарушение баланса жидкостей и электролитов, изменение активного транспорта, возрастание активности ферментов автолиза, изменение других ферментативных процессов, снижение проницаемости кишечника для питательных веществ. Нарушения в желудочно-кишечном тракте развиваются в соответствии с тяжестью лучевого поражения, являясь в отдельных случаях даже причиной гибели организма при костномозговом синдроме.
Центральная нервная система (ЦНС) - наиболее радиоустойчивая из всех критических систем. Ее решающая роль в летальном исходе лучевого поражения проявляется при действии массированных доз ионизирующей радиации. В ответ на облучение ткань мозга реагирует как единая система: прямые поражения нейронных структур и расстройства циркуляции, связанные с поражением стенок кровеносных сосудов, обычно сопутствуют друг другу. Повреждения капиллярных сосудов проявляются в виде набухания эндотелиальных клеток. В отличие от зрелой нервной ткани мозг молодых животных более радиочувствителен, чем другие ткани организма.
Облучение плода в утробе матери в сравнительно невысоких дозах приводит к полному разрушению целых его отделов. Высокая радиочувствительность нервной ткани эмбриона объясняется общей закономерностью, заключающейся в том, что в зависимости от времени формирования и дифференцировки органов и тканей в онтогенезе любые из них становятся крайне чувствительными к радиации независимо от их радиочувствительности во взрослом состоянии.
Оценивая биохимические и морфологические изменения ЦНС, следует отметить необычайно большую разницу в радиочувствительности для различных участков, в том числе и для соседних структур однотипных тканей мозга. Это объясняется тем, что наиболее радиочувствительны те микроструктуры, которые в момент облучения находятся в активном функциональном состоянии. Наиболее значительные изменения претерпевают сосудистые и секреторные условно-рефлекторные реакции, в меньшей степени - двигательные.
Нарушенная деятельность эндокринной системы приводит к глубоким изменениям регуляторных биохимических процессов, иммунобиологических и нейровегетативных реакций, к расстройству гемодинамики, терморегуляции, извращению регуляции и деятельности многих органов и систем.
К наиболее радиочувствительным органам эндокринной системы относятся половые железы. Другие железы внутренней секреции менее чувствительны, располагаясь по мере возрастания радиоустойчивости (по морфологическим признакам) в такой последовательности: надпочечники, гипофиз, щитовидная железа, островки поджелудочной железы и, наконец, паращитовидная железа. Радиоустойчивость этих желез связана с тем, что, их ткани состоят из высокодифференцированных функциональных клеток, практически не способных к физиологической регенерации.
Лучевое поражение семенников сопровождается биохимическими изменениями - снижается содержание нуклеиновых кислот, АТФ, креатина, холестерина, аскорбиновой кислоты, полисахаридов, угнетается сперматогенез. Облучение женских половых желез приводит к нарушениям менструального цикла, изменениям течения беременности, преждевременным родам, мертворождению, патологическому развитию эмбрионов, различным генетическим аномалиям потомства. Отмечено, что если семенники обладают значительной восстановительной способностью, то яичники у взрослой самки полностью лишены этой способности. Поэтому у самок в отличие от самцов стерильность обычно необратима.
Учитывая значение печени как «центральной биохимической лаборатории», ее барьерные функции, местонахождение на пути оттока крови из кишечника и т. д., можно понять причину того большого внимания, которое уделяют радиобиологи этому органу. Исследования показали, что печень высоко радиоустойчива, что связано с ее большой регенераторной активностью. Несмотря на многочисленные и глубокие биохимические изменения в печени облученных животных, все же не они причина непосредственной гибели организма.
Сложность оценки радиочувствительности органов дыхания состоит в том, что они содержат клеточные структуры, значительно различающиеся по устойчивости к радиации. Так, хрящевая ткань воздухоносных путей и плевра радиоустойчивы; лимфатическая ткань и сосудистая система легких, а также бронхиолярцый эпителий и клетки, выстилающие альвеолы, радиочувствительны. В результате общего облучения организма в органах дыхания возникают изменения, находящиеся в полном соответствии с развитием клинических и анатомических признаков лучевой патологии.
Ряд органов и тканей условно называют стабильными в связи с их высокой устойчивостью: морфологические, функциональные и биохимические изменения в них после облучения даже в высоких дозах незначительны. Их способность к физиологической регенерации выражена слабо или практически отсутствует. Однако постлучевые изменения стабильных органов и тканей все же вносят известный вклад в общую картину лучевой патологии. Типично стабильный орган - почки. Обычно поражение почек наблюдается при общем облучении животных в несколько десятков грей. Их высокая устойчивость, вероятно, связана с тем, что обновление почечных клеток либо отсутствует, либо выражено слабо.
Еще более устойчивы к действию ионизирующей радиации мышечная и соединительная ткани. Структурные элементы кожи характеризуются относительно большими различиями в радиочувствительности. Сравнительно высокой радиоустойчивостью обладают костная и хрящевая ткани. Однако в период роста они чувствительны к ионизирующей радиации.
В процессе развития лучевого поражения, особенно в фазе выраженных клинических изменений, резко снижается устойчивость организма к инфекциям: подавляется естественная устойчивость организма к возбудителям инфекционных заболеваний, угнетается приобретенный иммунитет, нарушаются все его формы. Снижение иммунитета при лучевой болезни, угнетение защитных механизмов обусловливаются развивающимися в организме аутоиммунными процессами. Подавление иммунитета в облученном организме представляет собой сложный многоступенчатый процесс, в основе которого лежит опосредованное действие ионизирующей радиации.
Помимо генетически обусловленных различий, наблюдаемых у объектов из разных филогенетических групп, возможны значительные вариации радиочувствительности у особей одного вида, находящихся в неодинаковых условиях, питания, аэрации, температуры и т. д. Кроме того, степень лучевого поражения организмов связана с возрастом, полом, физиологическим состоянием, интенсивностью различных процессов, активностью метаболических систем и другими факторами.
3 Действие ионизирующих излучений в зависимости от дозы и мощности дозы
Как уже отмечалось, действие ионизирующих излучений зависит от дозы облучения и мощности дозы, а также от вида частиц, обеспечивающих радиационной действие и времени, в течении которого получена определенная доза. Как уже отмечалось выше, радиационное воздействие происходит в любой среде, изменяет свойства любого объекта. В качестве примера можно привести облучение полиэтилена. Облучение изделий из полиэтилена дозами до 10 КГр снижает их механические свойства, способствует их деструкции. Дозы выше 104 Гр образуют трехмерную структуру вещества, повышают механические свойства изделий, у полиэтилена появляются новые свойства. Облучение дозами порядка 107 Гр вновь изменяют свойства полиэтилена, изделие приобретает свойства эластичности, «каучукоподобности».
В отличие от неживых объектов, биологические системы изменяют свои свойства при сравнительно небольших дозах и мощностях дозы. Общие закономерности величин доз, угнетающих жизненные процессы были приведены выше. Однако важное значение имеет не только величина дозы, но и ее мощность.
3.1 Действие малых доз ионизирующих излучений
Понятие «малая доза» неоднозначно. Исходя из приведенных выше различий в радиочувствительности живых организмов логично сделать вывод о различной величине «малой дозы» для разных организмов или периодов онтогенеза. Часто, в соответствии с антропоцентрическим подходом, малыми дозами считают дозы менее 50-100 мЗв однократно или 5-10 мЗв в год. Однако в научно-практических работах по изучению действия радиации на растения к малым дозам относили величины однократного облучения в 10 и более Гр. Вопрос о биологических эффектах действия малых доз излучения, особенно проблема их количественной оценки (как, впрочем, и любых иных антропогенных факторов малой интенсивности), продолжает оставаться предметом многочисленных дискуссий и полярных мнений по поводу их опасности для человека и среды его обитания.
В зависимости от особенностей биологического действия всю совокупность многообразных факторов физической, химической и биологической природы можно условно разделить на две большие группы: агенты (или факторы), обладающие порогом вредного действия, и агенты, лишенные таких свойств, для которых порога вредного влияния не существует. К числу «пороговых агентов» (т. е. если порог вредного действия не достигнут, биологические эффекты отсутствуют) относят многие ксенобиотики и некоторые виды неионизирующих излучений. К «беспороговым факторам» современная наука относит все виды ионизирующих излучений и некоторые токсиканты химической природы, обладающие канцерогенным и мутационным действием.
По определению, в условиях длительного хронического воздействия на организм «пороговых агентов» в количествах, равных или ниже установленного значения порога (по концентрации, дозе и т. п.), исключаются каких-либо вредные медико-биологические последствия у отдельных лиц, всего населения и его потомков.
Принципиально иной подход используют при прогнозировании и регламентации негативных эффектов в случае воздействия «беспороговых факторов». В мировой науке этот подход впервые был предложен в начале второй половины XX века и относился к ионизирующим излучениям. Только в последние годы этот подход распространен на область химических агентов, для которых получены доказательства их канцерогенного и генотоксического действия.
Концепция (точнее, рабочая гипотеза) беспорогового действия ионизирующих излучений постулирует линейную зависимость биологических эффектов от дозы облучения. Это значит, что отрицательные (но не детерминированные) вредоносные биологические эффекты воздействия ионизирующего излучения - злокачественные опухоли и наследственные нарушения - теоретически возможны при сколь угодно малой дозе облучения вплоть до значений, практически не отличающихся от нуля. При этом вероятность индукции таких эффектов тем меньше, чем ниже доза облучения.
Эффекты, которые порождаются воздействием малых доз, принципиально отличаются от лучевых поражений (лучевая болезнь, лучевые ожоги и т. д.), вызванных дозами порядка 70 - 100 бэр и выше, когда говорят о не стохастических или детерминированных соматических эффектах: увеличивается доза - увеличивается тяжесть поражения.
Детерминированные эффекты с высокой степенью вероятности персонифицированы, и степень тяжести поражения любого облученного индивидуума или группы пострадавших будет тем больше, чем выше доза облучения.
Для стохастических, вероятностных последствий облучения речь идет не о тяжести поражений, а о повышении частоты (вероятности) случаев проявления раковых заболеваний или наследственных дефектов в популяции людей и в том числе у каждого среднестатистического индивидуума. Следовательно, чем больше лучевая нагрузка на популяцию, тем вероятность выхода (частоты) отдаленных последствий будет выше.
Для осуществления соответствующих расчетов и оценок в радиационной защите введено специальное понятие, определяемое термином «коллективная доза облучения» (S). Она представляет собой произведение двух величин:
- средней эффективной индивидуальной дозы в облученной когорте;
- численности людей, которые подверглись облучению.
Обозначается S в человеко - зивертах или человеко - греях (чел-Зв; чел-Гр). Например, когорта населения численностью 1000 человек подверглась облучению средней индивидуальной дозой 0,01 Гр внешнего γ-облучения. Тогда S составляет 1000×0,01 = 10 чел-Гр. Если различные когорты людей получили одинаковую коллективную дозу, то теоретически ожидаемый абсолютный выход опухолей или наследственных дефектов будет равным независимо от численности облучаемых групп. Сказанное можно пояснить следующим примером.
Допустим, одна популяция численностью 1 млн. человек облучена средней эффективной индивидуальной дозой 0,001 Зв, а другая, численностью 10 000 человек, - дозой 0,1 Зв. Тогда коллективные дозы облучения в обоих когортах будут равны, и ожидаемый выход злокачественных опухолей также будет в принципе одинаковым. Для отдельного человека из первой группы, облученного дозой 0,001 Зв, вероятность рака будет в 100 раз меньше, чем во второй когорте, облученных дозой 0,1 Зв.
Линейная беспороговая концепция действия ионизирующих излучений была принята в качестве рабочей гипотезы международными научными организациями (НКДАР и МКРЗ) в основном для обоснования принципов и методов регламентации малых доз облучения. При ее обосновании исходили из теоретически корректных представлений о механизмах взаимодействия излучений с биосубстратами на молекулярном уровне, экспериментальных исследований на биологических моделях in vitro и на микроорганизмах. Из-за отсутствия сколько-нибудь надежных данных при действии малых доз данные о канцерогенных эффектах у человека при воздействии больших доз и больших мощностей доз были экстраполированы в область малых доз и низких мощностей доз (с введением некоторых поправочных коэффициентов, учитывающих меньшую биологическую эффективность малых доз).
Упомянутая рабочая гипотеза (а не доказанный на человеческих популяциях факт), будучи по сути своей консервативной, явно завышает реальный риск облучения в малых дозах и, следовательно, практически исключает возможную недооценку подобного рода последствий.
В то же время возникает много проблем, касающихся доказательства существования таких эффектов у человека. Согласно теории и соответствующим расчетам риск, точнее вероятность, проявления у людей в обсуждаемом диапазоне малых доз, особенно хронического облучения, - весьма редкое событие. Для выявления таких стохастических эффектов на фоне высоких уровней спонтанной патологии (рак и наследственные дефекты естественного происхождения) требуются популяции, исчисляемые многими сотнями тысяч и даже миллионами людей (без учета так называемых контрольных, т. е. без облучения, групп обследуемого населения). Эти эффекты нельзя наблюдать на единичных случаях - каждый конкретный исход случаен (человек, получивший и малую дозу, может заболеть, а получивший в 100 раз больше - остаться здоровым).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 |



