1 Сформулируйте закон действия масс.
2 Что называется скоростью химических реакций?
3 Что называется химическим равновесием системы?
1 Сформулируйте закон Вант-Гоффа.
2 Напишите выражение для скорости следующей реакции
![]()
Как изменится скорость данной реакции, если объем газовой смеси изотермически уменьшить в 2 раза?
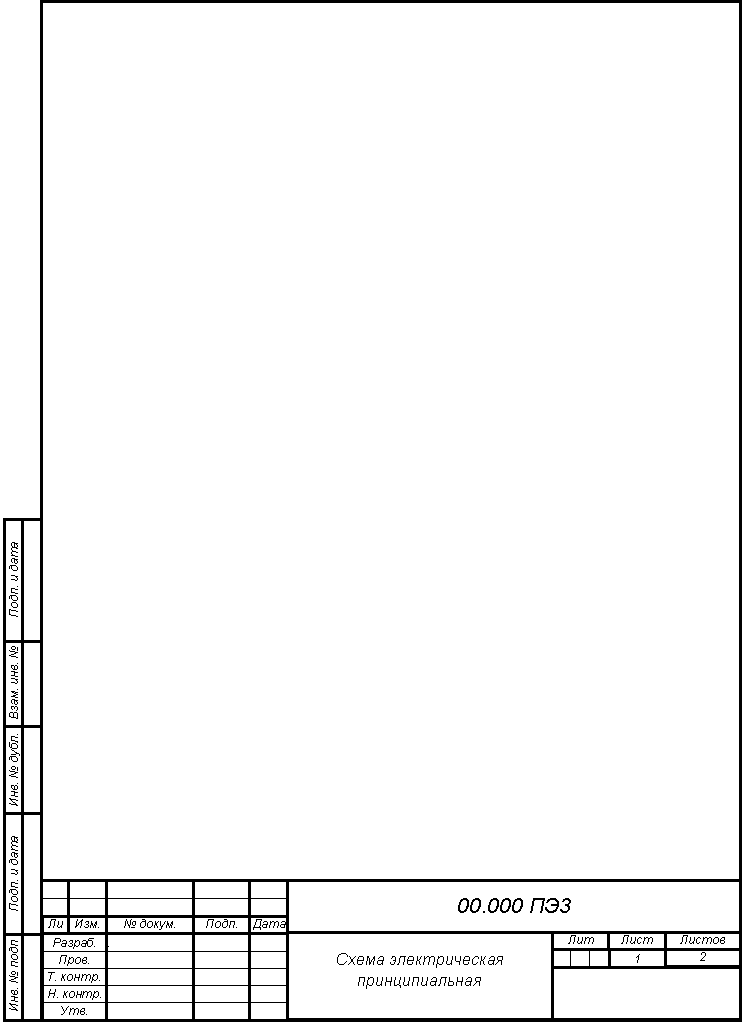
3 При помощи каких изменений концентраций реагирующих веществ можно сместить равновесие в сторону прямой реакции
![]()
7 Сформулируйте принцип Ле-Шателье
Лабораторная работа 6. Концентрация растворов
Цель работы. Освоить методы приготовления растворов заданной процентной концентрации из навески и из более концентрированного раствора.
Экспериментальная часть.
Опыт 1. Приготовление раствора заданной концентрации из навески. Этот способ применяется главным образом для приготовления растворов солей.
Получите у преподавателя задание на приготовление раствора определенной концентрации и объема.
Рассчитайте необходимое количество вещества для приготовления раствора заданной концентрации.
Взвесьте на технохимических весах с точностью до 0,01 г часовое стекло. Затем поместите на него сухую соль в количестве, примерно равном расчетному. Взвесьте часовое стекло с солью также с точностью до 0,01 г и подсчитайте массу соли.
Рассчитайте, исходя из массы соли, необходимое количество воды и отмерьте его мерным цилиндром.
Возьмите плоскодонную колбу и через воронку осторожно перенесите в нее навеску соли. Часовое стекло над воронкой обмойте небольшим количеством воды, отмеренной для растворения. Остальную отмеренную воду вылейте небольшими порциями так, чтобы всю соль с воронки смыть в колбу. Закройте колбу пробкой, встряхните ее несколько раз до полного растворения соли.
Измерьте плотность полученного раствора с помощью ареометра и проверьте правильность приготовления раствора, сравнив результаты измерения с табличными данными. Колбу с раствором сдайте лаборанту.
Опыт 2. Приготовление раствора заданной концентрации из более концентрированного раствора. Этот способ применяется главным образом для приготовления растворов кислот или аммиака.
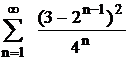 Получите задание у преподавателя.
Получите задание у преподавателя.
Измерьте ареометром плотность имеющегося в лаборатории концентрированного раствора заданного вещества.
Для этого налейте (под тягой) концентрированный раствор в цилиндр и опустите в него ареометр, следя затем, чтобы ареометр не касался стенок цилиндра, как показано на рисунке 1.
Запишите показания ареометра и найдите концентрацию раствора, используя табличные данные.
Если измеренное значение плотности окажется между двумя значениями в таблице, то значение процентной концентрации находят методом интерполяции по формуле 13.
![]() , (13)
, (13)
где с – процентная концентрация исследуемого раствора; d – плотность этого раствора; ![]() - ближайшее значение плотности с недостатком в таблице;
- ближайшее значение плотности с недостатком в таблице; ![]() - ближайшее значение плотности с избытком в таблице;
- ближайшее значение плотности с избытком в таблице; ![]() - процентная концентрация раствора, соответствующая плотности
- процентная концентрация раствора, соответствующая плотности ![]() ;
; ![]() - процентная концентрация раствора, соответствующая плотности
- процентная концентрация раствора, соответствующая плотности ![]() .
.
Используя табличные данные, найдите плотность раствора заданной концентрации и рассчитайте по формуле 14.
![]() , (14)
, (14)
как будут относиться друг к другу ![]() - объем концентрированного и
- объем концентрированного и ![]() - объем разбавленного раствора. Определите объемы концентрированного раствора и воды для приготовления раствора заданной концентрации.
- объем разбавленного раствора. Определите объемы концентрированного раствора и воды для приготовления раствора заданной концентрации.
Отмерьте маленьким цилиндром (под тягой) подсчитанный объем концентрированного раствора. Большим цилиндром или мензуркой отмерьте необходимый объем воды.
Воду перелейте в плоскодонную колбу, затем в нее же вылейте небольшими порциями концентрированный раствор, перемешивая его встряхиванием. Ополосните цилиндр полученным раствором. Закройте колбу пробкой и перемешайте содержимое. Если раствор нагрелся, охладите его до комнатной температуры.
Измерьте ареометром плотность приготовленного раствора и определите его концентрацию, используя табличные данные, рассчитайте процент ошибки.
Колбу с раствором сдайте лаборанту.
Лабораторная работа 7. Определение молекулярной массы растворенного вещества
 Цель работы. Освоить криоскопический метод определения молекулярной массы веществ.
Цель работы. Освоить криоскопический метод определения молекулярной массы веществ.
Экспериментальная часть. Определение молекулярной массы растворенного вещества криоскопическим методом.
Для проведения данной работы необходимо собрать установку, изображенную на рисунке 2. Установка состоит из стакана 1, с охлаждающей смесью, емкостью 700-750 мл, стакана 2, с чистым растворителем емкостью 200-250 мл, мешалки 3, термометра 4 с точностью до 0,1ºС.
Первый стакан служит термостатом. Заполните его охладительной смесью, состоящей из одной части соли NaCl и трех частей мелкого льда и снега. Температура охладительной смеси должна быть в пределах 3-3,5 ºС.
В стакан с емкостью 200-250 мл налейте 100 мл дистиллированной воды и поместите в охладительную смесь. Наблюдайте понижение столбика ртути термометра. Когда температура достигнет минус 1ºС, начинайте энергичное перемешивание воды мешалкой. При этом выпадут кристаллы льда, а столбик ртути начнет быстро подниматься вверх. Отмечайте ту температуру, до которой поднимется столбик ртути. Это и будет температура замерзания чистого растворителя. Измерение повторите дважды. Затем вместо стакана с водой поставьте стакан с раствором (100 мл воды + навеска определяемого вещества). Непрерывно перемешивая, следите за показаниями термометра. В момент появления первых кристалликов льда, отметьте температуру. Это и есть температура замерзания раствора. Не допускайте переохлаждения! Замерзание раствора в отличие от воды протекает при постоянном понижении температуры. Повторите измерение температуры замерзания раствора дважды. Измерения внесите в таблицу 4.
Молекулярную массу определяют по формуле 15.
 (15)
(15)
где К – криоскопическая постоянная воды равна 1,86; m1 – навеска определяемого вещества, г.; m2 – масса растворителя воды (Н2О), г.
Сравните вычисленную молекулярную массу с теоретической. Процент ошибки рассчитать по формуле 16.
 . (16)
. (16)
Таблица 4
МассаН2О (m2), г | Т замер. Н2О, ºС | Навеска m1, г | Т замер. раств., ºС | ||||
I | II | Ср. | I | II | Ср. | ||
1 Вычислите температуру кипения 5%-ного раствора сахара С12Н22О11 в воде. Эбуллиоскопическая константа воды равна 0,52 ºС.
2 Смещали 247 г 62%-ного и 145 г 18%-ного раствора серной кислоты. Какова процентная концентрация раствора после смешения?
3 Сколько воды следует прибавить к 1 л 12%-ного раствора NaOH (плотность 1,131 г/см3) для получения 2 М раствора NaOH?
4 Сколько грамм-эквивалентов содержится в: 6 молях Н2SO4; 0,5 молях Н2SO4; 10 молях NaCl?
5 Вычислите молярную и нормальную концентрацию 8%-ного раствора НNO3, плотность которого 1,2 г/см3. Сколько грамм кислоты содержится в четырех литрах этого раствора?
6 Сколько граммов АgNO3 потребуется для обменного взаимодействия с 6 мл 12,2%-ного раствора НСl (плотность 1,06 г/см3)
7 Смешали 400 мл 1,2 М раствора NaOH и 600 мл 1,8 М раствора NaOH. Какова концентрация полученного раствора?
8 Вычислите процентную концентрацию водного раствора метанола СН3ОН, температура кристаллизации которого минус 2,79 ºС. Криоскопическая константа воды 1,86 градусов.
Лабораторная работа 8. Электролитическая диссоциация
Цель работы. Определить электропроводность растворов электролитов. Сделать вывод о влиянии концентрации раствора электролита на величину электропроводности. Освоить составление уравнений ионообменных реакций.
Экспериментальная часть.
Опыт 1. Электропроводность растворов сильных и слабых электролитов.
Переключатель “электропроводность” поставьте в диапазоне от 10-2 до 10-1. В сосуд №1 налейте 100 cм3 0,5 М раствора H2SO4, в сосуд №2 налейте 100 см3 1,0 М раствора CH3COOH. Измерьте электропроводность растворов, последовательно устанавливая переключатели в положении 1 и 2. Данные опыта внесите в таблицу 5.
Сделайте вывод о свойствах исследованных электролитов. Напишите уравнения диссоциации.
Таблица 5
Номер сосуда | Электролит | Цена деления, См шкалы гальванометра в диапазоне 1 | Число делений | Электропроводность |
1 2 |
Опыт 2. Определение зависимости электропроводности слабого электролита от концентрации раствора.
Переключатель “электропроводность” поставьте в положение 1/R = f (c). В качестве слабого электролита возьмите растворы уксусной кислоты различной концентрации. По 100 см3 раствора CH3COOH налить в сосуды:№ 1 - 60% CH3COOH; № 2 - 40% СH3COOH; № 3 - 20% CH3COOH; № 4 - 10% CH3COOH; № 5 - 5% CH3COOH; № 6 - 1% CH3COOH. Измерьте электропроводность растворов, последовательно устанавливая переключатель “Растворы” от положения 1 до положения 6. Данные опыта занести в таблицу 6.
Постройте график зависимости электропроводности электролита от концентрации.
Сделайте вывод и объясните полученные результаты.
Таблица 6
Номер сосуда | Электролит | Цена деления, См шкалы гальванометра в диапазоне | Число делений | Электропроводность |
Опыт 3. Смещение ионного равновесия в растворе слабого основания.
Налейте в две пробирки по 2-3 см3 0,1 М раствора гидроксида аммония (NH3.H2О) и по 1-2 капли раствора фенолфталеина. Объясните причину изменения окраски индикатора, напишите уравнение диссоциации гидроксида аммония.
В одну из пробирок прибавьте немного кристаллического хлорида аммония и взболтайте содержимое пробирки. Сравните окраски обеих пробирок, пользуясь уравнением диссоциации. Объясните причину смещения равновесия в сторону недиссоциированных молекул гидроксида аммония.
Опыт 4.Амфотерные электролиты.
Налейте в пробирку 2-3 см3 раствора сульфата цинка и по каплям прибавляйте к нему раствор гидроксида натрия. Образовавшийся осадок распределите в две пробирки и подействуйте на него в одном случае 2% раствором соляной кислоты, а в другом - 10%-ным раствором гидроксида натрия.
Составьте уравнения реакций. Почему гидроксид цинка ведет себя в кислом растворе как основание, а в щелочном - как кислота?
Опыт 5. Обменные реакции в растворах электролитов.
Налейте в две пробирки по 2-3 см3 сульфида натрия. В первую пробирку прилейте примерно столько же раствора сульфата железа (II), во вторую – раствор сульфата меди (II). Наблюдайте образование осадков.
Напишите уравнения происходящих реакций в молекулярной, полной и сокращенной ионной формах.
Лабораторная работа 9. Гидролиз солей
Цель работы. Ознакомиться с типичными случаями и условиями протекания гидролиза солей.
Экспериментальная часть.
Опыт 1. Ознакомиться с типичными случаями и условиями протекания гидролиза солей.
В четыре пробирки налейте по 2 см3 свежеприготовленных растворов карбоната натрия, хлорида цинка, нитрата натрия и ацетата натрия. Определите рН растворов при помощи универсальной индикаторной бумаги. Полученные данные внесите в таблицу 7.
Таблица 7
Испытуемый раствор | Уравнение реакции диссоциации соли | Катионы (нионы), образующие прочные связи с водой | Уравнение реакции гидролиза соли | Состояние среды (рН) | |
Сокра-щенное | Молеку-лярное | ||||
Опыт 2. Зависимость гидролиза солей от различных факторов.
К раствору ацетата натрия прилейте одну-две капли фенолфталеина. Заметьте интенсивность окраски. Нагрейте пробирку до кипения. Как меняется интенсивность окраски? Объясните полученный результат. Дайте немного остыть пробирке и охладите ее в холодной воде. Что происходит?
Налейте в пробирку 1-2 см3 раствора хлорида висмута. Постепенно разбавляйте раствор дистиллированной воды до выпадения в осадок основной соли. К полученной основной соли висмута прибавьте из пипетки несколько капель концентрированной соляной кислоты до растворения осадка.
Напишите уравнение реакции гидролиза хлорида висмута. Укажите, как смещается равновесие гидролиза при разбавлении раствора соли и при увеличении концентрации соляной кислоты.
К 2-3 см3 хлорида алюминия прибавьте по каплям раствор карбоната натрия. Образование осадка Al(OH)3 является результатом взаимного усиления гидролиза двух солей.
Напишите уравнение реакций между хлоридом алюминия и карбонатом натрия с образованием карбоната алюминия и последующей реакцией между Аl2(CO3)3 и Н2О. Сделайте вывод о необратимости гидролиза.
Лабораторная работа 10. Определение жесткости воды
Цель работы. Ознакомление с различными видами жесткости; количественное определение карбонатной и временной жесткости; умягчение воды.
Экспериментальная часть.
Опыт 1. Определение карбонатной жесткости воды.
Определение карбонатной жесткости воды основано на взаимодействии гидрокарбонатов кальция или магния, содержащихся в воде, с соляной кислотой.
Налейте 50-100 см3 водопроводной воды в коническую колбу, прибавьте 2-4 капли индикатора метилоранжа (вода окрашивается в желтый цвет) и титруйте 0,1М раствором соляной кислоты НСl до перехода желтой окраски в оранжевую. Результаты титрования занесите в таблицу 8.
Таблица 8
Номер пробы | Объем воды, см3 | N HCl , нормальность кислоты | V HCl, мл израсходованного на титрование | V HCl, мл среднее |
Примечание: отбирают и титрируют две параллельные пробы воды.
Расчет жесткости воды произвести по формуле 23.
 . (23)
. (23)
Опыт 2. Определение общей жесткости воды.
Общую жесткость воды определяют титрованием пробы воды раствором трилона Б (Na2C10H14O8N2), с которым ионы Са2+ и Mg2+ дают прочные бесцветные комплексы. Образование комплексов, а следовательно, и титрование производится при рН = 9-10, что создается добавлением аммиачно-буферного раствора. Титрование производится в присутствии индикатора хром-синего или хром темно-синего.
В колбу для титрования налейте 50-100 см3 водопроводной воды, добавьте 5 см3 аммиачно-буферного раствора. Внесите несколько кристаллов индикатора хром темно-синего, предварительно смешанного с хлоридом калия. При этом раствор окрашивается в красно-фиолетовый цвет.
Проведите титрование содержимого колбы 0,1 н раствором трилона Б, при энергичном перемешивании до тех пор, пока появится синяя окраска. Результаты титрования занесите в таблицу 9.
Таблица 9
Номер пробы | Объем воды, см3 | N тр. Б, нормальность трилона Б | V тр. Б, см3 израсходовано на титрование | V тр. Б, см3 среднее |
Расчет жесткости воды производится по формуле 24.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



