Методические указания |
| Ф СО ПГУ 7.18.1/05 |
Министерство образования и науки Республики Казахстан
Павлодарский государственный университет им. С. Торайгырова
Кафедра химии и химических технологий
методические указания
по дисциплине Химия
для студентов специальностей «5В060700-Биология», «5В080200-Технология производства продуктов животноводчества»
Павлодар
Лист утверждения к методическим указаниям |
| Ф СО ПГУ 7.18.1/05 |
УТВЕРЖДАЮ
Декан ФХТиЕ
___________
«___»__________ 20 ___ г.
Составитель: к. х.н., ст. преподаватель
Кафедра химии и химических технологий
Методические указания
к лабораторным работам
по дисциплине Химия
для студентов специальностей «5В060700-Биология», «5В080200-Технология производства продуктов животноводчества»
Рекомендовано на заседании кафедры «__ » _______ 20__г. Протокол № 2
Зав. кафедрой ___________________________
Одобрена учебно-методическим советом факультета химических технологий и естествознания
« ___»_____________ 20__ г. Протокол № __
Председатель УМС_________________________
Основные понятия в химии. Газовые законы
Лабораторная работа 1. Определение молярной массы эквивалента цинка
Цель работы. Освоить метод определения молярной массы эквивалента металлов по вытеснению водорода из растворов кислот.
Химический процесс. Для определения молярной массы эквивалента цинка используют окислительно-восстановительную реакцию взаимодействия металлического цинка с разбавленной соляной кислотой.
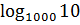
В ходе данной химической реакции цинк окисляется, а водород восстанавливается:
Исходя из данной окислительной полуреакции, фактор эквивалентности цинка равен ½, следовательно, молярная масса эквивалента цинка равна ½ его молярной массы.
Экспериментальная часть. Для определения молярной массы эквивалента цинка пользуются прибором, изображенным на рисунке 1.
 Прибор состоит из градуированной бюретки (2), соединенной резиновым шлангом (3) с воронкой (4), зафиксированным на штативе (1) и пробирки. Бюретка и пробирка плотно закрываются пробками. Бюретка, резиновая трубка и воронка должны быть заполнены водой.
Прибор состоит из градуированной бюретки (2), соединенной резиновым шлангом (3) с воронкой (4), зафиксированным на штативе (1) и пробирки. Бюретка и пробирка плотно закрываются пробками. Бюретка, резиновая трубка и воронка должны быть заполнены водой.
Перед началом опыта прибор проверяется на герметичность. Для этого кольцо штатива с воронкой опустите вниз и укрепите в неподвижном состоянии. Если прибор герметичен, то в начале при опускании воронки уровень воды в бюретке немного понизится, а затем останется постоянным. Если же уровень воды непрерывно будет понижаться, значит прибор не герметичен. Надо добиться герметичности.
Установите одинаковый уровень воды в бюретке и воронке, чтобы давление внутри прибора было равно атмосферному.
Снимите пробирку и налейте в нее (не смачивая стенки верхней части пробирки) 5 см3 разбавленной соляной кислоты (HCl).
Держа пробирку в наклонном положении, положите навеску цинка на сухую стенку пробирки (металл не должен соприкасаться с кислотой) и осторожно, не меняя положения пробирки, соедините ее с прибором. Проверьте, не нарушилась ли герметичность прибора. Отметьте и запишите уровень воды в бюретке, произведя отсчет по нижнему мениску жидкости. Легким постукиванием пальца по стенке пробирки стряхните цинк в кислоту. Под давлением водорода, образующегося при взаимодействии металла с кислотой, вода из бюретки вытесняется. Реакция протекает с выделением тепла.
После окончания реакции дайте пробирке остыть до комнатной температуры, приведите воду в бюретке и воронке к одинаковому уровню и запишите уровень воды в бюретке. Одновременно запишите температуру окружающего воздуха по термометру и атмосферное давление по барометру. Результаты опыта внесите в таблицу 1.
Таблица1
Навеска цинка, г | Условия опыта | Положение уровня воды в бюретке, см3 | Объем выделившегося водорода, см3 | ||
температура, °С | давление, Па (мм рт. ст.) | до опыта | после опыта | ||
mZn | t° | Pполн. | V1 | V2 |
|
Обработка результатов опыта
1 Приведите найденный объем водорода к нормальным условиям по формуле 8
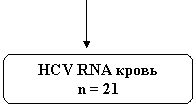 , (8)
, (8)
где ![]() - давление водяных при данной температуре, Па (мм рт. ст.),
- давление водяных при данной температуре, Па (мм рт. ст.), ![]() – атмосферное давление;
– атмосферное давление; ![]() - значение температуры, давления и объема при стандартных условиях; Т – температура К, Т = 273 + t.
- значение температуры, давления и объема при стандартных условиях; Т – температура К, Т = 273 + t.
2 Вычислите массу вытесненного водорода, учитывая что мольный объем водорода при нормальных условиях равен 22, 4 л и весит 2 г. Все данные переведите в одну систему измерений и составьте пропорцию.
22, 4 л - 2 г
V0 - Х г,
где Х г - масса водорода, г.
3 Вычислите молярную массу эквивалента цинка по формуле 9
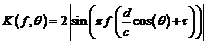 , (9)
, (9)
где ![]() - эквивалентная масса водорода, равная 1г/моль;
- эквивалентная масса водорода, равная 1г/моль; ![]() – масса выделившегося водорода, г;
– масса выделившегося водорода, г; ![]() - масса цинка, г.
- масса цинка, г.
4 Вычислите теоретическую эквивалентную массу цинка, зная его атомную массу и валентность.
5 Найдите ошибку опыта в % по формуле 10
 . (10)
. (10)
Полученный ответ покажите преподавателю. При получении относительной ошибки больше 10% эксперимент повторите и полученные вновь данные внесите в таблицу.
Лабораторная работа 2. Определение молекулярной массы оксида углерода (IV)
Цель работы. Освоить метод определения молекулярной массы газообразных веществ.
Химический процесс. Для определения молекулярной массы оксида углерода (IV) используются следующие реакции:

Из аппарата Киппа выходит смесь, состоящая из оксида углерода (IV), воды и хлороводорода.

В склянках Тищенко происходит улавливание хлороводорода (первая склянка) и удаление воды при пропускании через серную кислоту (вторая склянка).
Экспериментальная часть. Для определения молекулярной массы оксида углерода (IV) используется установка, изображенная на рисунке 2 и состоящая из аппарата Киппа 1, двух склянок Тищенко 2,3, плоскодонной колбы 4 емкостью 300-350 мл.
 |
Оксида углерода (IV), полученный в аппарате Киппа действием 10%-ного раствора соляной кислоты на мрамор, освобождается от хлорводорода в склянке 2, заполненной до половины раствором гидрокарбоната натрия, и высушивается концентрированной серной кислотой в склянке 3.
Чистую и сухую колбу плотно закройте резиновой пробкой. Отметьте уровень, до которого доходит пробка в горло колбы, парафиновым карандашом. Колбу с пробкой взвесьте на весах с точностью до 0,01 г и запишите массу колбы m1.
Наполните колбу диоксидом углерода. Для этого опустите в колбу до дна газоотводную трубку от склянки 3 и пропускайте диоксид углерода из аппарата Киппа в течение 3-4 мин. Проверьте степень заполнения колбы с помощью тлеющей лучинки. Затем, не закрывая кран, осторожно выньте стеклянную трубку и закройте колбу пробкой; пробка должна входить до отметки. После этого закройте кран аппарата Киппа.
Взвесьте колбу с оксидом углерода (IV) на весах с точностью до до 0,01 г, запишите массу колбы m2.
Повторите опыт с заполнением колбы оксидом углерода (IV), и снова ее взвесьте. Масса m3 должна отличаться от m2 не более ![]() 0,01 г. Если разница в массе превышает эту величину, заполните колбу в третий раз и снова взвесьте. Так повторяйте до тех пор, пока разность между двумя последовательными взвешиваниями станет не более
0,01 г. Если разница в массе превышает эту величину, заполните колбу в третий раз и снова взвесьте. Так повторяйте до тех пор, пока разность между двумя последовательными взвешиваниями станет не более ![]() 0,01 г. Массу колбы с оксидом углерода (IV) m2 запишите.
0,01 г. Массу колбы с оксидом углерода (IV) m2 запишите.
Запишите температуру и атмосферное давление по барометру.
Измерьте объем колбы, наполнив ее до метки водой. Воду из колбы вылейте в мерный цилиндр. Объем воды равен объему оксида углерода (IV) V. Запишите эту величину.
Обработка результатов опыта
1 При определении массы оксида углерода (IV) ![]() в объеме колбы необходимо учесть, что этим газом из колбы был вытеснен равный объем воздуха. Масса оксида углерода (IV) (формула 11) составит
в объеме колбы необходимо учесть, что этим газом из колбы был вытеснен равный объем воздуха. Масса оксида углерода (IV) (формула 11) составит
 , (11)
, (11)
где ![]() - масса воздуха в объеме колбы, г.
- масса воздуха в объеме колбы, г.
Величины ![]() и
и ![]() определены экспериментально. Массу воздуха необходимо рассчитать по уравнению Менделеева - Клайперона. Из этого уравнения вытекает, что
определены экспериментально. Массу воздуха необходимо рассчитать по уравнению Менделеева - Клайперона. Из этого уравнения вытекает, что
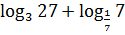 . (12)
. (12)
Значение универсальной газовой постоянной определите, исходя из единиц измерения давления и объема.
R = 0,082 л·атм/К·моль;
R = 62360 мл·мм рт. ст./К·моль;
R = 8,31 Дж/К·моль.
Так как средняя молекулярная масса воздуха составляет 29 г, Т = 273 + t, то масса воздуха составит
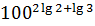 . (13)
. (13)
Затем определите массу оксида углерода (IV) ![]() .
.
2 Вычислите молекулярную массу оксида углерода (IV) по уравнению Менделеева-Клайперона.
3 Рассчитайте ошибку опыта в процентах по формуле 14
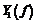 . (14)
. (14)
Контрольные вопросы и задачи
1 Что называется молекулярной массой вещества? В каких единицах она выражается?
2 Что называется молем? Какое количество вещества содержится в одном моле?
3 Что называется относительной плотностью газа?
4 Какая зависимость между относительной плотностью газа и его молекулярной массой?
5 Вычислите молекулярную массу вещества, если установлено, что масса 60 мл его паров при температуре 87 °C и давлении 524 мм рт. ст. равна 0,13 г.
6 Что называется эквивалентом элемента?
7 Закон эквивалентов и его математическое выражение.
8 Чему равен эквивалентный объем водорода (в литрах)?
9 Определите фактор эквивалентности ![]() в реакции с соляной кислотой
в реакции с соляной кислотой
![]()
10 Определите эквивалентную массу элемента в соединении, содержащем 60% кислорода.
Лабораторная работа 3. Периодическая система химических элементов
Цель работы. Изучить и установить изменение свойств элементов, их оксидов и гидроксидов в периоде и группе.
Экспериментальная часть.
Опыт 1. Изменение химического характера оксидов и гидроксидов третьего периода.
1.1 Взаимодействие металлического натрия с воздухом и водой. Выньте пинцетом из банки с керосином кусочек металлического натрия, положите его на фильтровальную бумагу и сделайте надрез. Обратите внимание на потускнение блестящей металлической поверхности свежего надреза. Отрежьте кусочек металла величиной со спичечную головку и бросьте его в химический стакан с водой. Будет наблюдаться энергичная реакция. К полученному раствору в химическом стакане прибавьте 1-2 капли фенолфталеина. Объясните изменение окраски. Напишите уравнение реакции.
1.2 Взаимодействие оксида магния с водой. Поместите в пробирку с водой немного сухого оксида магния. Добавьте 1-2 капли фенолфталеина. Нагрейте пробирку на спиртовке. Объясните изменение окраски, напишите уравнения реакции.
1.3 Горение серы. В колбу на 1/3 объема налить дистиллированной воды и добавить 2-3 капли метилоранжа, затем поместить в металлическую ложку кусочек серы величиной с горошину и нагреть в пламени горелки, как только сера загорится синим пламенем, внести ложечку в колбу с водой (не касаясь воды). Отверстие в колбе закрыть ватным тампоном. Когда сера сгорит, ложку вынуть и воду в колбочке взболтать. Наблюдать за изменением окраски в колбе. Написать уравнение реакции.
1.4 В третьем периоде найти амфотерный элемент и в пробирке получить его гидроксид, используя раствор соли этого элемента и гидроксид натрия. Содержимое пробирки разделить на две другие пробирки. В первую влить раствор соляной кислоты, во вторую – раствор гидроксида натрия до полного растворения осадков. Объясните происходящие явления реакции, напишите уравнения реакции. Заполните таблицу 2.
Опыт 2. Изменение химического характера оксидов и гидроксидов элементов 15 группы.
2.1 Свойства гидроксида сурьмы. В пробирку налейте 2-3 см3 раствора хлорида сурьмы (III) и к нему по каплям добавьте раствор гидроксида натрия до выпадения белого осадка (избегать избытка щелочи). Осадок распределите в две пробирки. В одну налейте 2%-ный раствор гидроксида натрия, а в другую 2%-ный раствор соляной кислоты. В обоих случаях добейтесь полного растворения осадков. Объясните происходящие явления. Напишите уравнения реакций.
2.2 Свойства гидроксида висмута. В пробирку налейте 2-3 см3 раствора хлорида висмута (III) и к нему по каплям добавьте раствор гидроксида натрия до выпадения белого осадка (избегать избытка щелочи). Осадок распределите в две пробирки. В одну налейте 2%-ный раствор гидроксида натрия, а в другую раствор соляной кислоты. В каком случае осадок не растворяется. Объясните происходящие явления. Напишите уравнения реакций. Заполните таблицу 3.
Таблица 2
Элемент | Na | Mg | Al | P | S | Cl |
Формула высшего оксида | ||||||
Формула гидроксида | ||||||
Химический характер оксидов и гидроксидов | ||||||
Вывод об изменении свойств элементов и их соединений в периоде |
Таблица 3
Элемент | N | P | As | Sb | Bi |
Формула высшего оксида | |||||
Формула гидроксида | |||||
Химический характер оксидов и гидроксидов | |||||
Вывод об изменении свойств элементов и их соединений в периоде |
Контрольные вопросы

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




