Тема 17. Элементы квантовой механики.
1. Корпускулярно - волной дуализм.
2.Соотношение неопределенностей Гейзенберга.
1.
На протяжении всей своей истории физика не раз оказывалась в ситуации, когда общепринятая теория не могла объяснить целого ряда явлений. Но всегда находился выход – создавалась новая теория, более общая, способная объяснить и старые, и новые факты.
Но в данном случае ситуация была несколько иная – новая теория квантов не представлялась более общей, чем волновая, в том смысле, что некоторые явления объясняемые квантовой теорией невозможно объяснить с точки зрения волновой теории и наоборот. Противоречие волна – частица казалось неразрешимым.
Экспериментально подтверждение корпускулярно-волнового дуализма для света позволило Луи де Бройлю в 1924 году выдвинуть гипотезу об универсальном характере этого явления. Де Бройль утверждает, что не только свет, но и другие частицы материи наряду с корпускулярными свойствами обладают также и волновыми свойствами.
По де Бройлю любой микрообъект можно характеризовать энергией и импульсом (корпускулярные свойства), а другой стороны – частотой и длиной волны (волновые свойства). Количественные соотношения, связывающие эти характеристики, такие же, как и у света, т. е.
![]() . (1)
. (1)
Смелость гипотезы де Бройля состояло в том, что данные соотношения постулировались не только для света, но и для других объектов микромира, в том числе и для таких которые обладают массой покоя. Из гипотезы де Бройля следует, что любой частице, обладающей импульсом « р » мы можем сопоставить волну, длина которой определяется выражением
![]() (2)
(2)
и называется длиной волны де Бройля.
В 1927 году гипотеза де Бройля получила экспериментальное подтверждение. Джермер и Девисон на опыте наблюдали дифракцию электронов при рассеивании на естественной дифракционной решетке, кристалле никеля. По распределению максимумов и минимумов в дифракционной картине можно было определить длину волны. Экспериментальные данные подтвердили гипотезу де – Бройля. Несколько позже дифракционные явления были обнаружены у нейтронов, протонов и других микрочастиц.
Открытие волновых свойств у частиц привело к возникновению новых методов исследования структуры вещества – электронной микроскопии, нейтронографии и других методов.
Экспериментально подтверждение гипотезы де Бройля показало, что перед нами универсальное свойство материи.
Но тогда возникает вопрос, почему мы не наблюдаем волновых свойств у человека? Расчет показывает, что для человека массой 60 кг, движущегося со скоростью ![]() длина волны де – Бройля
длина волны де – Бройля 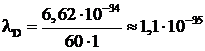 м. Обнаружить эту волну мы не можем, так как в природе периодических структур с таким периодом не существует.
м. Обнаружить эту волну мы не можем, так как в природе периодических структур с таким периодом не существует.
Экспериментальное подтверждение гипотезы де Бройля коренным образом изменило наши представления о микрообъектах.
Всем микрообъектам присущи и волновые, и корпускулярные свойства, но в то же время любую из частиц нельзя считать ни частей, ни волной в классическом понимании этого слова.
Это интересно. Опираясь на свою идею о волнах материи, де Бройль выводит формулу Планка ![]() .
.
2.
Двойственная природа частиц вещества, вынуждающая описывать микрочастицы как с помощью корпускулярных, так и волновых представлений, ставит вопрос о границах применимости понятий классической физики к объектам микромира.
В классической физике всякая частица движется по определенной траектории, так, что в любой момент времени точно определены ее координата и импульс.
Одно из основных отличий микрочастиц заключается в том, что она не имеет траектории и неправомерно говорить о точном значении ее координаты и импульса. В самом деле, понятие длины волны в данной точке не имеет смысла.
В 1927 году Гейзенберг, учитывая волновые свойства частиц и накладываемые этим ограничения, пришел к выводу о том, что объект микромира невозможно одновременно с одинаковой степенью точности охарактеризовать его координатой и импульсом. По Гейзенбергу, неопределенности в значениях этих величин удовлетворяют неравенству
![]() - (3)
- (3)
соотношение неопределенностей Гейзенберга.
Отсюда следует, что в случае если мы точно знаем положение частицы (![]() ), ее импульс совершенно не определен
), ее импульс совершенно не определен ![]() и наоборот.
и наоборот.
Невозможность одновременно точно определить координату и импульс частицы ни коим образом не связана с несовершенством методов измерения или измерительных приборов. Она является результатом специфики микрообъектов, отражающей особенности их объективных свойств.
Так как в классической физике принимается, что измерение координаты и импульса может быть произведено с любой точностью, то соотношение неопределенностей Гейзенберга является, таким образом, квантовым ограничением применимости законов классической механики к объектам микромира. Рассмотрим некоторые примеры. Преобразуем соотношение неопределенностей, так как ![]() , то
, то
![]() . (4)
. (4)
Рассмотрим движение электрона в кинескопе телевизора. Пусть скорость движения электрона ![]() , определена с точность до 1%, т. е.
, определена с точность до 1%, т. е.  . Тогда неопределенность координаты электрона
. Тогда неопределенность координаты электрона 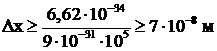 значительно меньше толщины пучка электронов и ею можно пренебречь. Таким образом, при расчете кинескопа телевизора электроны можно считать классическими частицами.
значительно меньше толщины пучка электронов и ею можно пренебречь. Таким образом, при расчете кинескопа телевизора электроны можно считать классическими частицами.
Рассмотрим движение электрона в атоме. Пусть неопределенность координаты электрона равна ![]() (электрон принадлежит атому). Тогда неопределенность скорости электрона
(электрон принадлежит атому). Тогда неопределенность скорости электрона 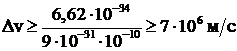 . Расчет показывает, что в атоме электрон движется со скоростью
. Расчет показывает, что в атоме электрон движется со скоростью  , другими словами, неопределенность определения скорости в 3 раза превышает само значение скорости. Следовательно, электрон в атоме нельзя считать классической частицей.
, другими словами, неопределенность определения скорости в 3 раза превышает само значение скорости. Следовательно, электрон в атоме нельзя считать классической частицей.
Каким же образом для представления такой величины как электрон, могут быть использованы без противоречия две столь различные между собой модели – корпускулярная и волновая. Н. Бор показал, что из-за соотношения неопреленностей эти модели никогда не могут войти в противоречие друг с другом, потому что чем больше уточняется одна модель, тем более неопределенной становится вторая. Оба этих аспекта – волновой и корпускулярный – не приходят в столкновение, потому что никогда не предстают одновременно. Чем более четкими оказываются в каком-либо явлении корпускулярные свойства, тем более незаметными и неясными оказываются его волновые свойства. Таким образом, электрону присущи два аспекта, и он предстает то в одном из них, то в другом, но никогда не предстает одновременно в обоих.


