m1 =
m2 =
m =
В тех случаях, когда после убывания массы наступает ее увеличение, обусловленное наличием окислительных процессов, за постоянную массу принимают последнюю убывающую массу.
Массовую долю влаги в продуктах (%) рассчитывают по формуле:
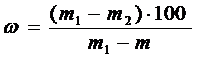 =
=
где m1 - масса бюкса с песком, стеклянной палочкой и навеской исследуемого продукта до высушивания, г.;
m2 - масса бюкса с песком, стеклянной палочкой и навеской исследуемого продукта после высушивания, г;
m - масса бюкса с песком и стеклянной палочкой, г.
За результат анализа принимают среднеарифметическое результатов двух параллельных определений, допускаемое расхождение между которыми не должно превышать 0,5 %.
Примечание. При определении массовой доли влаги в сушеных фруктах берут пробу 5-10 г (для размолотого зерна - 2-5 г) и сушат без песка.
Лабораторная работа № 9.
Мерная посуда.
Приготовить раствор в мерной колбе, подготовить бюретку, пипетку к работе.
Мерная посуда.
Пипетки.
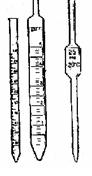 _______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
_______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Отбор аликвотной части
 ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Мерные колбы.
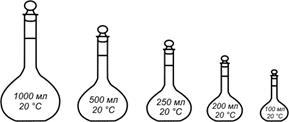
______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
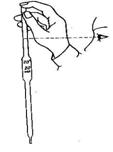
Наблюдение за правильностью установки мениска
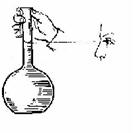 ____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Мерные цилиндры.

 ___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Бюретки.

_____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
_________________________________________________________________________________________________________________________________________________________________________________
Измерение объема по шкале бюретки
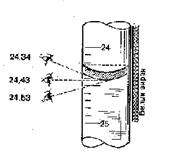
______________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Положение рук при титровании
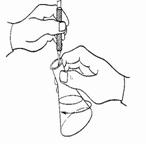
________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Лабораторная работа № 10.
Приготовить стандартный раствор гидроксида натрия, исходный раствор щавелевой кислоты, установить точную концентрацию раствора гидроксида натрия.
Цель работы – приготовить раствор гидроксида натрия, стандартный раствор щавелевой кислоты и установить точную концентрацию раствора гидроксида натрия.
Оборудование: техно-химические весы, аналитические весы, бюкс, мерная колба на 100 мл, плоскодонные колбы на 100 мл, бюретка, пипетка, колба для титрования.
Реактивы: раствор гидроксида натрия, 0,1 н. раствор щавелевой кислоты, фенолфталеин.
Ход работы.
1. Приготовление стандартного раствора гидроксида натрия.
Стандартный раствор удобно готовить в плоскодонной колбе. Для приготовления заданного объема 0,1 н. раствора щелочи сначала рассчитывают навеску:
m NaOH = СнVм. к.Э NaOH =
Навеску гидроксида натрия берут на технических весах, затем переносят навеску через воронку в мерную колбу.
2. Приготовление исходного раствора щавелевой кислоты – Н2С2О4 2Н2О.
Предварительный расчет:
m Н2С2О4 2Н2О = СнVм. к.Э Н2С2О4 2Н2О =
где Сн – нормальность; Vм. к. – вместимость мерной колбы, мл; ЭН2С2О4 2Н2О – эквивалентная масса щавелевой кислоты.
Навеску щавелевой кислоты берут на техно-химических, затем на аналитических весах, по разности. Для этого сначала взвешивают бюкс с навеской, переносят навеску через воронку в мерную колбу, а потом взвешивают пустой бюкс с остатками щавелевой кислоты, которые прилипли к стенке бюкса.
m бюкса с навеской =
m пустого бюкса =
m навески =
По разности узнают точную навеску, которая перенесена в мерную колбу. Тщательно смывают дистиллированной водой навеску с воронки, доводя раствор примерно до половины мерной колбы, перемешивают до полного растворения навески и доливают воду до метки, после чего перемешивают весь полученный раствор.
Рассчитывают точную нормальность полученного исходного раствора до четырех значащих цифр:
Т Н2С2О4 2Н2О= m Н2С2О4 2Н2О / Vм. к.=
Сн = 1000 Т Н2С2О4 2Н2О / Э Н2С2О4 2Н2О =
3. Установка нормальности и титра раствора щелочи по щавелевой кислоте.
Нормальность щелочи устанавливают прямым титрованием исходного раствора щавелевой кислоты. Для этого в подготовленную бюретку наливают раствор щелочи, заполняют кончик бюретки и доводят раствор щелочи до нулевой метки. В коническую колбу, в которой проводят титрование, пипеткой переносят точный объем исходного раствора щавелевой кислоты и добавляют 1 – 2 капли фенолфталеина. Титруют щавелевую кислоту щелочью до появления от одной капли щелочи бледно-розовой окраски, не исчезающей при перемешивании в течении 0,5 мин. Титрование повторяют до тех пор, пока три последних титрования не совпадут или не будет различаться не более чем на 0,1 мл. Окончательным считают среднее значение из результатов трех последних титрований.
V1=
V2=
V3=
Vср=
Титрование основано на реакции:___________________________________________
Расчет:
С1 V1 = С2V2
Т NаОН = CнNaOH Э NaOH / 1000=
Лабораторная работа № 11.
Определить кислотность муки методом нейтрализации.
Цель работы: определить кислотность муки, используя метод нейтрализации.
Оборудование: весы технические, коническая колба, вместимостью 100 мл (2 шт), пипетка, бюретка,
Реактивы: 0,1 н. раствор гидроксида натрия, фенолфталеин.
Ход определения.
Навеску муки около 5 г, взвешенную с точностью до 0,01 г, переносят в коническую колбу, вместимостью 100см3, добавляют небольшими порциями 30 мл дистиллированной воды. Полученную суспензию хорошо перемешивают до исчезновения комков и смывают с внутренней поверхности колбы частицы муки. Затем добавляют 5 капель фенолфталеина и при перемешивании титруют раствором NaOH до появления розового окрашивания, не исчезающего в течение 1-й мин.
V1 =
V2 =
V3 =
V cр =
Кислотность муки рассчитывают по формуле:
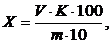 =
=
где V - объем раствора гидроксида натрия, израсходованный на титрование, л;
К - поправочный коэффициент концентрации раствора NaOH (KOH) к Сэк(NaOH) = 0,1000 моль/л;
100 - коэффициент пересчета результатов титрования на 100 г муки;
m - масса навески муки, г;
10 - коэффициент пересчета молярной концентрации эквивалентов гидроксида натрия из 0,1000 в 1,0000 моль/л.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



