с = 3.78·10-3 (моль/л) ·2∙79.9 (г/моль) ·103 (л/м3) = 604 г/м3 = 0.604 кг/м3.
2. При кондуктометрическом титровании 21.86 мл азотной кислоты 0.1352 М раствором КОН получены следующие данные: прибавлено миллилитров КОН 0; 11.26; 20.15; 38.32; соответствующие значения удельной электрической проводимости ![]() раствора (с поправкой на разбавление) равны соответственно 1.0000; 0.6079; 0.3635; 0.6050. Какова концентрация азотной кислоты?
раствора (с поправкой на разбавление) равны соответственно 1.0000; 0.6079; 0.3635; 0.6050. Какова концентрация азотной кислоты?
Решение. Построенный по экспериментальным данным график зависимости удельной электрической проводимости ![]() от объема V(KOH) прибавленного титранта представляет собой две прямые линии (сильная кислота и сильное основание), пересекающиеся при объеме 18.92 мл. Следовательно,
от объема V(KOH) прибавленного титранта представляет собой две прямые линии (сильная кислота и сильное основание), пересекающиеся при объеме 18.92 мл. Следовательно,
См(HNO3) · V(HNO3) = Cм(KOH) · V(KOH)
См(НNO3) = 0.1352моль/л ∙ 18.92 мл / 21.86 мл = 0.1169 моль/л. Примечание. При вычислениях нет надобности пересчитывать объемы в мл на объемы в л, поскольку объемы сокращаются.
3. Определение постоянной кондуктометрической ячейки. Установлено, что в кондуктометрической ячейке раствор хлорида калия KCI с концентрацией 0.1 моль/л имеет электрическое сопротивление 35.2 Ом. В той же ячейке раствор нитрата серебра AgNO3 с концентрацией 0.1 моль/л имеет сопротивление 42.4 Ом. Зная, что удельная электролитическая проводимость ![]() (KCI) раствора хлорида калия равна 1.29·10-1 См/см, вычислим: а) постоянную ячейки и б) удельную электролитическую проводимость
(KCI) раствора хлорида калия равна 1.29·10-1 См/см, вычислим: а) постоянную ячейки и б) удельную электролитическую проводимость ![]() ( AgNO3) раствора нитрата серебра. Примечание. Размерность См произносится как сименс.
( AgNO3) раствора нитрата серебра. Примечание. Размерность См произносится как сименс.
Решение.
Известно, что электрическое сопротивление R слоя раствора электролита, заключенного между электродами, прямо пропорционально толщине l этого слоя (расстояние между электродами) и обратно пропорционально площади s поверхности электродов:
![]() (1)
(1)
где ρ – удельное электрическое сопротивление и ![]() - удельная электрическая проводимость раствора.
- удельная электрическая проводимость раствора.
Отношение l/s называется постоянной кондуктометрической ячейки. Непосредственные измерения параметров l и s с помощью линейки приводят к большим ошибкам (нужно, чтобы электроды были строго параллельны и имели строго одинаковые размеры, что на практике выполнить затруднительно). Поэтому отношение l/s конкретной кондуктометрической ячейки определяют с помощью измерения Rя в этой ячейке раствора вещества, для которого известно точное значение ![]() , например, из справочника.
, например, из справочника.
а) Для определения постоянной кондуктометрической ячейки используем экспериментальный результат Rя = 35.2 Ом, полученный с помощью этой ячейки, и величину из справочника ![]() =1.29·10-1 См/см. Обе величины для 0.1 М раствора KCI.
=1.29·10-1 См/см. Обе величины для 0.1 М раствора KCI.
Как следует из (1), постоянная кондуктометрической ячейки определяется соотношением
l / s = Rя·![]() = (35.2 Ом) · (1.29·10-1 См/см)
= (35.2 Ом) · (1.29·10-1 См/см)
Поскольку 1 См = 1 Ом-1, имеем
l / s = 45.4·10-2 см-1
б) Электролитическая проводимость раствора AgNO3 с концентрацией 0.1 моль/л определяется следующим образом
![]() = ( l/ s) · (1/ Rя) = (45.4 10-2 см-1) · (42.4 Ом-1) = 1.07·10-2 См/см
= ( l/ s) · (1/ Rя) = (45.4 10-2 см-1) · (42.4 Ом-1) = 1.07·10-2 См/см
4. Гальванический элемент составлен из водородного электрода и цинкового электрода.
В результате измерения ЭДС гальванического элемента Zn – H, в котором [Zn2+ ] = 1M и ![]() атм, было установлено, что при 25оС Е = 0.45 В. Определить концентрацию ионов Н+ в водородном электроде.
атм, было установлено, что при 25оС Е = 0.45 В. Определить концентрацию ионов Н+ в водородном электроде.
Справочный материал. Стандартные равновесные электродные потенциалы полуреакций:
Zn2+(водн.) + 2е = Zn(тв.) ![]() (Анод)
(Анод)
2H+(водн,) + 2е = H2(г.) ![]() (Катод)
(Катод)
Решение. В гальваническом элементе протекает реакция
Zn(тв.) + 2H+(водн,) = Zn2+(водн.) + H2(г.)
Ее стандартная равновесная ЭДС
Е0 = ![]() .
.
Запишем уравнение Нернста для нахождения равновесной ЭДС Е:
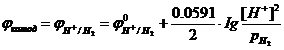
![]()
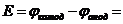
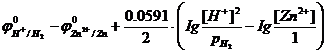
Е = Ео + 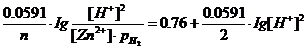
0.45 = 0.76 + ![]()
![]()
[H+] = 10-5.25 = 5.7·10-6 М
5. Потенциометрия.
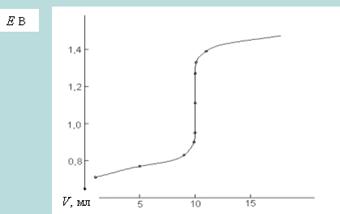
На рис. показана кривая титрования 10 миллилитров раствора FeSO4 раствором Ce(SO4)2 с концентрацией 0,1 н. По оси ординат отложены значения равновесного электродного потенциала ячейки, по оси абсцисс – суммарное количество добавленного титранта. Найти концентрацию исходного раствора FeSO4.
6. Вычислить равновесный электродный потенциал системы, образующейся при опускании инертного электрода в раствор, содержащий катионы двух - и трехвалентного железа с концентрациями [Fe2+] = 1 моль/л и [Fe3+] = 0.1 моль/л. 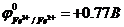
7. Дихроматометрическое титрование основано на реакциях окисления восстановителей дихроматом калия. Вычислить равновесный электродный потенциал системы, образующейся при опускании инертного электрода в раствор, содержащий ионы Cr2O72- и Cr3+ с концентрациями [Cr2O72-] = 1 моль/л и [Cr3+] = 0.1 моль/л. [H+] = 10-5 моль/л. Равновесный стандартный электродный потенциал 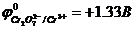
8. Перманганатометрическое титрование основано на реакциях окисления восстановителей перманганатом калия в кислой среде. Вычислить равновесный электродный потенциал системы, образующейся при опускании инертного электрода в раствор, содержащий ионы MnO4- и Mn2+ с концентрациями [MnO4-] = 1 моль/л и [Mn2+] = 0.1 моль/л. [H+] = 10-5 моль/л. Равновесный стандартный электродный потенциал ![]() .
.
9. Потенциометрия. Окислительно - восстановительное титрование. Ниже в таблице приведены результаты титрования 10,0 мл раствора FeSO4 0,1 н раствором Ce(SO4)2. Построить кривую зависимости φ от V(Ce(SO4)2) и найти эквивалентное количество добавленного титранта. Найти исходную концентрацию раствора сульфата железа(2).
№ | Суммарное количество добавленного титранта V(Ce(SO4)2), мл | φ, В |
1. | 1,00 | 0,71 |
2. | 9,00 | 0,83 |
3. | 9,90 | 0,90 |
4. | 9,99 | 0,95 |
5. | 10,01 | 1,27 |
6. | 10,10 | 1,33 |
7. | 11,00 | 1,39 |
10. Ячейка состоит из Pb электрода, погруженного в 0.015М раствор (CH3COO)2Pb, и Cd электрода, погруженного в 0.021М раствор CdSO4. Растворы соединены солевым мостиком, заполненным NH4NO3. Какова ЭДС ячейки при 25˚С? (Коэффициенты активности ионов в обоих растворах можно считать равными).
11. Каков рН раствора, если равновесный потенциал водородного электрода, измеренный при 25˚С относительно СВЭ, равен 0.703 В?
12. Ячейка состоит из двух проволочных Pt электродов, погруженных в стаканы, содержащие по 25 мл смеси 1М растворов хлоридов Fe(II) и Fe(III); растворы в стаканах соединены солевым мостиком. Добавление 1.0 мл раствора хлорида Sn(II) в один стакан вызывает появление разности потенциалов в 0.260 мВ. Принимая во внимание уравнение реакции
SnCl2 + 2FeCl3 →2FeCl2 + SnCl4
рассчитайте концентрацию раствора SnCl2.
13. Водный раствор (рН 5.0) проанализировали на содержание свободных F - ионов. Потенциал фторид - селективного электрода относительно подходящего электрода сравнения, погруженного в 100 мл анализируемого раствора, равен 120 мВ. Если к анализируемому раствору добавить точно 1.00 мл 0.1М раствора KF и перемешать, потенциал станет равным 108 мВ. Рассчитайте концентрацию фторид-ионов в анализируемом растворе.
14. Навеску металлического Zn массой 1.00 г растворили в 50 мл HCl и разбавили до 250 мл. В электролизер поместили 25 мл полученного раствора, добавили несколько капель раствора поверхностно-активного вещества, удалили растворенный кислород и зарегистрировали полярограмму в интервале потенциалов от 0 до -1 В относительно Hg анода. На полярограмме появилась волна с Е½ = -0.65 В высотой 7.6 см. К раствору в электролизере прибавили 5 мл 5·10-4М раствора CdCl2, удалили кислород, и вновь записали полярограмму. Потенциал полуволны не изменился, а высота увеличилась до 18.5 см. Рассчитайте процентное содержание примеси Cd в металлическом Zn.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 |



