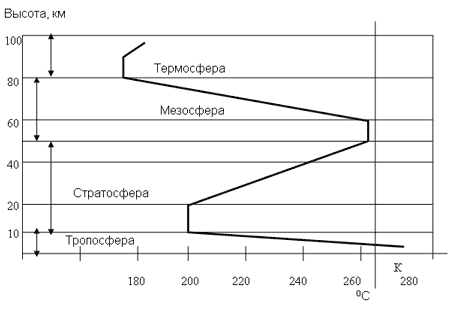
На высоте 1000 км находится экзосфера, откуда атмосферные газы рассеиваются в мировое пространство. И здесь происходит переход от атмосферы к межпланетному пространству.
Химический состав атмосферы неоднороден по высоте. На высотах до 90 км относительный состав постоянных компонент атмосферы остается практически постоянным. Свыше 90 км под влиянием ультрафиолетового излучения Солнца происходит диссоциация атмосферных газов и сильное изменение состава атмосферы с высотой.
Сплошная слоистая структура характерна для атмосферного аэрозоля - взвешенных в газообразной среде атмосферы жидких или твердых частиц земного и космического происхождения. Аэрозоли с жидкими частицами - туман, с твердыми - дым.
Сложным является и вертикальное распределение электронов и ионов в атмосфере, что выражается в существовании различных слоев ионосферы.
Состав компонент атмосферы Земли уникален - состоит преимущественно из азота и кислорода в процентном отношении объемной концентрации 78.1+20.9 ≈ 99%. Остальными компонентами являются углекислый газ, метан, закись азота, двуокись серы и др.
Наиболее важная переменная, составляющая атмосферы - водяной пар. Основная масса водяного пара сосредоточена в тропосфере, поскольку его концентрация быстро убывает с высотой. Среднее содержание водяного пара в вертикальном столбе атмосферы в умеренных широтах составляет 16-17 мм «слоя осажденной воды», т. е. такую толщину будет иметь слой сконденсированного водяного пара.
На атмосферные процессы, особенно на тепловой режим стратосферы, оказывает влияние озон. Озон вызывает поглощение ультрафиолетовой солнечной радиации.
Средние месячные значения общего содержания озона изменяются в зависимости от широты и времени года составляет 2.3 - 5.2 мм при наземных значениях давления и температуры.
В настоящее время отмечается влияние хозяйственной деятельности человека на разрушение озонового слоя атмосферы. Разрушителями озонового слоя могут быть фреоны (хладоны), представляющие собой группу галогеносодержащих веществ: Ф-11 (CFCl3), Ф-12 (CF2Cl2), Ф-22 (CHClF2) и др., кипящие при комнатной температуре, высоколетучие химически инертные у поверхности Земли, которые используются в холодильной промышленности и как распылители.
Поднимаясь в стратосферу фреоны подвергаются фотохимическому разложению с выделением иона хлора, служащего катализатором химических реакций, разрушающих молекулы озона, защищающих нашу планету от жесткого ультрафиолетового излучения.
В настоящее время ведется постоянное международное наблюдение (мониторинг) за озоновым экраном. В связи с угрозой разрушения озонового слоя многие страны сократили производство и потребление фреонов. Однако общий выпуск фреонов в мире растет, что приводит к возрастанию их концентрации в атмосфере. Среднее время жизни фреонов в атмосфере 70 - 100 лет. Темпы расширения озоновых дыр составляют 4 % в год.
Причины возникновения озоновых дыр являются как естественные, так и антропогенные воздействия. В частности - выбросы фреонов компоненты продуктов сгорания топлива, исчезновение лесов и др.
Вода является одним из наиболее важным компонентом экосистемы или биогеценоза. Вода как окись водорода H2O является простейшим устойчивым в обычных условиях химическим соединением водорода с кислородом.
Молекула жидкой воды состоит из объединения двух простейших молекул (H2O) 2 - дигидроль, льда - объединения трех простых молекул (H2O) 3 - тригидроль.
Общее количество воды на планете оценивается в 1,5-2,5x1024 г (от 1,5 до 2,5 млрд. км3).
Вода является одним из факторов формирования физической и химической среды, климата и погоды на нашей планете, возникновения жизни на Земле. Вода является обязательным компонентом практически всех технологических процессов промышленного и сельскохозяйственного производств, выступает как сырье - теплоноситель, транспортная система, растворитель и почти всегда, как среда, удаляющая отходы.
Отметим, что более 3/4 нашей планеты занимает вода (океаны, моря, льды на суше, реки, озера, болота).
Вода пронизывает все оболочки Земли, проникает в любые участки того пространства, где обитает человек и животные. Более того, наполняет растения и животных; человек тоже на 70 % состоит из воды.
Все водные объекты на поверхности Земли связаны между собой и образуют оболочку называемую андросферой.
Вода в природных условиях всегда содержит растворенные соли, газы и органические вещества. При концентрации солей до 1 г/кг вода считается пресной, до 25 г/кг солоноватой, более 25 г/кг - соленой. Наименее минерализированными водами являются атмосферные осадки, в которых в среднем концентрация солей составляет 10-20 мг/кг, затем пресные озера и реки. Соленость океана 35 г/кг.
Заметим, что вода - достаточно устойчивое соединение в обычных условиях. Распад молекул воды (термическая диссоциация) становится заметным лишь при температуре выше 1500 0C.
Разложение воды происходит также под действием ультрафиолетового (фото диссоциации) или радиоактивного излучения (радиолиз). При радиолизе воды кроме H2, O2 образуется также перекись водорода и ряд свободных радикалов.
Характерным химическим свойством воды является ее способность вступать в реакции присоединения, а также гидролитического разложения взаимодействующих веществ. Наиболее активные щелочные, щелочноземельные металлы реагируют с водой при комнатной температуре с выделением водорода и образованием гидроокисей:
2Na + 2H2O = 2NaOH + H2
Ca + 2H2O = Ca(OH) 2 + H2
Благородные металлы (золото, платина, серебро, палладий, рутений, радий), а также ртуть с водой не взаимодействуют.
Атомарный кислород превращает воду в перекись водорода: H2O+ O = H2O2
С азотом и водородом вода не взаимодействует, а с углеродом при высокой температуре дает водяной газ: С + H2O = CO + H2
Эта реакция может служить для промышленного получения водорода. Особый интерес представляет тяжелая вода, содержащая дейтерий: D2O(D2 = 2H - изотоп водорода
В общем объеме природных вод тяжелая вода составляет одну пятитысячную часть. Дейтерий был открыт в 1932 году американским ученым Г. Юри. Дейтерий используется во взрывчатой системе для водородной бомбы, в будущем может стать термоядерным горючим в энергетике. В воде потребляемой человеком, растворены важные для жизнедеятельности организма органические и неорганические вещества. Вода способствует электролитической диссоциации содержащихся в ней солей, кислот и щелочей выполняет роль катализатора разнообразных процессов обмена веществ в организме. Следует отметить государственный стандарт качества воды (ГОСТ-2874), который является нормативом при проектировании и эксплуатации хозяйственно-питьевых (коммунальных) водопроводов.
Эпидемиологическая безопасность воды обеспечивается очисткой сточных вод и их обезвреживанием, санитарной охраной водоемов, очисткой воды.
Содержание в воде хлоридов, сульфатов и продуктов разложения органических веществ(аммиак, нитраты и нитриты), а также солей азотной кислоты, широко применяемой в промышленности и сельском хозяйстве, может вызвать их накопление в пищевых продуктах и тяжелые отравления.
В связи с недостаточным или избыточным поступлением в организм микроэлементов с водой и пищей, среди населения встречаются характерные заболевания. Так, недостаточное содержание фтора в питьевой воде приводит к поражению зубов. Фтор в питьевой воде оказывает также влияние на фосфорно-кальциевый обмен и на процесс кальцификации костей.
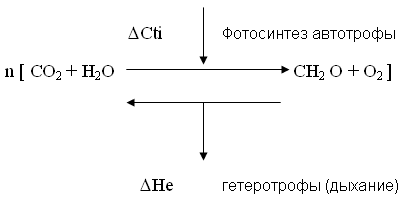
1.1.4 Перенос энергии, вещества и информации
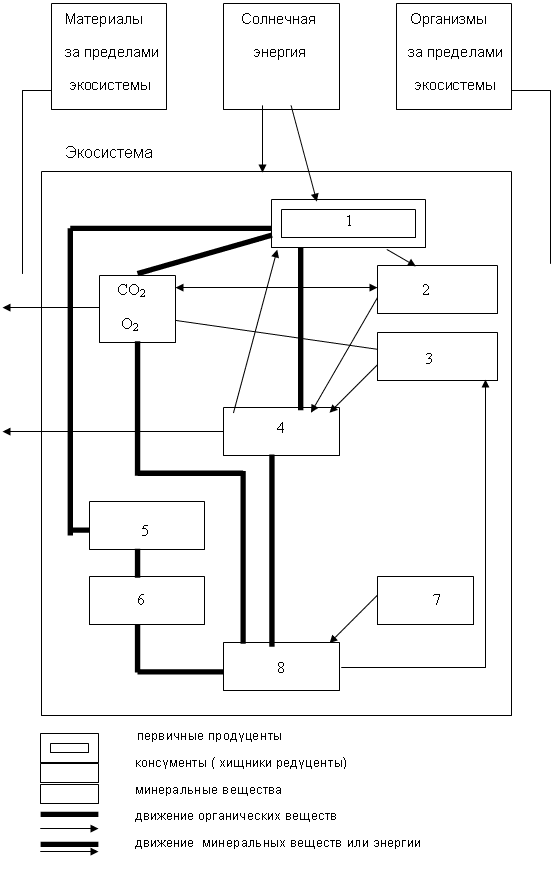
Сообщество – система совместно живущих в пределах некоторого естественного объема пространства автотрофных и гетеротрофных организмов.
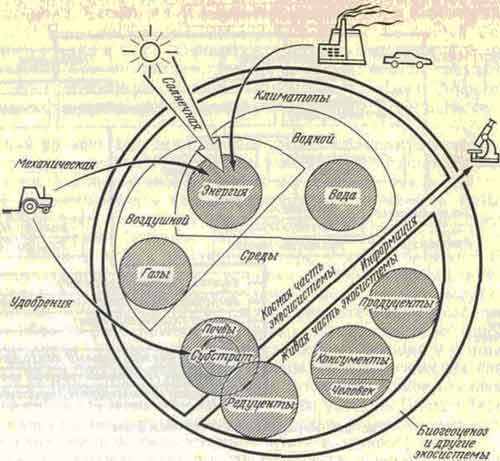
Общая схема экологической системы
Составляющие экологической системы |
1.2 Общесистемные обобщения

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 |