«Кислотные дожди».
Цель работы
- Изучить процессы сгорания серы: а) на воздухе, б) в кислороде Изучить растворение продуктов сгорания серы в воде Выяснить, как образуются кислотные дожди Изучить их влияние на растения
Что нужно для опыта Сжигание серы в воздухе:
- Серный цвет (порошок серы) Стеклянный цилиндр Ложечка для сжигания Часовое стекло Спиртовка Лист зеленого растения (хлорофитум) Набираем порошок серы в ложечку Поджигаем серу в ложечке в пламени спиртовки Вносим ложечку с горящей серой в цилиндр Наблюдаем белый дым от горения серы
Добавление воды
- С помощью промывалки вливаем в цилиндр воду В полученный раствор кладем лист зелёного растения хлорофитума Закрываем цилиндр часовым стеклом и оставляем на сутки
Что нужно для опыта Сжигание серы в кислороде:
- Серный цвет (порошок серы) Пероксид водорода и диоксид марганца (для получения кислорода) Стеклянный цилиндр Ложечка для сжигания Часовое стекло Спиртовка Лист зеленого растения (хлорофитум) Наливаем в цилиндр примерно 10 мл раствора пероксида водорода, добавляем диоксид марганца Начинается выделение кислорода по реакции 2H2O2 = 2H2O + O2 (диоксид марганца – катализатор реакции) Серу насыпаем в ложечку и поджигаем в пламени спиртовки Ложечку с зажженной серой вносим в цилиндр и кислородом Сера горит ярко-фиолетовым пламенем Образуется белый дым
Добавление воды
- С помощью промывалки вливаем в цилиндр воду В полученный раствор кладем лист зелёного растения хлорофитума Закрываем цилиндр часовым стеклом и оставляем на сутки
Через сутки
На фотографии видно, как сильно повреждаются листья хлорофитума при действии «кислотного дождя»
Добавили лакмус, мел и магний
- С помощью пипетки капаем на полоски красной и синей лакмусовой бумаги по 2 капли «кислотного дождя – раствора продуктов сгорания серы в воде Капаем «кислотный дождь» на кусочек мела Капаем «кислотный дождь» на магниевую стружку Красная лакмусовая бумага осталась без изменений, а синяя покраснела Мел запузырился, выделяется углекислый газ Магний начал растворяться, выделился водород
Выводы
- При проведении опыта окисление диоксида серы до триоксида серы не происходит. Но эта реакция идет в атмосфере и в промышленности при нагревании в присутствии катализатора. Кислотные дожди разрушают растительные клетки, растворяют магний и мел. Металлические детали и памятники архитектуры, если на них постоянно действуют кислотные дожди, будут разрушаться (из-за коррозии).
Чтобы предотвратить кислотные дожди, надо улавливать примеси диоксида серы (из трубы).
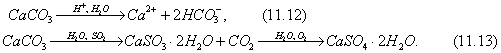
Основной реакцией, ответственной за разрушение мрамора и повреждения памятников, является образование сульфата, которое происходит на поверхности этих материалов. При этом окисление ![]() до
до ![]() происходит за счет каталитического действия таких поверхностных примесей, как
происходит за счет каталитического действия таких поверхностных примесей, как ![]() , копоть, влага, а также благодаря окисляющим серу бактериям. Обобщение большой информации, в том числе и рассмотренной выше, позволяет сделать ряд далеко идущих выводов о влиянии кислотных дождей на окружающую среду. В частности, можно утверждать, что:
, копоть, влага, а также благодаря окисляющим серу бактериям. Обобщение большой информации, в том числе и рассмотренной выше, позволяет сделать ряд далеко идущих выводов о влиянии кислотных дождей на окружающую среду. В частности, можно утверждать, что:
- кислотный дождь изменяет величину рН рек и озер и может вызвать их биологическую смерть;
- при поглощении почвами кислотный дождь выщелачивает основные природные минералы (калий, кальций, магний) и, унося их в подпочвенный слой, лишает деревья и растения питательных веществ;
- под влиянием кислотных дождей возрастает геохимическая подвижность алюминия, приводящая одновременно со снижением рН к возрастанию его концентраций и изменению его токсичных форм;
- кислотные дожди способствуют разрушению каменной кладки, а также архитектурных сооружений и памятников.
9. Изучение воздействия диоксида серы ( SO 2) на растения.
Загрязняющее вещество первоначально поступает в растение через устьица – отверстия, имеющееся на листьях и в нормальных условиях использующихся для газообмена. Диоксид серы, прежде всего, воздействует на клетки, которые регулируют открывание этих отверстий. Степень их открывания и факторы, влияющие на нее, в начальный период являются основными параметрами, определяющими интенсивность воздействия загрязнителей. Даже при очень малых концентрациях диоксид серы способен оказывать стимулирующее действие, в результате которого при достаточно высокой относительной влажности устьица остаются постоянно открытыми. В тоже время при высоких концентрациях диоксида углерода устьица закрываются. Кроме того, в случае высокой влажности устьица открываются, в случае низкой – закрываются.
Попав в межклеточные пространства листа, загрязняющее вещество вступает в контакт с мембраной окружающей клетку. При нарушении целостности этой полупроницаемой мембраны нарушается баланс питательных веществ и процесс поступления ионов.
Пройдя в клетку, диоксид серы взаимодействует с органеллами – метохондриями и хлоропластами, в том числе и с их мембранами, что может привести к весьма серьезным последствиям.
Однако сера необходима для нормального роста растений, и присутствие SO2 может оказывать влияние и на усвояемость серы. Растения потребляют серу в восстановленном состоянии. В присутствии SO2 основным продуктом становится сульфат; присутствует также цистеин, глютатион, и, по меньшей мере, одно не идентифицированное вещество. Основными промежуточными соединениями при восстановлении сульфатов являются сульфиты.
Возможна также дезактивация ферментов. Диоксид серы ингибирует различные биохимические реакции. Сульфиты, обладающие слабокислотными свойствами, дезактивируют некоторые ферменты, блокируя активные центры, препятствуя протеканию основной химической реакции; это явление известно как конкурентное ингибирование. Диоксид серы является конкурентным ингибитором дифосфаткарбоксилазы, препятствующим фиксации СО 2 в процессе фотосинтеза.
Хотя точный механизм действия SO2 на молекулярном уровне неизвестен, можно предположить, что основную роль играют присутствие избыточного количества окисленных форм серы, нарушение баланса с восстановленными формами и воздействие на жизненно важные ферменты.
Влияние диоксида серы на растения.
Наряду с действием SO2 на человеческий организм, большое значение имеет его влияние на растения. Концентрация SO2 1-2 млн-1 могут уже через несколько часов вызвать серьезное повреждение листьев в виде локализованных разрушений ткани (некрозов).У чувствительных растений хронические повреждения могут возникнуть уже начиная с концентраций 0.3 млн-1. Предельно допустимой даже для самых чувствительных растений считается концентрация 0.15 млн-1. Особенно подвержены воздействию SO2, помимо вечнозелёных хвойных деревьев, бобовые, а злаковые - ячмень.
Заключение
Хозяйственная деятельность человека, приобретая все более глобальный характер, начинает оказывать весьма ощутимое влияние на процессы, происходящие в биосфере. К счастью, до определенного уровня биосфера способна к саморегуляции, что позволяет свести к минимуму негативные последствия деятельности человека. Но существует предел, когда биосфера уже не в состоянии поддерживать равновесие. Начинаются необратимые процессы, приводящие к экологическим катастрофам. С ними человечество уже столкнулось в ряде регионов планеты.
Из-за увеличения масштабов антропогенного воздействия (хозяйственной деятельности человека), особенно в последнее столетие, нарушается равновесие в биосфере, что может привести к необратимым процессам и поставить вопрос о возможности жизни на планете. Это связано с развитием промышленности, энергетики, транспорта, сельского хозяйства и других видов деятельности человека без учета возможностей биосферы Земли. Уже сейчас перед человечеством встали серьезные экологические проблемы, требующие незамедлительного решения.
Для всего живого на Земле важны основные физические и химические свойства атмосферы как части природной среды. Давление атмосферы считается нормальным при величине у поверхности Земли 760,1 мм рт. ст. В пределах земного шара существуют постоянные области высокого и низкого давления, что обеспечивает динамику атмосферы и формирование системы господствующих ветров. Это обеспечивает вертикальное и горизонтальное перемешивание воздуха, рассеивание и ассимиляцию загрязняющих веществ.
Давление атмосферы мы не замечаем, хотя на каждого человека давит примерно около 12 т. воздуха. Для нас ощутимы лишь отклонения давления при подъеме на высоту (понижение), при погружении в воду (повышение). В абсолютном вакууме гибель живого наступает мгновенно. Однако исчезновение или резкое уменьшение атмосферного давления нашей планете не угрожает.
Прозрачность атмосферы имеет очень важное средообразующее значение. Именно от нее зависит проницаемость атмосферы для солнечных излучений видимых частей спектра. Количество (интенсивность) солнечной энергии определяет интенсивность фотосинтеза — единственного природного процесса фиксации солнечной энергии на Земле. Установлено влияние прозрачности на тепловой баланс Земли. Современные изменения прозрачности атмосферы в значительной мере определяются антропогенным влиянием, что уже привело к возникновению ряда проблем.
Весьма существенное значение имеет состояние газового баланса в атмосфере. Атмосфера в пределах тропосферы (до высоты 15—16 км), где заключено более 90% всей ее массы, состоит по объему из азота (78,09%), кислорода (20,96%), аргона (0,93%), углекислого газа (0,03%); она содержит также весьма малые доли инертных газов и озона.
Атмосферный азот является гигантским источником первичного «сырья» как для деятельности азотфиксирующих микроорганизмов и водорослей, так и для промышленности азотистых удобрений.
Без кислорода невозможно дыхание, а значит, энергетика многоклеточных животных. Вместе с тем кислород - это продукт жизнедеятельности, выделяемый фотосинтезирующими организмами. Накопление в ходе эволюции атмосферы и биосферы всего 1% кислорода создало условия для бурного развития современных форм жизни. При этом образовался озоновый экран - защита от космических лучей высоких энергий. Однако происходит катастрофическое уменьшение кислорода в атмосфере. За последние 10 лет количество его уменьшилось настолько, насколько уменьшилось за предыдущие 10 тыс. лет сокращения.
СПИСОК ЛИТЕРАТУРЫ:
1. , , Ладыгичев промышленных печей. Проектирование плавильных комплексов. Справочное издание. Т.1, кн.2. / Под ред. . - М. - Теплотехник, 2006. - 775 с.
2. , , Кочнов эффективности дожигания и охлаждение технологических газов крупнотоннажных дуговых сталеплавильных печей. Изв. вузов. Черная металлургия, 2009, №11. С.49-55.
3. , , Ладыгичев агрегаты: теплотехника, управление и экология. Справочное издание. В 4-х книгах, кн.1 / Под ред. . - М.: Теплотехник, 2005. - 768 с.
4. , , и др. Газоструйный стержневой излучатель. Патент РФ № 000. Опубл. 15.10.1994.
5.Ломаева загрязнений окружающей среды.- Тюмень, 1998.
6. , , Гущина практикум школьника. Методическое пособие для учителя. Издательский дом «Федоров». Издательство учебная литература, 2006.
7. , , Гущина практикум школьника. Методическое пособие для учащихся. Издательский дом «Федоров». Издательство учебная литература, 2005.
8. Ашихмина мониторинг: учебно-методическое пособие. М. : Академический проект Альма Матер, 2008.
9.Боголюбов жизненного состояния леса по сосне «Экосистема», 1999 // http://karpolya. ru/uploads/fajly/05sosny. pdf.
10. Биоиндикация загрязнений наземных экосистем / под ред. М: Мир, 1988.
11. Илькун атмосферы и растения. Киев: «Наукова думка», 1978.
12. , Мазепа -морфологические изменения хвои сосны в техногенных условиях. Журнал Лесоведение №1. 1987.
13. Рисунок «Хлорозы и некрозы хвои» //
14. и др. Здоровье людей и окружающая среда (учебное пособие);
15. и др. Охрана окружающей среды. Санкт-Петербург : Гидрометеоиздат 1991;
16. Болбас промышленной экологии. Москва : Высшая школа, 1993.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 |



