Hematology 2005
© 2005 The American Society of Hematology
Multimodality Therapies and Optimal Schedule of Antibodies: Rituximab in Lymphoma as an Example
Комбинированная терапия и оптимальный режим применения моноклональных антител: на примере ритуксимаба при лимфомах
Автор перевода
Michele Ghielmini
С момента своего первого использования у человека более 10 лет назад, ритуксимаб стал неотъемлемым компонентом лечения всех видов В-клеточных лимфом. Его иммуномодулирующий эффект так же способствовал росту использования препарата при неопухолевых гематологических заболеваниях (например, при идиопатической тромбоцитопенической пурпуре, криоглобулинемии) и негематологических заболеваниях (при ревматоидном артрите и других аутоиммунных заболеваниях). Несмотря на широкое использование, оптимальный режим назначения препарата, как в виде монотерапии, так и в составе комбинированной терапии, до сих пор до конца не разработан. Данный обзор сосредоточен на выборе наиболее подходящего режима применения ритуксимаба у больных с лимфомой.
Ритуксимаб в виде монотерапии
В 1997 году ритуксимаб в дозе 375 мг/м*2 в неделю в течение всего 4 недель был одобрен Центром по контролю за лекарствами и пищевыми продуктами США (US FDA) для лечения индолентных лимфом. Этот оригинальный режим применения был разработан на основе данных 1 фазы двух исследований, демонстрировавших безопасность и эффективность такой дозировки [1]. Объяснение выбора такой дозы базировалось в основном на эмпирических и логических заключениях. На момент получения одобрения от FDA другие режимы применения ритуксимаба изучены не были, и из-за своей безопасности и эффективности [2] данный режим стал стандартом на следующие несколько лет. Тем не менее, некоторые данные требовали изучений для подтверждения эффекта ритуксимаба. Все аспекты данного режима фактически могут быть пересмотрены: единая доза, количество введений, продолжительность лечения, интервал между курсами и скорость введения (Рисунки 1-3).
Рисунок 1. Режимы индукции ремиссии с использованием монотерапии ритуксимабом.
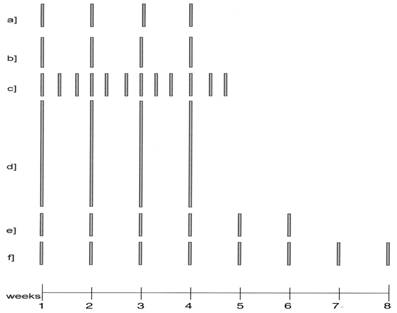
Примечание: Высота столбиков графика пропорциональна назначаемой дозе препарата.
Рисунок 2. Режимы использования ритуксимаба в комбинации с химиопрепаратами
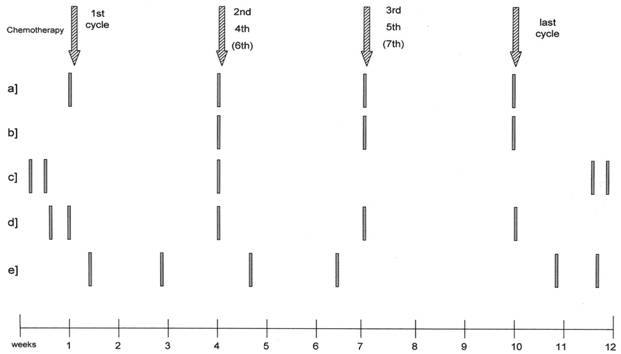
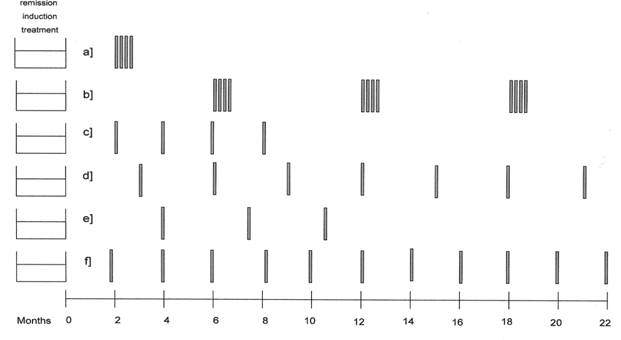
Рисунок 3. Режимы консолидации или продления ремиссии с использованием монотерапии ритуксимабом.

Доклинические данные о дозах и режиме применения
Ритуксимаб имеет множество возможных механизмов действия. Некоторые из них зависят от активации комплемента и иммунной системы организма, таким образом, исследования in vitro могут быть нерепрезентативными в отношении эффекта in vivo. Большинство исследований in vitro полагают, что зависимость ответа организма от дозы находится в пределах порога в 10-25 мг/мл, после которого кривая уровня препарата начинает падать, возможно, из-за «насыщения» рецепторов или других эффекторных механизмов [3]. Это не означает, что концентрация 10-25 мг/мл должна быть целевой для больного. Стабильные уровни ритуксимаба в плазме крови предполагают насыщение всех доступных рецепторов CD20, таким образом, любой измеримый уровень ритуксимаба является доказательством достаточного количества препарата в организме больного. Тем не менее, фармакокинетические данные из осевого исследования, определившего, что концентрация 25 мг/мл в течение в среднем 3 месяцев была связана с ответом на лечение [4], говорят о том, что режим, поддерживающий такой уровень в крови, может быть рекомендован эмпирически.
Единая доза
В оригинальном исследовании 1 фазы не было замечено дозозависимой токсичности при использовании ритуксимаба в дозе 375 мг/м*2. Эта доза была выбрана на основании ограниченной доступности препарата на 2 фазе исследования. С того момента только ограниченное число исследований оценивали эффект более высоких или низких доз. Coiffier и соавторы в небольшом рандомизированном исследовании сравнили назначение 375 мг/м*2 и 500 мг/м*2 при агрессивных лимфомах. Разницы в частоте ответа и продолжительности ответа выявлено не было [5]. У пациентов с хроническим лимфолейкозом (ХЛЛ) O’Brien и соавторы увеличивали дозу ритуксимаба с 375 мг/м*2 до 2250 мг/м*2 в неделю, всего лечили 4 недели [6]. Даже хотя исследование не было рандомизировано, сравнение небольших групп больных показало прямую взаимосвязь доза-ответ без возрастания токсичности. Несмотря на эти обнадеживающие данные, подобных исследований в отношении других лимфопролиферативных заболеваний проведено не было, возможно, из-за так называемой «экономической» дозозависимой токсичности. Данные, полученные на больных ХЛЛ, не могут быть экстраполированы на «солидные» лимфопролиферативные заболевания, поскольку клетки ХЛЛ экспрессируют низкие уровни антигена CD20 на своей поверхности, а при этом заболевании наблюдается уникально высокий уровень циркулирующих антигенов CD20 [7].
Продолжительность недельного лечения
Хотя частота ремиссий при 4-недельном курсе является удовлетворительной и сравнимой с другими режимами монохимиотерапии, вскоре стало очевидно, что продолжительность ремиссий и доля полных ремиссий так или иначе были меньше, чем при обычной химиотерапии. Для улучшения результатов лечения исследователи попытались продлить курс лечения до 6-8 недель [8, 9]. К сожалению, это было сделано в небольших пилотных исследованиях II фазы, что подтвердило некоторое улучшение в частоте полных ремиссий (что даже привело к регистрации 8-недельного «пролонгированного» режима лечения), хотя в дальнейшем эти данные не подтвердились. В целом, сегодня у нас нет существенных данных в пользу продления стандартного 4-недельного курса лечения.
Оптимальная продолжительность лечения ритуксимабом
РК анализ первого осевого исследования эффективности ритуксимаба показал, что у пациентов с более высоким и длительным уровнем препарата в крови частота ремиссий более высока [4]. Эти данные позволили предположить наличие прямой зависимости между продолжительностью воздействия препарата на клетки опухоли и возникновением ремиссии, что привело к удлинению периода лечения сверх стандартных 4 недель. Hainsworth и соавторы разработали стратегию программной повторной терапии, которая состояла из регулярного назначения 4-недельного курса ритуксимаба каждые 6 месяцев, всего 4 курса. В двух исследованиях II фазы (одно было посвящено фолликулярной лимфоме и лимфоме из малых лимфоцитов (ФЛ), другое – ХЛЛ) они показали, что продолжительность ремиссии была значительно большей при использовании такой программы, нежели при стандартном 1-месячном лечении [10, 11]. В последующем рандомизированном исследовании пациентов с рецидивами ФЛ, в котором пациенты могли получать дальнейшие курсы лечения ритуксимабом 1 раз в 6 месяцев, либо при необходимости ввиду наличия рецидива, авторы показали, что даже при учете значительно большей продолжительности ремиссий на программной повторной терапии, общая эффективность ритуксимаба не различалась в двух ветках исследования [12]. При выборе оптимального подхода к лечению врач должен учитывать финансовую сторону вопроса, т. к. пациент сэкономит часть денег (на 20% меньше использовалось ритуксимаба в группе больных, леченных «по необходимости»), и напротив, выгоду для здоровья пациента, т. к. у него будет меньше рецидивов и больше продолжительность ремиссий. Европейская Совместная Онкологическая Группа (ECOG) в настоящее время проводит исследование на большой группе больных с целью определения сопоставимости эффекта ритуксимаба при стандартных схемах лечения и при повторном лечении ритуксимабом рецидивов. Исследование RESORT рандомизировало впервые диагностированных больных ФЛ, ответивших на ритуксимаб в любом из этих двух режимов. Другой подход выбрала Швейцарская Группа по клиническому изучению рака (SAKK). Она рандомизировала больных с ФЛ или с лимфомой из мантийных клеток (ЛМК), леченных стандартным 1-месячным курсом ритуксимаба, либо одним таким курсом («индукция») плюс 1 инфузия ритуксимаба каждые 2 месяца, всего 4 курса. Последний из указанных курсов привел к удлинению лечения до 9 месяцев, а всего ритуксимаб действовал примерно около 1 года. В этом исследовании было показано, что пациенты с ФЛ, ответившие на курс индукции, имели в 2 раза более длительную ремиссию при пролонгированном курсе лечения [13], в то время как пациенты с ЛМК не имели статистически значимых различий между курсами [14]. SAKK в настоящее время проводит исследование, сравнивающее 9-месячный режим лечения с 5-летним курсом лечения, с целью определения эффективности пролонгированной терапии ритуксимабом для поддержания длительной ремиссии.
Интервал между назначениями препарата
Период полужизни ритуксимаба составляет 1 неделю, но средняя продолжительность поддержания активных уровней препарата в кровотоке – около 3 месяцев [4]. Следовательно, необходимость инфузий препарата с 1-недельным интервалом является дискутабельной. Даже с учетом того, что некоторые авторы утверждают, что первые дозы ритуксимаба должны назначаться через короткие интервалы времени, чтобы соединиться со всеми рецепторами CD20 на злокачественных В-клетках и перевести химиорезистентные клетки в химиочувствительные [15], эта гипотеза до настоящего времени не подтверждена. Поскольку доза ритуксимаба, используемая в обычном режиме, как правило, является излишней, курс лечения 1 раз в 3 недели, либо реже, будет не менее эффективным. В проспективном PK-based исследовании Gordan и соавторы указали оптимальный интервал между введениями. Приняв 25 мг/мл за целевую концентрацию препарата в сыворотке крови, они измерили концентрацию ритуксимаба у пациентов, леченных 1 месяц, и вводили дополнительно 1 дозу препарата каждый раз при падении концентрации ниже порогового уровня 25 мг/мл [16]. Используя эту стратегию, большинство пациентов смогут поддерживать активные уровни препарата в крови с интервалом между инфузиями в 3 месяца. У всех пациентов сохранится активный уровень препарата в крови, если они лечились каждые 2 месяца. Таким образом, мы можем заключить, что инфузия ритуксимаба каждые 2-3 месяца должна быть достаточной для воздействия активных концентраций препарата на опухоль. Это взято за основу многими исследовательскими группами в качестве поддерживающей стратегии лечения.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |


