Публикация доступна для обсуждения в рамках функционирования постоянно
действующей интернет-конференции “Бутлеровские чтения”. http:///readings/
Поступила в редакцию 6 февраля 2014 г. УДК 544.72+544.77.
Влияние состава дисперсионной среды на устойчивость
и электрокинетические свойства билирубина
© Родионова1+ Екатерина Юрьевна, Дмитриева*+2 Ирина Борисовна
и
Кафедра физической и коллоидной химии. Санкт-Петербургская государственная химико-фармацевтическая академия. Ул. Профессора Попова, 14. г. Санкт-Петербург, 197376. Россия.
Тел.: (812) 234-11-38. E-mail: *****@***ru , *****@***ru , *****@***ru
_______________________________________________
*Ведущий направление; +Поддерживающий переписку
Ключевые слова: билирубин, устойчивость дисперсий, электрокинетические свойства, электрокинетический потенциал, микроэлектрофорез, изоэлектрическая точка.
Аннотация
Методом микроэлектрофореза и фотометрии исследованы электрокинетические свойства и устойчивость водных дисперсий билирубина в зависимости от состава дисперсионной среды (рН, концентрация одно, двух и трехзарядных электролитов, аминокислот). Кислотно-основное равновесие для водных дисперсий билирубина устанавливается в течение нескольких часов. рН изоэлектрической точки билирубина, определенное методом микроэлектрофореза в растворе хлорида калия, составляет 3.9±0.1. Показано, что взаимодействие билирубина с простейшими аминокислотами, катионами железа(II, III) носит специфический характер.
Введение
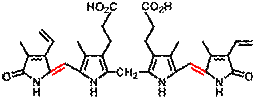
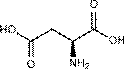
Тетрапиррольные соединения включают две больших подгруппы: макроциклические тетрапирролы и линейные тетрапирролы. И первая и вторая группы тетрапиролов широко распространены в природе и играют огромную роль в биологических процессах. Макроцик-лические пирролы представлены порфиринами и корриноидами. Ранее нами рассматривались коллоидные свойства природных порфиринов – хлорофилла и гемоглобина [1-4]. В настоящей работе анализируются электрокинетические характеристики одного из представителей линейных тетрапирролов – билирубина (структурная формула приведена на рис. 1).
|
Рис. 1. Структура молекулы билирубина |
Билирубин (лат. bilis желчь, ruber красный) – один из желчных пигментов, образую-щийся при разложении гемоглобина крови. Билирубин и другие желчные пигменты служат как продуктами, так и субстратами метаболизма порфиринсодержащих молекул, а также он является одним из естественных антиоксидантов, ингибирующих развитие процессов окисли-тельного стресса, поэтому нормальные физиологи-ческие концентрации данного пигмента считаются жизненно необходимым [5].
В живых организмах билирубин и биливердин образуют молекулярные комплексы с белками плаз-мы крови (альбумином и др.), в составе которых они транспортируются в печень, где подвергаются реакции конъюгации с глюкуроновой кислотой, а обра-зующиеся при этом водорастворимые глюкурониды выводятся из организма. При нарушении этого механизма происходит увеличение концентрации билирубина в крови и других тканях. Высокие концентрации билирубина (гипербилирубинемия) угнетают процессы окислитель-ного фосфорилирования и снижают потребление кислорода, что приводит к повреждению тканей.
Поэтому выделению билирубина из организма уделяется особое внимание. Наиболее распространенными методами удаления билирубина являются адсорбционные, электрохими-ческие и фотохимические методы [5].
Из исследований, проводимых в области коллоидной химии, основное внимание уде-ляется адсорбции билирубина из плазмы крови (например, "hemoperfusion treatment" в колон-ках с различными адсорбентами: активированным углем, агаром, синтетическими волокнами, альбумином, посаженным на макросетчатые смолы, полиакриламидом, полилизина на хитоза-новых сферах, стирен-дивинил-бензоловыми смолами, poly-EGDMA-HEMA микросферами и др. [6]), и из водных растворов. Поскольку в организме билирубин может находиться в свободном состоянии или быть связанным с альбумином, то во многих работах, посвященных адсорбции билирубина встречаются адсорбенты, модифицированные альбумином [7], либо проводится сравнительное исследование адсорбции билирубина и альбумина [8].
В молекуле билирубина присутствуют и основные, и кислотные группы (рис. 1). Карбо-ксикислотные группы образуют водородные внутримолекулярные связи с лактамными и пиррольными группами, поэтому билирубин имеет крайне низкую растворимость в воде [5, 9].
В щелочных водных растворах растворимость билирубина повышается за счет образо-вания дианиона, что сопровождается разрывом двух из шести внутримолекулярных водо-родных связей, а в кислых растворах молекулы билирубина коагулируют. Появление электро-кинетического потенциала на поверхности билирубина в водных растворах обусловлено адсорбцией протонов на пиррольных группах и гидроксил-ионов на карбоксильных группах. В зависимости от того, адсорбция каких ионов преобладает, меняются знак и величина электрокинетического потенциала частиц. В физиологических жидкостях помимо воды при-сутствуют катионы и анионы неорганических веществ, белки, аминокислоты, которые также влияют на адсорбцию протонов и гидроксил-ионов.
Электрокинетический потенциал является мерой агрегативной устойчивости дисперс-ных систем, характеризует способность билирубина взаимодействовать с белками (альбуми-ном), солями желчи [9]. Адсорбционные свойства билирубина в значительной степени опре-деляют оптические свойства его дисперсий [10]. Поэтому целью данной работы является комплексное изучение электрокинетических, адсорбционных свойств и устойчивости водных дисперсий билирубина в зависимости от состава дисперсионной среды (рН, концентрация одно, двух и трехзарядных электролитов, аминокислот).
Экспериментальная часть
В качестве объекта исследований использовался билирубин ЗАО "Вектон". Все химические реактивы, используемые в работе, были класса ХЧ. Для приготовления растворов использовалась бидистиллированная вода. В работе использовалась 1% дисперсия билирубина, приготовленная сле-дующим образом: навеска билирубина растиралась в ступке в небольшом количестве исследуемого раствора до образования густой пасты, затем добавлялся весь объем раствора.
Электрокинетический потенциал (ζ-потенциал) частиц билирубина определялся методом микро-электрофореза [11, 12]. Погрешность измерений электрокинетического потенциала не превышала 10%. Величина электрокинетического потенциала рассчитывалась по уравнению Гельмгольца-Смолуховс-кого. Уравнение использовалось без поправок, так как выполнялись условия ka >> 1, где k – обратная толщина ДЭС, а – радиус частиц.
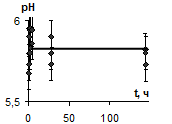
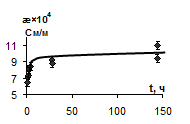
Выполнены исследования зависимости электропроводности, рН, электрокинетического потен-циала водных дисперсий билирубина от времени контакта фаз. Примеры этих зависимостей для водной дисперсии билирубина представлены на рис. 2, 3.
|
|
Рис. 2. Зависимость значений рН водных дисперсий билирубина от времени контакта фаз | Рис. 3. Зависимость значений удельной электропроводности водных дисперсий билирубина от времени контакта фаз |
Анализ полученных зависимостей показывает, что адсорбционное равновесие в системе уста-навливается в течение нескольких часов. Для удобства все дальнейшие измерения проводились при времени контакта фаз – 24 часа.
Результаты и их обсуждение
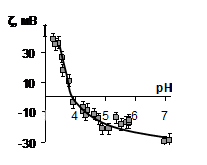
Рассмотрим влияние рН на электрокинетический потенциал билирубина, в растворе хлорида калия (принимается, что хлорид-ионы и ионы калия являются индифферентными для билирубина) (рис. 4). рН изоэлектрической точки билирубина в растворе хлорида калия – 3.9±0.1. При значениях рН, меньших 6.2, электрокинетический потенциал частиц билирубина положителен вследствие адсорбции ионов водорода, а при больших значениях – отрицателен из-за адсорбции ионов гидроксила.
|
Рис. 4. Зависимость электрокинетического потенциала водных дисперсий билирубина от рН в растворе хлорида калия с концентрацией 5·10-4 моль/л |
Желчнокаменная болезнь обусловлена нарушением обмена билирубина (и/или холестерина), характеризуется образованием камней в желчном пузыре или в протоках с возможным развитием опасных осложнений. рН желчи слабощелочная (около 7.3-8). При таком состоянии большая часть молекул билирубина должна находиться в виде ди-аниона и заряд молекул должен препятствовать их коагу-ляции, однако большую часть желчных камней составляет именно билирубин [14, 15].
Для любой дисперсной системы одной из главных характеристик является ее устойчивость, то есть способность "противостоять" агрегации и седиментации. Следствие про-цессов агрегации и седиментации билирубина – образование желчных камней. Исследование агрегации билирубина в зависимости от состава раствора и времени контакта фаз позволяет определить условия наибольшей устойчивости водных дисперсий билирубина.
Процесс коагуляции изучался по изменению оптической плотности (ΔA – разность между исходным значением оптической плотности и значением оптической плотности в рассматриваемый момент времени) в зависимости от состава водной фазы и времени коагу-ляции. На рис. 5, 6 приведены зависимости изменения оптической плотности от рН водных дисперсий в присутствии хлорида калия (5·10-4 моль/л) при времени коагуляции 60 минут.
Изменение оптической плотности дисперсий связано с нарушением устойчивости дис-персных систем. Нарушение устойчивости обусловлено двумя процессами – агрегацией час-тиц (увеличение рассеяния света), и седиментацией (под действием силы тяжести в зави-симости от плотности частиц дисперсной фазы по сравнению с плотностью дисперсионной среды они могут либо всплывать, либо оседать, вследствие чего оптическая плотность будет уменьшаться).
Максимум на кривых зависимостей изменения оптической плотности от рН соответст-вует значению изоэлектрической точки билирубина, которая совпадает со значением изо-электрической точки, определенной методом микроэлектрофореза рис. 4. Рассмотрим зави-симость изменения оптической плотности от электрокинетического потенциала: минималь-ные значения электрокинетического потенциала соответствуют максимальному изменению оптической плотности, то есть наименьшей устойчивости дисперсной системы.
Такая зависимость коагуляции частиц от концентрации адсорбирующихся на них ионов наглядно демонстрирует закономерности классической теории ДЛФО: если частицы имеют высокий электрический потенциал и достаточной толщины диффузный слой (большие значе-ния электрокинетического потенциала), то при перекрывании двух частиц энергия электро-статического отталкивания преобладает над энергией межмолекулярного притяжения.
Отметим, что полученных зависимостей недостаточно для объяснения образования желчных камней. Как и большинство биологических жидкостей, желчь представляет собой сложную систему, в которую помимо воды входит огромное количество всевозможных соеди-нений, включая катионы металлов [14, 15]. При слабощелочном рН желчи для частиц били-рубина противоионами будут катионы металлов и их присутствие, особенно двух - и трехзарядных будет влиять как на адсорбцию протонов и гидроксил-ионов, так и на электро-кинетический потенциал.
|
|
Рис. 5. Зависимость изменения оптической плотности водных дисперсий билирубина от рН в растворах КСl (5·10-4 моль/л) для времени коагуляции 1 ч | Рис. 6. Зависимость изменения оптической плотности водных дисперсий билирубина от значений электрокинетического потенциала в растворах КСl (5·10-4 моль/л) для времени коагуляции 1 ч |
Ранее показано для водных дисперсий гемоглобина и хлорофилла [2, 3], что катионы железа адсорбируются на них специфически (то есть не простое кулоновское взаимодейст-вие). Ионы железа сильно гидролизуются, гидролизованные ионы в растворе поляризуются и способны адсорбироваться в сверхэквивалентных количествах, кроме того железо, являясь переходным металлом способно образовывать комплексы как с ионами в растворе, так и на поверхности, вследствие ярко выраженных акцепторных свойств катионов железа.
|
|
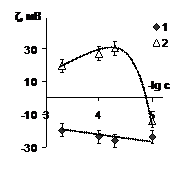
Рис. 7. Зависимость электрокинетического потенциала водных дисперсий билирубина от отрицательного логарифма концентрации катионов железа(II) (1) и катионов железа(III) (2) | Рис. 8. Зависимость электрокинетического потенциала водных дисперсий билирубина от рН в растворах сульфата железа(II) (1) и хлорида калия (2) с концентрацией 5·10-4 моль/л. |
На рис. 7, 8 представлены зависимости электрокинетического потенциала водных дисперсий билирубина от концентрации катионов железа и от рН. Влияние концентрации двух - и трехзарядного железа на электрокинетический потенциал водных дисперсий били-рубина соответствует классической теории ДЭС: увеличение концентрации двухзарядных противоионов вызывает уменьшение абсолютных значений электрокинетического потен-циала, а трехзарядных – уменьшение и перезарядку поверхности.
На рис. 8 отчетливо видно, что присутствие катионов железа(II) смещает изоэлектри-ческую точку в щелочную область. Смещение изоэлектрической точки свидетельствует о специфической адсорбции катионов железа.
|
|
Рис. 9. Глицин | Рис. 10. Аспарагиновая кислота |
Поскольку из крови и тканей били-рубин выводится в комплексе с альбу-мином, а также может взаимодействовать с другими белками, причем это взаимо-действие может быть специфическим, как, например, для азотсодержащих гете-роциклических соединений [16], исследуем воздействие составляющих белков – простейших аминокислот на примере глицина и аспарагиновой кислоты (рис. 9, 10) на водные дисперсии билирубина.
Рассмотрим влияние глицина и аспарагиновой кислоты на электрокинетический потен-циал водных дисперсий билирубина в зависимости от рН (рис. 11). В водной среде глицин и аспарагиновая кислота существуют в виде катионной, анионной или цвиттер-ионной формы. На билирубине могут сорбироваться одновременно различные ионные формы как за счет простого, электростатического взаимодействия, так и за счет специфического взаимодействия.
Сравнение изоэлектрических точек билирубина в растворах глицина, аспарагиновой кислоты и хлорида калия говорит о преобладании специфической сорбции анионных форм аминокислот, так как изоэлектрическая точка смещается в кислую область.
На рис. 12 изображена зависимость электрокинетического потенциала билирубина от концентрации глицина и аспарагиновой кислоты. Как отмечено ранее, потенциал-образую-щими ионами являются протоны и гидроксил-ионы, однако в присутствии глицина и аспара-гиновой кислоты добавляется сорбция анионных форм аминокислот, что сказывается на значениях электрокинетического потенциала – уменьшаются положительные значения элект-рокинетического потенциала и по абсолютной величине увеличиваются отрицательные значе-ния.
|
|
Рис. 11. Зависимость электрокинетического потенциала водных дисперсий билирубина от рН в растворах глицина, аспарагиновой кислоты и хлорида калия с концентрацией 5·10-4 моль/л | Рис. 12. Зависимость электрокинетического потенциала водных дисперсий билирубина от отрицательного логарифма концентрации глицина и аспарагиновой кислоты |
|
|
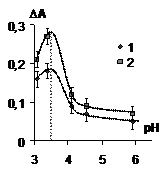
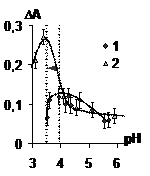
Рис. 13. Зависимость изменения оптической плотности водных дисперсий билирубина от рН в растворах глицина (5·10-4 моль/л) для времени коагуляции 30 минут (1) и для времени коагуляции 1 час (2) | Рис. 14. Зависимость изменения оптической плотности водных дисперсий билирубина от рН в растворах хлорида калия(1), глицина(2) и аспарагиновой кислоты(3) (5·10-4 моль/л) для времени коагуляции 1 час |
Глицин практически не влияет на рН раствора, поэтому главным фактором будет специфическая адсорбция его анионной формы на глицине – потенциал изменяется совсем незначительно. Аспарагиновая кислота из-за наличия двух карбоксильных групп имеет более ярко выраженные кислотные свойства, поэтому увеличение ее концентрации сказывается на рН раствора. Изменение рН раствора и специфическая сорбция анионной формы вызывают перезарядку поверхности. Анализ полученных зависимостей показывает, что решающее значение имеет и специфическая адсорбция аспарагиновой кислоты, и увеличение концент-рации протонов с увеличением концентрации аспарагиновой кислоты.
Данные, полученные для глицина и аспарагиновой кислоты, подтверждаются измене-нием оптической плотности во времени при различных значениях рН (рис. 13 на примере глицина). Максимум на кривых соответствует наименьшей устойчивости дисперсной систе-мы, и находится при рН изоэлектрической точки билирубина в растворах глицина. Как видно из рис. 14 максимумы на кривой зависимости изменения оптической плотности от рН для глицина по сравнению с хлоридом калия смещаются в кислую область, это смещение соот-ветствует смещению изоэлектрической точки на зависимости электрокинетического потен-циала от рН (рис. 12). Аналогичные результаты получены для аспарагиновой кислоты.
Процесс коагуляции идет во времени и характеризуется уменьшением оптической плотности (рис. 13, 14). Из рисунков видно, что наибольшей коагулирующей способностью обладает глицин.
Заключение
Исследования водных дисперсий билирубина показали, что они являются типичными коллоидными системами, свойства которых определяются природой дисперсной фазы (били-рубин) и составом дисперсионной среды. Взаимодействие билирубина с веществами, содер-жащимися в дисперсионной среде, определяет размеры поверхности частиц билирубина, их заряд, положение изоэлектрической точки, устойчивость дисперсий, влияет на их оптические свойства, на способность билирубина взаимодействовать с биологически активными вещест-вами.
При физиологических значениях рН электрокинетический потенциал частиц билирубина имеет достаточно большие отрицательные значения (< -30 мВ), поэтому повышение или уменьшение концентрации солевого фона, в частности солей железа, увеличение концент-рации аминокислот, белков, способность к специфическому взаимодействию является основ-ной причиной коагуляции билирубина.
Результаты исследований могут быть использованы при изучении процессов образова-ния желчных камней и разработке профилактических мер борьбы с желчекаменной болезнью, при подборе адсорбентов для выведения билирубина из организма, изучения механизмов взаимодейтвия билирубина с белками и так далее.
Выводы
1. Впервые проведены комплексные исследования зависимости электрокинетического потен-циала и устойчивости водных дисперсий билирубина от состава дисперсионной среды.
2. Адсорбционное равновесие в водных дисперсиях билирубина устанавливается в течение нескольких часов.
3. Изоэлектрическая точка билирубина, определенная методом микроэлектрофореза (в раст-воре хлорида калия), равна рНиэт=3.9±0.1. Полученное значение изоэлектрической точки подтверждено фотометрическими исследованиями устойчивости.
4. Катионы железа(II, III) сорбируются на билирубине специфически, так как смещают значе-ние рН изоэлектрической точки в щелочную область.
5. Увеличение концентрации трехзарядных катионов железа вызывает перезарядку поверх-ности, а двухзарядных – уменьшение абсолютных значений электрокинетического потен-циала в соответствии с классической теорией ДЭС.
6. Взаимодействие между билирубином и анионными формами аминокислот носит специ-фический характер. Коагулирующая способность возрастает в ряду хлорид калия – аспара-гиновая кислота – глицин.
Литература
[1] , , Чухно свойства гемоглобина в водных растворах НСl и KCl. Бутлеровские сообщения. 2012. Т.30. №6. С.103-107.
[2] , , Чухно свойства гемоглобина в водных растворах 1-, 2- и 3-зарядных ионов. Бутлеровские сообщения. 2013. Т.34. №6. С.135-140.
[3] , , Чухно свойства хлорофилла в водных растворах 1-, 2- и 3-зарядных катионов. Бутлеровские сообщения. 2013. Т.34. №6. С.130-134.
[4] , , Назипова ионов Н+ и ОН- на хлорофилле, влияние рН на устойчивость водных дисперсий хлорофилла. Бутлеровские сообщения. 2013. Т.34. №5. С.124-130.
[5] Антина билирубина и его аналогов. М.: КРАСАНД. 2009. 352с.
[6] Adil Denizli, Mustafa Kocakulak, Erhan Pişkin. Bilirubin removal from human plasma in a packed-bed column system with dye-affinity microbeads. Journal of Chromatography B: Biomedical Sciences and Applications. 1998. Vol.707. Iss.1-2. P.25-31.
[7] Alexander Timin, Evgeniy Rumyantsev, Alexey Solomonov. Synthesis and application of amino-modified silicas containing albumin as hemoadsorbents for bilirubin adsorption Journal of Non-Crystalline Solids. 2014. Vol.385. P.81-88.
[8] , , Севериновская комплекса билирубина с альбумином на поверхности высокодисперсного кремнезема. Коллоидный журнал. 2005. Т.67. №6. С.748-752.
[9] M. Paige Nittler, Rajan A. Desai, David A. Salikof, William E. Kurtin, Michelle M. Bushey. Bile salt micellar electrokinetic chromatography of bilirubin and related compounds. Journal of Chromatography A. 1997. Vol.779. P.205-214.
[10] G. Blauer, D. Harmatz Optical properties of bilirubin-serum albumin complexes in aqueous solution: II. Effects of electrolytes and of concentration. Biochimica et Biophysica Acta (BBA) - Protein Structure. 1972. Vol.278. Iss.1. P.89-100.
[11] , , Мартынов солей одно-, двух - и трехзарядных катионов металлов на сорбцию Н+ и ОН - ионов на декстране. Бутлеровские сообщения. 2011. Т.27. №14. С.47-54.
[12] I. B. Dmitriyeva, K. P. Tikhomolova, A. S. Chukhno, P. P. Prokopovich, V. M. Starov. Investigation of the electrosurface properties of NiO and Fe2O3 in azole solutions. Colloids and Surfaces A: Physicochem. Eng. Aspects. 2007. Vol.241. No.1-3. P.45-59.
[13] , Астахов , элементный, аминокислотный, структурный состав желчных камней. Бутлеровские сообщения. 2012. Т.32. №12. С.90-95.
[14] Henning Wittenburg Hereditary liver disease: Gallstones. Best Practice & Research Clinical Gastroenterology. 2010. Vol.24. No.5. P.747-756.
[15] Jayanta Roy-Chowdhury, Namita Roy-Chowdhury, and Peter L. M. Jansen. Chapter 74 - Bilirubin Metabolism and Its Disorders. Zakim and Boyer's Hepatology (Fifth Edition). 2006. P.1449-1474.
[16] , , Бриллиантова взаимодействия белков с биологически активными азотсодержащими гетероциклическими соединениями при различных значениях pH. Бутлеровские сообщения. 2013. Т.34. №5. С.91-99.
[17] , , Мартынов точка белков в водных растворах азолов. Вестник СПбГУ. 2011. Сер.4. Вып.2. С.124-133.