_________ Вписать текст или числовое значение величины
 Вписать формулу или название вещества
Вписать формулу или название вещества
|
Указать условия протекания химической реакции

Лабораторно-практическое занятие № 1 (2 часа, СРС – 2 часа)
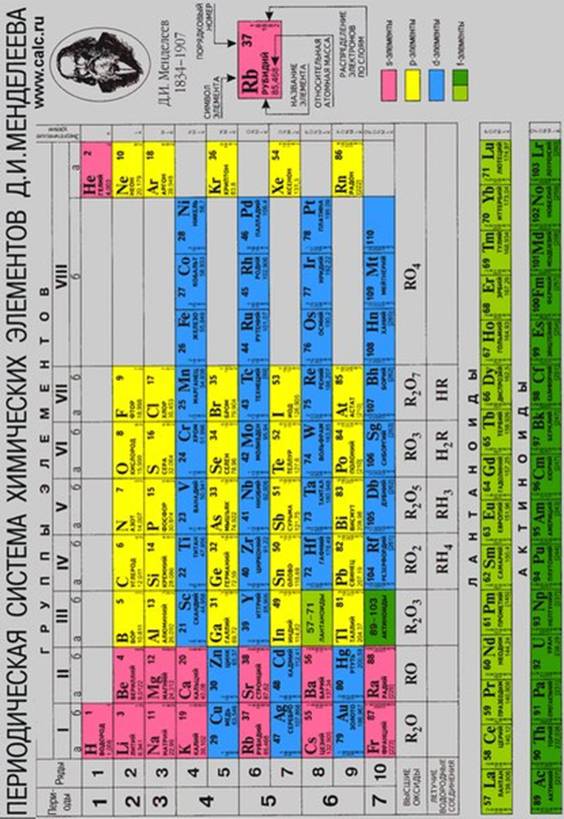
Тема: Периодический закон и периодическая система химических элементов
. Строение атома. Химическая связь
Цель: на основе теоретических знаний Периодического закона и периодической системы химических элементов уметь характеризовать свойства атомов в зависимости от положения элемента в периодической системе.
Задачи: Уметь
- характеризовать строение электронных оболочек атомов в зависимости от положения элемента в периодической системе;
- составлять электронные конфигурации атомов в возбужденном и невозбужденном состоянии;
- определять виды химической связи в соединениях;
- определять валентность и степень окисления элементов в формулах.
Знать
- периодический закон и структуру периодической системы ;
- электронное строение атомов элементов;
- виды химической связи: полярная и неполярная ковалентные связи, ионная, водородная, металлическая;
- строение веществ неорганической природы.
Вопросы и задания
1. Периодический закон : _____________________________________________
________________________________________________________________________________
________________________________________________________________________________
_______________________________________________________________________________________
![]() 2. Все вещества состоят из молекул. Молекулы состоят из атомов. Атом состоит из ____________________ и ____________________. Ядро состоит из________________ и _________________. Количество протонов равно количеству электронов и равно порядковому номеру элемента. В целом атом частица _________________________________.
2. Все вещества состоят из молекул. Молекулы состоят из атомов. Атом состоит из ____________________ и ____________________. Ядро состоит из________________ и _________________. Количество протонов равно количеству электронов и равно порядковому номеру элемента. В целом атом частица _________________________________.
3. Составьте схему «Строение атома»
 |
4. Заполните таблицу
атом S – сера | атом Cu - медь | |
Число электронов | ||
Число протонов | ||
Число нейтронов | ||
Суммарный заряд | ||
Относительная атомная масса |
5. Состояние электрона характеризуется квантовыми числами:
Главное квантовое число __________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
Орбитальное квантовое число______________________________________________________
________________________________________________________________________________
________________________________________________________________________________
Магнитное квантовое число _______________________________________________________
________________________________________________________________________________
________________________________________________________________________________
Спиновое квантовое число ________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
6. Для составления электронных конфигураций атомов элементов необходимо помнить о трех принципах:
1) Принцип Паули : ______________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
2) Правило Гунда: ________________________________________________________________
________________________________________________________________________________
________________________________________________________________________________
3) Принцип наименьшей энергии: __________________________________________________
________________________________________________________________________________
________________________________________________________________________________
7. Составьте электронные конфигурации для атомов элементов:
N | |
Si | |
Cl | |
Ca | |
Cr | |
Fe |
8. Установите соответствие между характеристиками и их изменениями в пределах подгрупп и периода, значками ↑ - увеличивается, ↓ - уменьшается, -//- не изменяется.
Характеристика | Подгруппа | Период | |
1 | Радиус атома | ||
2 | Металлические свойства | ||
3 | Окислительные свойства | ||
4 | Электроотрицательность | ||
5 | Энергия ионизации | ||
6 | Энергия сродства к электрону |
9. Проследите, как меняются свойства высших оксидов элементов III периода. Какие соединения образуются при их взаимодействии с водой?
Элементы III периода | |||||||
Высший оксид (RmОn) | |||||||
RmОn + Н2О | |||||||
Свойства |
|
 |  |
![]()
![]()
![]()
![]()




11. Заполните таблицу «Типы химической связи и механизмы их образования»
Вид химической связи | Природа взаимодействующих частиц | Механизм образования | Формула вещества |
12. Установите соответствие между формулой соединения и типом химической связи: NаI, HBr, K2S, H2O, CCl4, Cl2, Mg, NH4Cl, N2, HCl, FeCl3, Na, NH4OH, KI, HF.
ковалентная полярная | ковалентная неполярная | ковалентная по донорно-акцепторному механизму | ионная | металлическая | водородная |
Задачи
1. В V периоде периодической системы пришлось поменять местами два соседних элемента, поставив элемент с большей атомной массой перед элементом с меньшей атомной массой, иначе нарушается периодический закон.
Это элементы:_____________________________.
В чем выражалось бы это нарушение?_______________________________________________

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 |




