, учитель химии
МБОУ «Бутовская СОШ» Яковлевского района
ХИМИЯ (УМК )
Технологическая карта
(структура урока рассматривается в соответствии с концепцией урока
и требованиями федеральных государственных образовательных стандартов, ФГОС ОО)
Тема | Алюминий: физические и химические свойства | |
Цели (методическая) | Создание организационных условий на уроке для усвоения и практического применения материала по теме «Алюминий: физические и химические свойства» | |
Основное содержание темы, термины и понятия | Содержание темы предполагает:
| |
Планируемый результат | ||
Личностные умения - проявление эмоционально-ценностного отношения к учебной проблеме; - проявление творческого отношения к процессу обучения; - принятие и понимание ценности полученных знаний | Метапредметные умения Познавательные: - умение находить сходство и различие между объектами, обобщать полученную информацию; - умение вести наблюдение; - умение прогнозировать ситуацию. Регулятивные: - умение выполнять учебное задание в соответствии с целью; - умение соотносить учебные действия с известными правилами; - умение выполнять учебное действие в соответствии с планом. Коммуникативные: - умение формулировать высказывание; - умение согласовывать позиции и находить общее решение; - умение адекватно использовать речевые средства и символы для представления результата. | Предметные умения -умение объяснять состояние электрона в атоме, металлические свойства согласно положению элемента в Периодической системе - умение характеризовать физические свойства алюминия как металла, амфотерность оксидов и гидроксидов алюминия; - умение составлять уравнения реакций, характеризующих свойства алюминия, проводить химические опыты с алюминием и его соединениями. |
Организация образовательного пространства | ||
Межпредметные связи | Ресурсы | Формы работы |
Физика 9 (понятие о металлах с позиции физики). Тема «Алюминий, его физические и химические свойства». | 1) Схема 1 «Характеристика алюминия»: строение атома, металлическая химическая связь, характеристика простого вещества, химические свойства алюминия. 2) Схема 2 «Производство алюминия и его применение». 3) Самостоятельная работа к контролю знаний Мультимедийный проектор, таблицы «Электронное строение атомов химических элементов», ПСХЭ , коллекции металлов. |
(обозначения предлагаются обучающимся на уроке) |
ТЕХНОЛОГИЯ ИЗУЧЕНИЯ ТЕМЫ | ||
I этап. Самоопределение к деятельности | ||
Цели деятельности | Ситуативное задание | Планируемый результат |
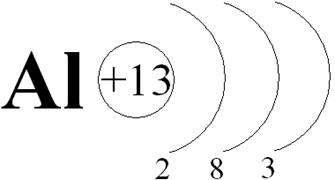
- актуализировать имеющиеся знания, связанные с понятиями строении атомов металлов, металлической химической связью, восстановительными свойствами металлов | Задание 1. Сравните строение атома алюминия с одним из щелочных металлов (просмотр схемы 1).
Задание 2. Химические свойства алюминия, как металла: взаимодействие с простыми (кислородом, азотом, углеродом) и сложными веществами (кислотами, солями, щелочами, оксидами металлов - восстановление металлов из их оксидов) (работа с учебниками: химические свойства, амфотерность оксида гидроксида алюминия)
Задание 3. Где и в каком качестве используется алюминий? Какие физические свойства этого металла объясняют области его применения?
(просмотр схемы 2) | Личностный: - проявление интереса к поставленной проблеме
Предметный: - умение объяснять строение атома алюминия как металла в сравнении с другими атомами; - умение объяснять взаимосвязь строения кристаллической решетки алюминия с физическими свойствами. Коммуникативные УУД: -умение работать с информацией на опережение; -умение работать в паре. |
II этап. Учебно-познавательная деятельность | ||
Цели деятельности | Учебные задания на «знание» (З), «понимание» (П), «умение» (У) и методы работы с информацией | Планируемый результат |
научить школьников: формулировать понятия: физические свойства металлов, химические свойства металлов, амфотерность составлять: электронно-графические формулы атомов химических элементов, составлять уравнения химических реакций, характеризующих свойства металла; объяснять: области применения металла в соответствии с его физическими свойствами, строением кристаллической решетки | Проблема: обобщить изученный материал, выполнить закрепляющие задания. Обучающимся предлагается задание Задание 4. Напишите уравнения реакций алюминия с веществами: бромом, разбавленной серной кислотой, раствором сульфата меди (2), оксидом хрома (3), расплавом и раствором гидроксида натрия. Первое уравнение напишите в свете ОВР, а второе в ионном виде. Проверка правильности выполнения задания. Обобщение материала.
| Регулятивные УУД - умение выполнять учебное задание в соответствии с целью.
Коммуникативные УУД - умение выполнять учебные задания в паре.
Предметный результат: умение давать характеристику химическим и физическим свойствам. |
Диагностика качества освоения темы | ||
Цель – установить степень усвоения темы « Алюминий, его физические и химические свойства» |
Задание 5. (П). Обучающиеся выполняют самостоятельную работу. Взаимопроверка в парах, сопоставление с эталоном. | Регулятивные УУД - умение выполнять задание в соответствии с целью. Предметный результат: умение характеризовать строение атома, ядра атома, состояние электрона в атоме, электронные конфигурации атомов. |
III этап. Интеллектуально-преобразовательная деятельность | ||
Цели деятельности | Варианты заданий | Планируемый результат |
- стимулировать интерес к выполнению заданий частично-поискового и эвристического характера; - научить школьников: ориентироваться в разных вариантах выполнения задания; планировать свои действия в соответствии с учебным заданием, представлять результат свой деятельности. | Задание 1. (репродуктивный уровень). 1.Изобразите электронную формулу алюминия, покажите распределение электронов по орбиталям. Какие степени окисления характерны для алюминия? 2.Объясните, почему алюминий, относящийся к активным металлам, часто не вытесняет водород из воды и менее активные металлы из солей? Задание 2. (частично-поисковый уровень). 1.С какими из перечисленных ниже веществ реагирует алюминий: а)хлор; б)сера; в)серная кислота; г)гидроксид калия; д)хлорид калия? Составьте уравнения реакций. 2. Напишите уравнения соответствующих реакций, с помощью которых можно осуществить следующие превращения: Al → NaAl(OH)4 ↓ ↑ AlCl3 → Al(OH)3 → Al2O3 Задание 3. (эвристический уровень). 1.Вычислите объём водорода (н. у.), который образуется при растворении алюминия массой 8,1 г в водном растворе щелочи. 2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: Al → Al2(SO4)3 → Al(OH)3 → Al(NO3)3 → KAl(OH)4. | Личностный: - творческое отношение к процессу выбора и выполнения заданий. Познавательный: - умение использовать методы наблюдения и прогнозирования для выполнения задания Регулятивный: - умение выполнять учебное действие в соответствии с планом Коммуникативный: - умение адекватно использовать речевые и символьные средства для представления результата. |
IV этап. Рефлексивная деятельность
| ||
Цели деятельности | Самоанализ и самооценка ученика | Результат деятельности |
научить школьников: - соотносить полученный результат с поставленной целью; - оценивать результат своей деятельности; - оценивать результат учебной деятельности. | Самоанализ I. Задание на самоанализ. Ответьте на вопросы. -Что узнал нового? - Что меня удивило? - Что показалось трудным? - Как я буду преодолевать трудности? - Как вы думаете, почему гуманитариям необходимо иметь представление о сложном строении атома? Самооценка II. Задание на самооценку. Закончите предложения: Я доволен(льна) тем, что сегодня самостоятельно смог(ла) ……………….. Я не доволен(льна) тем, что сегодня ………………… | *Заполняется учителем после освоения темы учащимися. |
Домашнее задание:§13, №3, |
| |
Приложения к содержанию урока
Схема 1 «Характеристика алюминия. Строение атома»
|
|
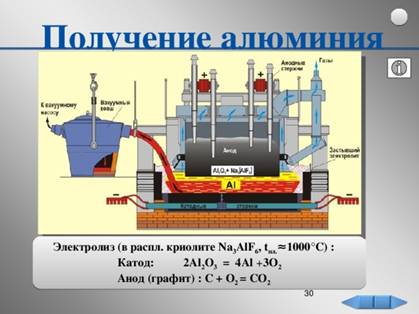
Схема 2 «Производство алюминия и его применение»
|
|
Самостоятельная работа (подготовка к контрольной работе)
Вариант 1
1. Напишите уравнения реакций алюминия со следующими веществами: хлором, разбавленной серной кислотой, оксидом хрома(III), раствором сульфата меди(II).
2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Al(ОН)3→ AlCl3→ Al(OH)3→ Al2O3
3. По каким внешним признакам вы сможете отличить изделия из алюминия от изделий из других материалов?
Ответы и решения:
1.
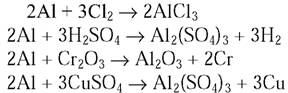
2.
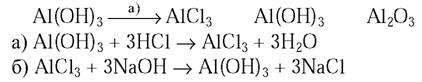
Вариант 2
1. Допишите уравнения химических реакций: а) Fe2O3 + Al → в) Al(ОН)3 + NaOH → б) Al2(SO4)3 + ВаС12 → г) Al + O2 →
В окислительно-восстановительных реакциях укажите окислитель и восстановитель.
2. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Al(NO3)3 → Al(ОН)3; Al2O3 → Al2(SO4)3; Al → AlС13
3. Опишите области применения алюминия и укажите свойства, на которых оно основано.
Ответы и решения:
1.
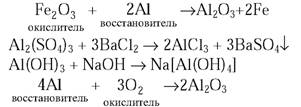
2.
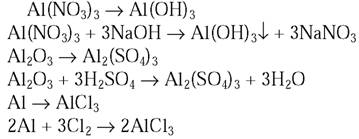
3. Алюминий применяется в самолетостроении, для изготовления проводов, в металлургии, при этом используются его легкость, высокая электропроводность и восстановительная способность.
Источники информации
1. Габриелян, . 9 класс: учеб. для общеобразоват. учреждений [Текст] / . – 2-е изд., стереотип. – М.: Дрофа, 2013. – 286 с.: ил.
2. Габриелян, . 9 класс: рабочая тетрадь [Текст]/ . – 3-е изд., стереотип. – М.: Дрофа, 2014. – 89 с.: ил.
3. Методические рекомендации к изучению темы «Алюминий» [Электронный ресурс] Режим доступ: https://infourok. ru/urok-po-himii-na-temu-metalli-392721.html, загл. с экрана