Вещество - это форма материи, обладающая массой (масса не равна нулю). Химия изучает большей частью вещества, организованные в атомы, молекулы, ионы и радикалы.
Простое вещество— вещество, состоящее из атомов одного химического элемента.
Сложное вещество, или соединение— вещество, состоящее из атомов разных химических элементов.
Моль - единица измерения количества вещества. Обозначается н. 1 моль — это такое количество вещества, в котором содержится столько же структурных единиц (атомов, молекул, ионов, радикалов), сколько атомов содержится в 0,012 кг изотопа углерода 12С.
Число Авогадро – 6,02 * 1023 частиц, количество частиц содержащихся в одном моле.
Ион (греч. iov - идущий)- электрически заряженные частицы, образовавшиеся из атомов (или атомных групп) в результате присоединения или потери электронов
Химическая реакция - превращение одного или нескольких исходных веществ (реагентов) в отличающиеся от них по химическому составу или строению вещества (продукты реакции).
Химический элемент - это вид атомов, характеризующийся определенными зарядами ядер и строением электронных оболочек.
Химическая формула - это условная запись состава вещества с помощью химических знаков (предложены в 1814 г. Й. Берцелиусом) и индексов (индекс - цифра, стоящая справа внизу от символа. Обозначает число атомов в молекуле). Химическая формула показывает, атомы каких элементов и в каком отношении соединены между собой в молекуле.
Атомная единица массы - единица измерения масс атомов, молекул и элементарных частиц. Численно равна 1/12 массы атома 12С – 1,66*10-27кг.
&1.2.2 Основные законы химии
Закон сохранения масс – масса веществ вступивших в реакцию равна массе веществ образовашихся в ходе реакции
Закон постоянства состава - любое определенное химически чистое соединение независимо от способа его получения состоит из одних и тех же химических элементов, причем отношения их масс постоянны, а относительные числа их атомов выражаются целыми числами.
Закон Авогадро - в равных объёмах различных газов, взятых при одинаковых температуре и давлении, содержится одно и то же число молекул (1 моль газа содержит 6,02*1023 частиц )
Уравнение Менделеева – Клапейрона (уравнение состояния идеального газа) — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
![]()
![]()
&2. Классификация неорганических веществ. Номенклатура
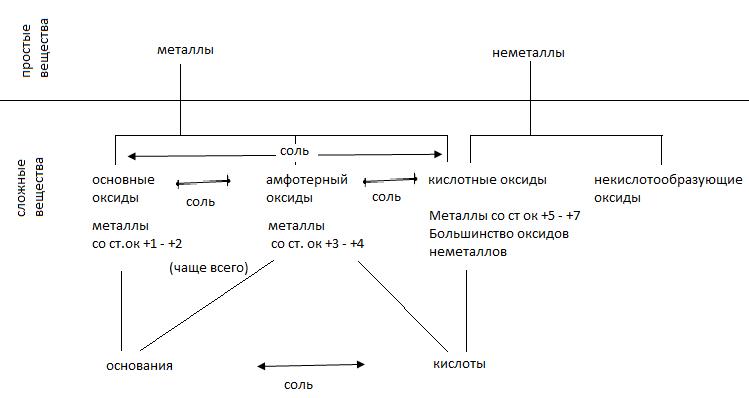
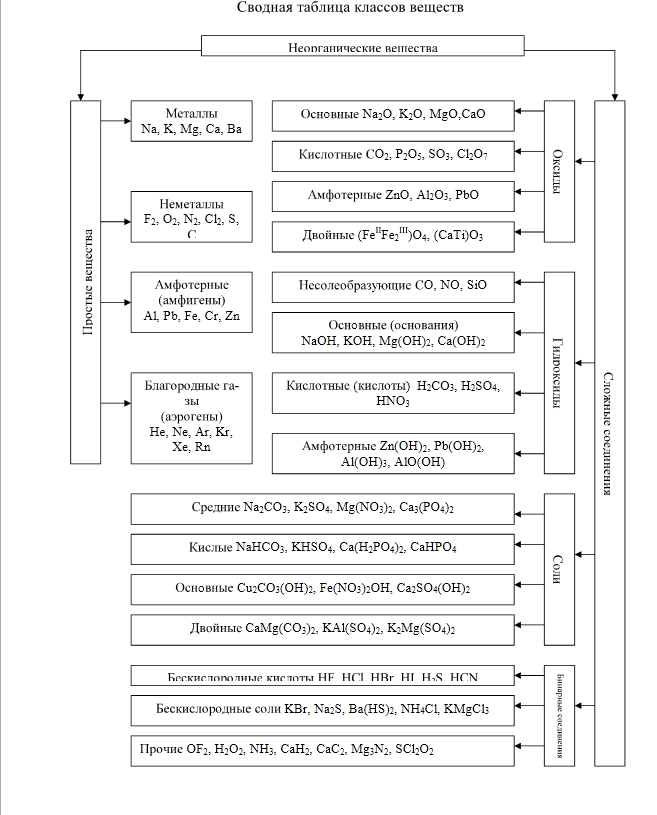
2.1 Генетическая связь
Металл: Ca CaO Ca(OH)2
CaSO4
Неметалл: S SO3 H2SO4
Металл - группа элементов, в виде простых веществ обладающих характерными металлическими свойствами, такими как высокие тепло - и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск.
Неметалл - химические элементы с типично неметаллическими свойствами, которые занимают правый верхний угол Периодической системы
Оксид - бинарное соединение химического элемента с кислородом в степени окисления −2, в котором сам кислород связан только с менее электроотрицательным элементом. К исключениям относятся, например, дифторид кислорода OF2.
Гидроксиды - соединения металлов с водой. Известны гидроксиды почти всех химических элементов; некоторые из них встречаются в природе в виде минералов. Гидроксиды щелочных металлов называются щелочами. Гидроксиды имеют вид : Me(OH)x
Кислота - химические соединения, способные отдавать катион водорода (кислоты Брёнстеда) либо соединения, способные принимать электронную пару с образованием ковалентной связи (кислоты Льюиса)
Соль - это сложные вещества, которые в водных растворах диссоциируют на катионы металлов и анионы кислотных остатков. ИЮПАК определяет соли как химические соединения, состоящие из катионов и анионов. Есть ещё одно определение: солями называют вещества, которые могут быть получены при взаимодействии кислот и оснований с выделением воды
2.2 Номенклатура
Названия простых веществ
Простые вещества называют, как правило, так же, как и соответ-ствующие элементы. Свои собственные названия имеют только ал-лотропные модификации углерода (алмаз, графит, карбин, фуллере-ны) и вторая модификация кислорода (озон). При названиях алло-тропных модификаций остальных элементов обычно указывают ее краткую физическую характеристику (белый, красный, черный фосфор, кристаллическая и пластическая сера, серое и белое олово и т. д.).
Бинарные соединения
В формулах двухэлементных соединений, состоящих из металла и неметалла, символ металла записывают на первом месте, то есть слева, а символ неметалла – справа. В соединениях из двух металлов или неметаллов первым записывают символ того элемента, ко-торый стоит в периоде развернутой Периодической системы левее, а в группе – ниже. Исключение составляют благородные газы, помещаемые как бы в нулевую группу и начинающие этот условный ряд и водород, который в этом ряду неметаллов традиционно помещают между элементами V и VI групп. Кислород записывают на первом месте только в соединениях со фтором. Примеры: MnI2, FeO, CuAl2, FeNi3, XeO4, CH4, AsH3, H2S, BrF3, ClO2, OF2. Названия бинарных соединений составляют из двух слов. В русском языке первым словом обозначают более электроотрицательный элемент (реальный или условный анион), составляя его из латинского корня названия элемента с окончанием - ид, вторым сло-вом является русское название менее электроотрицательного эле-мента (реального или условного катиона) в родительном падеже:
NaCl - хлорид натрия;
B2O3-оксид бора;
Al2S3-сульфид алюминия;
Mg3N2-нитрид магния.
В случае, если менее электроотрицательный элемент имеет несколько положительных степеней окисления, в названии следует указать либо его степень окисления, либо число атомов аниона, используя числовые приставки:
приставка | Кол-во атомов | приставка | Кол-во атомов | приставка | Кол-во атомов |
Ди- | 2 | Тетра- | 4 | Гекса- | 6 |
Три- | 3 | Пента | 5 | Гепта- | 7 |
FeCl3 –х лорид железа(III);
FeCl2 - дихлорид железа;
SF6 - гексафторид серы;
SF4 - фторид серы(IV);
PbO2 - диоксид свинца;
PbO - оксид свинца(II);
Pb3O4 - оксид свинца (II, IV);
N2O4 - тетраоксид азота.
В последнем примере однозначность написания формулы по названию обусловлена отсутствием у азота степени окисления (VIII).
Если соединение содержит катионы нескольких металлов или анионы нескольких неметаллов, то при написании формулы придерживаются того же порядка, как и в случае соответствующих бинарных соединений, а называют вещество справа налево, используя дефис:
SnBrCl3 - трихлорид-бромид олова;
KNaCl2 - хлорид натрия-калия;
Cu2Cl2O - оксид-хлорид меди(II);
CaTiO3 - оксид титана(IV)-кальция;
Кислородсодержащие кислоты
Названия этого класса соединений строятся из группового слова «кислота» и прилагательного, которое составляется из русского корня названия элемента, окончания - ая - и суффиксов, указывающих, насколько степень окисления кислотообразующего элемента отличается от максимальной.
Для высшей или единственной степени окисления применяют суффиксы - н-, - ов-, - ев - :
H3BO3 - борная кислота; H2CO3 - угольная кислота;
H2SiO3 - кремниевая кислота; H2CrO4 - хромовая кислота;
HNO3 - азотная кислота; HPO3 - метафосфорная кислота;
HReO4 - рениевая кислота; H3PO4 - ортофосфорная кислота.
Приставки орто - и мета - применяют, чтобы различать названия кислот, молекулы которых отличаются только «содержанием воды».
Если возможны две степени окисления, то для низшей используют суффиксы - ист-, - овист-:
H2SeO3 - селенистая кислота; H2TeO3 - теллуристая кислота;
HAsO2 - метамышьяковистая кислота;
H3AsO3 - ортомышьяковистая кислота.
В случае трех возможных степеней окисления кислотообразующего элемента, помимо упомянутых суффиксов, для самой низкой (обычно +1) применяется составной суффикс - новатист-:
H3PO2 - фосфорноватистая кислота;
H2N2O2 - азотноватистая кислота.
В названиях кислот с четырьмя различными степенями окисления последовательно используют суффиксы - н-, - новат-, - ист - и - новатист-:
HClO4 - хлорная кислота; HClO3 - хлорноватая кислота;
HClO2 - хлористая кислота; HClO3 - хлорноватистая кислота.
Для того, чтобы различить кислоты, содержащие разное количе-ство атомов кислотообразующего элемента в одной степени окис-ления, применяют числовые приставки:
H2Cr2O7 - дихромовая кислота; H2Cr3O10 - трихромовая кислота;
H2S2O5 - дисернистая кислота;
Оксокислоты, в которых атомы кислорода замещены на атомы серы (частично или полностью) или на пероксогруппы (-О-О-), по-лучают к своему названию приставку соответственно тио - или пероксо - (по необходимости, с числовой приставкой):
H2S2O3 (H2SO3S) - тиосерная кислота;
H2CS3 - тритиоугольная кислота;
HNO4 (HNO2(O2)) - пероксоазотная кислота;
H2S2O8 (H2S2O6(O2) - пероксодисерная кислота.
Название солей
Название солей неорганических соединений состоят из традиционных названий катионов и анионов. Если элемент в образуемых им оксоанионах проявляет одну степень окисления, то название аниона оканчивается на - ат:
(NH4)2CO3 - карбонат аммония; K4SiO4 - ортосиликат калия;
NaBiO3 - висмутат натрия; LiBO2 - метаборат лития.
В случае двух степеней окисления ещё используют окончание - ит:
BaSeO4 - селенат бария; FeAsO4 - ортоарсенат железа(III);
BaSeO3 - селенит бария; Fe(AsO2)2 - метаарсенит железа(II).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



