Уравнение Шредингера – уравнение, описывающее изменение в пространстве и во времени чистого состояния электрона, задаваемое волновой функцией (волновая функция – вероятность обнаружения объекта (электрона) в одном из чистых состояний).
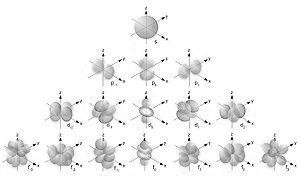
Пространство вблизи ядра, в котором вероятность нахождения электрона достаточно велика (примерно девяносто процентов), называется орбиталью. Это пространство ограничивается поверхностью, то есть объемной геометрической фигурой.
Атмана орбиталь – одноэлектронная волновая функция, полученная решением уравнения Шредингера.
Орбитали (электронные облака) отличаются не только размерами, так и формой.
Атомная орбиталь описывается 4 квантовыми числами.
- главное квантовое число – введено Бором – «n» - определяет энергетический уровень электрона на орбите. n принимает значение целых чисел от 1 до ∞. ∞ означает отрыв электрона от атома.
- орбитальное квантовое число – введено Зоммерфельдом - «l» - определяет форму атомной орбитали. l принимает значение от 0 до n-1/
Значение l | 0 | 1 | 2 | 3 |
обозначение | s | p | d | F |
- магнитное квантовое число – «m»- определяет пространственное расположение орбитали (см. выше) – опыт П. Зеемана в 1896 г, вводится уравнением Шредингера.
m принимает целые значения от – l (орбитальное квантовое число) до l (значения идут через «ноль»)
- спиновое квантовое число – «s» - введено Паули в 1924 – угловое вращение электрона
s = ±Ѕ
правила заполнения электронных орбиталей:
- принцип Паули (правило запрета) – два и более электрона не могут иметь все одинаковые квантовые числа (не могут находится в одинаковых квантовых состояниях).
- правило Хунда – модуль суммарного спинового числа должен быть максимальный
- правило Клечковского (правило n+l) – эмпирическое правило – при заполнении орбитальных оболочек атома более предпочтительны (а значит более энергетически выгодны – заполняются раньше) те состояния, для которых сумма главного квантового и орбитального чисел минимальна.
&4. Периодическая система химических элементов
Предшественники и продолжатели
1772 Л. Гитон де Морво составил первую таблицу «химически простых» веществ. А. Лавуазье использовал ее в своей книге «Начальный учебник химии», опубликованной в 17К9 г. 1817-1К29 И. Дёбернейнер открыл несколько триaд элементов и их соединений, в которых эквивалентный вес центрального элемента триады являлся средним из эквивалентных весов двух других элементов (например, СаО, SrO, ВаО илы NiО, СuО, ZnO).
1843 Л. Гмелин включил V-образнсе построение из 16 триад в 4-е издание своего «Справочника по химии».
1857 Ж. Дюма опубликовал таблицу 32 элементов из 8 колонок, показывающую взаимоотношения элементов.
1862 А. де Шанкуртуа впервые расположил элементы н порядке возрастания атомных весов; в публикации 1863 г. он придав этому ряду форму пространственной спирали, расположив сходные элементы друг под другом.
1864 Л. Мейер опубликовал таблицу валентностей для 49 элементов.
1864 У. Одлинг составил почти правили зую таблицу, в 17 вертикальных колонках которой были размещены 57 элементов.
1865 Дж. Ньюлендс после двух лет работы над различными вариантами классификации элементов предложил закон октав; он также правильно предсказал атомный вес еще неоткрытого элемента германия 1868-1869 Л. Мейер построив кривую атомных объемов и составил периодическую таблицу (таблица опубликована лишь в 1895 г.).
1869 сформулировал свой периодический закон: «свойства элементов находятся в периодической зависимости от их атомных весов» и опубликовал несколько вариантов периодической таблицы, один из них содержал 63 элемента.
1871 усовершенствовал свою таблицу и предсказал открытие 10 элементов (ныне они известны как Sс, Gа, Ge, Тc, Rе, Ро, Fг, Ra, Аc, и Ра). С поразительным предвидением он полностью описал свойства четырех из них (Sс, Gа, Ge и Ро). Заметим, однако, что в то время было невозможно предсказать существование благородных газов или число лантанидов.
1894-1898 Лорд Рэлей, У. Рамзай и М. Траверс открыли и затем выделили благородные газы (Не), Ne, Аr, Кr, Хе.
1913 Н. Бор объяснил форму периодической таблицы на основе своей теории строения атома и показал, что возможно существование лишь 14лантаноидов.
1913 Г. Мозли обнаружил закономерности в характеристических рентгеновских спектрах элементов, установил смысл атомного (порядкового) номера элемента Z и подтвердил правильность расположения элементов в периодической таблице (закон Мозли).
1940 Э. Макмиллан и Ф. Эйблсон синтезировали первый трансурановый элемент 93Np. Другие трансурановые элементы были синтезированы Г. Сиборгом с сотрудниками в течение следующих 15 лет.
1944 Г. Сиборг выдвинул актинидную гипотезу и предсказал существование в этой группе 14 элементов (вплоть до Z= 103).
Периодический закон открыт в 1869 году.
Современная формулировка периодического закона:
Периодическое изменение свойств элементов и их соединений зависит от периодически повторяющейся подобной структуры электронной оболочки их атомов.
Наглядным выражением периодического закона является периодическая система элементов.
В периодической системе каждый элемент имеет свой порядковый номер, смысл которого теперь совершенно ясен: этот номер равен заряду ядра атома и числу электронов в оболочке атома.
Современный вариант периодической системы утвержден Международным союзом по теоретической (чистой) и прикладной химии – ИЮПАК – в 1989 году.
Система элементов слагается из периодов (горизонтальные строки) и групп (вертикальные столбцы).
Периодов в системе семь: 1 – 3 –малые, остальные – большие, седьмой – не завершен. Номер периода указывает на число уровней в атоме данного элемента.
Групп в системе - 18, они обозначаются арабскими цифрами.
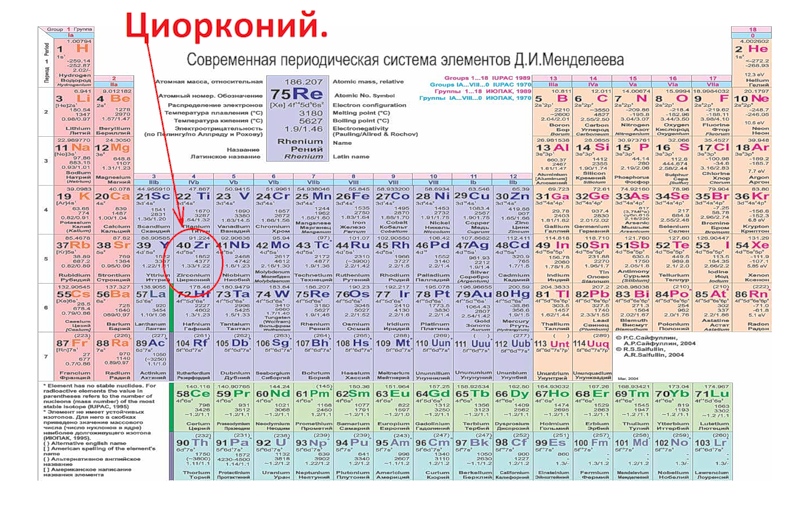
Вариант таблицы используемая в России –7 периодов (горизонтальные ряды) и 8 групп (вертикальные ряды). Группы делятся на главные (заполняются s - и p - электроны внешнего уровня) и побочные (заполняются d-электроны предвнешнего и f-электроны предпредвнешнего уровня).
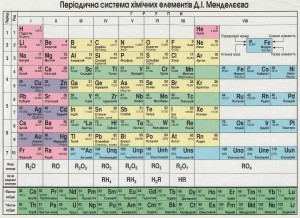
Номер группы – количество электронов на внешнем уровне (для главной подгруппы) – максимальная положительная степень окисления элемента (кроме кислорода, фосфора и благородных газов).
Электроотрицательность атома, величина, характеризующая способность атома в молекуле притягивать электроны, участвующие в образовании химической связи. Известно несколько способов вычисления Э. Так, согласно Р. Малликену (1935), мерой Э. может служить сумма ионизационного потенциала атома и его сродства к электрону; Л. Полинг предложил (1932) другой, более сложный способ вычисления. Оказалось, однако, что все способы практически приводят к одинаковым результатам.
Степень окисления - численная величина электрического заряда, приписываемого атому в молекуле в предположении, что электронные пары, осуществляющие связь, полностью смещены в сторону более электроотрицательных атомов.
Изменение свойств
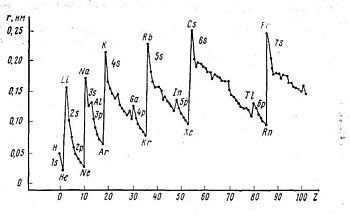
рис. Изменение радиусов по периоду и по группе.
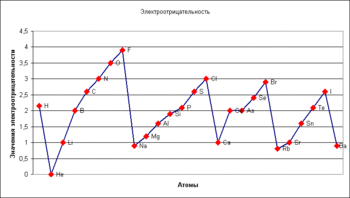
рис. Изменение электроотрицательности
&5. Химическая связь
5.1 Общие положения.
Молекулы химических веществ представляют собой сложную систему атомных ядер и электронов. Атомы в молекуле удерживаются преимущественно силами электростатического характера. В этом случае говорят, что они связаны химической связью. Химическая связь осуществляется s - и p-электронами внешнего и d-электронами предпоследнего слоя. Эта связь характеризуется следующими параметрами:
1. Длиной связи – межъядерным расстоянием между двумя химически связанными атомами.
2. Валентным углом – углом между воображаемыми линиями, проходящими через центры химически связанных атомов.
3. Энергией связи – количеством энергии, затрачиваемой на ее разрыв в газообразном состоянии.
4. Кратностью связи – числом электронных пар, посредством которых осуществляется химическая связь между атомами.
Атом в молекуле – понятие условное, т. к. его энергетическое и электронное состояние в корне отличается от изолированного атома. Если мы будем сближать два протона, то между ними возникнут силы отталкивания, и о получении устойчивой системы говорить не приходится.
В образовании химической связи участвуют s-, p - и d-электроны, имеющие различную геометрическую конфигурацию электронных облаков и различные знаки волновых функций в пространстве. В зависимости от симметрии электронных облаков, в результате перекрывания которых образуется химическая связь, суммарное электронное облако будет иметь различную симметрию, в соответствии с которой они распадаются на три вида: у-, р - и д - связи.
у-связь осуществляется при перекрывании облаков вдоль линии, соединяющей центры атомов, при этом максимальная электронная плотность достигается в межъядерном пространстве и имеет цилиндрическую симметрию относительно линии, соединяющей центры атомов.
Как видно из рис. 2.4., в образовании у-связи в силу своей шаровой симметрии всегда принимают участие s-электроны. Они образуют у - связь в
результате перекрывания со следующими электронами другого атома: s-, рХ-, d(x2-y2)-электронами. Возможность образования у-связи s-электронами не исчерпывается, она может образоваться в случае перекрывания и других электронных облаков, таких, как двух pX или pX и d(x2-y2).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



