Лекция №1. Строение и физические свойства
биологических мембран
План лекции
Функции биологических мембран (БМ) Химический состав и структура биологических мембран Жидкостно-мозаичная модель БМ БМ как электрический конденсатор Методы исследования структуры БМИсследование биологических мембран занимает центральное место в молекулярной и клеточной биологии и имеет важнейшее значение для фармации и медицины. Биологические мембраны отграничивают внутреннее содержимое клетки от внеклеточного пространства (обеспечивают автономность клетки), обеспечивают взаимодействие клетки с окружающей средой, с соседними клетками. Биологические мембраны участвуют в транспорте ионов, питательных веществ, передаче сигналов и преобразовании энергии. Их дисфункции зачастую приводят к развитию таких тяжелых заболеваний, как болезнь Альцгеймера, Паркинсона, диабет, рак, инфаркт и многие другие.
Биологические мембраны (от латинского слова membrana-перепонка) - функциональные структуры клетки, ограничивающие цитоплазму и большинство внутриклеточных структур, а также образующие единую внутриклеточную систему канальцев, складок и замкнутых полостей. Толщина биологической мембраны редко превышает -10нм и видима только посредством электронного микроскопа.
Функции биологических мембран (БМ)
- БМ образует регулируемый и избирательный барьер, который отделяет содержимое клетки от окружающей среды и регулирует транспорт веществ между содержимым клетки и окружающим клетку раствором. Клеточная мембрана избирательно снижает скорость продвижения молекул в клетку и из неё. Она определяет, каким молекулам можно проникнуть в клетку, а каким оставаться за её пределами. Матричная функция БМ обеспечивает взаимное расположение и ориентацию белков. Механическая функция биологических мембран обеспечивает механическую прочность, автономность по отношению к окружающей среде клеток и внутриклеточных структур.
Кроме этих основных функций биологические мембраны выполняют множество других важных функций в живом организме, к которым относятся рецепторная функция, энергетическая (синтез и гидролиз аденозинтрифосфорной кислоты - АТФ на внутренней мембране митохондрий), генерация и проведение биофизического потенциала.
Химический состав и структура биологических мембран
Биологические мембраны построены в основном из белков, липидов и углеводов.
Соотношение между липидами и белками может значительно варьировать в различных клетках. Липиды мембраны бывают трех видов: глицерофосфолипиды (фосфолипиды), сфингофосфолипиды и стероиды (холестерол).Молекула глицерофосфолипида состоит из остатка трёхатомного спирта глицерола, атомы водорода двух гидроксильных групп которого замещены на две длинные цепи жирных кислот. Третий атом водорода гидроксильной группы глицерина замещён остатком фосфорной кислоты, к которому, в свою очередь, присоединён остаток одного из азотистых оснований (холин, этаноламин, серин, инозитол). В молекуле фосфолипида можно выделить две части - полярную головку (остаток глицерина, остаток фосфорной кислоты и азотистое основание) и неполярные хвостики (остатки жирных кислот) (Рис. 1).
![]()

Рис.1. Структура молекулы фосфолипида
Головка и хвостики сильно отличаются по своим физическим свойствам. Головка молекулы фосфолипида гидрофильна (″любит воду″). Она хорошо растворима в воде. Хвостики - гидрофобны (″боятся воды″). Они легко растворяются в липидах и органических растворителях, но водой отталкиваются. Таким образом, в целом молекула фосфолипида имеет амфифильные свойства (Рис.2).

Рис.2. Амфифильные молекулы фосфолипидов
В воде, благодаря своей амфифильности, фосфолипиды мембран самоорганизуются в виде двойного слоя, являющегося структурной основой биомембран. (Рис. 3). Немецкие ученые Gorter и Grendel доказали, что такая бислойная фосфолипидная структура является основой мембраны клетки.

Рис.3. Бислойная фосфолипидная структура.
Физическое состояние фосфолипидного бислоя зависит от температуры. Если температура превышает критическую точку, бислой представляет собой жидкость. Если температура падает ниже критической точки, мембранные фосфолипиды становятся твердыми. Мембрана теряет текучесть, и движение молекул в ней ограничивается.
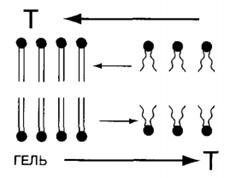 Рис.4. Схема фазовых переходов бислоя.
Рис.4. Схема фазовых переходов бислоя.
Существует несколько видов движения молекул липидов: колебание, вращение, латеральная диффузия (перемещение молекул в пределах своего слоя), флип-флоп (перемещение молекул из одного слоя липидов в другой, происходит редко).

Рис. 5. Формы подвижности липидов в БМ
Жидкостно-мозаичная модель БМ
Согласно современной жидкостно-мозаичной модели мембраны (модель Сингера и Николсона), липидный бислой является основой мембраны. Молекулы фосфолипидов расположены в нём так, что их длинные оси параллельны и ориентированы перпендикулярно к поверхности мембраны. Мембрана сохраняется в жидком состоянии благодаря температуре клетки и химическому составу жирных кислот.

Рис.6. Жидкостно-мозаичная модель мембраны (Сингер и Николсон, 1972г.): фосфолипидный бислой; периферические и интегральные белки
Белки мембраны подразделены на два вида. Молекулы первого типа являются гидрофильными. Эти белки, называемые периферическими, соединены с поверхностью мембраны сравнительно слабыми электростатическими силами. Белки второго вида имеют как гидрофильные, так и гидрофобные группы. Их молекулы более или менее погружены в мембрану, и удерживаются в ней более прочными гидрофобными силами. Некоторые белки пронизывают мембрану от ёё внутренней до внешней поверхностей - интегральные белки (Рис. 6). Многочисленные белки мембраны выполняют различные функции (метаболическую, транспортную, рецепторную и т. п.). Функции белков мембраны существенно зависят от строения их молекул.
БМ как электрический конденсатор
Биологическую мембрану можно рассматривать как электрический конденсатор (Рис.7).

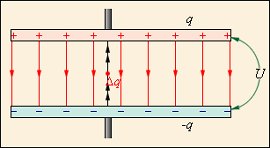
Рис. 7. Мембрана, как конденсатор
Проводниковые пластины конденсатора образуют электролиты наружного и внутреннего растворов (внеклеточного и цитоплазмы). Проводники разделены липидным бислоем. Липиды – диэлектрики с диэлектрической проницаемостью е = 2.
Емкость плоского конденсатора: ![]()
![]() (1),
(1),
где электрическая постоянная е0 = 8,85 10-12 Ф/м - электрическая постоянная, d - расстояние между пластинами конденсатора.
Удельная ёмкость на единицу площади поверхности мембраны составляет 0,5⋅10-2 Ф/м2:
Cуд![]()
![]() (2)
(2)
Отсюда можно найти расстояние между пластинами конденсатора, примерно соответствующее в нашем случае толщине липидной части мембраны:
ℓ = ![]()
![]() м ≈ 3 -4 нм (3)
м ≈ 3 -4 нм (3)
Результат соответствует по порядку величины толщине неполярной части бимолекулярного слоя липидов.
Методы исследования структуры БМ
Современная жидкостно-мозаичная модель БМ была сформирована на основе экспериментальных исследований. Важнейшая информация о структуре мембран, о взаимном расположении атомов мембранных молекул была получена с помощью рентгеноструктурного анализа и электронной микроскопии.
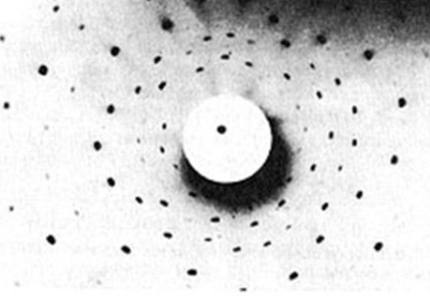
Рентгеноструктурный анализ основан на изучении дифракции коротковолновых рентгеновских лучей на атомах (Рис. 8). Рентгеноструктурный анализ позволяет обнаруживать упорядоченность в расположении атомов и определять параметры упорядоченных структур (например, расстояния между кристаллографическими плоскостями).
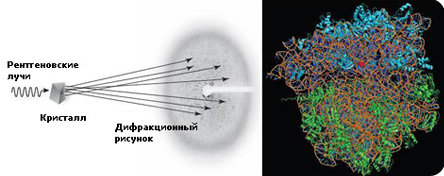
Рис.8. Схема рентгеноструктурного анализа рибосомы.
|
|
|
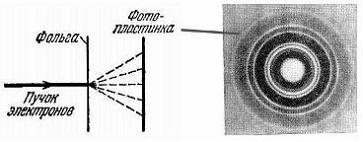
Рис.9.Особенности рентгенограмм кристалла (NaCl) и молекулы ДНК и поликристалла (золотая фольга.
Рентгеновское излучение, входя в кристалл на некоторую глубину, отражается от системы параллельных плоских сеток по законам геометрической оптики (Рис. 10). Отраженные лучи, идущие по одному направлению, интерферируют между собой. Вследствие интерференции отраженный пучок будет обладать заметной интенсивностью только в том случае, если разность хода лучей, рассеянных двумя соседними плоскостями семейства, будет равна целому числу длин волн. Обозначим расстояние между кристаллографическими плоскостями через d, а угол, составленный падающим лучом с плоской сеткой (угол скольжения), через и. Разность хода Д между лучами, рассеянными двумя ближайшими сетками, равна (см. Рис. 10) Д = ab + bc = 2dsinи. Дифракционный максимум будет наблюдаться тогда, когда Д равно целому числу длин волн, т. е. когда выполняется условие:
2dsinи = kл (4),
где k = 1, 2, 3... - порядок дифракционного максимума.
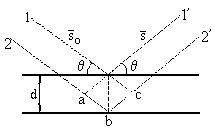 Рис. 10. Рассеяние рентгеновского излучения на атомах
Рис. 10. Рассеяние рентгеновского излучения на атомах
Формула (4) впервые была выведена крупнейшим русским кристаллографом и англичанами отцом и сыном Брэггами. Формула Вульфа - Брэггов (4) лежит в основе дифракционных методов определения и анализа структуры кристаллов. Зная длину рентгеновской волны л, можно по углу скольжения и (определяется экспериментально), соответствующему дифракционному максимуму k - го порядка, определять параметр кристаллической решетки d:
d=![]()
![]() (5)
(5)
Исследования дифракции рентгеновских лучей подтвердили относительно упорядоченное расположение липидных молекул в мембране – двойной слой с более или менее параллельно расположенными жирнокислотными хвостами; дали возможность точно определить расстояние между полярной головой липидной молекулы и метильной группой в конце углеводородной цепи.
Наибольшие успехи в раскрытии особенностей строения биологических мембран были достигнуты в электронно-микроскопических исследованиях.

Рис.11. Просвечивающий электронный микроскоп (ПЭМ) и растровый электронный микроскоп (РЭМ) (фото с еlementy. ru/lib/430816)
В просвечивающих электронных микроскопах (ПЭМ), в которых электроны с энергиями от 1 кэВ до 5 МэВ проходят сквозь объект, изучаются образцы в виде тонких пленок, фольги, срезов и т. д. толщиной от 1 нм до 10 мкм. Порошки, микрокристаллы, аэрозоли можно изучать, нанеся их предварительно на подложку − тонкую пленку для исследования в ПЭМ или массивную подложку в растровых электронных микроскопах (РЭМ). Поверхностную и приповерхностную структуру массивных тел толщиной существенно больше 1 мкм исследуют с помощью РЭМ, отражательных и зеркальных, а также ионных проекторов и электронных проекторов.
Как известно, световой микроскоп не позволяет рассмотреть детали объекта меньше примерно половины длины волны света (около 200 нм). В световом микроскопе можно разглядеть отдельные клетки, однако он совершенно непригоден для изучения биологических мембран, толщина которых в 20 раз меньше предела разрешения светового микроскопа.
Разрешающая способность микроскопа ограничена явлением дифракции. Поэтому, чем меньше длина волны по сравнению с деталями исследуемого объекта, тем меньше искажения. Предел разрешения z пропорционален половине длине волны л:
z~л/2
Согласно формуле де Бройля длина волны движущегося электрона:
![]() (6), где
(6), где
m – масса электрона, v – его скорость, р – импульс электрона.
Электронам, разогнанным до больших скоростей, тоже присущи волновые свойства, в том числе явление дифракции, однако при достаточно больших скоростях длина волны де Бройля достаточно мала и соответственно мал предел разрешения электронного микроскопа. У электронов, ускоренных в электрическом поле с напряжением U= 105 В, скорость
V= ![]()
![]() ≈108
≈108 ![]()
![]() , а длина волны де Бройля л≈0,005 нм.
, а длина волны де Бройля л≈0,005 нм.
Однако в силу некоторых конструктивных особенностей электронного микроскопа его предел разрешения z составляет не тысячные доли нанометров, а порядка z≈0,5 нм, что, однако, уже позволяет рассмотреть отдельные детали строения биологических мембран.
В электронном микроскопе достигается увеличение в сотни тысяч раз, что позволило исследовать строение клетки, клеточных органелл и биологических мембран.
Недостатком электронной микроскопии является деформация живого объекта в процессе исследования. В электронном микроскопе нельзя рассматривать живую клетку. Перед началом электронно-микроскопических исследований клетка проходит через многие стадии предварительной обработки: обезвоживание, закрепление, ультратонкий срез, обработка препаратов соединениями тяжелых металлов, плохо пропускающих электроны (например, осмия или марганца) с целью повышения контрастности изображения. При этом изучаемый объект значительно изменяется. Несмотря на это, успехи в изучении клетки при помощи электронного микроскопа несомненны.
При помощи электронной микроскопии удалось получить изображение биологических мембран, на снимках видно двухслойное строение мембраны. Новая информация о строении мембраны была получена с помощью метода «замораживание-скол-травление». По этому методу клетку охлаждают до очень низкой температуры в жидком азоте. Охлаждение проводится с очень большой скоростью (около 1000 градусов в секунду). Затем клетки раскалываются специальным ножом и помещаются в вакуум. Твёрдая стеклообразная вода быстро возгоняется, освобождая поверхность скола (этот процесс и называют травлением). После травления получают реплику (отпечаток со сколотой поверхности), наносят на нее смесь углерода и платины и фотографируют в электронном микроскопе. Мембраны при скалывании расщепляются вдоль границы двух липидных монослоёв, и поэтому можно видеть их внутреннее строение (Рис.12).

Рис. 12. Интегральные белки, обнаруженные методом «замораживание-скол-травление. biomembrane. jpg
Было обнаружено, что имеются белковые молекулы, погруженные в липидный бислой и даже прошивающие его насквозь, что привело к существенному изменению представлений о строении мембран.
К методам изучения динамики мембран, позволяющим исследовать их, не разрушая, относятся флуоресцентный метод и методы радиоспектроскопии – ЭПР и ЯМР. Эти методы дают сведения о движении и взаимодействии мембранных молекул и отдельных частей молекулы. Было выяснено, что при физиологических условиях липидные молекулы находятся в жидком агрегатном состоянии. Метод ЭПР показал, что не вся поверхность биологической мембраны покрыта белками. Так, например, большая половина поверхности мембраны кишечной палочки образована полярными головками липидов.
Список литературы
, , Физика и биофизика. – М.: «ГЭОТАР-Медиа», 2015. , Медицинская и биологическая физика. – М.: «ГЭОТАР-Медиа», 2009. Физика и биофизика. Stanuprofi. ru , Медицинская и биологическая физика. – М.: «ИНФРА-М», 2012. . Физик в гостях у биолога. М.: «Издательство МЦМО», 2015.