ҒЫЛЫМИ-ЗЕРТТЕУ ЖҰМЫСЫНЫҢ ТАҚЫРЫБЫ:
«Кристаллическое и аморфное состояние твердого вещества»
І ОРЫНҒА
ОРЫНДАҒАН: Алматы қаласы
КММ «№51 мектеп-гимназияның 9 сынып оқушысы Арарат Арина
Ғылыми жетекшісі: химия және биология пәнінің мұғалімі
Бектенова Балхаш Ташмахамбетовна
Твердые тела могут существовать в двух существенно различных состояниях, отличающихся своим внутренним строением и свойствами. Это кристаллическое и аморфное состояние твердых тел.
Кристаллы – твердые тела, атомы, ионы или молекулы которых образуют упорядоченную периодическую структуру (кристаллическую решетку). Причем этот пространственный порядок сохраняется на огромных «по атомным масштабам» расстояниях. Атомы,
находящиеся на противоположных гранях монокристалла, могут быть удалены на десятки
сантиметров, и в то же время они, будто чувствуя друг друга, располагаются параллельно.
При этом между ними находятся миллиарды других атомов, так же четко взаимно расположенных. [3]
Если весь кусок вещества представляет собой один кристалл, то такое тело называется монокристаллом или просто кристаллом. В других случаях тело представляет собой множество мелких кристалликов, причудливо сросшихся между собой, например, кусок рафинада. Такие тела называют поликристаллическими.
Кристаллическое состояние характеризуется наличием четко выделяемых естественных граней, образующих между собой определенные углы. Кристаллы могут иметь от четырех до нескольких сотен граней. Но при этом они обладают замечательным свойством –
какими бы ни были размеры, форма и число граней одного и того же кристалла, все плоские грани пересекаются друг с другом под определенными углами. Углы между соответственными гранями всегда одинаковыми.
Кристаллы каменной соли, например, могут иметь форму куба, параллелепипеда,
призмы или тела более сложной формы, но всегда их грани пересекаются под прямыми
углами. Грани кварца имеют форму неправильных шестиугольников, но углы между гранями всегда одни и те же – 120°.
Закон постоянства углов, открытый в 1669 г. датчанином Николаем Стено, является
важнейшим законом науки о кристаллах — кристаллографии [5].
Второй вид твердого состояния – аморфное состояние. Амморфные веществма не имеют упорядоченной структуры и в отличие от кристаллов не расщепляются с образованием кристаллических граней; как правило они изотропны, то есть не обнаруживают различных свойств в разных направлениях, не имеют определённой точки плавления.
Некоторые вещества могут находиться в любом из этих двух состояний. Например, если расплавить кристаллический кварц (температура плавления около 1700° С), то при охлаждении он образует плавленый кварц, с другими физическими свойствами, одинаковы
ми по всем направлениям. Аморфное состояние - неустойчивое состояние твердых тел, которые стремятся со временем перейти в кристаллическую форму, хотя этот процесс может протекать достаточно долго.
1.2. Форма кристаллов
Приглядевшись к кристаллам внимательнее, можно увидеть еще одну характерную для них особенность: кристаллы разных веществ отличаются друг от друга своими формами. Кубики кристаллов каменной соли не спутаешь с игольчатыми кристаллами азотнокислого калия. Однако формы кристаллов различных веществ могут быть очень похожими. А главное не в этом. Ведь не всегда кристалл вырастает многогранником - это удается ему лишь при благоприятных условиях, когда ничто не мешает ему при росте. Каков же самый характерный, самый основной признак кристалла? Ответ такой. Самой характерной особенностью кристалла – является его атомная структура, правильное симметричное, закономерное расположение атомов.
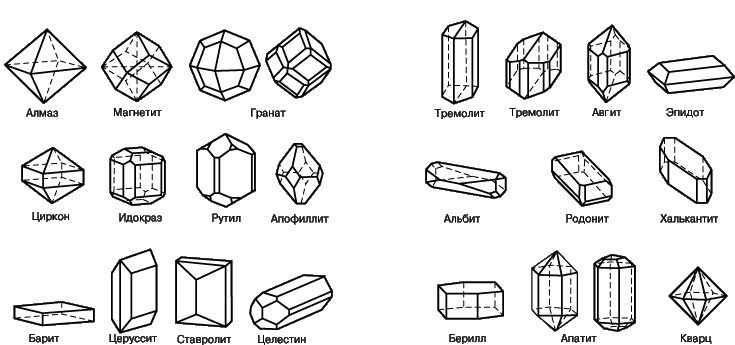
Некоторые кристаллы имеют довольно простую форму, но их комбинации могут создавать очень сложные многогранники. [4 ]Атомы могут выстраиваться в достаточно причудливые структуры, напоминающие тетраэдры, параллелепипеды, икосаэдры и прочие геометрические фигуры. В науке о кристаллах — кристаллографии — в зависимости от симметрии расположения атомов выделяют 6 кристаллических групп, которые распадаются на 32 класса.
В результате получается несколько сотен различных форм макроорганизации кристаллических тел. Причем на форму монокристалла влияет не только форма элементарной атомной ячейки, но и те условия, в которых происходит рост кристалла.
1.3. Природные кристаллы
Как же растут кристаллы в природе? Например, при застывании магмы. Это процесс роста кристаллов из расплавов. Магма представляет собой смесь многих веществ, у которых различны температуры кристаллизации. Чем медленнее застывает магма, тем больше успевают вырасти кристаллические зерна составляющих ее минералов. Впрочем, величина кристалликов зависит еще и от многих других причин.
Самый известный кристалл в природе – это кристалл поваренной соли. Свыше пятисот лет назад древнерусские солевары научились извлекать соль из соляных источников. Вода в соленых источниках горько-соленая, в ней растворено много различных солей. Летом, когда под лучами палящего солнца вода озер быстро испаряется, из нее начинают выпадать кристаллы солей. Эти кристаллы плавают на поверхности озера и оседают на дне, на прибрежных камнях, на досках, на любом твердом предмете, попавшем в озеро. Даже рука, опущенная на несколько минут в озеро, покрывается тонким слоем соли. Сила кристаллизации соляных пластов столь велика, что, расширяясь, они выдавливаются из земли, становясь на ребро.
Обыкновенная столовая соль, хлористый натрий, без которого человек не может обойтись, представляет собой очень мелкие кристаллики, в земле же соль встречается иногда в виде очень больших кристаллов - так называемой каменной соли.
Особенно интересна кристаллизация подземных вод в пещерах. Капля за каплей просачиваются воды и падают со сводов пещеры вниз. Каждая капля при этом частично испаряется и оставляет на потолке пещеры вещество, которое было в ней растворено. Так постепенно образуется на потолке пещеры маленький бугорок, вырастающий затем в сосульку. Эти сосульки сложены из кристалликов. Навстречу им начинают расти вверх такие же длинные столбы сосулек со дна пещеры. Иногда сосульки, растущие сверху (сталактиты) и снизу (сталагмиты), встречаются, срастаются вместе и образуют колонны. Так возникают в подземных пещерах узорчатые, витые гирлянды, причудливые колоннады.
Кроме того, камни образуются и в организме человека: желчные камни в печени, камни в почках и мочевом пузыре, мельчайшие отложения в сосудистой оболочке глаза.
Некоторые живые организмы представляют собой настоящие “фабрики” кристаллов. Кораллы, например, образуют целые острова, сложенные из микроскопических мелких кристалликов углекислой извести.
Драгоценный камень жемчуг тоже построен из мелких кристаллов, которые вырабатывает моллюск жемчужница. Если в раковину жемчужницы попадает песчинка или камешек, то моллюск начинает откладывать перламутр вокруг пришельца. Слой за слоем нарастает на песчинке перламутр, образующий шарики жемчуга.
1.4. Искусственные кристаллы
Для многих отраслей науки и техники требуются кристаллы очень высокой химической чистоты с совершенной кристаллической структурой. Кристаллы, встречающиеся в природе, этим требованиям не удовлетворяют, так как они растут в условиях, весьма далеких от идеальных. Кроме того, потребность во многих кристаллах превышает запасы в природных месторождениях. Из более чем 3000 минералов, существующих в природе, искусственно удалось получить уже больше половины.
Искусственные кристаллы пробовали выращивать еще в XVI веке, но научились этому
делу только в середине XX столетия. Кристаллы соли, сахара и квасцов в счет, конечно, не
идут, поскольку водорастворимые химические соединения умеют превращаться в причудливые горы и леса с незапамятных времен. Сегодня растят не только то, что необходимо
для промышленного применения, но и просто красивые камни для украшений, типа фианитов и изумрудов. Значение сверхчистых кристаллических материалов в нашей жизни
огромно. Электроника использует особо чистый кристаллический кремний, сапфир, рубин
и кварц, машиностроение — искусственные алмазы, корунд, рубин, нитевидный углерод. [3]
Особый класс материалов составляют так называемые жидкие кристаллы. Эти уникальные вещества, сочетающие в себе подвижность жидкости и анизотропию твердого
тела, по сути кристаллами не являются и выглядят, как обычная мутная жидкость, если их
налить в стакан. Но в виде тонкого слоя, заключенного между двумя стеклянными пластинами с токопроводящим покрытием, они превращаются в тот самый ЖК-дисплей, без
которого не обходятся сегодня ни сотовые телефоны, ни персональные компьютеры.
Глава 2. ОБРАЗОВАНИЕ КРИСТАЛЛОВ
2.1. Кристаллизация
КРИСТАЛЛИЗАмЦИЯ - процесс образования кристаллов из паров, растворов, расплавов, из вещества в другом кристаллическом или аморфном состоянии. Кристаллизация начинается при достижении некоторого предельного условия, например, переохлаждения жидкости или пересыщения пара, когда практически мгновенно возникает множество мелких кристалликов — центров кристаллизации. [6]Кристаллики растут, присоединяя атомы или молекулы из жидкости или пара. Рост граней кристалла происходит послойно, края незавершенных атомных слоев (ступени) при росте движутся вдоль грани. Зависимость скорости роста от условий кристаллизации приводит к разнообразию форм роста и структуры кристаллов (многогранные, пластинчатые, игольчатые, скелетные, дендритные и другие формы, карандашные структуры и т. д.). В процессе кристаллизации неизбежно возникают различные дефекты.
2.2. Методы выращивания кристаллов
Основными методами получения совершенных кристаллов большого диаметра являются методы выращивания из расплава, из растворов и из паровой (газовой) фазы.
Выращивание монокристаллов из расплава
Наиболее распространенные способы выращивания монокристаллов. В настоящее
время более половины технически важных кристаллов выращивают из расплава. Этими
методами выращивают элементарные полупроводники и металлы, оксиды, галогениды и другие вещества. В ряде случаев из расплава выращиваются монокристаллы, в состав которых входит пять и более компонентов. Веществами, наиболее подходящими для выращивания из расплава, являются те, которые плавятся без разложения, не имеют полиморфных переходов и характеризуются низкой химической активностью.
Кристаллизация из паровой (газовой) фазы
Широко используется для выращивания как массивных кристаллов, так и эпитакси-
альных пленок, тонких (поликристаллических или аморфных) покрытий, нитевидных и
пластинчатых кристаллов. В методах выращивания, основанных на физической конденса-
ции кристаллизуемого вещества, вещество поступает к растущему кристаллу в виде соб-
ственного пара, состоящего из молекул их ассоциаций — димеров, тримеров и т. д.
Кристаллизация из растворов
Под кристаллизацией из растворов подразумевается рост кристалла соединения, химический состав которого заметно отличается от химического состава исходной жидкой фазы.
Кристаллизацию из растворов применяют при выращивании веществ, разлагающихся
при температурах ниже температуры плавления или имеющих несколько полиморфных
модификаций. Рост кристаллов осуществляется при температурах ниже температуры
плавления, поэтому в выращенных такими методами кристаллах отсутствуют дефекты,
характерные для кристаллов, выращенных из расплава.
При выращивании кристаллов из низкотемпературных водных растворов проводят
кристаллизацию путем изменения температуры раствора, пересыщение создается за счет
снижения температуры в зоне растущего кристалла.
Кристаллизация при химической реакции основана на выделении твердых продуктов в
процессе взаимодействия растворенных компонентов. Такой способ кристаллизации воз-
можен лишь в том случае, если растворимость получаемого кристалла будет ниже раство-
римости исходных компонентов. Обычно химические реакции в растворе протекают с
достаточно большой скоростью, создаются высокие пересыщения и происходит массовое
выделение мелких кристаллов. Ограничение скорости достигается либо использованием
слабо растворенных исходных продуктов, либо регулированием скорости поступления
веществ в зону реакции.
2.3.Способы кристаллизации
Для осуществления процесса кристаллизации в растворе необходимо создать пересыщение. По способам его создания различают два основных метода кристаллизации: 1) охлаждение горячих насыщенных растворов и 2) удаление части растворителя путем выпаривания.
Растворимость большинства веществ уменьшается с понижением температуры. Поэтому при охлаждении горячих растворов возникает пересыщение, обусловливающее выделение кристаллов. Этот способ также получил название политермической или изогидрической кристаллизации, поскольку при его осуществлении количество растворителя (например, воды) остается постоянным.
Перевод исходного раствора, в пересыщенное состояние можно осуществить и за счет частичного удаления растворителя при выпаривании раствора. Такой способ получил название изотермической кристаллизации, так как выпаривание насыщенного раствора происходит при постоянной температуре его кипения.[7]
Выбор того или иного метода кристаллизации зависит, в первую очередь, от характера изменения растворимости вещества при различной температуре. Для солей, растворимость которых резко уменьшается с понижением температуры, целесообразной является изогидрическая кристаллизация. В этом случае даже при сравнительно небольшом охлаждении раствора из него будет выделяться значительное количество соли. Именно изогидрической кристаллизацией получают большинство солей с резко выраженной прямой растворимостью (NaNO3, К2Сr2О7, NH4C1, CuS04-5H20 и др.). В тех случаях, когда растворимость соли почти не меняется при изменении температуры, кристаллизация охлаждением становится неэффективной и применяется изотермическая кристаллизация. Кривая растворимости, например NaCl, показывает, что при охлаждении насыщенного раствора из него выпадает лишь очень небольшое количество соли, поэтому кристаллизация NaCI проводится всегда выпариванием. (Приложение )
Изотермическая кристаллизация применяется также для солей с обратной растворимостью, например для Na2S04, растворимость которого, начиная с 32,4° С, уменьшается с повышением температуры. Для кристаллизации солей с резко выраженной обратной растворимостью иногда используют просто нагревание раствора до высоких температур. Так, например, получают безводный кристаллический сульфит натрия Nа2S0з и сульфат марганца MnS04.
При добавлении к раствору вещества, понижающего растворимость выделяемой соли, можно вызвать пересыщение раствора и кристаллизацию. Подобный метод кристаллизации получил название высаливания.
Вещества, добавляемые в раствор, обычно имеют одинаковый ион с кристаллизуемой солью. Характерными примерами процессов высаливания являются: кристаллизация железного купороса из травильных растворов при добавлении в них концентрированной серной кислоты, высаливание NaCI из рассолов за счет введения в них хлористого магния или хлористого кальция; получение безводного сульфата натрия добавлением к его растворам NaCI; высаливание поваренной солью хлористого бария из гидросульфидных щелоков и др.
Высаливающее вещество лучше вводить в раствор в виде насыщенного раствора, так как при добавлении твердого высаливателя на нем может осаждаться кристаллизующаяся соль, что вызовет замедление или даже прекращение растворения осадителя. В некоторых случаях для выделения соли к раствору добавляют вещества, понижающие растворимость кристаллизуемой соли. Так, для высаливания сульфата натрия из водного раствора можно использовать аммиак, метиловый или этиловый спирты и др. Аналогично кристаллизуют железный купорос из травильных растворов при добавлении ацетона.
Кристаллизация в результате химической реакции, в том числе в результате химического осаждения. Пересыщение можно создать за счет проведения химических реакций. Образующееся в результате вещество выделяется в виде кристаллической фазы из раствора.



