Немецкий химик предложил в 1865 году изображать структурную формулу бензола в виде цикла из шести углеродных атомов с чередующимися простыми и двойными связями.
Строение молекулы бензола
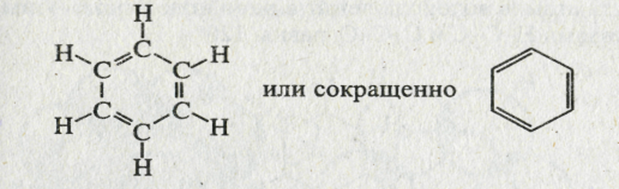
Это бесцветная, летучая, огнеопасная жидкость с характерным запахом. Бензол не растворяется в воде, но хорошо растворяется в органических растворителях, и сам является растворителем для многих веществ.
Бензол ядовит. Систематическое вдыхание его паров вызывает лейкемию и анемию. Другие ароматические углеводороды менее опасны.
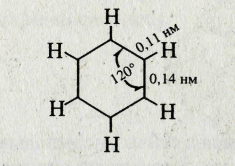
Согласно современным представлениям молекула бензола имеет строение плоского шестиугольника, стороны которого равны между собой и составляют 0,14 нм. Это расстояние является средним значением между величинами 0,154 нм (длина одинарной связи) и 0,134 нм (длина двойной связи). Не только углеродные атомы, но и связанные с ними шесть атомов водорода лежат в одной плоскости. Углы, образованные связями Н-С-С и С-С-С, равны 120°:
Все углеродные атомы в молекуле бензола находятся в состоянии sр2-гибридизации. Каждый из них связан тремя своими гибридными орбиталями с двумя такими же орбиталями двух соседних углеродных атомов и одной орбиталью атома Н, образуя три у-связи. Четвертая, негибридизованная 2р-орбиталь атома углерода, ось которой перпендикулярна плоскости бензольного кольца, перекрывается с подобными орбиталями двух соседних углеродных атомов, расположенных справа и слева.
Схема образования у-связей и р-связей в молекуле бензола
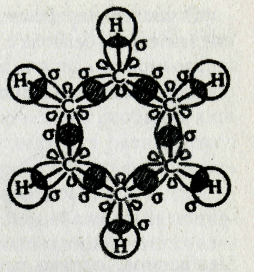
Такое перекрывание происходит над и под плоскостью бензольного кольца. В результате образуется единая замкнутая система р-электронов. В результате такого равномерного перекрывания 2р-орбиталей всех шести углеродных атомов происходит «выравнивание» простых и двойных связей, т. е. в бензольном кольце отсутствуют классические двойные и одинарные связи. Равномерное распределение р-электронной плотности между всеми углеродными атомами, обусловленное р-электронной делокализацией, и является причиной высокой устойчивости молекулы бензола.
В силу особенностей строения молекулы бензол занимает как бы промежуточное положение между предельными углеводородами и непредельными, т. е. может вступать как в реакции замещения, так и в реакции присоединения.
При реакциях замещения образуются вещества, которые используют для производства практически важных продуктов.
Реакция хлорирования бензола протекает в присутствии катализатора. Это так называемая реакция электрофильного замещения.
Реакции замещения:
1. Галогенирование в присутствии катализатора (FeCl3)
С6H6 + Cl2 → С6H5Cl + HCl хлорбензол (фенилхлорид ).
2. Нитрование в присутствии H₂SO₄(конц.)
С6H6 + HNO3 → С6H5NO2 + H2O нитробензол
3.Алкилирование бензола, реакция Фриделя-Крафтса)
в присутствии AlCl3 :
С6H6 + С2H5Cl → С6H5С2H5 + HCl этилбензол.
Реакции присоединения:
1. Гидрирование
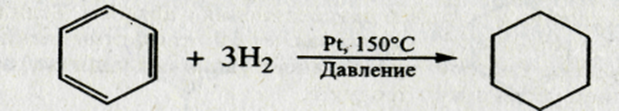
2. Галогенирование
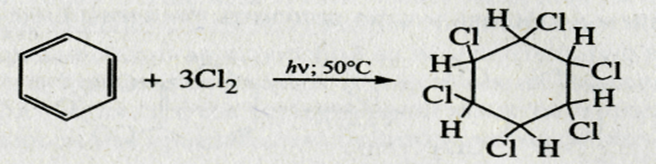
Реакция горения
Бензол горит сильно коптящим пламенем
2С6Н6 + 15О2 → 12 СО2 + 6 Н2О
Получение бензола
1. Тримеризация ацетилена (Реакция Зелинского)
При пропускании ацетилена при 400°C над активированным углем с хорошим выходом образуется бензол и другие ароматические углеводороды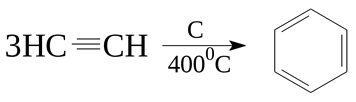
3. Из циклоалканов дегидрированием
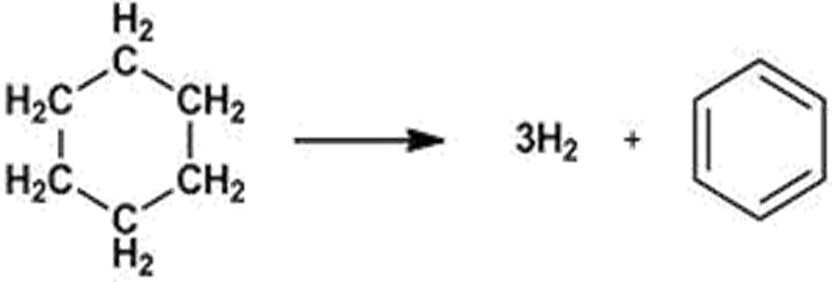
3. Из алканов дегидрированием
СН3 - СН2 - СН2 –CH2- СН2 – СН3 C6H6 + 4H2
Гомологи бензола
Номенклатура
Систематическое название всех ароматических углеводородов — арены, а бензола —бензен. Гомологи бензола рассматривают как замещенные бензола и цифрами указывают положение заместителей. Однако систематическая номенклатура допускает название «бензол», а для некоторых гомологов бензола — тривиальные названия: винилбензол (I) называютстиролом, метилбензол (II) —толуолом, диметилбензол (III) —ксилолом, изопропилбензол (IV) —кумолом, метоксибензол (V) —анизоломи т. д.:
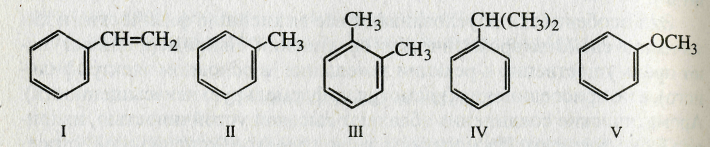
Ароматические радикалы имеют общее название — арилы (Аr). Радикал С6Н5- называютфенилом(от старого названия бензола — «фен»).
Изомерия.
Общая формула гомологов бензола СnН2n-6. Все шесть атомов водорода в молекуле бензола одинаковы и при замещении одного из них на один и тот же радикал образуется одно и то же соединение. Поэтому однозамещенный бензол изомеров не имеет. Например, существует только один метилбензол:

При замещении двух атомов водорода на метальные группы образуются три изомера — ксилолы, которые отличаются друг от друга расположением заместителей в кольце:



орто-диметилбензол, мета-диметилбензол, пара-диметилбензол,
или 1,2-диметилбензол или 1,3-диметилбензол или 1,4-диметилбензол
(о-ксилол) (м-ксилол) (п-ксилол)
Вместо буквенного обозначения (орто-, мета-, пара-, или сокращенно: о-,м-, п-) можно пользоваться цифровым: 1,2-, 1,3-, 1,4-. Изомеры могут отличаться характером заместителей:


пропилбензол изопропилбензол (кумол)
Физические свойства
Низшие члены гомологического ряда бензола — обычно жидкости с характерным запахом. С повышением молекулярной массы увеличивается температура кипения.
Углеводороды, в состав которых входит не более одного бензольного кольца, как правило, легче воды. Ароматические углеводороды нерастворимы в воде, но хорошо растворяются во многих органических растворителях.
Химические свойства
Основными химическими реакциями, в которых участвует бензольное кольцо, являются замещение, присоединение и окисление. Учитывая строение ароматических углеводородов, следует отметить, что для них наиболее характерными будут реакции электрофильного замещения.
I. Реакции электрофильного замещения. К ним относятся реакции галогенирования, нитрования, сульфирования, реакции алкилирования и ацилирования (реакции Фриделя-Крафтса) и др. Все они протекают практически по одному механизму.
1.Реакция галогенирования.
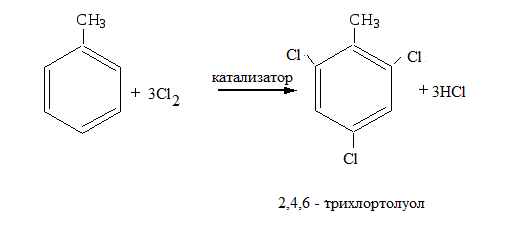
2, Реакция нитрования
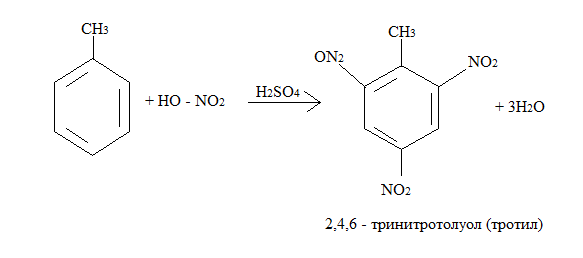
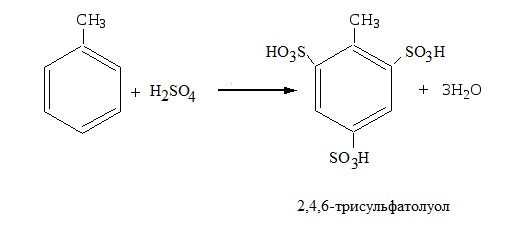
3.Реакция сульфирования
II. Реакции окисления Гомологи бензола окисляются легко.
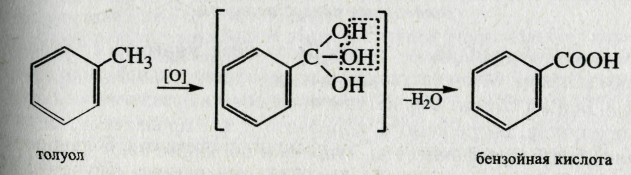
При этом окисляется связанная с бензольным ядром боковая цепь, которая превращается в карбоксильную группу
III. Реакции присоединения. Эти реакции протекают с большим трудом. Только в особых условиях (высокая температура, облучение УФ светом, катализатор) толуол может проявлять слабо выраженный непредельный характер и присоединять водород или галогены. Например, в присутствии катализатора (платина, никель или палладий) бензол вступает в реакцию гидрирования с образованием циклогексана
1. Реакция гидрирования
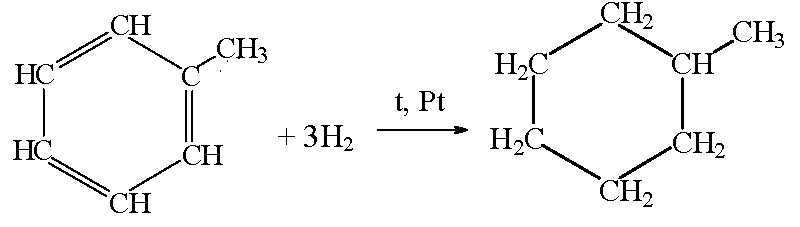
2. Реакция горения.
C7H8 + 9O2 7CO2 + 4H2O
Получение
Основными природными источниками ароматических углеводородов являются каменный уголь и нефть. Гомологи бензола можно получать также и синтетическим путем.
1. Ароматизация предельных углеводородов
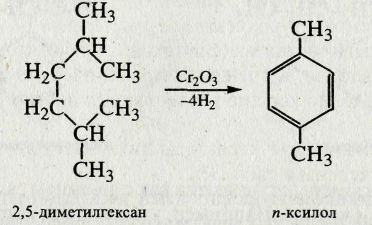
2. Реакция Вюрца—Фиттига. Эта реакция подобна синтезу Вюрца. Она также идет через стадию образования металлорганических соединений, но в данном случае продукты реакции можно сравнительно легко разделить
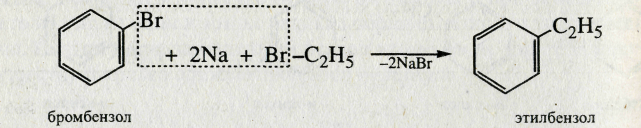
3. Дегидрирование циклоалканов
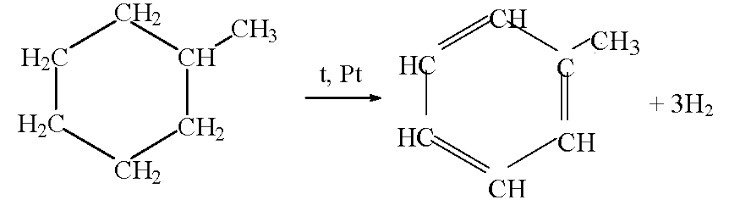
4. Реакции Фриделя—Крафтса
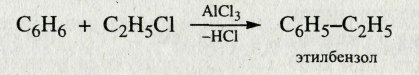
5. Восстановление по Клеменсену
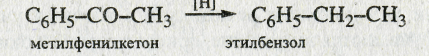
6. Синтез из солей ароматических кислот
![]()
Отдельные представители
Бензол (бензен) С6Н6 — легкая бесцветная жидкость со специфическим запахом. Мало растворим в воде. Бензол служит сырьем для производства различных химических продуктов: нитробензола, хлорбензола, стирола и др. Применяют для синтеза красителей, пестицидов, полимеров, ПАВ, взрывчатых веществ и фармацевтических препаратов. Служит добавкой к моторному топливу для повышения октанового числа.
Толуол (метилбензол) С6Н5-СН3— бесцветная жидкость, легче воды. Используют для производства красителей, взрывчатых веществ (тротил, тол) и лекарственных препаратов. Является хорошим растворителем для некоторых полимеров.
Ксилолы (диметилбензолы) С6Н4(СН3)2.Технический ксилол — смесь трех изомеров (орто-, мета - и пара-). Применяют в качестве растворителя лакокрасочных материалов, высокооктановой добавки к авиационным бензинам.
Винилбензол (стирол) С6Н5-СН=СН2— бесцветная жидкость с приятным запахом. Нерастворим в воде. Легко полимеризуется. Используют в основном для получения полимера — полистирола, бутадиенстирольного каучука и АБС-пластиков.
Приложение 1
Задания для предварительного контроля знаний студентов.
Тестовое задание по теме : «Алкины»
Выберите один или несколько правильных ответов:
Какое из данных веществ является алкином?
а) С7Н8 б) С7Н14 в) С7Н12 г) С7Н16
2. Какая из данных общих формул характерна алкинам?
а) СnH2n+1 б) СnH2n+2 в) СnH2n-2 г) СnH2n
3.Найдите из перечисленных формул 3,3- диметилпентин-1
CH₃ CH₃
а) CH≡C-C-CH₃ б) CH3-C-C≡CH в) CH3-CН-CН2-СН2-С≡CH
C2H5 CH₃ CH₃
CH₃
г) CH≡C-C-CH2- CH2- CH₃
CH₃
4. Какие из перечисленных реакций характерны для алкинов?
а) замещения
б) присоединения
в) разложения
г) обмена
5.Какой углеводород является гомологом ацетилена?
а) С3Н6 б) С3Н4 в) С3Н8 г) С4Н10
6.Какая реакция идет по типу реакции присоединения?
а) С3Н4+О2
б) С3Н6+Сl2
в) С3Н6+О2
г) С3Н4+Сl2
7.Укажите изомерные вещества из числа предложенных.
а) СН3-СН2-СН-С≡СН
С6Н13
б) СН3-СН-СН-С≡СН
С2Н5 СН3
в) СН3-СН2-СН2-СН2-С≡СН
СН3 СН3
г) СН3-С-СН2- СН2- СН-С≡СН
С2Н5
8.Какому названию соответствуют данная формула?
СН3-СН2-СН-С≡СН
С2Н5
а)3-метилбутин-1
б)3-метилбутин-1
в)3-этилпентин-1
г)3-этилгексин-1
9. Какой реакцией можно получить ацетилен?
а) СН4
б) С2Н6+Сl2
в) С2Н4+ Сl2
г) С2Н4+НСl
10. Реакции присоединения характерны для:
а) бутина
б) пропана
в) циклопропана
г) бутадиена-1,3
Ответы к тестовому заданию по теме: «Алкины»
в в а а, б б г а, г в а а, в, гЭталоны ответов
«0» - «1» ошибка - 5 баллов
«2» - «3» ошибки – 4 балла
«4» - «5» ошибок – 3 балла
Более «5» ошибок – 2 балла
Осуществить превращения:
1 вариант
Этин метан →бутан→бутен→ бутадиен 1,3 → 1,4-дибромбутен-2.
2 вариант
1.Пропен→пропин→хлор-пропен→дихлорпропан.
Приложение 2
Задания для заключительного контроля знаний по теме : «Ароматические углеводороды»
Вопросы для фронтального опроса:
1. Какая общая формула соответствует гомологическому ряду аренов?
2. Какие типы реакций характерны для бензола?
3. Какими растворами можно распознать гексен, бензол?
4. Какие из веществ способны присоединять (при соответствующих
условиях) водород: гексен, бензол, ацетилен, метан?
5. Почему пламя бензола сильно коптящее?
Задания высокого уровня
1. Этилбензол в больших количествах идет на получение ценного мономера – стирола C6H5 – CH = CH2. Составьте уравнение реакции. Укажите, является ли стирол гомологом бензола.
2. Стирол обесцвечивает бромную воду. За счет чего это происходит: двойной связи (винила) или бензольного ядра? Ответ подтвердите уравнением реакции.
3. Стирол вступает в реакцию полимеризации. Получающийся полимер – полистирол – широко используют для получения различных пластмассовых изделий. Составьте уравнение реакции полимеризации.
Задания среднего уровня
Осуществите превращение: CH4 → X → Y → C6H12
Задания низкого уровня
1. Составьте все изомеры состава C4H10 и назовите их по систематической номенклатуре.
ПРЕЗЕНТАЦИЯ
Зажать кнопку «ctrl» и кликнуть левой кнопкой мыши по слову «презентация».

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 |




