в) бензойная (рКа= 4,17), г) изоникотиновая (рКа= 1,80).
Из β-николина получите никотинамил (Витамин РР). Из β-николина получите Ν,Ν-диэтиламид никотиновой кислоты (кордиамин). Приведите схему получения изониазида (гидрозид изоникотиновой кислоты) Приведите схему получения фтивозида. Напишите схемы реакций никотиновой кислоты со следующими реагентами: 1) НСl, 2) СН3I, 3) СН3СOСl, 4) NаОН (Н2О), 5) С2Н5ОН (Н+), 6) SОСl2, 7) NН3, 8) t0 , ОН-. Назовите продукты. Напишите уравнения реакций, позволяющие осуществить следующие схемы химических превращений: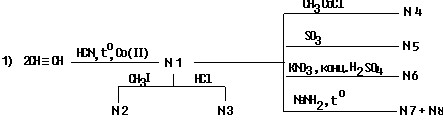
Назовите продукты.
Шестичленные ГЦС с двумя гетероатомами.
Напишите структурные формулы следующих соединений:а) 1,2-диазин, б) 2,4,6-тригидроксипиримидин, в) Ν-оксидпиразина,
г) пиперазин, д) урацил, е) цистозин
2. Напишите схемы получения
а) пиримидина из малонового эфира и мочевины
б) пиразина из этилендиамина и глиоксаля
Назовите приведенные соединения: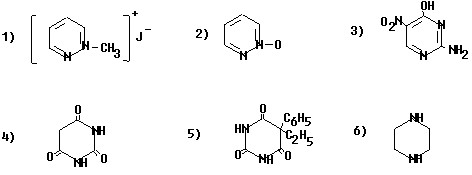
Напишите уравнения реакций следующих превращений:
С2Н5ОNa C2H5I C2H5ONa C2H5I
Малоновый эфир ----→ А --→ Б ----→ В ---→ Г- С2Н5ОН - С2Н5ОН
мочевина NaOH
Г ----→ Д ↔ Е ---→ К
- С2Н5ОNa
Br2 4NH3 CHO-CHO [O]
СН2 = СН2 -→ N 1 ---→ N 2 -----→ N 3 ---→ N 4-2H2O - H2O
NaNH2, NH3
------→ N 5
| CH3COOH
N 4 --------→ N 6
| [H
-------→ N 7
Охарактеризуйте электронное строение пиридазина, пиримидина и пиразина. Объясните почему эти соединения, несмотря на наличие двух основных центров, образуют соли только с одним эквивалентом кислоты. Расположите в ряд по убыванию основности, если рКа пиридазина - 2,33, пиримидина - 1,3 и пиразина - 0,6. Ответ поясните. Сравните реакционную способность пиримидина и пиридина в реакциях SE и SN. Напишите реакции. Наличие каких электродонорных заместителей в молекуле пиримидина способствует протеканию реакции SE. Напишите схему нитрования 2-амино-гидроксипиримидина и бромирование 2-аминопиримидина. Напишите схемы таутомерных преврощений урацила, тимина и цитозина. Назовите вид таутомерии.
Kонденсированные ГЦС.
Напишите структурные формулы следующих соединений: гипоксонтин, ксонтин, мочевая кислота, аденин, гуанин, теофиллин, теобронин, кофеин. Назовите следующие соединения:
В
POCl [Н] ↓↑ Nа
мочевая кислота --→ А -→ Б -→ Г| НСl
--→ Д
КОН NН3 [Н] NаNО2, НСl НСl
2,6,8-трихлорпурин --→ А -→ Б -→ В -----→ Г --→ ДАлколоиды
Напишите структурные формулы: а) 3,7-диметилксонтин, б)2,6-диокси-1,5,7-триметилпурин, в) 3-(α-пиперидил)-пиридин. Напишите структурные формулы: а)пиперидина, б) хинолина, в) изохинолина, г) пурина, д) тропана, е) индола. Какие соединения называется алкалоидами. Методы выделения из растительного сырья. Объясните почему алколоиды проявляют основные свойства. Как можно выделить свободное основание алколоида? Напишите схему взаимодействия никотина с соляной кислотой. Напишите структурную формулу морфина. Укажите какие гетероциклы составляют основу мезина. Получите из морфина кодеин, как можно отличить эти вещества? Напишите схемы реакции хинина с 1) КСl, 2) изб. НСl, 3) Br2 (ССl4). Напишите схему взаимодействия атропина с НСl. Напишите схему кислотного гидролиза кокаина. Назовите продукты. Самостоятельная работа: Студент самостоятельно отвечает на вопросы индивидуальных билетов по заданной теме. Задание на следующее занятие:Углеводы. Моносахариды.
Опыты 146-156 на стр. 380.Упр. 1, 2, 20 на стр. 377.
9. Литература: I. т. 3, стр. 126-150.
IV. стр. 351-378.
VII. стр. 236-247.
ЗАНЯТИЕ 13
1. Тема: Углеводы. Моносахариды.
Продолжительность: 4 часа. Цель занятия: Сформировать знания стереохимического строения, таутомерных форм и закономерностей реакционной способности моносахаридов. Целевые задачи: к концу занятия студент должен: Знать классификацию моносахаридов. Объяснять понятия эпимер, аномер. Писать таутомерные превращения и объяснять явление мутаротации. Объяснять правила перехода от проекционных формул Колли-Толленса к формулам Хеуорса. Демонстрировать знания реакционной способности моносахаридов. Уметь проводить качественные реакции.5. Исходный уровень знаний.
7. Самостоятельная работа.
Значение углеводов. Распространение в природе. Способы получения моносахаридов. Физические свойства. Аскорбиновая кислота - лактон-2-кето-L-гулоновой кислоты. Кислотные свойства. Конформации моносахаридов. Брожение сахаров. Отдельные представители: глюкоза, манноза, галактоза, ксилоза, арабиноза, 2-дезокси-D-рибоза, рибоза, фруктоза, сорбоза, ксилит, дульцит, маннит, сорбит, 2-амино-2-дезокси-D-глюкоза, нейраминовая кислота. Биологическая роль D-глюкуроновой кислоты. Аскорбиновая кислота, глюконат кальция, ксилит, сорбит, использование в медицине. Экспериментальная часть:II. Опыты 146-156 на стр. 380.
Упр. 1, 2, 20 на стр. 377.
Kонтроль и оценка преподавателем результатов усвоения темы. Задание на следующее занятие:Полисахариды.
II. Опыты 157-161 на стр. 389.
Упр. 1, 2, 16 на стр. 387.
11. Демонстрация: таблицы, модели, слайды, мультимедиа.
Литература: I. т. 3, стр. 151-164.IV. стр. 378-400.
VII. стр.247-258.
ЗАНЯТИЕ 14
Тема: Полисахариды. Продолжительность: 4 часа. Цель занятия: Сформировать знания принципов строения, таутомерных форм дисахаридов и закономерностей реакционной способности ди - и полисахаридов. Целевые задачи: к концу занятия студент должен: Знать классификацию дисахаридов. Называть дисахариды по систематической номенклатуре. Писать таутомерные превращения восстанавливающих дисахаридов. Демонстрировать знание реакционной способности ди - и полисахаридов. Уметь проводить качественные реакции.
5. Исходный уровень знаний.
Таутомерия моносахаридов. Химические свойства моносахаридов и их производных. Основные учебные вопросы. Проверка домашнего задания. Классификация, номенклатура олиго - и полисахаридов. Общие химические свойства восстанавливающих и невосста-навливающих дисахаридов. Гидролиз лактозы, целлобиозы, мальтозы, сахарозы. Инверсия, инвертный сахар. Применение исчерпывающего алкилирования метилйодидом или диметилсульфатом с последующим гидролизом перметилата в анализе структуры олигосахаридов. Ацилирование. Взаимодействие с гидроксидом меди (11) на холоду.6.4. Химические свойства восстанавливающих дисахаридов.
Цикло-оксотаутомерия лактозы, целлобиозы, мальтозы. Явление мутаротации. Реакции окисления бромной водой, раствором Фелинга, реактивом Толленса, гидроксидом меди (11) при нагревании. Реакции присоединения (с водородом, циановодородом и др.). Реакции присоединения-отщепления с гидроксиламином, фенил-гидразином. Образование озазонов. Полисахариды. Крахмал, составные части крахмала (амилоза, амилопектин). Гликоген. Химические свойства крахмала (реакции исчерпываю-щего метилирования, ацетилирования). Ступенчатый гидролиз крахмала. Клетчатка (целлюлоза). Действие щелочи на целлюлозу. Получение сложных эфиров с азотной кислотой, уксусным ангидридом. Получение ксантогената целлюлозы. Получение карбоксиметилцеллюлозы, диэтиламиноэтил-целлюлозы. Самостоятельная работа. Физические свойства ди - и полисахаридов. Гомополисахариды: декстраны, пектиновые вещества. Гетерополисахариды: гиалуроновая кислота, хондроитинсульфа-ты, мукополисахариды. Гепарин. Применение простых и сложных эфиров целлюлозы. Экспериментальная часть:II. Опыты 157-161 на стр. 389.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 |




