Оборудование и реактивы: пробирки, штатив, мензурка, наждачная бумага, Растворы дихромата калия, серной кислоты, иодида калия, перманганата калия, сульфата железа (II), сульфата меди, сернистокислого натрия, железный гвоздь.
Выполнение работы:
Опыт № 1. Окислительные свойства бихромата калия.
Налить в пробирку 1-2 мл бихромата калия (К2Сr2O7). Добавить к нему около 2 мл разбавленной серной кислоты (H2SO4) и прилить равный объем раствора KI. Наблюдайте пожелтение раствора вследствие выделение йода. Напишите уравнение ОВР. Составьте электронные схемы, обозначив окислитель и восстановитель.
Опыт №2. Восстановительные свойства сульфата железа.
Налить в пробирку 1-2 мл перманганатата калия (КМnO4). Добавить к нему около 2-х мл разбавленной серной кислоты (H2SO4) и прилить равный объем раствора FeSО4. Наблюдайте обесцвечивание раствора. Напишите уравнение ОВР. Составьте электронные схемы, обозначив окислитель и восстановитель.
Опыт №3.
Налить в пробирку 3-4 мл сульфата меди (CuSO4). Зачистить наждачной бумагой железный гвоздь и опустить его в раствор CuSO4. Наблюдайте появление выделяемого медно-красного осадка на железном гвозде. Напишите уравнение ОВР. Составьте электронные схемы, обозначив окислитель и восстановитель.
Опыт №4. Окислительные свойства марганцевогокислого калия в зависимости от реакции среды.
A) реакция в кислой среде. Налейте в пробирку 1-2 мл раствора КМnO4 и около 2 –х мл разбавленной серной кислоты. Прилейте раствор сернисто-кислого калия Na2SO3 и наблюдайте полное обесцвечивание окраски вследствие образования MnSO4. Составьте уравнение реакции, пользуясь таблицей окислителей - восстановителей и принимая во внимание, что Na2SO3 окисляется в Na2SO4.
Б) реакция в щелочной среде. Налейте в пробирку 1-2 мл раствора КМnO4 и около 2-х мл КОН. Прилейте раствор сернисто-кислого калия Na2SO3 и наблюдайте появление зеленой окраски вследствие образования марганцовистого калия К2МnO4. Составьте уравнение реакции.
B) реакция в нейтральной среде. Налейте в пробирку 1-2 мл раствора КMnО4 и прибавьте около 2-х мл Н2O. Прилейте раствор сернисто-кислого калия Na2SO3. Наблюдайте выделение бурого осадка двуокиси марганца - Мn02. Составьте уравнение реакции, учитывая, что в число исходных веществ входит вода а в число продуктов реакции-гидроксид калия, почему? До каких продуктов восстанавливается КМn04 в зависимости от реакции среды?
Контрольные вопросы:
1.Что называется степенью окисления? Какую роль играет данное понятие при рассмотрении окислительно – восстановительных процессов?
2.Дайте определение окислительно – восстановительным реакциям. Чем они отличаются от обменных реакций?
3.Какие типы окислительно – восстановительных процессов вы знаете?
4.В чём сущность процессов окисления и восстановления?
5.Какие вещества могут проявлять окислительно – восстановительную двойственность? Приведите примеры.
6.Как изменяются в процессе реакции степени окисления окислителя и восстановителя?
7. Какие применяют методы для составления уравнений ОВР?
8. Какое правило лежит в основе метода ионно – электронного баланса?
9. Объясните влияние среды на протекание окислительно – восстановительных реакций?
10.Можно ли предсказать направление окислительно – восстановительных реакций?
11.Какие простые вещества элементов периодической системы обладают наиболее сильными окислительными и восстановительными свойствами?
12. Назовите часто применяемые окислители и восстановители.
Контрольные задания:
1. Составьте схемы электронного баланса, расставьте коэффициенты в уравнениях реакций:
а) HNO3 + С → СО2 + NO + H2O;
б) HNO3 + AsH3 → H3AsO4 + NO2 + H2O;
2.Написать уравнения реакций :
а) КI + КNO2 + Н2SO4 =
б) КNO2 + КМnО4 + Н2SO4 =
3.Пользуясь ионно – электронным методом, составить ионные и молекулярные уравнения реакций, протекающих по схемам:
а) СlO3Ї + NO2Ї → ClЇ + NO3Ї
б) МnO42 + Н2О → МnO4Ї + МnO2 + OHЇ
4. Определить эквиваленты КСlO4, если это вещество в процессе реакции восстанавливается:
а) до КСl б) до Сl2.
5. Какой объем раствора дихромата калия, содержащего 14,7 г К2Сr2O7 в 1 л, необходим для окисления 2 л децимолярного раствора сероводорода в присутствии разбавленной серной кислоты? Ответ : 1,33 л.
6. Сколько литров углекислого газа при 27 0С и 100 кПа получится при взаимодействии в сернокислом растворе 79 г КМnO4 с оксалатом натрия Nа2С2О4? Ответ: 62,4 л.
7.В какой среде меньше расходуется окислителя КМnO4: в кислой, нейтральной или щелочной? Почему?
8 Закончить составление уравнений внутримолекулярных окислительно –
восстановительных реакций и указать, какой атом или ион выполняет функцию восстановителя, а какой окислителя:
а) KNO3 → KNO2 + ……
б) AgNO3 → AgNO2 + NO2 + ……
в) NH4NO3 → N2O + ……
9. Сколько литров 30 % - ной соляной кислоты и пиролюзита, содержащего 90% двуокиси марганца прореагировали между собой, если выделившийся хлор при температуре 17 ◦ С и давлении 100 кПа занимал объем 8 л? Ответ : 161,4 г кислоты и 32,5 г МnO2
10. Как теоретически предсказать возможность самопроизвольного протекания окислительно – восстановительных реакций?
Лабораторное занятие 12
Тема: «Работа гальванического элемента. Расчет ЭДС гальванического элемента. Формула Нернста» (1 час)
Цель занятия: формирование понятий о электродном потенциале, гальваническом элементе.
Обрудование и реактивы: химические стаканы 50 мл, стеклянная изогнутая трубка, милливольтметр, рН-метр. IM и 0,1М растворы сульфата цинка, IM раствор сульфата меди, раствор хлорида калия.
Выполнение работы:
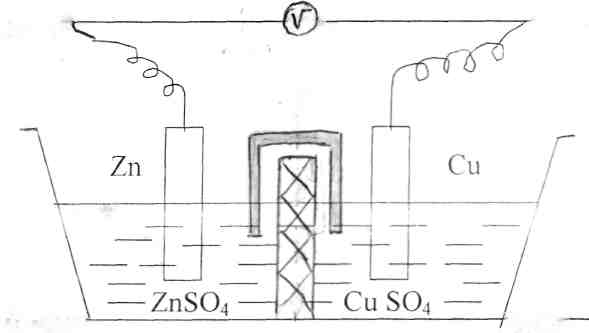
Устройство для непосредственного преобразования энергии химической реакции в электрическую энергию называется гальваническим элементом. Рассмотрим работу медно-цинкового гальванического элемента.
Рис. I Схема медно-цинкового гальванического элемента
Элемент составлен из цинковой пластины, погруженной в раствор сульфата цинка и медной пластины; погруженной в раствор сульфата меди. Оба раствора соприкасаются друг с другом. Они разделены перегородкой из пористого материала, пропускающего сульфат-ионы. При работе гальванического элемента протекает суммарная реакция:
Zn + CuSO4 = ZnS04 + Сu
Здесь процессы окисления и восстановления разделены в пространстве, и чтобы осуществить процесс восстановления ионов меди, электроны от окислителя переходят по проводнику, т. е. создают ток по внешней цепи. Цинковый электрод источник электронов, поступающих во внешнюю цепь, принято называть отрицательным (анод), а медный электрод - положительным (катод). Уравнения электродных процессов, протекающих при работе гальванического элемента:
анодный процесс, окисление: Zn - 2ё = Zn
катодный процесс, восстановление: Сu+2 + 2ё = Сu°
Гальванический элемент можно записать в виде краткой электрохимической схемы:
А(-) Zn/ ZnS04// CuSO4, /Cu (+) К
А (-) Zn / Zn+2 // Сu+2 / Сu ° (+) К
где одна черта означает границу между электродами и раствором, две черты - границу между растворами, в скобках знаки электродов, причем анод записывается слева, катод - справа. Необходимое условие работы гальванического элемента - разность потенциалов его электродов. Электрод с меньшим потенциалом является анодом. Электродвижущая сила гальванического элемента (Э. Д.С.) - величина положительная и определяется как разность потенциалов катода и анода.
Э. Д.С = ЕК-Еа
1. ЗНАЧЕНИЕ ТЕМЫ. Действие гальванического элемента основано на протекании в нем окислительно - восстановительной реакции, в которой пространственно разделены процессы окисления и восстановления, а электроны от окислителя к восстановителю направлены по металлическому проводнику. Осуществление этого процессаnна практике позволяет промышленности получить самые различные виды электрических батареек, аккумуляторов и других источников постоянного электрического тока.
2. ЦЕЛЬ РАБОТЫ: Научиться работать с гальваническим элементом, писать уравнения электродных процессов, иметь понятие об ЭДС элемента.
ХОД РАБОТЫ:
Опыт 1. Составление гальванических элементов.
Один из микростаканчиков заполнить IM раствором сульфата цинка, другой - IM раствором сульфата меди. Соединить стаканчики электролитным мостиком, заполненным насыщенным раствором хлорида калия в смеси с агар-агаром. Опустить в раствор сульфата цинка узкую цинковую пластинку, а в раствор сульфата меди - медную. Соединить электрическим проводом опущенные пластинки с гальванометром или другим регистрирующим прибором. Наблюдать отклонение стрелки гальванометра, указывающее на возникновение электрического тока.
Опыт 2. Составление концентрационного гальванического элемента. Наполнить микростаканчики раствором сульфата цинка разной концентрации: первый стаканчик - 1 M ZnS04, второй - 0,01 M ZnS04. Соединить стаканчики электролитным мостиком. Опустить в каждый стаканчик цинковые полоски и соединить их проводом с гальванометром. Отклоняется ли стрелка гальванометра? Написать уравнения химических реакций, протекающих на электродах гальванических элементов, и суммарное уравнение химической реакции в результате которой возникает электрический ток в данном элементе. В каком направлении перемещаются электроны во внешней цепи? Выписать из приложения к лабораторному практикуму числовые значения стандартных электродных потенциалов меди и цинка и вычислить ЭДС медно-цинкового элемента. Какие ионы и в каком направлении перемещаются в растворе? Вычислить стат. ЭДС серебр. концентрационного гальванического элемента. Представить преподавателю отчет письменный на утверждение о проделанной работе.
Контрольные вопросы:
1. Напишите молекулярные и ионные уравнения возможных реакций вытеснения металлов из их солей другими металлами и укажите стрелками переход электронов:

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 |



