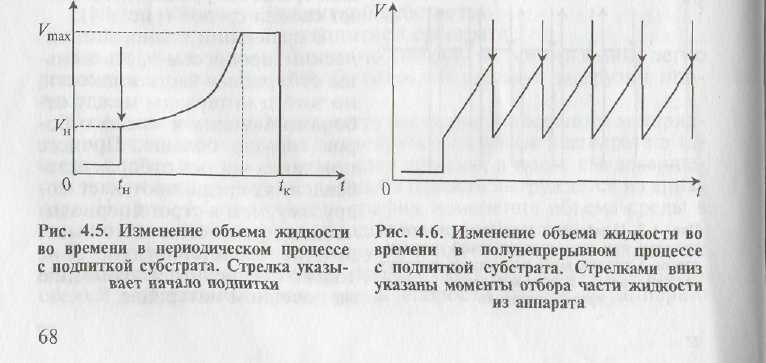
Следует отметить, что во всех случаях здесь имеется в виду основной материальный поток жидкости. Воздух, например, для аэробной ферментации добавляется непрерывно даже и в периодических процессах; то же часто бывает при добавлении щелочи для регулирования величины рН или жидкого пеногасителя.
2. ОСНОВНЫЕ ПАРАМЕТРЫ ПЕРИОДИЧЕСКОЙ ФЕРМЕНТАЦИИ
Рассмотрим теперь более подробно периодическую ферментацию.
Основные параметры процесса. После того как в аппарат загрузили среду, создали необходимую температуру, добавили посевной материал и стали подавать воздух для аэрации, собственно говоря, и начался процесс ферментации. Как следить за протеканием этого процесса? Для этого необходимо время от времени или непрерывно определять, какие изменения происходят в ферментационной среде.
Обычно состояние процесса характеризуется следующими основными параметрами:
концентрация биомассы микроорганизмов X;
концентрация питательной среды — субстрата (или его основного компонента) S;
концентрация продукта Р.
Все эти концентрации приведены к единице объема среды.
Фазы периодической ферментации. Рассмотрим, как изменяется концентрация биомассы в процессе периодической ферментации (фазы ферментации) (рис. 4.7).
В начале ферментации некоторое время микроорганизмы как бы приспосабливаются к новой среде, их концентрация не меняется. Этот период называется лаг-фаза. Далее начинается рост — это фаза ускорения роста. Третья фаза — фаза наиболее интенсивного роста, происходит наибольший относительный прирост биомассы. Это фаза экспоненциального роста. Затем скорость роста (относительная) начинает уменьшаться — это фаза замедления роста. Достигнув некоторой максимальной величины, концентрация
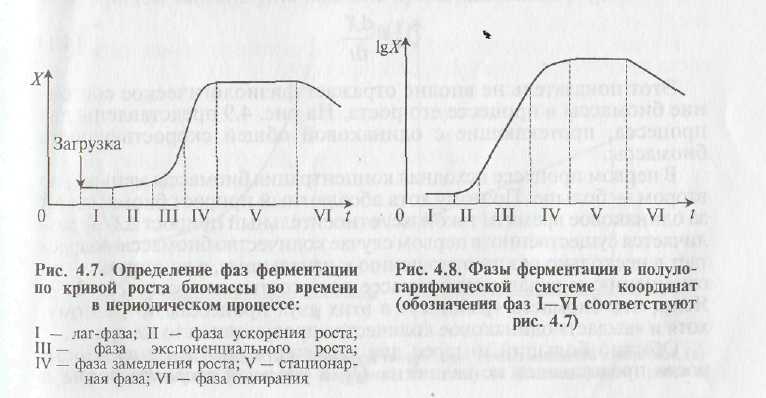
биомассы лалее перестает возрастать. В этой фазе — стационарной — в среде истощаются питательные вещества и накапливаются продукты обмена, тормозящие рост. Биомасса растет и одновременно происходит гибель части клеток (автолиз), так что общая концентрация сохраняется постоянной. И наконец, в фазе отмирания автолиз начинает преобладать над ростом, и концентрация биомассы микроорганизмов снижается.}
Эту кривую лучше изображать в полулогарифмических координатах \gX~ t (рис. 4.8).
Здесь участок роста, имеющий постоянный наклон, сразу выделяет фазу экспоненциального роста. Остальные фазы также легко определяются.
НЕПРЕРЫВНОЕ КУЛЬТИВИРОВАНИЕ МИКРООРГАНИЗМОВ
Есть две разновидности непрерывных процессов: процессы полного вытеснения, или тубулярные, и процессы полного перемешивания, или хемостатные.
9.1. ТУБУЛЯРНЫЙ ПРОЦЕСС
Питательная среда и посевной материал непрерывно поступают в аппарат, в котором нет обратного смешения. Аппарат выполнен в виде длинной трубы большого диаметра (рис. 9.1).
Жидкость на входе в аппарат смешивается с посевным материалом. По мере их продвижения в аппарате одновременно осуществляются рост биомассы и процесс ферментации. Движение не обязательно должно быть горизонтальным. В аппарате башенного типа жидкость движется снизу вверх. Такой способ часто выбирают для анаэробных процессов. Например, есть башенный способ производства пива.
Время движения жидкости t1 от входа в аппарат до любого сечения по длине потока l можно рассчитать как
![]()
(9.1)
где А — площадь сечения потока; F— объемный расход жидкости.
На выходе из аппарата (при l = L) время пребывания жидкости составляет:
![]()
(9.2)
Кривая изменения концентрации субстрата S, биомассы X и продукта Р по длине аппарата аналогична кривой изменения во времени в периодическом процессе — с учетом связи t и l.
Таким образом, тубулярный процесс с учетом закономерностей протекания процесса ферментации полностью подобен периодическому.
Некоторую сложность вызывает необходимость непрерывной подачи посевного материала. Ее можно избежать путем организации рециркуляции части потока с выхода аппарата на вход (рис. 9.2).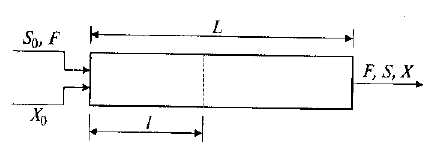
Рис.9.1. Схема тубулярного непрерывного процесса ферментации

Рис. 9.2. Схема тубулярного непрерывного процесса с рециркуляцией посевного материала
Преимуществом тубулярного процесса является возможность более полного исчерпания субстрата (как и в периодическом процессе), недостатком — невозможность организовать аэрацию во всех зонах по длине аппарата, большая склонность к инфицированию.9.11. ПРЕИМУЩЕСТВА И НЕДОСТАТКИ НЕПРЕРЫВНОГО СПОСОБА КУЛЬТИВИРОВАНИЯ МИКРООРГАНИЗМОВ
Ниже указаны преимущества и недостатки непрерывного способа культивирования микроорганизмов по сравнению с периодическим способом.
ПРЕИМУЩЕСТВА
1. Рост биомассы можно поддерживать неопределенно долго.
2. Можно исключить влияние физических или химических факторов на рост и на образование продукта при постоянной скорости роста.
3. Можно за счет разбавления поддерживать постоянную концентрацию биомассы.
4. Можно длительно поддерживать рост, лимитированный одним заданным субстратом, и изучать влияние лимитирования на состав клеток и их активность.
5. Состав среды можно оптимизировать методом импульсных добавок.
6. При непрерывном культивировании удобно определять кинетические константы, выход биомассы.
7. Результаты, полученные при непрерывном культивировании, часто более надежны и воспроизводимы, чем в периодическом процессе.
8. Процесс имеет большую производительность и относительно малое непродуктивное время (лишь в период запуска).
9. Облегчены механизация и автоматизация.
10. При постоянстве технологических режимов постоянно и качество продукта.
11. Невысокий износ измерительных приборов в связи со стерилизацией.
12. Снижается опасность контакта обслуживающего персонала гс микроорганизмами.
13. Непрерывные процессы можно использовать для автоселекции микроорганизмов.
НЕДОСТАТКИ
1. Меньшая гибкость, регулировать можно лишь некоторые параметры (скорость разбавления, среду, концентрацию кислорода, температуру).
2. Более высокие требования к постоянству качества сырья.
3. Большие капитальные вложения (непрерывная стерилизация среды, автоматизация и т. д.).
4. Трудно обеспечить непрерывное дозирование нерастворимых твердых субстратов.
5. Больше опасность инфицирования из-за большей длительности культивирования.
6. Возможность «вырождения» культуры (за счет автоселекции) из-за большого времени культивирования.
7. Не всегда можно достичь оптимального выхода продуктов метаболизма, не связанных с ростом.
8. Пристеночный рост и агрегатирование клеток могут вызвать вымывание культуры из аппарата.
I 9. Трудно культивировать в непрерывном режиме мицелиаль-ные культуры из-за их вязкости и гетерогенности.10. Непрерывный процесс предъявляет повышенные требовав ния к надежности оборудования. I
Вопросы для повторения
1. Расскажите о тубулярном процессе непрерывного культивирования микро-. организмов, его сходстве с периодическим процессом ферментации.
2. Назовите недостатки тубулярного процесса непрерывного культивирования микроорганизмов.
3. Опишите хемостатный процесс непрерывного культивирования с одиночным реактором.
4. Почему в хемостатном непрерывном процессе не требуется подачи посевного материала?
5. Приведите математический анализ хемостатного процесса на основе модели Моно. *
6. Как зависит от начальной концентрации субстрата при постоянной скорости протока концентрация биомассы микроорганизмов и остаточная концентрация субстрата?
7. Как зависит концентрация биомассы и остаточная концентрация субстрата от скорости разбавления при постоянной концентрации субстрата на входе?
8. Как доказать, что удельная скорость роста биомассы в хемостатном процессе равна скорости разбавления?
9. Что происходит с хемостатным процессом, если скорость роста культуры возрастает или снижается по сравнению со скоростью разбавления?
10. Как осуществляется саморегулирование в хемостате?
11. Как определить скорость разбавления, при которой происходит вымывание культуры из хемостатного процесса?
12. При какой скорости разбавления производительность по биомассе в хемостате является максимальной?
13. Как сравнить производительность по биомассе непрерывного хемостатного процесса и периодического процесса ферментации?
14. В каком процессе производительность по биомассе больше: в хемостатном или в периодическом процессе ферментации?
15. Как изменяются хемостатные кривые при лимитировании различными субстратами и при клеточном росте на стенках аппарата?
16. Как изменяется хемостатная кривая в случае лимитирования роста культуры растворенным кислородом?
17. Чему равна критическая скорость разбавления при лимитировании роста культуры кислородом?
18. При какой скорости разбавления производительность хемостата, лимитированного кислородом, максимальна?
19. Как объяснить явление автоселекции в непрерывном хемостате?
20. Что произойдет, если новый мутант растет с меньшей скоростью, чем исходная культура?
21. Дайте анализ хемостата с рециркуляцией биомассы клеток. Как изменяется производительность в сравнении с обычным хемостатом?
22. Двухстадийный хемостат: как изменяются концентрации биомассы и субстрата во втором аппарате?

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 |




