2) клеточная деструкция;
3) бактериальная деструкция;
4) механодеструкция.
По источникам компонентов, участвующих в деструктивном процессе, биодеструкцию имплантата можно разделить на два типа: неклеточная и клеточная. К первому типу относится неферментативный гидролиз, т. е. гидролитическая деструкция в слабых электролитных растворах, которыми является тканевая жидкость или сыворотка. К клеточному типу разрушения относятся все остальные процессы, поскольку именно клетки являются основными источниками ферментов, перекиси водорода. Кроме того, клетки утилизируют продукты распада биоматериала, обладая фагоцитарной активностью. Механические нагрузки и в том и в другом случае усиливают эффект протекающих процессов.
Основные понятия, которые необходимо знать после изучения материала данной лекции: полимерлі нанобөлшектердің құрылысы, қасиеттері, медицинада және фармацияда қолданылуы
Вопросы для самоконтроля:
Полимерлі нанобөлшектектер фармацияда қолданылуын сипаттаныз Полимерлі нанобөлшектер дегеніміз не? Полимерлі нанобөлшектерінің қасиеттері?Рекомендуемая литература:
1. Высокомолекулярные соединения: Учебник для вузов. М.: Академия, 2010, 368 с. С.4-18
2. , Физиологически активные полимеры. –М.: Химия, 1986. С. 5-11.
3. Полимеры в фармации / Под редакцией . – М.: Медицина, 1985. С. 7-10.
Лекция 15-18 – Физиологически активные полимеры
План лекции:
Собственная физиологическая активность водорастворимых полимеров Механизм действия ФАП Стратегия синтеза. Тактика синтеза. Реакции, применяемые в синтезе физиологически активных полимеров.Под собственной физиологической активностью полимеров понимают активность, которая связана с полимерным состоянием и не свойственна низкомолекулярным аналогам или мономерам. Механизмы проявления собственной физиологической активности включают в себя физические эффекты, связанные с большой массой, осмотическим давлением, конформационными перестройками а также могут быть связаны с межмолекулярными взаимодействиями с биополимерами организма.
По проявляемой физиологической активности синтетические полимеры могут быть разделены на пять больших групп.
Нейтральные полимеры с неспецифической активностью Поликатионы Полианионы Синтетические аналоги нуклеиновых кислот. Полимеры с различными другими функциональными группами.Возможны два основных механизма действия ФАП. В соответствии с первым из них ФАП на всех этапах действует как полимерное соединение и действующее начало не выделяет. Такие полимеры иногда называют «истинными» ФАП, они напоминают ФАП с собственной активностью, но в отличие от последних низкомолекулярные аналоги этих ФАП тоже активны. Другой механизм действия ФАП «прививочного» типа заключается в том, что в тот или иной момент ФАП отщепляет действующее начало, которое оказывает эффект в низкомолекулярном виде. В этом случае полимер выполняет ряд вспомогательных функций, в основном — транспортных, повышая эффективность действия ФАВ.
Для ФАП существует две главных стратегии синтеза. Первая из них заключается в создании полимерной цепи посредством (со)полимеризации или (со)поликонденсации соответствующих мономеров, вторая состоит в химической модификации готовых полимерных молекул.
В соответствии с первой стратегией синтез ФАП начинается с получения соответствующих мономеров - виниловых, акриловых и аллильных. Эти мономеры обычно получают введением ненасыщенных групп в молекулы ФАВ. Синтез ФАП из указанных мономеров обычно заключается в радикальной полимеризации. Остаток ФАВ, который содержит различные функциональные группы, не должен участвовать в процессе полимеризации. Особенно нежелательна даже минимальная химическая модификация остатка ФАВ в ходе полимеризации, которая может привести к изменению ожидаемой физиологической активности полимера. Общая схема синтеза ФАП (со) полимеризацией приведена на рис. 1.
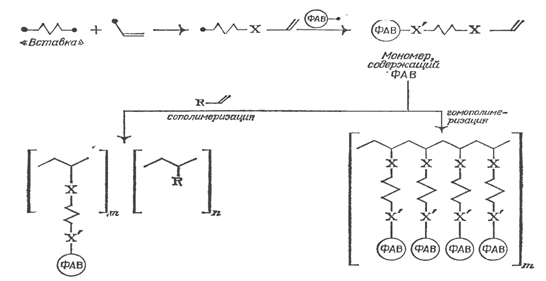
Рисунок 1. Схема синтеза ФАП со(полимеризацией)
Преимущества синтеза ФАП (со)полимеризацией: простота и универсальность этого метода для карбоцепных полимеров.
Основной вопрос тактики синтеза заключается в выборе оптимальных способов образования связей полимера-носителя со «вставкой» (X) и «вставки» с ФАВ (X'). Существенным моментом тактики синтеза ФАП является выбор реакционной среды. Желательно проводить модификацию полимеров в растворе во избежание получения композиционного неоднородного ФАП. Растворитель должен обеспечивать наиболее развернутую конформацию модифицируемого полимера как до, так и после реакции. Растворитель не должен вызывать агрегацию полимера. Если полимер не растворим в применяемом растворителе, то он должен в нем хорошо набухать, чтобы свести диффузионные ограничения к минимуму. Низкомолекулярные компоненты реакции в этом случае должны быть растворимыми.
Хорошая очистка синтезированных водорастворимых ФАП очень существенна для проявления физиологической активности. Она включает два этапа. Первый из них заключается в освобождении полимера от низкомолекулярных примесей: солей, исходных реагентов, продуктов реакции. Для этой цели используют переосаждение, диализ, ультрафильтрацию и молекулярно-ситовую хроматографию. Второй этап очистки синтезированных ФАП заключается во фракционировании полимерных продуктов реакции по составу и М. Используемые на данном этапе методы в основном хроматографические.
Основные требования к реакциям модификации: высокая эффективность; проведение реакции в условиях, не вызывающих существенной деструкции или сшивания полимера; сведение к минимуму побочных реакций, приводящих к введению в полимер новых функциональных групп или к нежелательной модификации присоединяемого ФАВ; однозначность протекания реакции, приводящая к единственному типу связи ФАВ с полимером-носителем.
В физиологических условиях полимеры-носители должны быть химически инертны. Для присоединения ФАВ или ФАВ со «вставкой» к полимеру-носителю один из двух участников реакции приходится активировать — переводить в реакционно-способное, часто мало устойчивое соединение. Превращения активированных групп в большинстве случаев неоднозначны. Помимо образования нужной химической связи они превращаются в исходные соединения и дают побочные продукты.
Для образования прочных связей X между полимером-носителем и ФАВ, ФАВ с «вставкой» или с «вставкой» обычно используют 0-, Н - или С-алкилирование. Более приемлемы эпоксиды, реагирующие в относительно мягких условиях и образующие дополнительную гидроксильную группу у б-углеродного атома:

Эпоксидные циклы входят в состав эпоксипропильных групп, которые присоединены к полимерам в виде простых или пространственно затрудненных сложных эфиров.
Наиболее популярный и самый мягкий метод образования гидролитически стабильных связей — восстановительное N-алкилирование. Оно состоит во взаимодействии альдегидов с первичными аминами и последующем восстановлении, обычно борогидридами.
![]()
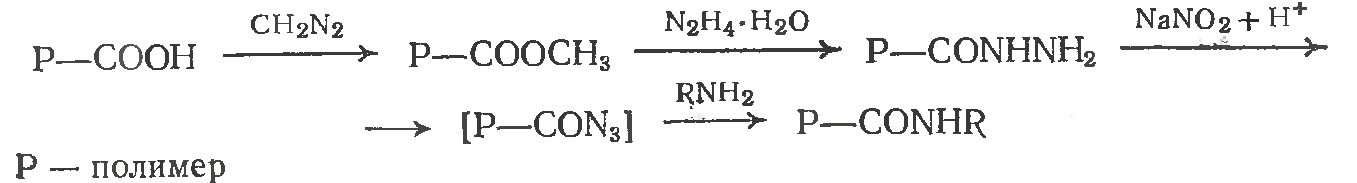
Ацилазиды (смешанные ангидриды карбоновой и азотистоводородной кислот) менее активны, чем эпоксиды. Способы их получения многостадийны, что приводит к образованию различных функциональных групп из-за незавершенности промежуточных реакций, а также из-за побочных реакций распада ацилазидных групп.
Основные понятия, которые необходимо знать после изучения материала данной лекции: Собственная физиологическая активность водорастворимых полимеров, механизм действия ФАП, стратегия синтеза, тактика синтеза, реакции, применяемые в синтезе физиологически активных полимеров.
Вопросы для самоконтроля:
Что такое физиологически активные полимеры? На чем основано действие ФАП? Каков механизм действия ФАП?Рекомендуемая литература:
1. Высокомолекулярные соединения: Учебник для вузов. М.: Академия, 2010, 368 с. С.4-18
2. , Физиологически активные полимеры. –М.: Химия, 1986. С. 5-11.
3. Полимеры в фармации / Под редакцией . – М.: Медицина, 1985. С. 7-10.
Лекция 19, 20 – Полимерные наночастицы
План лекции:
Полимерные наночастицы: структура, строение Области применения полимерных наночастиц в медицинеНаночастица (nanoparticle) – изолированный твёрдофазный объект размером 1–100 нм, имеющий отчётливо выраженные границы. По строению различают:
- простые наночастицы (состоящие из одного химического соединения, например, наночастицы оксида бора или серебра);
- сэндвич-наночастицы;
- многокомпонентные (многофункциональные) наночастицы для достав - ки лекарств.
Содержат внутреннее ядро, которое может быть твердым (напри - мер, квантовые точки), жидким (например, липосомы) или содержать препарат в типичном для него агрегатном состоянии.
Примеры применения наночастиц в медицине:
- наночастицы золота способны деспирализовать ДНК («unzipping» process). Данное направление исследований актуально с точки зрения понима - ния возможной токсичности наночастиц и упрощения техники манипуляции отдельными генами;
- золотые наночастицы используются в качестве носителя антиканцеро - генного препарата доксорубицина (doxorubicin, DOX; допущен к использова - нию FDA), связанного с молекулами ДНК. Одна золотая наночастица диамет - ром 15,5 нм способна связать до 100 молекул DOX.
Полимерные материалы обладают рядом преимуществ, определяющих эффективность их применения в технологиях доставки: биосовместимость, способность к биодеградации, функциональная совместимость. Типичными соединениями, которые представляют основу для создания полимерных наночастиц, являются полимолочная и полигликолевая кислоты, полиэтиленгликоль, поликапралактон и др., а также их различные сополимеры.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |



