УДК 579.64:631.46(574.1)
, к. б.н., , к. б.н., , к. б.н., ,
, ,
КЛАСТЕРНО-ТАКСОНОМИЧЕСКИЙ АНАЛИЗ МИКРОБНЫХ СООБЩЕСТВ ПОЧВ ЗАПАДНО-КАЗАХСТАНСКОЙ ОБЛАСТИ
С ПОМОЩЬЮ МЕТОДОВ СОВРЕМЕННОЙ МЕТАГЕНОМИКИ
В статье приведена апробация методики выделение ДНК почвенной микробиоты на примере каштановых почв (Kastanozems) Западно-Казахстанской области. Был проведен таксономический анализ библиотек почвенного микробиома, согласно которому наибольшую долю в микробных сообществах проанализированных почв составляют филумы Actinobacteria и Proteobacteria. Заметную долю в составе микробиомов исследованных образцов занимают археи.
Ключевые слова: Микробиома, почвенные микроорганизмы, ПЦР, секвенирование, таксономия, тип почвы, ДНК, агроэкология, мониторинг, молекулярная биология, 16s рРНК, метагеном.
, к. б.н., , к. б.н., , к. б.н., ,
, ,
ҚАЗІРГІ ЗАМАНҒЫ МЕТАГЕНОМИКА ӘДІСТЕРІНІҢ КӨМЕГІМЕН БАТЫС ҚАЗАҚСТАН ОБЛЫСЫНЫҢ ТОПЫРАҒЫ МИКРОБТЫ БІРЛЕСТІГІНІҢ КЛАСТЕРЛІ-ТАКСОНОМИКАЛЫҚ ТАЛДАУЫ
Мақалада Батыс Қазақстан облысының топырағының (Kastanozems) мысалында топырақ микробиотының ДНҚ бөлу әдістемесін тексеру жүргізілді. Топырақтық микробиом жиынтығының таксономикалық талдауы жүргізілді, оған сәйкес зерттелген топырақ үлгілерінің микробты бірлестіктерінде Actinobacteria және Proteobacteria филумдары көп үлеске ие. Зерттелген үлгілердің микробиомдарының құрамында айтарлықтай үлесті археилар иеленген.
Кілт сөздер: микробиома, топырақ микроағзалары, ПЦР, секвенирлеу, таксономия, топырақ түрі, ДНҚ, агроэкология, мониторинг, молекулярлы биология, 16s рРНК, метагеном.
N. K. Sergaliev, с. b.s., E. E. Andronov, с. b.s., A. G. Pinaev, с. b.s., M. G. Kakishev, A. T. Zhiengaliev, M. A. Volodin, A. Zh. Turbaev
CLUSTER-TAXONOMIC ANALYSIS OF MICROBIAL COMMUNITIES OF SOIL IN WEST KAZAKHSTAN USING THE METODS OF MODERN METAGENOMICS
Abstract - The article presents the results of research on the use of the soil microbiota condition as an indicator of the agro-ecological condition of the soil. We carried out a taxonomic analysis of the soil microbiome libraries, according to which the Actinobacteria and Proteobacteria phyla dominate the microbial communities of the analyzed soils. The Archaea form a large part of the microbiome of the studied samples.
Key words: Microbiome, soil microorganisms, PCR, sequencing, taxonomy, soil type, DNA, agroecology, monitoring, molecular biology, 16s rRNA, metagenome
В мировой микробиологии за последние двадцать лет произошла настоящая революция, связанная с пониманием истинных масштабов биологического разнообразия прокариот. Произошло это во многом благодаря бурному развитию и внедрению в экологическую практику методов молекулярной биологии. На сегодняшний день исследования в области молекулярной экологии микроорганизмов объединяются под общим названием - метагеномные исследования. Этот термин был выбран исходя из аналогии со статистическим методом мета-анализа (анализа массива эмпирических фактов направленных на решение сходных задач). Смысл его заключается в изучении сходных, но не идентичных единиц генетической информации. Объектом изучения метагеномики является метагеном – генетический материал, полученный непосредственно из окружающей среды без предварительного культивирования микроорганизмов.
Традиционные методы анализа почвы дают весьма грубые и неоднозначные результаты, например, почвы с одними и теми же агрохимическими характеристиками могут иметь кардинальные различия в плодородии. Ответственными за такие различия часто являются трудновыявляемые факторы. Далеко не всегда удается выявить весь микробный состав той или иной почвы, так как большая часть микроорганизмов являются просто не культивируемыми в лабораторных условиях. Поэтому традиционный микробиологический подход к исследованию почвенных микроорганизмов не дает полной картины о микрофлоре исследуемых почв, а значит, не позволяет дать полную оценку микробиологическим процессам, протекающим в ней. В настоящей работе для характеристики почв выбран ее микробиом, главной составной частью которого является геномный пул микроорганизмов – та частью почвы, которая наиболее чутка к любым изменениям. Связь особенностей микробиома почвы и ее плодородия почти не исследована. Для понимания этой связи требуется проведение комплексной работы.
Основным направлением данного исследования является применить методы современной метагеномики для оценки почвенного микробиома. Основная идея, лежащая в основе исследований - анализ структуры почвенного микробиома с использованием методов современной метагеномики (секвенаторов нового поколения, обеспечивающих одновременное чтение десятков тысяч нуклеотидных последовательностей) как чувствительного индикатора состояния почвы, в котором отражается весь комплекс ее свойств, включая биологические, а также широкий ряд трудно учитываемых или неучитываемых факторов, влияющих на почвенное плодородие и сельскохозяйственный потенциал почв. В дальнейшем на основе данных массового скринига почв Западно-Казахстанской области предполагается разработать систему микробиомного мониторинга почв сельскохозяйственного назначения, обеспечивающую адекватную оценку их агроэкологического состояния и разработку методов оптимизации использования почв [1,2,3].
Методика
Отбор проб почв проводился согласно ГОСТ 17.4.4.02-84. Точечные пробы отбирали на площадке из двух слоев 0-10 см. и 10-20см. по диагонали с таким расчетом, что бы каждая проба представляла собой часть почвы, типичной для генетических горизонтов или слоев данного типа почвы.
Для проведения молекулярно-биологических исследований микробиома почвенных образцов была применена типичная схема эксперемента. Схема типичного эксперимента заключается в выделении и очистке совокупной ДНК из образца, отобранного из окружающей среды, ПЦР-амплификации определенных участков генома, их клонировании с последующим определением и анализом нуклеотидных последовательностей (секвенированием). В том случае, когда секвенированию подвергается вся выделенная ДНК, речь идет о новейшей области исследования, называемой «метагеномикой», т. е. описанием совокупного генома всех живых организмов данного местообитания. Частным случаем метагеномики является ограничение секвенируемых участков таксономически значимыми генами, например, широко используемыми в молекулярной таксономии рибосомальными генами 16S рРНК (для прокариот) и 18S рРНК (для эукариот). Такие исследования позволяют наиболее полно выявить таксономический состав анализируемого микробного сообщества. Результатом секвенирования библиотеки рибосомальных генов является набор нуклеотидных последовательностей длиной от 200 до 1500 пн, количество которых для одного проанализированного образца варьирует от 100 до 1-2 тысяч последовательностей. Дальнейший анализ полученных нуклеотидных последовательностей предполагает их таксономическую характеристику (путем сравнения с образцовыми базами данных), сопоставление библиотек друг с другом, вычисление коэффициентов генетического разнообразия и. т.д.
Для выделения ДНК из почвы нами была применена методика основанная на экстракции c последующей очисткой методом электрофореза в агарозном геле и выделения из блоков агарозы, содержащей ДНК, с абсорбцией на тонкодисперсной окиси кремния [4].
Сравнительный кластерно-таксономический анализ библиотек полученных из нативных почв проводили на сайте RDP (http://rdp. cme. msu. edu/) с использованием расстояния по Morisita-Horn, кластеризация по алгоритму UPGM.
Результаты и их обсуждения
В ходе работ была создана коллекция из 20 образцов почв, относящихся к основным типам почв Западно-Казахстанской области, представляющих собой целинные земли (Таблица 1). Данные об отобранных пробах приведены в таблице 1.
Таблица 1 - Пробы почв Западно-Казахстанской области
Тип почв | Место отбора | Образец | GPS координаты | Глубина отбора |
Солонец каштановый | п. Актау | 01_SOLON_AKT_1 | N50є56.869ґ E 051є07.938ґ | 0-10 см |
02_SOLON_AKT_1 | 10-20 см | |||
Темно-каштановая неполноразвитая | п. Актау | 03_TKASHT_AKT_2 | N51є00.150ґ E 050є09.025ґ | 0-10 см |
04_TKASHT_AKT_2 | 10-20 см | |||
Темно-каштановая малоразвитая | п. Актау | 05_TKASHT_AKT_3 | N51є00.532ґ E 051є18.278ґ | 0-10 см |
06_TKASHT_AKT_3 | 10-20 см | |||
Солончак | п. Новопавловка | 07_SOLON_NVPL_4 | N51є05.473ґ E 051є42.515ґ | 0-10 см |
08_SOLON_NVPL_4 | 10-20 см | |||
Лугово-каштановые | п. Новопавловка | 09_LKASHT_NVPL_5 | N51є08.774ґ E 051є39.234ґ | 0-10 см |
10_LKASHT_NVPL_5 | 10-20 см | |||
Темно-каштановая среднемощная | п. Новопавловка | 11_TKASHT_NVPL_6 | N51є06.823ґ E 051є39.694ґ | 0-10 см |
12_TKASHT_NVPL_6 | 10-20 см | |||
Светло-каштановые | п. Талдыапан | 13_SKASHT_TLD_7 | N49є33.450ґ E 050є16.249ґ | 0-10 см |
14_SKASHT_TLD | 10-20 см | |||
Каштановая | п. Кушум | 15_KASHT_KUSH_8 | N50є52.599ґ E 051є06.489ґ | 0-10 см |
16_KASHT_KUSH_8 | 10-20 см | |||
Чернозём южный | п. Щукино | 17_CHRZ_SHUK | N51є40.301ґ E 050є48.889ґ | 0-10 см |
18_CHRZ_SHUK | 10-20 см | |||
Пойменная каштановая | ЗКО г. Уральск пойма реки Урал | 19_POJM_URA | N51є07.731ґ E 051є21.848ґ | 0-10 см |
20_POJM_URA | 10-20 см |
Из данных образцов была получена тотальная ДНК. На рисунке 1 представлена картина электрофоретического разделения сырого экстракта почвенной ДНК, полученного на первой стадии выделения.
Почвенная ДНК на рисунок 1 фрагментирована, но не деградирована, (размер фрагментов около 5-10 тыс. п. н.). В данном случае фрагментация ДНК является следствием интенсивного встряхивания с матриксом (FastPrep 24, 1 мин, макс. интенсивность).
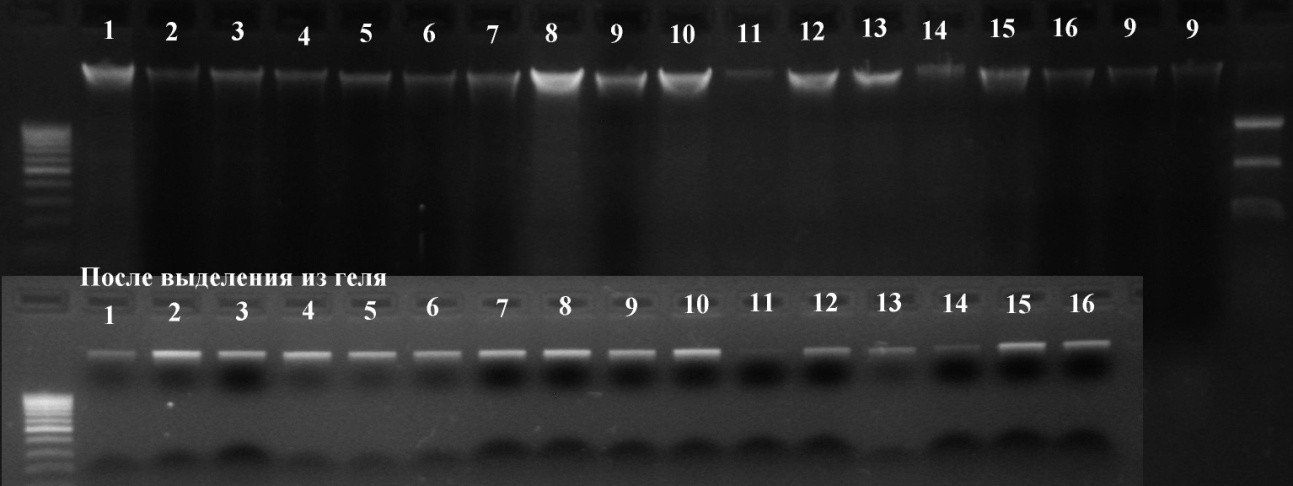
Рисунок 1 - Почвенная ДНК
Данное обстоятельство не существенно ни для создания библиотек гена 16S рРНК, однако может стать проблемой для исследований, в которых требуется, например, клонирование высокомолекулярных фрагментов почвенной ДНК. В этом случае предпочтение следует отдавать методам ферментативного разрушения почвенных микроорганизмов, либо использовать более щадящие режимы разрушения образцов. Деградация ДНК проявляется в образовании протяженных «шлейфов» с максимумом концентрации, смещенным в сторону низкомолекулярных компонентов. Препараты деградировавшей ДНК непригодны для дальнейшего использования за исключением особых случаев. В данном эксперименте признаков деградации ДНК не выявлено.
Гуминовые компоненты и РНК могут сорбировать довольно большое количество бромистого этидия, так, что его не хватает для окраски ДНК. В этом случае в пробах с высоким количеством ДНК ее количество может быть недооценено. Для исключения данного эффекта гель можно окрасить после электрофореза. Как видно из рисунка 1, скорости электрофоретической миграции гуминовых компонентов гораздо выше, чем скорость миграции фракции ДНК. Именно на этой особенности основана дальнейшая очистка препарата ДНК. Процесс отделения гуминовых компонентов ясно виден в геле во время электрофореза при обычном освещении. Затем вырезают блок агарозы, содержащий ДНК, и проводят окончательную очистку препарата методом с сорбцией ДНК на окиси кремния [5,6].
На рисунке 2 показаны результаты электрофоретического разделения образцов почвенной ДНК после очистки сырого экстракта с использованием сорбции на диоксиде кремния.
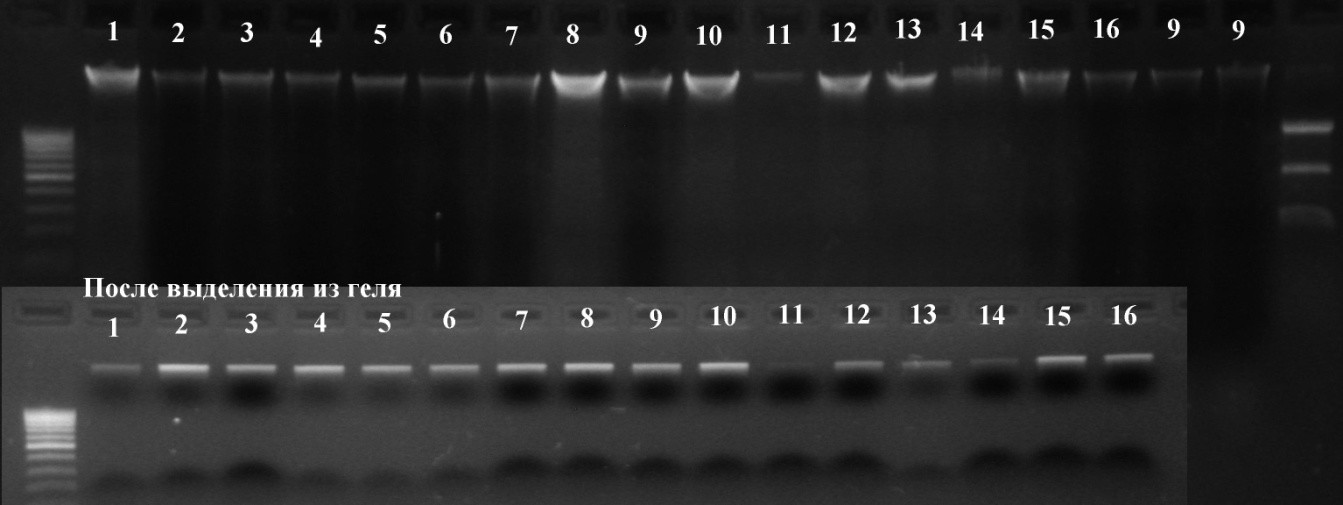
Рисунок 2 - Препараты почвенной ДНК очищенные методом электрофореза
Определение концентрации ДНК показало, что метод позволяет выделять до 2-5 мкг ДНК из 1 г почвы, что свидетельствует о высоком выходе. Кроме того, выделенная ДНК отличается высокой чистотой (для почвенной ДНК), так как эффект ингибирования не наблюдается при концентрации ДНК в реакции ПЦР до 0,2 нг/мкл.
Было проведено исследование почвенного микробиома высокопроизводительным секвенированием. С использованием 20 мультиплексных fusion-праймеров и почвенной ДНК, выделенной из 20 образцов почв, были получены 20 ампликонных библиотек фрагмента гена 16S рРНК. Самый легкий фрагмент соответствует библиотеке, серия фрагментов большего размера соответствует мультимерам, образующимся при выделении фрагмента из геля.
Их концентрации были выровнены с использованием гель-денситометрии, затем амплификаты были объединены, переочищены путем выделения суммарной библиотеки из геля (рисунок 3). Разрушение мультимеров проводили путем прогревания библиотеки при 65 °С в течение 10 мин с последующим охлаждением на льду.
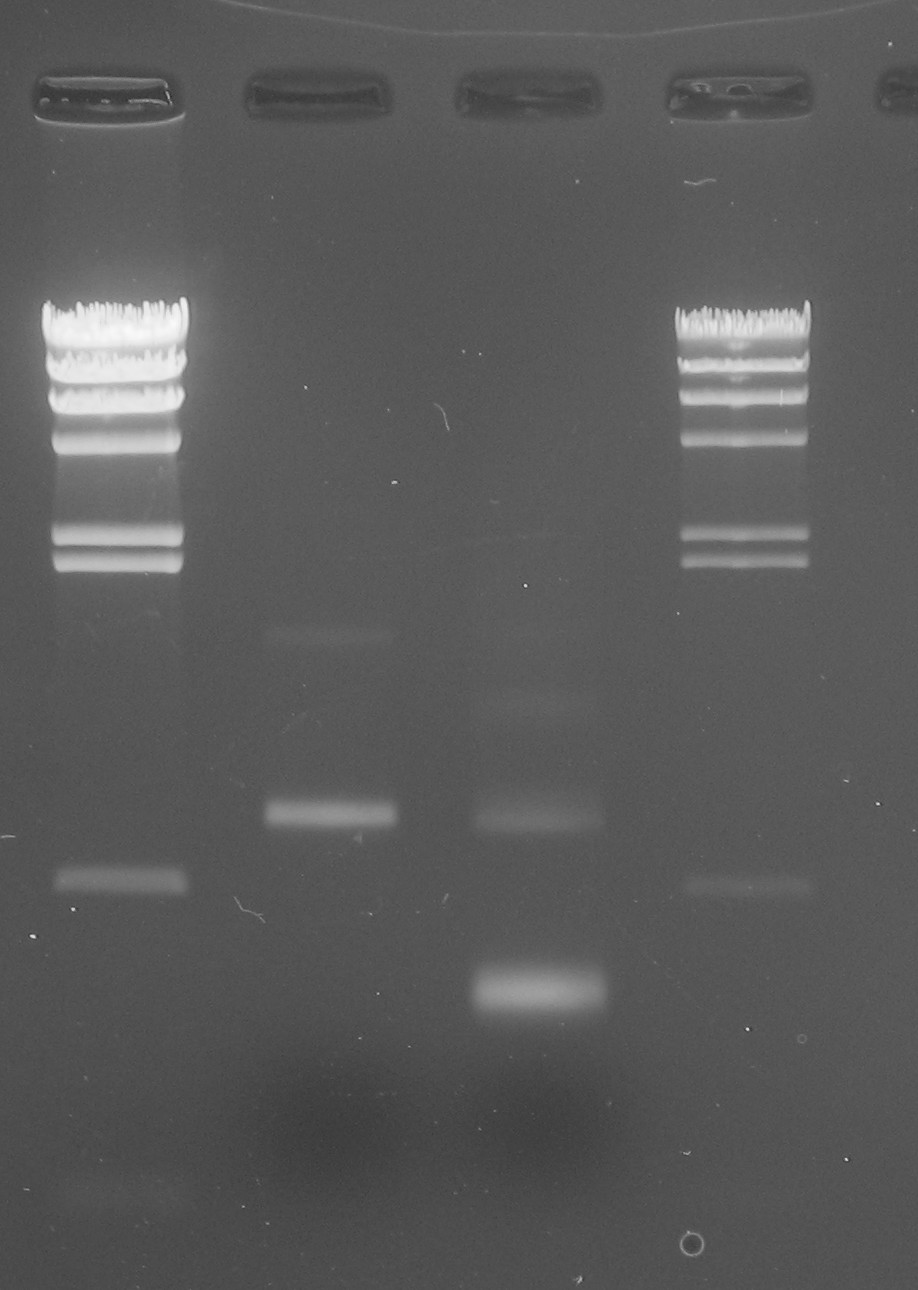
Рисунок 3 - Ампликонная библиотеки образцов почв
После очистки суммарной библиотеки ее концентрация была нормирована на 10 млн. копий фрагмента гена 16S рРНК на мкл с использованием точного определения концентрации на флюориметре (краситель SYBR-gold, прибор QUBIT, Invitrogen).
Секвенирование библиотеки было проведено в точном соответствии с рекомендациями к прибору GS Junior (Roche). На первом этапе была проведена эмульсионная ПЦР, затем обогащение библиотеки, которое составило 15% (при допустимом интервале 5-20%) и, наконец, собственно секвенирования, которое прошло без нарушений. В общей сложности было получено около 100 000 нуклеотидных последовательностей, после фильтрации коротких последовательностей, последовательностей низкого качества, последовательностей с нечетко читаемыми праймерами и мультиплексными идентификаторами осталось 46 883 нуклеотидных последовательностей, что соответствует примерно 2 300 последовательностей на образец (с разбросом от 1 084 до 4 378 последовательностей на образец).
При анализе по доменальному распределению во всех образцах выявлено два основных домена – домен Bacteria и Archaea причем с явным преобладанием первого домена.
Наибольшее количество архей встречается в образцах темно-каштановой неполно развитой почвы с глубины отбора 0-10 см. п. Актау чуть более 10% и каштановой почвы с глубины отбора 10-20 см. п. Кушум около 10% (рисунок 4).
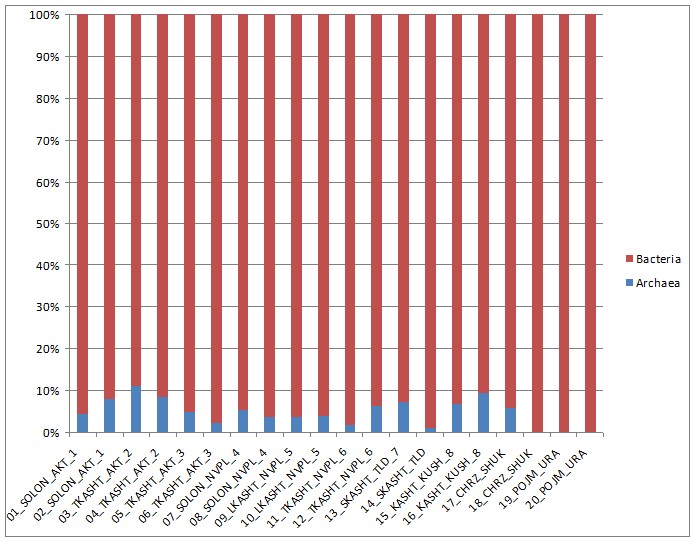
Рисунок 4 – Доменное распределение микробов в образцах нативной почвы
Причем отмечается отсутствие или незначительное количество представителей домена Archaea в образцах почв чернозёма южного п. Щукино глубина отбора 10-20 см и пойменной каштановой почвы с поймы реки Урал города Уральска, глубина отбора 0-10 см, 10-20 см. Отсутствие представителей домена Archaea в пойменной каштановой почве вероятно объясняется кратковременным затоплением и как следствие заполнением свободных пор водой. Такие анаэробные условия для Archaea являются неблагоприятными. Способность организмов некоторое время переживать неблагоприятные внешние факторы, в данном случае несущественно. Также вероятно влияют плотность почвы, содержание органического вещества, на доминальное распределение микробов почв. Исследователи обычно исследуют положение организма относительно внешних факторов, т. е. какие условия наиболее оптимальны и типичны для исследуемого организма. Такие агроэкологические факторы как сбитость, уплотнение почвы очень сильно влияют на соотношение микробов. Также нельзя забывать что одни и те же культуры микроорганизмов при разных условиях проявляют себя по разному, т. е. весьма чувствительны к агроэкологическому состоянию. Весьма вероятно, что по степени воздействия различных фаз почвы на распределение микробов в почве на первом месте стоит твердая, далее жидкая и газовая, хотя все фазы одновременно влияют на микробы. В следующем году более детально будут проанализированы влияние различных агроэкологических факторов на распределение микробов почвы. А также будут сравнены и выявлены закономерности отличия нативных почв с аффектированными аналогами. Такое сравнение характерно для исследований сукцессионных изменений в экосистеме. Особенностью таких исследований является изучение влияния внешних факторов на динамическую систему в данном случае почву.
Проводя кластерно-филумный анализ выявлено 27 филумов, явно преобладающие филумы Actinobacteria 23 – 38 % , Proteobacteria 9-48 %, а так же неатрибутируемые филы 13-32% (рисунок 5).
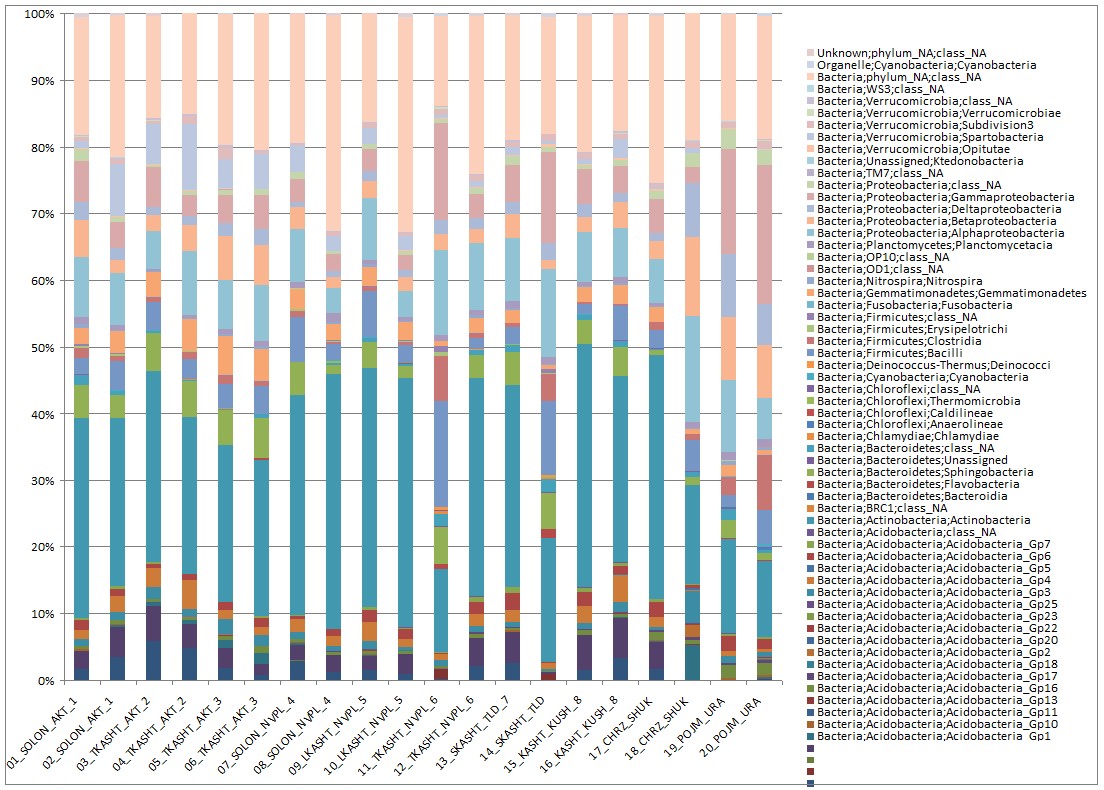
Рисунок 5 – Филумное распределение микробов в образцах нативной почвы
Наибольшее количество филума Actinobacteria 38.13 % отмечено солончаке п. Новопавловка, почва взята с глубины 10-20 см., наименьшее 11.33 % в пойменной каштановой почве с поймы реки Урал города Уральска, глубина отбора 10-20 см. Филум Proteobacteria наименьше представлен в 9,33 % в солончаке п. Новопавловка, почва взята с глубины 10-20 см., наибольшее 48,38 % в пойменной каштановой почве с поймы реки Урал города Уральска, глубина отбора 0-10 см. Неатрибутируемые филы широко распространены в солончаке п. Новопавловка, почва взята с глубины 10-20 см. – 32,28 % и 32,32 % в лугово-каштановых нативных почвах отобранных в п. Новопавловка с глубины 10-20 см. Наименьшее 15,02 % в темно-каштановой неполноразвитой почвы отобранной в п. Актау с глубины 10-20 см.
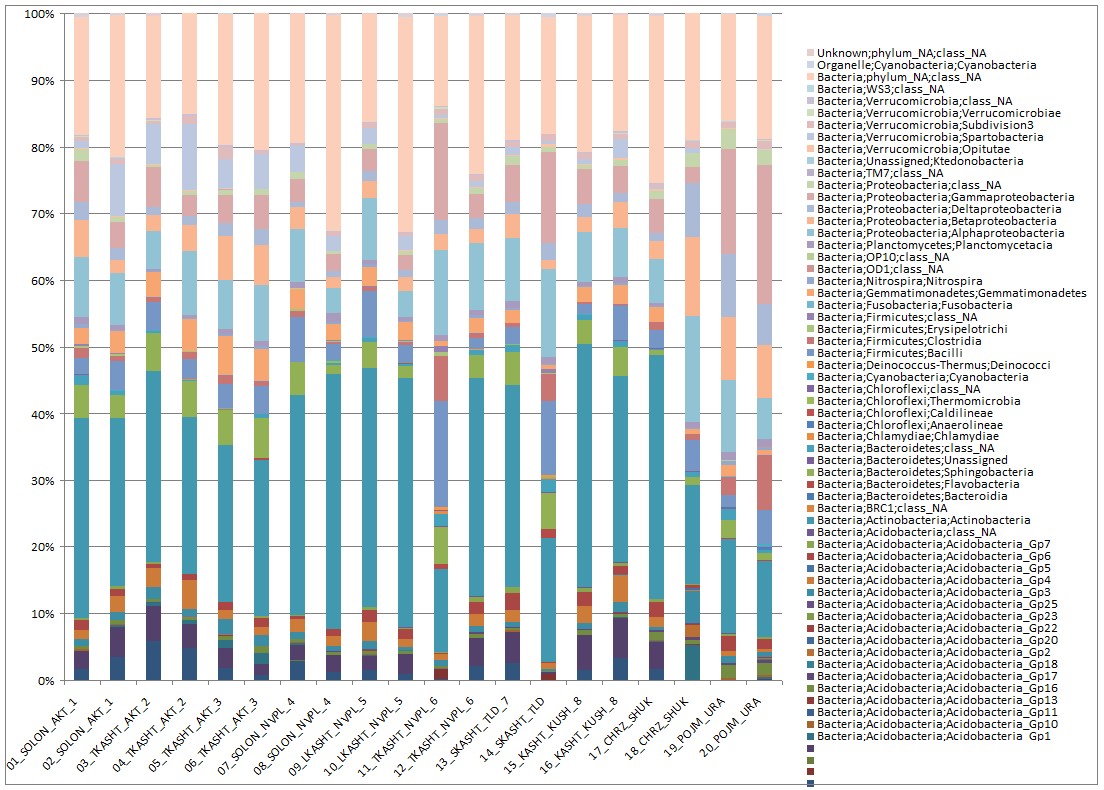
Рисунок 6 – Классовое распределение микробов в образцах нативной почвы.
При проведении кластерного анализа распределения по классам выявлено 63 класса из которых 15 неатрибутируемые. Преобладающим классом является класс Actinobacteria вирирующий от 11 -38 % в разных образцах, пойменно-каштановая пойма реки Урал г. Уральск глубина отбора 10-20см. – 11,33 % и 38,13 % почва солончакового типа п. Новопавловка, глубина отбора 10-20 см. (рисунок 6)
Наибольшее количество неатрибутируемого класса наблюдалось из домена Bacteria неатрибутируемого филума 13-32 %. 32,28 % почва солончакового типа п. Новопавловка, глубина отбора 10-20 см. и 13,49 % темно-каштановая среднемощная п. Новопавловка глубина отбора 0-10 см.
Распределение микробов по отрядам составило 110 отрядов из них 28 отрядов неатрибутируемые (рисунок 7).
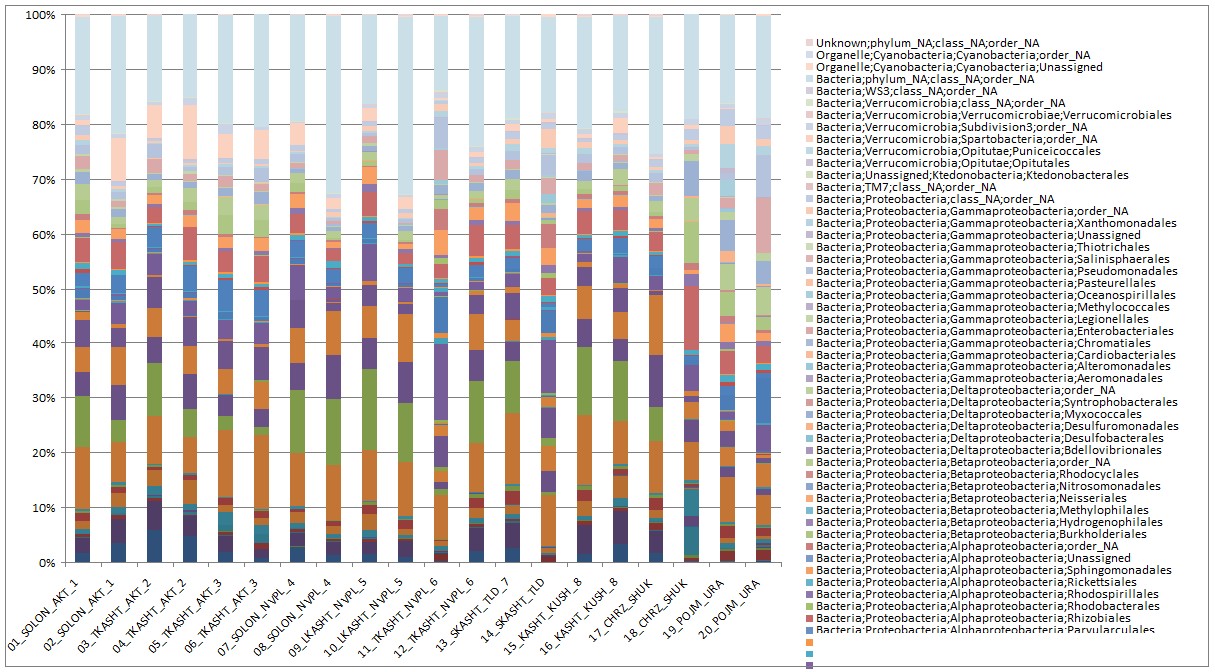
Рисунок 7 –Распределение микробов по отрядам в образцах нативной почвы
Доминирующим отрядом так же является Actinomycetales из класса Actinobacteria 5-13 % и 13 – 32 % неатрибируемых Bacteria по отрядному и вышестоящей классификации.
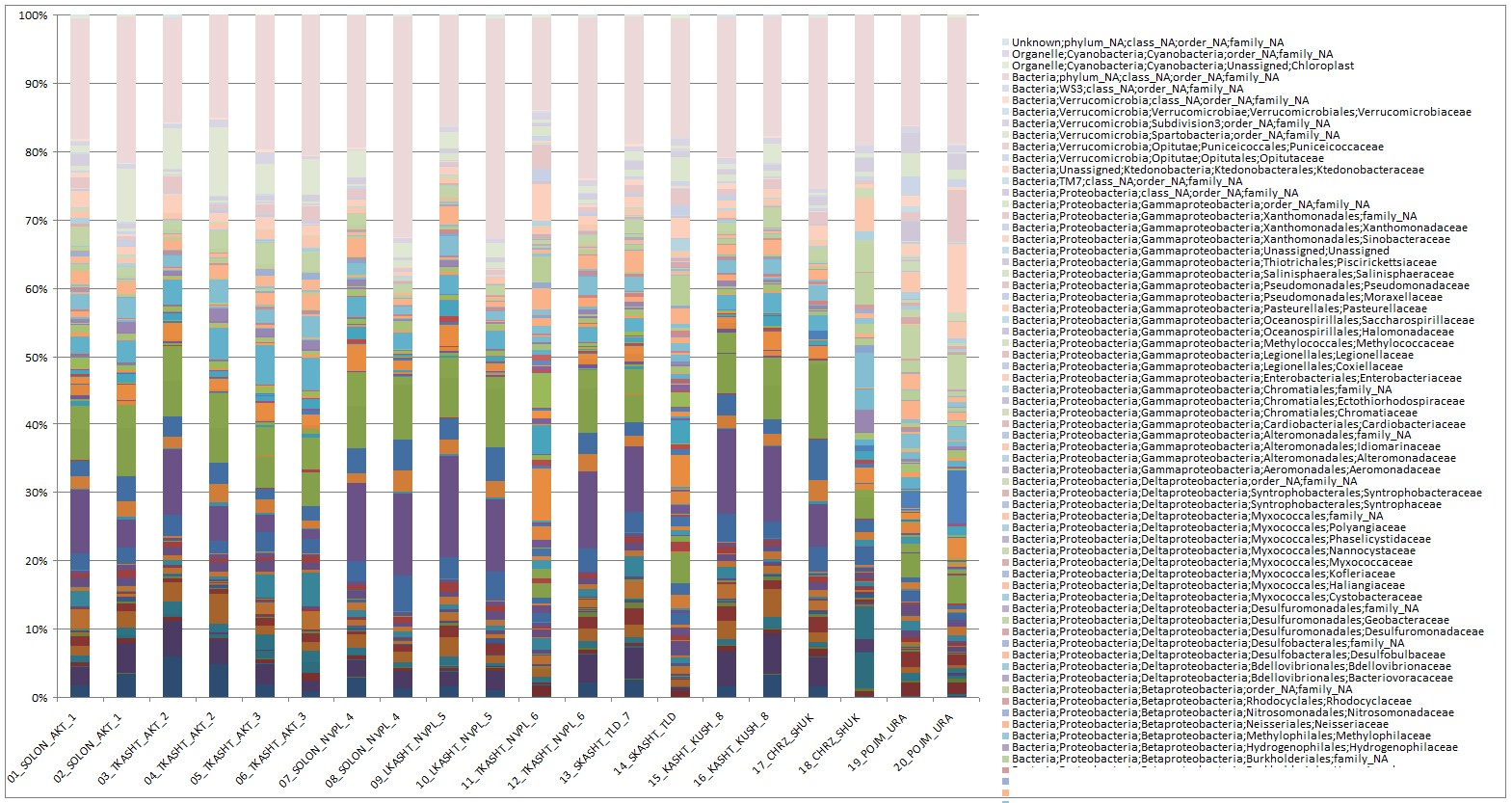
Рисунок 8 – Распределение микробов по семействам в образцах нативной почв
Выявлено 215 семейств из них преобладают неатрибируемые 47 семейств бактерий с частотой распределения 13-32%, когда как других семейств менее 10% (рисунок 8).
При кластеризации по родовому распределению выявлено 474 рода из них 126 неатрибируемые, число распределения их по образцам почв варьирует 15-32 %, когда как других родов не более 5 % в образце.
Так же мы провели построение кластерного дерева по семействам и родам. Деревья построены по результатам кластерного анализа – по родам, также с учетом неатрибутируемых таксонов и соответствующий родству по агрохимическим показателям (рисунок 9).
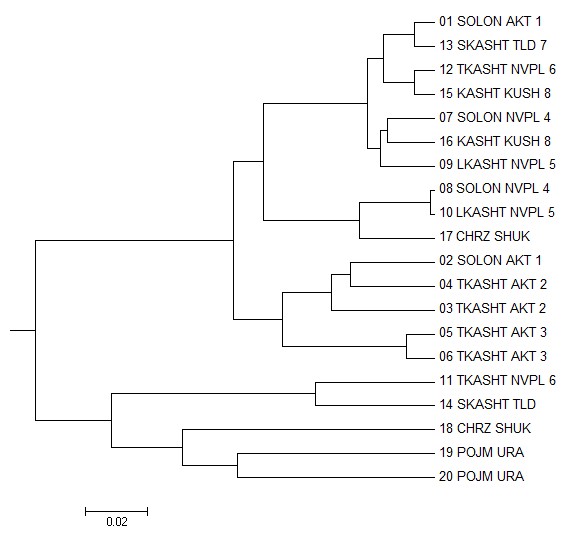
Рисунок 9 – Кластерный анализ микробиома нативных почв
Западно-Казахстанской области
Заключение
В ходе проведенных исследований, выявлено то что неатрибутируемых последовательностей в почве очень много, это видно на таксономических диаграммах, причем чем ниже ранг, тем их больше больше, они могут иметь самое важное значение при попытках связать свойства почвы с ее характеристиками.
Проведен кластерный анализ нативных почв от домена до рода. Выявлено два основных домена – домен Bacteria и Archaea причем с явным преобладанием первого домена. Причем отмечается отсутствие или незначительное количество представителей домена Archaea в образцах почв чернозёма южного п. Щукино глубина отбора 10-20 см и пойменной каштановой почвы с поймы реки Урал города Уральска, глубина отбора 0-10 см, 10-20 см. Отсутствие представителей домена Archaea в пойменной каштановой почве вероятно объясняется кратковременным затоплением и как следствие заполнением свободных пор водой. Такие анаэробные условия для Archaea являются неблагоприятными. Способность организмов некоторое время переживать неблагоприятные внешние факторы, в данном случае несущественно. Выявлено 27 филумов с явно преобладающими филумумами Actinobacteria 23 – 38 % , Proteobacteria 9-48 %, а так же неатрибутируемые филы 13-32%, 63 класса из которых 15 неатрибутируемые, преобладающим атрибируемым классом является класс Actinobacteria. Доминирующим отрядом так же является Actinomycetales из класса Actinobacteria и неатрибируемый отряд домена Bacteria. Выявлено 215 семейств из них преобладают неатрибируемые 47 семейств бактерий с частотой распределения 13-32%, когда как других семейств менее 10% . При кластеризации по родовому распределению выявлено 474 рода из них 126 неатрибируемые, число распределения их по образцам почв варьирует 15-32 %, при этом других родов не более 5 % в образце. Отмечается явная тенденция увеличения неатрибируемых бактерий в образцах почв анализируя распределение бактерий от филумов до рода. Возможно, данные бактерии играют важную роль в оценке микробиома и его связи с агрохимическим состоянием почвы.
Проводимые работы выполнялись в целях реализации научно-исследовательского проекта «Использование методов современной метагеномики в оценке агроэкологического состояния почв Западного Казахстана» в рамках бюджетной программы 055 «Научная и/или научно-техническая деятельность», номер государственной регистрации - 0112РК00513
Литература
1. Brajesh, K. Singh, Soil genomics [Text] / Colin D. Campbell, Soren J. Sorenson et al. // Nature Reviews Microbiology – 2009. – V.7 – P. 756. – ISSN 1740-1526.
2. Gerlach, W. WebCARMA: a web application for the functional and taxonomic classification of unassembled metagenomic reads [Text] / S. Jьnemann, F. Tille // BMC Bioinformatics. – 2009. – V.10. – P.430. - ISSN 1471-2105.
3. Warnecke, F. Metagenomic and functional analysis of hindgut microbiota of a wood-feeding higher termite [Text] / P. Luginbьhl, N. Ivanova // Nature. – 2007. – V.450. – P. 560 – 565. – ISSN 0028-0836.
4. , , , , Использование методов современной метагеномики в оценке микробиоты почв Западно-Казахстанской области // Вестник КазНУ. Серия биологическая. – 2013. – № 1 (57). – С. 133-138.
5. Andronov E. E., Petrova S. N., Pinaev A. G., Pershina E. V., Rahimgalieva S. Zh., Ahmedenpv K. M., Gorobec A. V., Sergaliev N. H. Research the structure of microbial community in soils of different degrees of salinity using T-RFLP and Real-Time PCR// Eurasian soils. – 2012. - № 2. - P. 173-183.
6. , , Применение молекулярно-биологических методов при исследовании почвенно-микробиологических процессов // Наука и образование. – 2013. – № 1 (30). – С. 27-29.
, кандидат биологических наук, врио ректора Западно-Казахстанский аграрно-технический университет им. Жангир хана
, кандидат биологических наук, заведующий лаборатории микробиологического мониторинга и биоремедиации почв Всероссийского научно-исследовательского института сельскохозяйственной микробиологии
научный сотрудник лаборатории микробиологического мониторинга и биоремедиации почв Всероссийского научно-исследовательского института сельскохозяйственной микробиологии
, докторант PhD, научный сотрудник научно-исследовательского института биотехнологии и природопользования.
, магистр почвоведения и агрохимии, научный сотрудник научно-исследовательского института биотехнологии и природопользования
, магистр почвоведения и агрохимии, научный сотрудник научно-исследовательского института биотехнологии и природопользования
Турбаев Акылбек Жыксынгалиевич, магистр сельскохозяйственных наук, научный сотрудник научно-исследовательского института биотехнологии и природопользования
090009, г. Уральск, ул. Жангир хана 51, тел/
е-mail: *****@***ru




