Система контроля включает измерительные преобразователи (датчики) кислотности, температуры, мутности среды, отражающей размножение организмов.
В целом культиватор представляет собой автоматизированное устройство, управляемое по программе с учетом показаний датчиков. Объемы культиваторов могут быть различны – от сотен литров до полулитра.
Культиватор для бактерий иногда называют ферментером.
Выращивание микроводорослей осуществляется под лампами дневного света или в автоматизитрованных устройствах – люминостатах.
Лабораторное оборудование. В небольших количествах бактерии часто культивируют на чашках Петри с плоским стеклянным дном и с крышкой, предотвращающей попадание посторонних бактерий из воздуха. Инфузории можно культивировать в лабораторных условиях в чашках Петри, а также в пробирках или колбах.
2.2.4. Идентификация организмов
Убедиться, что получен нужный вид микроорганизма, весьма непросто. Выращенная популяция (группа особей) микроорганизмов напоминает мутную взвесь в объеме питательной среды или плесень на ее поверхности.
Существует целая группа методов идентификации видов:
- по форме колонии (учитываются цвет, форма, складчатость и др.); по потреблению добавляемых субстратов (анализируют, потребляет ли организм типичные для него виды углеводов, белков); по прорастанию на других средах (колонию пересевают на дифференциально-диагностические среды, на которых растут только известные виды); по устойчивости к известным антибиотикам; по окраске колонии стандартным методом, например по Граму (после окраски синим красителем и добавления затем этилового спирта грам-положительные бактерии сохраняют окраску, грам-отрицательные не сохраняют, что обусловлено разным составом их оболочек); по форме микроорганизмов под микроскопом: кокки – круглые или гроздевидные организмы, палочки–бациллы, бациллы со спорами (п.2.2.6), вибрионы – изогнутые палочки, спирохеты или спириллы – спиралеобразные; по характеру светорассеяния или поглощения излучения колониями (японскими учеными в начале 90-х гг. XX в. выявлена специфичность инфракрасных спектров многих бактерий); по другим физическим свойствам.
2.2.5. Коллекции организмов
Выявленные диагностические признаки позволяют сделать вывод о культивировании необходимого штамма. Так называется чистая культура микроорганизмов одного вида, у которого изучены морфологические и физические особенности. Штаммам присваивается идентификационный номер, они поддерживаются в коллекциях.
Коллекциями называются системы долговременного поддержания лабораторно выращенных организмов. Коллекции поддерживают в крупных НИИ микробиологического профиля, на микробиологических производствах и на биологических факультетах университетов.
Обычно из них берут и хорошо изученные организмы в целях разработки БСС. При описании экспериментов с БСС всегда должен быть указан источник, откуда взяты организмы.
2.2.6. Модификация организмов
Живые белковые объекты весьма трудно хранить или фиксировать на поверхностях. Поэтому многие организмы, полученные в чистом виде, затем подвергают модификации (п. 2.2.6) для перевода в новую более удобную жизнеспособную форму. Для этих целей разработана группа биотехнологических процессов.
Иммобилизация (обездвиживание). Это важнейший биотехнологический процесс, позволяющий защитить организмы от вымывания при воздействии жидкостей. Для иммобилизации микроорганизмов требуется или осадить их на поверхность, или встроить организмы внутрь каких-то малорастворимых веществ. Процедура должна быть технологичной, обеспечивать высокую адгезию (сцепление) и сохранять жизнеспособность организмов, доступ к ним субстратов и кислорода [22, 53].
Осаждение живых организмов чаще всего производят методом центрифугирования. В центрифугу под углом 30–40° закладываются закрытые пробирки, в которые заливается питательная среда с организмами, а на дно кладется пористый фильтр. Пробирки начинают вращаться с большой скоростью. В результате действия на вещество центробежных сил более плотные слои опускаются вниз, а менее плотные всплывают вверх. Мутная от бактерий или окрашенная в зеленый цвет от водорослей среда после центрифугирования становится прозрачной, а на фильтре образуется пленка из организмов.
В качестве физических веществ-носителей биообъектов часто используются желе, или иначе, гели (лат. “застывающие вещества”) биологического происхождения (агар, желатин, коллаген) или синтетические полимеры.
Микроорганизмы, включенные в гели, имеют меньшую чувствительность, чем осажденные на фильтровальных материалах, но для создания аналитических систем с высокой стабильностью и воспроизводимостью результатов предпочтение следует отдать методу включения в гели.
Лиофилизация. Это обезвоживание при низких температурах (от –40 до –60° С) и давлении, стимулирующих процессы испарения.
Лиофилизованные бактерии превращаются в порошкообразное вещество, которое затем можно хранить в обычном морозильнике. При добавлении порошка в питательный раствор жизнеспособность бактерий восстанавливается. Следует отметить, что не все виды живого могут быть подвергнуты лиофилизации. Необходимо подбирать режим изменения температуры и давления, чтобы внутри организмов не образовалось кристалликов льда, повреждающих живое.
В России применяются установки для лиофилизации типа “Иней”.
Криоконсервация [15]. Ряд форм организмов, например сперматозоиды крупного рогатого скота, сохраняет свою жизнеспособность при помещении в жидкий азот и последующем размораживании.
Спорообразование. Бактерии рода Bacillus, Clostridium образуют эндоспоры, находящиеся внутри клетки (п. 1.2.3). Это толстостенные долгоживущие образования, устойчивые к нагреванию и коротковолновому облучению. Споры бактерий можно держать в холодильнике или внутри порошков, например крахмала для B. subtilus. При внесении спор в питательную среду они прорастают и возобновляют процесс роста-размножения.
Инцистирование. Некоторые инфузории (например C. shteini) при неблагоприятных условиях укрываются в оболочках – цистах [8]. Для стимуляции инцистирования инфузории после выращивания подвергают охлаждению, а затем образовавшиеся цисты собирают и прикрепляют на носитель (например картон), на котором их можно хранить годами при комнатной температуре. При внесении цист в питательную среду из них появляются инфузории.
2.2.7. Понятие о генной инженерии
Принцип генной инженерии. Генетическая инженерия предназначена для получения вида организма с заданными свойствами, кодируемыми участками ДНК. Эти методы позволяют, например, “встроить” в бактерию ген, обусловливающий ее свечение, создать ДНК с заданной последовательностью нуклеотидов. Достижения генной инженерии связаны с изучением механизмов синтеза белка и передачи наследственной информации у бактерий E. coli.
Общие представления о передаче наследственной информации были приведены в п. 1.2.3. Основной механизм генетической инженерии осуществляется с помощью ферментов, катализирующих трансформацию ДНК. Он включает [12] следующие этапы:
1) в цитоплазме синтезируется матричная РНК (носитель информации о строении белков);
2) с помощью фермента (обратной транскриптазы) из мРНК в ядре клетки образуется чужеродная ДНК, которая несет информацию о синтезе нового белка. К концам этой ДНК могут прикрепляться нуклеотиды;
3) ДНК вируса или фрагмент ДНК (плазмида) (п. 1.2.3) “разрезается” ферментом рестриктазой и к ее концам прикрепляется чужеродная ДНК, которая закрепляется другим ферментом ДНК-лигазой;
4) вирус с чужеродной ДНК, попадая из среды в клетки бактерий, вызывает копирование своей ДНК с новым геном уже самими клетками бактерий.
Плазмида с чужеродной ДНК попадает из среды в цитоплазму бактерии и становится носителем новой генетической информации. За счет обмена участками с ДНК бактерий клетка получает новый ген, который встраивается в ее ДНК. Организм с новыми свойствами можно выращивать в ферментерах.
Существует предел получения массы белков обычными бактериями, которые гибнут после достижения определенного числа поколений. Этого предела числа поколений от одной клетки нет у раковых клеток. Скрещивая с ними организмы с новыми ДНК, можно получить неограниченную массу новых белков.
Синтез белка используют для получения нужных ферментов или для передачи клеткам бактерии гена выработки этих ферментов.
2.3. Организмы как биохимические преобразователи (БХП)
2.3.1. БПХ с подвижными организмами
Данный тип БХП [22, 53] позволяет:
- использовать множество этологических реакций организмов (п. 1.4) и реакции роста-размножения (п. 1.5), которые отражают интегральное влияние многих факторов внешней среды на живое; наиболее дешево и долговременно поддерживать жизнеспособность БХП; применять в качестве БХП организмы, полученные методами генной инженерии (п. 2.2.7), что позволяет получать их с новыми, детерминированными свойствами.
Недостатком данного типа БХП является трудность оценки влияния на них отдельных веществ в биологических или природных средах.
Для применения организмов в качестве БХП необходимо выбрать количественно измеряемую характеристику их реакции, изменяющуюся при воздействии анализируемых веществ.
Рост-размножение как БХП. Существует несколько разновидностей тест-реакций данного БХП.
а) Прирост популяции. Для оценки тест-реакций размножения наиболее удобно использовать характеристики процессов деления одноклеточных организмов. Потребление ими субстрата S приводит к росту популяции, который обычно описывается нелинейной кривой [5].
На ней выделяют следующие участки (рис.1):
- лаг-фазу – стадию, когда организмы еще не приспособились к среде; лог-фазу – экспоненциальный прирост концентрации С организмов
![]()
(13)
где m – удельная скорость роста;
- фазу насыщения, когда сказывается влияние лимитирующих факторов среды, например выделение продуктов метаболизма в среду; фазу деградации – преобладание гибели над рождаемостью.
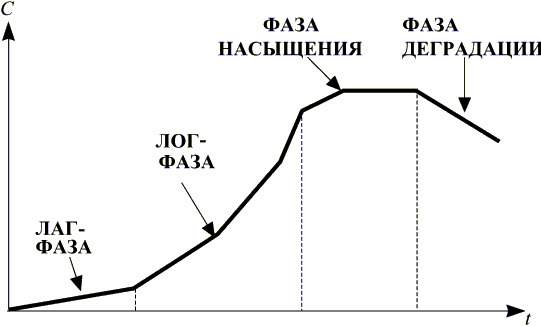
Рис. 1. Кривая роста - размножение одноклеточных организмов ( С - концетрация, t - время ) [5]
При размножении микроорганизмов на жидких питательных средах увеличивается мутность сред (п. 2.2.2). Степень мутности оценивается либо визуально (уменьшение, сохранение прежней мутности, увеличение) в баллах, либо методами оптического контроля (п. 3.1).
Микробиологические методы анализа в данном случае часто оказываются более информативными, чем химические, так как позволяют определять не валовое содержание элементов, а их физиологически активные формы. Продолжительность анализа с использованием быстро растущих культур составляет не менее 3,5...4 ч [53].
БХП этого типа используют для выявления вредных веществ. По различию характеристик прироста в опыте и контроле (п. 2.1) определяют предельную концентрацию вещества, обнаруживаемую организмами ( рис. 2.). Для оценки токсичности в питательные среды с микроорганизмами вводят не только растворы исследуемых химических веществ, но и экстракты, извлекаемые с помощью растворителей из тканей, почв и т. п.
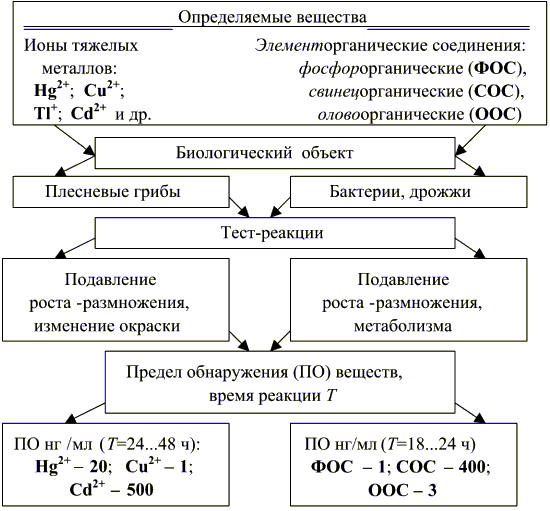
Рис. 2. Характеристики БХП с микроорганизмами [53]
Обнаружены виды инфузорий, позволяющие определять относительную пищевую ценность белков – ОПЦ (п. 1.1.2). Если белок, которым питается инфузория T. Pyriformis, содержит полный набор аминокислот, она растет быстро, если хотя бы одной аминокислоты не хватает, то ее рост замедляется. В некоторых случаях для этой цели применяют цистообразующие инфузории С. shteini [8].
б) Зоны подавления. Бактериальные клетки, растущие на агаризованных средах (п. 2.2.2), образуют хорошо различимые колонии (по виду похожие на пятна плесени). Если в питательный агар, на котором выросли колонии, добавляют антибиотик, токсикант или, наоборот, биологический стимулятор, то возникает зона подавления роста или стимуляции роста (уменьшение или расширение колонии). Диаметр этих зон является линейной функцией концентрации определяемых веществ в некотором ее интервале [53].
При постоянном составе среды, оптимальных для данного организма рН и температуре величина зон зависит от толщины питательного слоя: чем тоньше слой, тем больше зона.
Таким способом по изменению формы и размеров пятен плесени, образованных грибками рода Aspergillus, на агаре, в который добавлен токсикант, выявляют малые концентрации нитратов ртути (II), кадмия, таллия.
в) Химические свойства питательной среды. При размножении в водной среде дрожжи или микроскопические грибы в процессе дыхания выделяют газы, которые изменяют кислотность питательной среды.
Это свойство БХП используется в БСС для оценки токсичности воды и почвы. После помещения сухих дрожжей (Sacharomyces cerevisae) в пробу воды защелачивание пробы указывает на отсутствие в ней токсикантов [39]. При взаимодействии питательной среды с токсикантом возникает ее закисление, что выявляется в результате измерения рН (п. 3.2.4).
В НПО «Питательные среды» для обнаружения антибиотиков в моче разработана тест-система, которая с помощью цветового рН-индикатора обнаруживает изменение кислотности мочи, возникающее при размножении в ней бактерий B. subtillus. В качестве питательной среды иcпользуется дыхательный субстрат (глюкоза). Данные бактерии могут быть сохранены также в виде спор (п. 2.3.2). В табл. 4 указаны характеристики БХП на основе субстратов и организмов, выделяющих газы, изменяющие pH водной среды.
Таблица 4
Характеристики бактериальных БХП [3]
Субстрат | БО | Газ | Раствор |
Углеводы | Организмы-аэробы | CO2 | H2CO3 |
Белки, соединения азота | Бактерии-денитрификаторы | NH3 | NH4OH |
Сульфаты | Анаэробные серобактерии | H2S | H2S |
Этологические реакции организмов как БХП (п. 1.4). Можно выделить БХП данного типа с несколькими тест-реакциями.
а) Таксисы. Для возникновения таксисов необходимо в среде создать градиент (неоднородность распределения) химического вещества, чтобы организм мог выбрать направление уменьшения вредного воздействия.
Существуют различные методы создания градиента:
- применение камеры, разделенной на две части мембраной (камера Бойдена для организации таксиса лейкоцитов); нанесение капли отпугивающего вещества на студенистую среду (п. 2.2.2), на которой растет колония микроорганизмов; вещество будет медленно диффундировать, а бактерии уходить из этой зоны, образуя кольцо (метод используемый для контроля активности антибиотиков). Эта реакция была обнаружена в XIX в. Бейеринком, но стала исследоваться с 1970-х гг.;
- погружение капилляра с микроорганизмами в жидкость с тестируемым веществом и, наоборот, – капилляра с веществом в среду с микроорганизмами (используется для оценки качества пресной и морской воды) [55]; контакт веществ с различными вязкостями [17, 29], которые можно либо наслаивать сверху, либо вносить шприцем под слой другого вещества (используется для оценки токсичности водных сред и активности антибиотиков, рис. 3, 4).
Характеристиками таксиса могут быть концентрация организмов через определенное время, которая измеряется оптическими приборами (пп. 3.1.4, 3.1.7), параметры распределения концентрации по длине кюветы.
Среди перспективных организмов для БХП на основе таксисов можно назвать водоросль – ряску. Она реагирует на химические вещества сразу за счет нескольких биологических механизмов: как изменения цвета фотосинтетических пигментов (пп. 1.2.1, 2.5.4), так и фототаксиса листьецов (маленьких листочков) – их схождения или расхождения на поверхности воды. Это позволяет не только обнаруживать вредные вещества, но и дифференцировать их по механизмам воздействия на живое.
б) Кинезы. Скорость движения инфузорий повышается при введении в среду их обитания микроколичеств этанола, сахарозы, фурфурола, альдегидов, уксусной кислоты, хлоридов кальция и аммония; при добавлении хлорида бария движение клеток, наоборот, замедляется. Подвижность сперматозоидов крупного рогатого скота замедляется в вытяжке полимеров, если в их составе находятся вредные вещества [15].
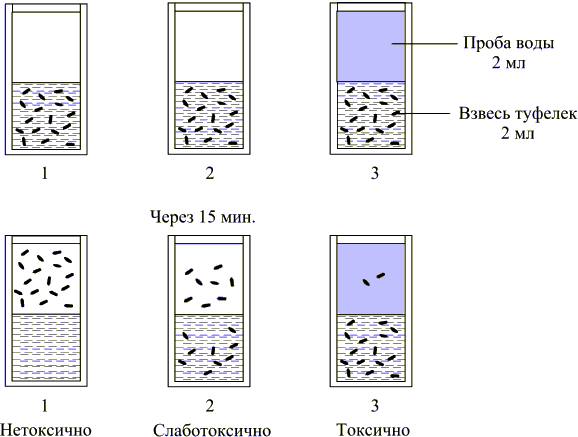
Рис. 3. Хемотаксис инфузорий туфелек [17]
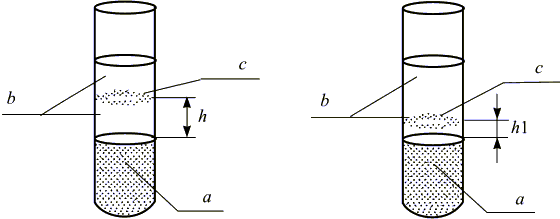
Рис. 4. Хемотаксис бактерий,
где a - МПБ, содержащий культуру Bacillus subtilis;
b - исследуемая проба: с - кольцо бактерий;
h - высота подъема кольца бактерий в контроле и h1 в пробе с токсикантом
Для описания тест-реакций кинезов организмов в их движении выделяют прямолинейные перемещения и «дрожание», т. е. колебания в пределах некоторой ограниченной зоны. В зависимости от типа движений выбирается метод измерения (пп. 3.1.7, 3.1.8).
в) Движения органов. При оценке чистоты воды в качестве тест-реакции используют некоторые физиологические показатели дафний, например, частоту сердечных сокращений, движения их ножек. При добавлении токсиканта сначала наблюдается общее возбуждение, переходящее в депрессию, а затем в результате нарушения деятельности органов движения, дыхания, кровеносной и нервной систем наступают потеря подвижности и летальный исход. Частоту как переменный сигнал удобно контролировать, например, фотометрическим методом (п. 3.1).
г) Локомоции. В качестве тест-реакции могут использоваться локомоции (п. 1.4.1) микроскопических червей – нематод. В разбавленных растворах токсикантов они быстро изгибаются то в одну, то в другую сторону, совершая как бы S-образные движения. С повышением концентрации движения становятся вялыми, замедляются [53].
Локомоции насекомых (например, жуков, комаров), описываемые скоростью и траекторией ходьбы или полета, изменяются при воздействии малых концентраций ядохимикатов или наркотических веществ и, следовательно, могут быть использованы в качестве тест-реакции.
2.3.2. БХП с модифицированными организмами
Особенность БХП на основе иммобилизованных организмов (п. 2.2.6) состоит в том, что они, помещенные в гель или в пористый материал, часто находятся в состоянии субстратного голода.
В этом случае для уменьшения потребления энергии в клетках снижается уровень обмена веществ, а основным путем воздействия стимула является его диффузия из внешней среды через стенки клеток и их последующее ферментное преобразование. Поэтому реакция БХП на основе иммобилизованных организмов более медленная, чем у подвижных клеток в питательной среде [22].
Чувствительность иммобилизованных микроорганизмов понижена и проявляется или к жизненно необходимым веществам, поддерживающим энергетику клетки, каталитическое разложение которых требует минимума энергии, или к токсичным веществам, вызывающим гибель организмов.
Основными тест-реакциями БХП являются метаболические, т. е. организм становится живым биокатализатором для преобразования субстрата в продукт ферментативных реакций. Поэтому иммобилизованные организмы часто используются в виде ферментного преобразователя с увеличенным сроком действия за счет того, что организмы сохраняют жизнеспособность дольше, чем ферменты. В прил 3. приведены продукты ферментативных реакций, выделяемые клетками.
Способность лиофилизованных клеток достаточно быстро восстанавливать жизнеспоособность и проявлять реакции метаболизма используется в методике «Микротокс» (Microtox) для оценки загрязнений окружающей среды по люминесценции бактерий (п. 2.5.1).
На биотехнологических предприятиях культивируют штаммы светящихся бактерий, которые затем модифицируют в порошковую лиофилизованную форму. Полученный бактериальный порошок хранят в морозильнике. При анализе этот порошок добавляют в питательную среду. Для БХП необходимо обеспечить два температурных режима: один для восстановления жизнеспособности бактерий, другой для протекания люминесцентной тест-реакции [16,18].
Полученные методом криоконсервации БО применяют в БСС «Биотехническая система для измерения индекса токсичности вытяжек полимеров» по изменениям кинезов сперматозоидов крупного рогатого скота (п. 2.2.5). Отбор БО осуществляется из банков станций осеменения, где они хранятся в жидком азоте. После размораживания двигательная активность сперматозоидов восстанавливается. Их дозируют, выдерживают в среде с вытяжкой из полимеров, а затем измеряют показатели скорости БО (п. 3.1.8).
При использовании данного вида модификации БО следует учитывать, что хотя наибольшая их часть остается жизнеспособной, небольшая часть их может погибнуть. Это обусловливает необходимость различения движения живых БО от движения мертвых, переносимых в вытяжке конвекционными потоками.
Споры бацилл применяют в БСС – бактериальных тест-системах для выявления антибиотиков (п. 2.3.1).
Цисты используют в БСС для оценки качества кормового белка (п. 2.3.1). Важным преимуществом инцистирования инфузорий является то, что они покидают свои цисты на одной и той же стадии развития, что улучшает воспроизводимость результатов эксперимента [8].
2.4. Методы подготовки структур организмов
2.4.1. Выделение веществ из тканей и клеток
Чтобы выделить необходимые вещества из тканей и клеток, необходимо разрушить их оболочки, в результате чего образуется смесь из макромолекул и органелл. При этом требуется сохранить жизнеспособность биологических объектов [5].
Культивирование тканей. В подразд. 2.2 были рассмотрены проблемы культивирования микроорганизмов. Ткани также выращиваются в специальных питательных средах, но их жизнеспособность труднее поддерживать искусственно.
Некоторые клетки ткани, например лейкоциты периферической крови, приобретают способность к делению и созданию клона вне организма при добавлении в питательную среду белково-полисахаридного препарата ФГА.
Этот метод культивирования применяется для исследования хромосом.
Гомогенизация (с греч. «однородный»). Это метод образования однородного вещества из тканей и клеток. В простейшем виде процесс представляет собой механическое растирание клеток. Применяется также ультразвуковое разрушение оболочек клеток.
Для успешного выделения ферментов из клеточного содержимого необходимо очень тонкое измельчение исходного материала, вплоть до разрушения субклеточных структур: митохондрий (п. 1.2.2), ядер и др., которые содержат в своем составе многие ферменты. Особое внимание при выделении ферментов уделяют проведению всех операций в условиях, исключающих денатурацию белка, так как она всегда связана с потерей ферментативной активности. Этому способствует проведение операций в присутствии защитных добавок и при температуре много ниже температуры денатурации (п. 1.1.2).
Осмотическое разрушение. Создается методом изменения осмотического давления, которое возникает при диффузии солевого раствора через полупроницаемые мембраны клетки. Если давление внутри клетки больше чем снаружи (концентрация соли во внешней среде меньше, чем во внутренней), она распухает и взрывается, если наоборот – сдавливается.
2.4.2. Очистка веществ
Процедура очистки включает разделение веществ (РВ) на фракции. Эти методы необходимы для получения субклеточных структур, белков, нуклеиновых кислот. Из смеси ферментов или белков требуется оставить только один. Задача выделения чистых белков одна из самых сложных. Для ее решения применяется целая группа методов РВ.
РВ по растворимости. Процесс частичного разделения вещества с помощью растворителя, в котором по-разному растворимы различные составляющие вещества, называется экстракцией. Широко распространен метод РВ экстракцией глицерином или спиртами, при котором сохраняются нативные, т. е. природные свойства ферментов.
РВ по устойчивости к рН и температуре. Смесь доводят до уровней pH и температур, при которых одни органеллы и макромолекулы разлагаются, а другие сохраняют жизнеспособность. Особенно удобно с этой точки зрения выделять из смеси белков структуры термофильных бактерий (п. 1.1.2), которые не коагулируют при температуре выше обычной. Это позволяет после нагрева до температуры 50…55 °C легко выделить белки только данных организмов.
РВ по плотности. Метод основан на центрифугировании (п. 2.2.6) клеточных структур.
Например, для разделения нуклеиновых кислот в их смесь добавляется хлористый цезий, создающий при центрифугировании распределение плотности по высоте. После окончания центрифугирования нуклеиновые кислоты в зависимости от плотности образуют слои в пробирке, всплывшие на разную высоту. Освещая пробирку ультрафиолетом, различные нуклеиновые кислоты выявляют за счет полосы поглощения их азотистых оснований (п. 2.5.5).
РВ по заряду. Белки обладают зарядом (п. 1.1.2), величина и знак которого меняются в зависимости от кислотности среды. Этот эффект лежит в основе электрофореза – разделения белков по знаку заряда при приложении высокого постоянного напряжения к среде с известным рН, содержащей белки. В этом случае разноименно заряженные белки движутся к разным электрическим полюсам.
РВ по размерам молекул. При пропускании веществ через ультрафильтры с размерами пор в десятки (сотни) мкм задерживаются более крупные, а проходят менее крупные молекулы белков.
РВ по подвижности компонентов. На данном принципе основан метод хроматографии. В первых хроматографах, разработанных , жидкое вещество пропускалось сверху вниз через длинную трубку (колонку), заполненную пористым сорбирующим веществом. Более подвижные компоненты из смеси проходили вниз, а менее подвижные оставались наверху. В качестве пористого вещества часто используют волокнистую бумагу или целлюлозу. Для выделения сорбированных белков их затем вымывают из пористого материала веществом-растворителем (элюэнтом), не повреждающим живое
РВ по видам ионов. Иногда в качестве хроматографического сорбента применяют ионообменные смолы, которые позволяют задерживать вещества с определенными ионами.
РВ белков по сродству с антигенами или антителами. Для очистки и стандартизации антител используется аффинная (с греч. «сродство») хроматография [5, 32]. Она основана на свойстве связывания антител антигенами (пп. 1.2.4, 2.5.6).
Антитела – это белки иммуноглобулины, вырабатывающиеся организмом в ответ на иммунизацию организма – введение антигена (вирусов, чужеродных бактерий) в кровь, мышцу лабораторных животных, птиц. Антитела появляются не только в крови у животных, но и в желтках яиц, снесенных иммунизированными птицами.
Иммунный ответ на введение одного антигена сопровождается синтезом антител, различающихся по структуре и функциям. Это иммуноглобулины (Ig) пяти классов (G, D, E, A, M), которые связывают различное число молекул антигена. У молекулы или бактерии существуют отдельные участки (антигенные детерминанты), которые и вызывают образование антител.
Принцип аффинной хроматографии состоит в том, что смесь белков, например, капля крови иммунизированного животного, в которой находятся белки-иммуноглобулины (антитела) пропускается через колонку с полисахаридными шариками, к которым прикреплены определенные антигены (п. 1.2.4). Они связывают из всех белков только специфические антитела, т. е. иммуноглобулины, которые имеют наибольшее сродство к данным антигенам. Связанные антитела затем вымывают из колонки кислым или щелочным раствором. Один цикл аффинной хроматографии позволяет очистить белки в 1000 раз и более (выделить 1 вид белка из 1000).
Для расширения круга объектов аффинной хроматографии было изучено, какие объекты могут являться антигенами. Оказалось, что антигенами могут быть клетки микроорганизмов, вирусы, белки, полисахариды. Они называются полноценными, так как вызывают выработку антител сами по себе. Были открыты неполноценные антигены (гаптены), которые сами не вызывают появления антител, но если их осадить на белок или биополимеры, то они становятся иммуногенными. Таким способом получают антитела к антибиотикам, витаминам, гормонам, лекарственным препаратам. Для выделения подобных антител их пропускают через колонку с гаптенами, осажденными на гормонах и других веществах, превращенных в антигены.
Нуклеиновые кислоты не вызывают появления антител, однако антитела к ним синтезируются, если они находятся в комплексе с белками. Антигенными детерминантами нуклеиновых кислот являются их участки – три - и тетрануклеотиды.
Возможно, наоборот, осадить на сорбенте колонки антитела и выделять антибиотики, гормоны, комплексы белков с нуклеотидами и др. антигены.
Биотехнологические методы очистки органических веществ постоянно обновляются и модернизируются.
2.4.3. Модификация
Наиболее распространенный способ модификации субклеточных структур и веществ – иммобилизация (п. 2.2.6).
Для защиты от вымывания часто применяют химические методы иммобилизации БО, основанные на их «пришивании» к поверхности химическими связями. Подобными методами производят иммобилизацию ферментов, антигенов или антител. Немодифицированные субклеточные структуры в биотехнологии используются крайне редко.
2.5. Биологические вещества и структуры, применяющиеся для биохимических преобразователей
2.5.1. Ферменты
Несмотря на всю сложность получения ферментов и малый выход очищенного ферментного белка (доли миллиграммов на грамм исходной биомассы – менее 0,1%) они остаются наиболее распространенными БО для БХП, так как позволяют решать аналитические задачи выделения веществ из смеси и определение их концентрации в различных средах, тканях и органах живого. При этом следует учесть, что выделенный чистый фермент работает иначе, чем в клетке, где он образует комплексы с ее структурами. Поэтому его действие вне клетки не может полностью моделировать метаболизм организма (п. 1.1.3).
Другое применение выделенных ферментов заключается в том, что они образуют элементы алгоритма синтеза новых белков, реализуя набор операций по их сборке и расчленению.
Ученые 70-х гг. XX в. относились к ферментам как к капризным, быстро разлагающимся веществам, меняющим свою активность во времени. Позже чистые ферменты стали хранить в глицерине и в смеси с белком альбумином, что увеличило продолжительность их активности. Методы иммобилизации (пп. 2.2.6, 2.4.3) позволили существенно повысить устойчивость ферментов. Поэтому всемирный рынок ферментов уже в 1993 г. оценивался в сумму свыше $990 млн.
В прил. 2 приведена таблица, где указаны области применения ферментов сегодня – от заквасок для молока и пива или осветлителей для соков до моющих средств, в которых они выступают в качестве биодобавок.
Чувствительность и воспроизводимость реакции БХП зависит в основном от качества гомогенизации клеток, выделения и очистки фермента (п. 2.4.2), т. е. от инфраструктуры, которая должна обеспечивать работу БХП. Разработчик БСС при этом полагается на поставщиков ферментов.
Ферменты можно наносить в виде простейшего БХП на бумагу, вносить в состав мембран на гелевой или иной основе или применять в виде экстрактов [22, 46].
Применение ферментов в качестве аналитического инструмента предполагает организацию метаболических реакций и измерение количества субстрата или продукта. Можно выделить целую группу тест-реакций ферментных БХП.
Преобразование химических веществ. В БСС для оценки загрязнения окружающей среды определяется активность ферментов дыхательного цикла аэробного дыхания (цикла Кребса, п. 1.2.2):
янтарная кислота + F ––––® фумаровая кислота + F,
(14)
где F – фермент сукцинатдегидрогеназа, выделяемый из митохондрий печени рыб. Янтарная кислота в свою очередь образует с индикатором окрашенное соединение (п. 3.1), что позволяет измерить потребление субстрата ферментативной реакции.
Активность липаз, катализирующих разложение жиров, часто определяют с помощью простого теста, заключающегося во внесении фермента в каплю оливкового масла и измерении скорости растекания капли за счет расщепления жиров.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |




