Биопотенциал нервной ткани (п. 1.3.1), измеряемой с помощью микроэлектрода, позволяет индицировать воздействие на нее кислот, щелочей, некоторых тяжелых металлов, фармакологических препаратов. По усилению либо угнетению биоэлектрической активности нерва лягушки можно оценивать содержание хлорида марганца. Высокой чувствительностью к микроэлементам обладают мозговые сосуды. На основе метода измерения биоэлектрической импульсной активности антеннул (рецепторов) краба были созданы БХП для обнаружения 20 аминокислот.
БХП для выделения веществ из смесей. Существенно, что с помощью тканевых БХП возможно выделять вещество из смесей. БХП на основе тканей корней хрена позволяет по разложению H2O2 определять концентрацию перекисей не только в водных растворах, но и в органических растворителях. Аскорбиновую кислоту с помощью тканей растений можно определять в смесях органических кислот, фенолов, аминокислот и глюкозы.
К недостаткам тканевых биосенсоров следует отнести трудность стандартизации БО, что ухудшает воспроизводимость результатов анализа.
Активированная хемолюминесценция. Хемолюминесценцией называется свечение, сопровождающее некоторые биохимические реакции. Клетки и ткани животных обычно излучают свет в процессе жизнедеятельности, но такой слабый, что его долгое время не удавалось обнаружить. Эффект активированной хемолюминесценции (АХЛ) заключется в тысячекратном усилении свечения в присутствии некоторых веществ-активаторов – физических факторов и химических веществ (п. 3.1.9).
Некоторые вещества-активаторы (кумарин и его соединения) усиливают хемолюминисценцию, возникающую при окислении липидов (п. 1.1.2), при котором образуются возбужденные молекулы. Активатор свечения люминол усиливает свечение тканей в присутствии атомарного кислорода и радикалов OH–. Поэтому диагностика с применением АХЛ связана с реакциями, приводящими к их образованию.
Атомарный кислород возникает при разложении пероксида водорода (H2O2 = H2O + O) в присутствии металлов переменной валентности и гемсодержащих (железосодержащих) веществ. В отличие от O2 атомарный кислород обладает значительно большей химической активностью.
У больных инфарктом миокарда в моче могут появляться небольшие концентрации гемсодрежащего белка – миоглобина, которые усиливают свечение люминола в присутствии Н2О2 . Активные формы кислорода возникают при заживлении ран (п. 1.2.4), что позволяет контролировать эти процессы по проявлению эффекта АХЛ. Клетки крови выделяют активные формы кислорода при действии кратковременных электрических импульсов или при добавлении к лейкоцитам суспензии бактерий, которые они воспринимают как чужеродных агентов. Такой же эффект возникает при добавлении к клеткам крови кристаллов кварца, сульфата бария и других химических веществ, получивших название стимулов АХЛ. Способность клеток крови вырабатывать активные формы кислорода отражает общую сопротивляемость организма.
2.5.3. Фотосинтезирующие пигменты
В тканях организмов-фотоавтотрофов (п. 1.2.1) содержатся пигменты, поглощающие солнечное излучение и преобразующие его в химическую энергию. Фотосинтезирующие пигменты делятся на две группы – хлорофиллы и каротиноиды. Они различаются по строению и оптическим свойствам.
В БСС используются фотосинтетические пигменты, включенные в ткань листа, а также находящиеся во взвеси микроводорослей, в осажденном после центрифугирования слое водорослей, в гомогенате (измельченной ткани) листьев.
Можно выделить несколько тест-реакций пигментов.
а) Поглощение. Хлорофиллы поглощают главным образом красный и сине-фиолетовый свет, отражая зеленый свет, что придает растениям зеленую окраску (рис. 5). При загрязнении среды хлорофиллы распадаются первыми, при этом возникает явление хлороза – пожелтение части растительной ткани.
Каротиноиды – желтые, оранжевые, красные и коричневые пигменты. Они имеют три максимума поглощения в сине-фиолетовой области спектра (рис. 5,а). Каротиноиды обычно не видны на фоне хлорофиллов, но обнаруживаются при их распаде. При полном подавлении фотосинтеза вредными веществами возникает явление некроза (отмирания ткани растений).
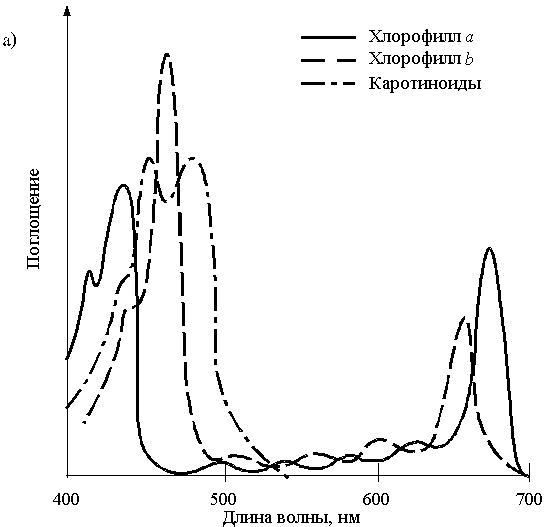
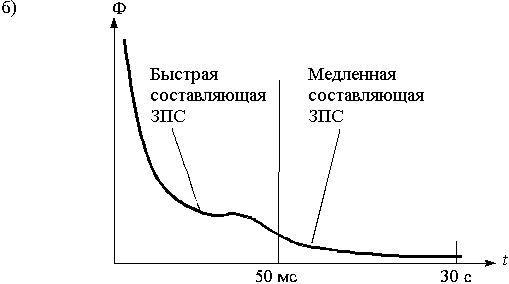
Рис. 5. а) спектры поглощения хлорофиллов a и b и каротиноимдов
б) кривая замедленного послесвечения (ЗПС) хлорофилла - a
б) Поглощение и рассеяние возникают за счет того, что пигменты включены в состав хлоропластов, образующих рассеивающие и поглощающие частицы ткани листа.
в) Флуоресценция. Пигменты характеризуются спектром возбуждения – зависимостью интенсивности флуоресценции (кратковременной люминесценции) пигментов от длины волны в результате их возбуждения источниками излучения [43].
Например, при освещении хлорофиллов кратковременным, мощным импульсом сине-фиолетовых длин волн возникает эффект испускания пигментами излучения красных длин волн. Интенсивность свечения за время, много меньшее мс, достигает пика, затем быстро (за десятки мс) уменьшается в тысячи раз, после этого медленно спадает до нуля в течение нескольких секунд (рис. 5,б). Вещества, подавляющие фотосинтез (п. 1.2.1), уменьшают амплитуду быстрой составляющей послесвечения.
Измерение спектров поглощения и послесвечения позволяет определять концентрацию пигментов для оценки степени загрязнения среды.
Спектр поглощения гомогената листьев или взвеси водорослей измеряют с помощью спектрофотометра (п. 3.1.3). Поверхность ткани с поглощающими частицами пигментов анализируется методами измерения отраженного потока (п. 3.1.5). Послесвечение пигментов обычно исследуют путем нанесения однородного слоя носителей пигментов на поверхность вещества, не обладающего свойством люминесценции (3.1.9).
2.5.4. Носители генетической информации
Свойства хромосом, используемые в БХП. Согласно международной классификации хромосом человека они нумеруются попарно по мере уменьшения их длины от 1 до 22-й. Их классифицируют по морфологическим признакам: форме, величине, положению связки (центромеры) и по расположению локусов, окрашенных разными видами красителей, в том числе флуоресцентными.
При рассмотрении структурной изменчивости хромосом под действием вредных факторов выделяют три основных вида нарушений: разрывы хромосом, ведущие к образованию фрагментов (делеций), перестановки локусов внутри хромосом и обмен локусами между разными хромосомами. Последние два вида перестройки хромосом называются аберрациями.
Исследование делеций и аберраций хромосом широко используется для оценки мутагенности загрязнений окружающей среды, воздействующих на живое в течение времени, за которое сменилось несколько десятков поколений клеток у животных или растений.
Клетки лейкоцитов возможно получать лабораторным методом (п. 2.4.1), поэтому в 1971 г. Международная организация здравоохранения при ЮНЕСКО рекомендовала для анализа мутагенных эффектов загрязнителей (в том числе сельскохозяйственных ядов) метод изучения структурных мутаций хромосом с помощью клонов лейкоцитов.
Свойства ДНК, применяемые в БХП [3, 13]. Двойная цепь нуклеотидов, не свернутая в трехмерную структуру, позволяет наблюдать и контролировать следующие тест-реакции:
- поляризацию света оптически активным веществом ДНК; поглощение излучения в ультрафиолетовой области за счет азотистых оснований ДНК (хромофор, п. 1.2.3); поглощение излучения в других областях спектра при взаимодейсвии с различными химическими веществами, которые присоединяются к ДНК всегда в фиксированном месте цепи, при этом поглощение будет пропорционально концентрации вещества; комплементарность, т. е. объединение цепей нуклеотидов ДНК; удлинение и укорочение цепи ДНК при воздействии некоторых ферментов мутагенных веществ; образование множеством молекул ДНК структуры жидкого кристалла (п. 3.1.10).
Гибридизация, ДНК-зонды. Новая ДНК может возникать в результате обмена фрагментами ДНК или их соединения. Этот процесс называется гибридизацией ДНК. Для выявления наследственных болезней используют ДНК-зонды, т. е. ДНК, копирующие участки генов. Их получают из мРНК (п. 2.2.7). Необходимые фрагменты помечают изотопом. Если болезнь обусловлена отсутствием гена, то эффект гибридизации ДНК пациента с ДНК-зондом понижается, т. е. не возникает эффекта его прикрепления. Так диагносцируют наследственные мутации (отсутствие необходимых участков генов).
Из цепочек нуклеотидов путем ферментных перестроек возможно создавать геномные последовательности для диагностических и терапевтических целей [11, 40].
Например, разработана искусственная нуклеиновая кислота (НК), соответствующая области генома вируса гепатита С [11]. Искусственную НК помещают в условия, способствующие ее скрещиванию (гибридизации) с геномом вируса гепатита С. Обнаружение продукта гибридизации является показателем наличия генотипа вируса гепатита С. Это способ создания вакцины и антител против вируса гепатита С.
2.5.5. Комплекс антиген-антитело
Свойства комплекса антиген-антитело. Образование комплекса антиген-антитело в процессе преципитации (пп. 1.2.4, 2.4.2) изменяет физико-химические свойства исходных белковых молекул.
При формировании БХП можно использовать следующие тест-реакции [32, 33] комплекса антиген-антитело:
- образование крупных клеточных агрегатов, если антиген расположен на поверхности клеток (антитела «склеивают» клетки, и они оседают на дно); образование отчетливых линий в густеющем геле (п. 2.2.6) с клетками-антитигенами после того, как туда добавляют антитела за счет возникновения клеточных агрегатов; увеличение силы тяжести, действующей на поверхность, если на ней иммобилизованы антитела, а клетки с антигенами находятся в питательной среде (образование комплекса приводит к выпадению осадка), что используется в гравиметрических датчиках (п. 3.3); изменение электрических свойств (емкости) антигена и антитела при образовании комплекса, суммарная емкость которого уменьшается за счет последовательного соединения емкостей исходных биообъектов (п. 3.2.1); изменение оптических и электрических характеристик приповерхностного слоя электрических проводников при осаждении на них комплекса (п. 3.1.6).
Воздействие комплекса антиген-антитело на нервные клетки. Подобный комплекс может воздействовать на проводимость нервных клеток (п. 1.3.1). Если рецепторный белок (G-белок, п. 1.3.2) нервной клетки является антигеном для антител, то его связывание в комплекс приводит к возникновению электрофизиологических эффектов: уменьшению потенциала действия и изменению его полярности.
Перспективным направлением является создание БХП с использованием мембран нервных клеток, в которые встроены антитела. Тогда образование комплекса антиген-антитело изменяет электрический потенциал мембраны.
2.5.6. Комплекс антиген–антитело–фермент
В иммуно-ферментном анализе (ИФА) [21, 32] реакция фермента с субстратом используется в качестве индикатора наличия антител к определенным антигенам (пп. 1.2.4, 2.5.5). Реакцию субстрат-фермент используют для обнаружения комплексов антиген-антитело вместо прежнего, радиоактивного метода, при котором антитела метили изотопами.
Гетерогенный ИФА. Данный анализ включает подготовку веществ и материалов и проведение собственно анализа.
Подготовительные этапы ИФА:
1) культивирование, очистка (п. 2.4.2) антигена Aг, например вирусного белка, который должен иметь сродство не менее чем к двум классам антител;
2) иммобилизация антигена (обычно химическим путем, (п. 2.4.3) на дно и стенки прозрачной ячейки Аг;
3) культивирование, очистка антител (Аг) – Aт;
4) культивирование носителей ферментов, выделение из них ферментов и очистка (получение энзимов E);
5) прикрепление к анителам фермента-энзима в качестве метки (Ат+ E).
Для реализации последнего этапа необходимо подобрать фермент, который длительно сохраняет свою активность, не теряет ее при связывании с анителом (или антигеном), обладает высокой избирательностью к субстрату, катализирует реакцию с изменением цвета субстрата.
Например: пероксидаза хрена (F) катализирует реакцию:
AH2 + H2O2 + F ——® A + H2O + F
(24)
В качестве AH2 подбирается соединение, которое в пероксидазной реакции превращается в окрашенную форму с максимумом оптического поглощения при длине волны 414 нм.
«Прикрепление» фермента к антителу осуществляется разными способами:
- разъединением белковых антител ферментами нуклеазами (катализирующими разложение молекул белка на компоненты) и соединением реакционно-способных частей антител с ферментом; связыванием антитела с промежуточным ферментным белком Ат–Б, а основного фермента – с его ингибитором ИБ –E (п. 2.5.1), в результате чего ингибитор соединяет цепь Ат–Б ИБ –E = Ат + E; методами генной инженерии (п. 2.2.7).
На подготовительных этапах создают диагностикумы – наборы иммунохимических реагентов для определения антигенов (или антител) и полистироловые многолуночные планшеты, на которые нанесены антигены определенных вирусных или инфекционных заболеваний.
Этапы выполнения гетерогенного ИФА:
1) взятие у пациента пробы крови для анализа на наличие антител
(АтП);
2) одновременное добавление в ячейку планшета с иммобилизованными на ее поверхности антигенами раствора «меченых» антител и пробы крови пациента;
3) связывание антигенов с антителами «мечеными» энзимами
(Аг +Ат+ Е)
или антителами из пробы крови пациента
(Аг+ АтП);
4) отмывание ячейки от крови;
5) образование в ячейке прикрепленного к поверхности комплекса антиген-антитело, меченого энзимом* (при связывании антигенов с антителами растворов диагностикума)
*(Аг + Ат + Е)
и не меченого° (при связывании антигенов с антителами пробы),
°(Аг+ АтП)
и добавление в ячейку субстрата (S) ферментативной реакции:
*(Аг + Ат + Е) + S = *(Аг + Ат + P) + E,
(25)
°(Аг+ АтП) + S;
6) образование продукта ферментативной реакции, который полностью заполняет дно ячейки, если в пробе не было антител
P P P P P P P P P P
или не полностью, если антитела в пробе крови были
P P P P P P P;
7) отмывание ячейки от субстрата, антител и антигенов, фиксация слоя продукта на дне ячейки в виде тонкого окрашенного слоя, поглощающего излучение источника света;
8) измерение прозрачности (оптической плотности слоя) специализированным вертикальным фотометром – денситометром (п. 3.1.1).
Осаждая на поверхности планшета антитела и используя помеченные ферментом антигены, аналогично можно обнаруживать антигены в пробе.
Гетерогенный ИФА называется сэндвич-метод (пластиковая подложка, антиген, антитело с ферментом образуют своего рода «бутерброд»). В англоязычной литературе подобный вид ИФА именуется ELISA (enzyme-linked immunosorbent assay) – реакция фермента, связанного с иммуносорбентом.
Гомогенный ИФА. В нем используются антитела Ат и антигены, меченные ферментом Аг+E. При образовании комплекса антигенантитело фермент инактивируется. Потеря активности может быть связана с изменением активного центра фермента или с тем, что антитело закрыло доступ к субстрату. Когда же появляются свободные антигены, то они, конкурируя за антитела, восстанавливают активность фермента.
Иногда используют ферменты, катализирующие биолюминесценцию (п. 2.5.1), что позволяет выявить наличие антител пациента по уменьшению свечения лунок планшета.
Ограничения ИФА. Возможности увеличения чувствительности ИФА ограничиваются фоном анализируемого соединения, т. е. наличием его не только в анализируемом образце, но и в используемых реактивах и растворителях. К ограничениям ИФА относится также наличие в тестируемых образцах кофакторов, ингибиторов и стимуляторов активности ферментов. Еще один недостаток — ИФА не позволяет различать нативные белки и их биологически неактивные фрагменты, сохранившие антигенные детерминанты. Ограничением ИФА является его применимость лишь к хорошо изученным системам, где есть очищенные антигены и высокоспецифические антитела.
Чувствительность ИФА. Высокая чувствительность в сочетании с быстротой анализа, возможностью одновременного тестирования большого количества образцов, наличие различных диагностикумов являются неоспоримыми достоинствами ИФА. Поэтому ИФА находит широкое применение в здравоохранении, различных областях сельского хозяйства, в экологии.
Реагенты для проведения ИФА сегодня стали коммерческими продуктами и могут быть приобретены по каталогам известных фирм.
Применение ИФА. Любое заболевание можно быстро и точно диагностировать путем идентификации возбудителя, его отдельных антигенных компонентов, антител к этим компонентам или веществ, не свойственных здоровому организму и синтезируемых при его патологических состояниях.
Диспансеризация населения, эпидемиологические обследования, выявление отравлений, наличия наркотиков в крови, определение содержания лекарственных соединений в тканях, вирусные заболевания растений, определение антибиотиков, витаминов и других биологически активных соединений при отборе активных штаммов-продуцентов в промышленной биотехнологии, контроль за качеством медицинских препаратов из донорской крови на отсутствие вирусов-возбудителей СПИДа и гепатита В – это лишь небольшой перечень практического применения ИФА. Современные фундаментальные исследования в биохимии, клеточной физиологии и иммунологии, микробиологии, вирусологии, онкологии трудно представить без ИФА.
Если протестировать пробу крови к набору антигенов, можно выявить Аг, к которым у человека не вырабатывается Ат, и получить своеобразный «паспорт» защитной системы организма, называемый «иммунным статусом». Его изменение у находящихся долгое время в загрязненной среде людей и животных может стать объективным показателем ослабления организма.
3. Измерительные преобразователи биосенсорных систем.
При формировании БСС используются самые различные типы физико-химических преобразователей – оптические, электрохимические, гравиметрические, микроаналитические, механические.
Применение измерительных преобразователей (ИП) зависит от того, какие свойства БХП изменяются при воздействии на них веществ или физических полей.
3.1. Оптические
3.1.1. Денситометрические
Денситометры измеряют оптическую плотность среды:
D = –lg(Фпр/Ф0),
(26)
где Ф0 и Фпр – падающие на среду и прошедшие через нее потоки.
Оптическая плотность определяется свойством вещества поглощать или рассеивать излучение. Например, в случае образования окрашенного соединения в результате ферментативной реакции.
Примером использования денситометрического ИП в сочетании с БХП антиген–антитело–фермент (п. 2.5.6) является фотометр для иммуноферментного анализа ELISA [21]. Это БСС, измеряющая малые значения ослабления проходящего потока. Обычно из спектра мощного источника излучения (галогенной лампы) с помощью светофильтра выделяется необходимый диапазон длин волн. Поток, прошедший через светофильтр, распределяется с помощью световодов по восьми каналам измерительных фотометров. На выходе световодов линзы формируют тонкий вертикальный луч, проходящий через лунки планшета на фотоприемники. Измеренная оптическая плотность ячеек планшета зависит от наличия антител в тестируемой пробе крови. Более подробное описание работы данной БСС приведено в разд. 4.
3.1.2. Колориметрические
Колориметры – приборы, измеряющие концентрацию C оптически однородного вещества по оптической плотности D окрашенного раствора.
Для этого в среду с БХП добавляют химическое вещество, которое, соединяясь с субстратом или продуктом БХП, образует равномерно окрашенный раствор. Его оптическая плотность, согласно закону Бэра:
D = C e b,
(27)
где e – коэффициент экстинкции (удельного пропускания) окрашенного раствора (постоянная величина), b – толщина слоя раствора.
ИП этого типа применяют в БСС для оценки переработки углерода, в котором в качестве БХП используются ферменты аэробных бактерий (п. 1.2.2), перерабатывающие соединения углерода с выделением продукта СО2. Индикатор на основе раствора Ba(OH)2 образует с продуктом БХП цветной раствор соли.
В БСС для оценки активности биологического окисления аналогичный ИП используется с другим БХП на основе фермента сукцинатдегидрогеназы, выделенного из митохондрий разрушенных и гомогенизированных клеток печени (п. 1.2.2). Фермент катализирует реакцию преобразования субстрата (янтарной кислоты) в продукт (фумаровую кислоту). Индикатор на основе хлорфенольного соединения образует с субстратом цветную растворимую соль, оптическая плотность которой уменьшается по мере разложения субстрата.
3.1.3. Спектрофотометрические
Спектрофометры состоят из: источника излучения с широким диапазоном длин волн; монохроматора с призмой, разлагающей излучение в спектр, из которого выделяется необходимый участок с помощью регулируемой щели; фотоприемника, измеряющего прошедший через щель поток в диапазоне длин волн lD.
Спектрофотометры позволяют обнаружить вещество по спектру поглощения, а также идентифицировать штаммы бактерий по различию их спектров поглощения в инфракрасной области длин волн, или нуклеиновые кислоты по спектру поглощения в ультрафиолетовом диапазоне.
Эти ИП применяют в БСС для оценки воздействия загрязнений воды на фотосинтез (п. 1.2.1). В этом случае используется БХП на основе фотосинтезирующего пигмента (хлорофилла-а), выделенного из тканей растений (п. 2.5.3). С помощью ИП измеряют спектр поглощения пигментом видимого света [43].
ИП могут также применяться в БСС для оценки метаболизма (п. 1.1.3) с БХП на основе ферментов (п. 2.5.1), когда различны спектры поглощения субстрата и продукта ферментативной реакции.
3.1.4. Турбидиметрические и нефелометрические
БО в питательной среде при падении на них светового потока создают эффект рассеяния. При прохождении через мутную среду с большой концентрацией БО световой поток ослабляется. Чем более мутная среда (т. е. чем больше концентрация в ней БО), тем меньше проходящий через нее поток излучения.
Рассеяние излучения БО зависит [23, 54] от следующих факторов:
- соотношения радиуса а и длины волны l падающего на них излучения, т. е. от коэффициента дифракции r0 =2pa/l; площади оптического сечения SБО, пропорциональной pa2 сотношения показателей преломления частицы nБО и среды nс (mБО= nБО/nс); концентрации СБО в единице объема.
Концентрацию БО, образующих мутный слой толщиной b и ослабляющий излучение, измеряют турбидиметрами (от лат. «турбид» – мутность). Полезный сигнал турбидиметра пропорционален exp(– CSБО b).
Если БО не создают мутного слоя, то их концентрацию измеряют нефелометрами ( от лат. «нефело» – облако), улавливая рассеянный ими поток под углом к падающему излучению. При условии, что mБО » 1, а плотность частиц в объеме невелика, полезный сигнал нефелометра пропорционален kC, где k – константа прибора.
При увеличении размеров БО меняется распределение интенсивности рассеянного света под разными углами. Вперед рассеивается больше, чем назад. Этот эффект позволяет изучать изменение морфологии БО (размеров, формы).
Турбидиметры используют в БСС, разработанных фирмами «Abbott» и «ROSHE» для контроля активности антибиотиков с БХП на основе роста-размножения бактерий. Нефелометры для аналогичных целей с измерением разности рассеянных потоков на малых и средних углах были разработаны фирмой «Science spectrum» [18].
3.1.5. Рефлектометрические
Метод рефлектометрии основан на измерении потока излучения, отраженного от поверхности БО. Если эта поверхность одновременно рассеивает и поглощает излучение, то отраженный поток будет отбрасываться в разные стороны. Чтобы собрать это излучение, измерения проводят в шаре с отражающими шероховатыми стенками. Тогда фотоприемник внутри шара будет улавливать рассеянный поток, интенсивность которого определяется как
J = Ф0(rбО /S)[1/(1 – rст)]
(28)
где Ф0 – поток, падающий на БО, S – площадь шара, rбО, rст – коэффициенты отражения БО и стенки соответственно.
В свою очередь коэффициент отражения рассеянного света определяется по эмпирической формуле Кубелки-Мунка-Гуревича:
(1 – rбО)2/ 2rбО = c /s,
(29)
где c – коэффициент поглощения слоя вещества, s – показатель рассеяния слоя. Более подробно ИП описан в работах проф. .
Данный ИП используется в БСС для оценки загрязнений окружающей среды с БХП на основе фотосинтезирующих пигментов, находящихся в тканях листьев. Для этой цели в фотометрический шар помещают стопку листьев и измеряют отраженный поток. Листья перекладывают в случайном порядке N раз, в результате получают множество величин Фотр1 … ФотрN, характеризующих распределение фотосинтезирующих пигментов. Подобный вид приборов начинает разрабатывать фирма «ЛОМО» (С-Петербург).
3.1.6. Рефрактометрические
Рефрактометры – приборы для измерения показателя преломления (ПП) среды. Методы измерения, применяемые в БСС, получили общее название ИП нарушения полного внутреннего отражения (НПВО). Этот эффект возникает как в оптических волокнах, так и в призмах при падении света под углом.
Волоконно-оптические ИП. Основаны на нарушении прохождения светового потока через оптическое волокно, изогнутое в форме петли. Эффект НПВО возникает, когда ПП среды nс, окружающей стеклянное волокно, будет больше ПП этого волокна nв.
Уменьшение потока DФ за счет НПВО, обусловленного выходом части излучения в оболочку:
DФ= k (nс – nв),
(30)
где k – коэффициент пропорциональности.
Данный ИП может применяться в БСС для оценки метаболизма с БХП на основе ферментов, если ПП субстрата меньше ПП стекла, а ПП продукта, образованного в результате ферментативной реакции, всего на 10–7 больше ПП стекла.
НПВО происходит, когда среда непосредственно контактирует с материалом оптической нити. Поэтому эффект НПВО возникает также при осаждении на волоконную нить слоя биомолекул (рис. 6), что позволяет контролировать реакции образования биологических комплексов [69].
Волоконно-оптические ИК ИП. Полезным эффектом НПВО, связанным с применением волоконной оптики в БСС, является выход излучения из световода в среду, поглощающую инфракрасное излучение. Тогда оптическая плотность волоконного ИП:
D = aвL + f (aИК с),
(31)

Рис. 6. Биосенсор на основе оптического волокна [3]
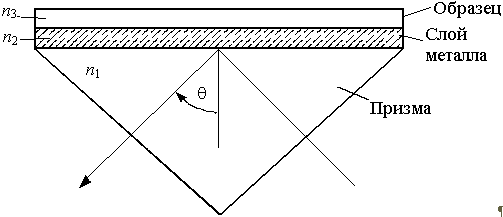
Рис. 7. Возбуждение излучательных плазмонов методом НПВО в призме Кречмана: - угол падения света; n1, n2, 3 - показатели преломления призмы, слоя металла и исследуемого образца соответственно [3]
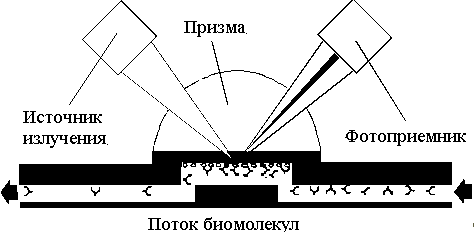
Рис. 8. Схема образования комплексов биомолекул в измерителях поверхностного плазмонного резонанса [59]
где L – длина световода, aв – коэффициент поглощения волокна, aИК с – коэффициент поглощения среды в ИК области излучения. Через волокно подается излучение различных длин волн ИК-спектра. Учитывая, что многие микроорганизмы обладают специфичными ИК-спектрами, волоконная ИК-спектроскопия может использоваться для выявления изменений свойств биологических объектов.
Поверхностный плазмонный резонанс [3, 25, 56, 59, 60]. Эффект НПВО в треугольной призме при падении инфракрасного излучения на ее основание проявляется, если оно покрыто тонкой пленкой металла или полупроводника, на которой возникают плазмоны – квантовые колебания поверхностных зарядов.
Их влияние приводит к тому, что интенсивность отраженного излучения спектра при определенном угле падения резко падает. Значение данного угла зависит от ПП приповерхностного слоя (рис. 7). Положение минимума отраженного потока смещается даже при изменении ПП слоя всего на 10–10.
Эти сверхмалые изменения отражают, например, образование комплекса антиген-антитело (п. 2.5.5) или трансформацию комплексов биомолекул на поверхности тонкой пленки золота. Подобный метод (surface plasmon resonance) был разработан в 1970-е гг. Лидбергом для выявления способности биологических организмов к образованию комплексов.
На основе этого метода для иммуноанализа шведской фирмой Pharmacia Biosensor AB создана [25,59] БСС «BIACORE» (рис. 8), а фирмой Аffinity Sensor для аналогичных целей – БСС «IASys» [60] с БХП на основе реакции антиген–антитело.
Это фотометрические БСС либо с проточной подачей антител (BIACORE), либо с нанесенными антителами на стенку стандартной кюветы (IASys). В них предусмотрена система подготовки поверхностей пластинок для иммобилизации антител, антигенов, микроорганизмов и клеток. В БСС входят системы перемешивания сред и термостатирования кювет и проточных ячеек.
3.1.7. Флуктуационные
Пусть БО образуют равномерную концентрацию С в среде и движутся в ней, случайно меняя направление. Если с помощью сфокусированного источника излучения сформировать тонкий луч, улавливаемый фотоприемником, то каждое пересечение луча БО, будет создавать флуктуацию оптического потока, которую можно полагать случайным событием, а множество событий – случайным потоком с интенсивностью L. Среднее число mT таких пересечений БО за время
mT =L T = kC,
(32)
где k – коэффициент, зависящий от вида БО и параметров просвечиваемого слоя. Приемник преобразует изменения БО светового потока в амплитуду импульсов. На их величину влияет поглощение излучения слоем БО с концентрацией С. Поэтому за время T среднее значение случайного сигнала
Um(T) = КС exp(–aC),
(33)
где коэффициент К зависит от параметров ИП и времени усреднения T, а a=SБО b, поскольку характер экспоненциальной зависимости такой же, как и при измерении полезного сигнала турбидиметра (п. 3.1.4).
Многие плавающие инфузории обладают локомоциями (п. 1.4.1), характеризующимися прямолинейными перемещениями со случайным изменением направления (п. 2.3.1). Размеры инфузорий довольно велики (0,1 мм), поэтому «на просвет» можно обнаруживать флуктуации от единичных подвижных инфузорий.
Данный метод применен [17] в БСС типа «БИОТЕСТЕР» для оценки токсичности водных сред с БХП на основе хемотаксиса инфузорий P. caudatum (п. 2.3.1).
3.1.8. Флуктуационно-корреляционные
N движущихся БО, находящихся в лазерном луче, рассеивают свет, создавая случайные флуктуации не только интенсивности излучения, но и его частоты (за счет эффекта Доплера). Множество флуктуаций интенсивности, измеряемых с помощью фотоприемника, образует случайный процесс I(t) .
На него влияют два источника флуктуаций: 1) пересечение БО луча лазера; 2) перемещение БО внутри луча на расстояние, сравнимое с длиной волны лазера. Эти факторы обусловливают [44]появление двух частотных компонент спектральной плотности S(w) [44] случайного процесса:
S (w) = S1 (w) + S2 (w).
(34)
Подвижность быстрых БО с небольшими концентрациями в объеме, например сперматозоидов, анализируют по первой ее компонент
S1 (w)= f (w, v1, DN ),
(35)
где DN – изменение числа БО в объеме; v1 – множество скоростей поступательного движения БО на расстояние, большее диаметра луча.
Подвижность малых БО с большой концентрацией и небольшими скоростями (например бактерий с количеством 107 в объеме) исследуют с помощью второй компоненты спектральной плотности:
S2 (w) = f (w, v2, Q),
(36)
где v2 – множество скоростей смещения частиц на расстояние, большее длины волны лазера; Q – коэффициент, характеризующий плотность размещения БО в объеме.
Подобный ИП применен [15] в разработанной во ВНИИМП (Москва) БСС для измерения коэффициента токсичности вытяжек полимеров с БХП на основе локомоций сперматозоидов крупного рогатого скота (п. 2.3.2).
Лазерный зонд с длиной волны 0,6328 мкм создает пучок излучения диаметром 25 мкм. В результате подсчета числа флуктуаций за 10...60 с измеряется показатель подвижники
Мп = ACv1,
(37)
где С – концентрация подвижных клеток; А – коэффициент, зависящий от конструктивных особенностей прибора и вида биообъекта.
3.1.9. Биолюминометрические
Применение в БХП биолюминесценции и активированной хемилюминесценции рассмотрено в пп. 2.3.2, 2.5.1, 2.5.2. В данном подразделе речь идет лишь о физических основах и средствах измерения люминесценции.
Энергия возбужденного атома (молекулы) может принимать лишь определенный и характерный для данного атома дискретный ряд значений. При переходе с более высокого энергетического уровня QM на более низкий QN атом (молекула) излучает квант с длиной волны lMN:
QM – QN = hc/lMN,
(38)
где h – постоянная Планка = 6,626·10–34 Дж·с; с – скорость света = 3 ·108 м/c.
Если люминесценция возникает за счет поглощения атомами излучения, то количественно ее характеризуют
энергетическим выходом:
hэн = Фл/Фв,
(39)
где Фв – возбуждающий поток, Фл – поток люминесценции,
или квантовым выходом:
hкв = Nл /Nв,
(40)
где Nл – число квантов люминесценции, Nв – число квантов возбуждающего излучения.
Спектр люминесценции не зависит от длины волны возбуждения, поэтому он характеризует исследуемое вещество. Кратковременная люминесценция называется флуоресценцией, долговременная – фосфоресценцией.
Сверхслабая люминесценция БО может усиливаться в присутствии физических или химических веществ-активаторов. Химические активаторы вступают в реакции с органическим веществом, способствуя образованию новых возбужденных молекул, испускающих излучение. Физические активаторы увеличивают величину квантового выхода возбужденной молекулы с сотых долей процентов до единиц процентов и более.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |




