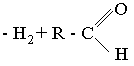Выделение газов [3]. Наиболее широкое распространение получили БСС для определения глюкозы в крови с помощью ферментативной реакции:
глюкоза + O2 + F => глюконовая кислота + H2O2 + F,
(15)
где F – фермент глюкозоксидаза (п. 3.2.3).
Для оценки активности фермента нитрогеназы используется ее свойство преобразовывать газ ацетилен в этилен.
Изменение кислотности. Газы, выделяемые в результате ферментативных реакций, при пропускании через водную среду могут изменять ее кислотность (п. 2.3.1).
Выделение тепла. Многие ферментативные реакции идут с выделением тепла [3]. Некоторые типы подобных реакций были указаны в п. 1.2.2. Наиболее простой подход использован в ферментных БХП, в которых фермент или иммобилизовали на поверхности устройства для измерения температуры или помещали в мембрану, надетую на это устройство.
Достоинством данных БХП было обеспечение возможности контроля тепловыделения в течение длительного времени, а также в проточных системах. Методы измерения тепла описаны в п. 3.4.
Электрокатализ. Некоторые ферменты проявляют активность в форме ускорения обмена электронами между субстратом и электродом. Транспорт электронов может происходить [7] несколькими путями:
а) за счет промежуточного низкомолекулярного переносчика электронов – медиатора, который сначала окисляется ферментом, а затем восстанавливается на электроде;
б) за счет биоэлектрокатализа – прямого переноса электронов ферментами.
В качестве медиатора в раствор фермента добавляют вещество – переносчик электронов (ферроцен) или белки – переносчики электронов (п. 3.2.5).
Биоэлектрокатализ был открыт в 1978 г. советскими учеными (, , и др.). Прямой перенос электронов возникает у ферментов: медьсодержащей оксидазы – лакказы, пероксидазы, гидрогеназы, катализирующих соответственно окисление веществ кислородом (п. 1.2.1), распад H2O2, присоединение групп водорода. Это свойство используется для преобразования продукта H2O2 в электрический ток на электроде.
Многие ферменты катализируют окисление сахаров, аминокислот с выделением H2O2. В этом случае фермент пероксидаза используется для трансформации концентрационного сигнала в электрический:
AH2 (белок, углевод) + O2 –® A + H2O2 (оксидаза),
(16)
H2O2 –® H2O + 2 e– (пероксидаза).
(17)
Цепь реакций позволяет измерять концентрацию сахаров и белков, участвующих в обмене веществ, по величине тока на электродах (п. 3.2.4, 3.2.5).
Биолюминесценция (БЛ). Способностью к БЛ обладают бактерии, грибы, моллюски, насекомые [9, 10,16]. Механизм световых реакций у разных видов включает окисление субстрата люциферина ферментом люциферазой (п. 1.1.3).
Выделено несколько типов ферментов FL, катализирующих реакции БЛ.
а) FL1 – люцифераза насекомых. Ее выделяют из светоизлучающих органов («лампочек») светляков. Реакция катализа проходит в присутствии АТФ – энергетического соединения, необходимого для дыхания (п. 1.2.2).
АТФ при реакции преобразуется в АМФ:
люциферин+ АТФ +F ®
®окисленный люциферин +АМФ +фотон + F L1.
(18)
При отсутствии АТФ биолюминесценция не наблюдается. На этом принципе основан самый чувствительный метод измерения АТФ, когда в изучаемый раствор добавляют люциферин и люциферазу, измеряя свечение.
б) FL2 – ферменты медуз. Из этих организмов выделяется способный к свечению белок фотопротеин. Он содержит связанный люциферин, который светится за счет окисления ферментом в присутствии ионов Ca2+. Белок под названием экворин добавляют в изучаемый объект и по свечению следят за динамикой свободного кальция.
в) FL3 – ферменты люминесцентных бактерий. Свечение бактерий катализируется бактериальной люциферазой. Очищенный фермент обладает способностью к свечению только в присутствии трех субстратов: кислорода (S1), альдегида (S2) и сложного белка (S3), играющего важную роль в аэробном дыхании. Добавляя в раствор постоянные концентрации двух субстратов и фермент – бактериальную люциферазу, по возникающему свечению обнаруживают наличие и концентрацию третьего субстрата.
Если в раствор вносят S2+S3+FL3, можно определять концентрацию О2 (S1) по свечению, интенсивность которого линейно зависит от концентрации О2 в диапазоне 10–8 – 10–6 моль/л.
Если внести в раствор S1+S3+F L3, то по возникновению люминесценции появляется возможность определять альдегиды (S2), к которым, например, относятся половые гормоны насекомых (ферромоны). Ими, например, самки ночных бабочек, привлекают к себе самцов. По свечению раствора удается изучать метаболизм гормонов у одной особи насекомого.
После внесения в раствор смеси S1+S2+FL3 образуется БХП для определения необходимых для люминесценции сложных белков (S3). Ими являются компоненты белков дыхательного цикла на основе витамина B2. Их концентрацию можно измерять по интенсивности свечения.
В свою очередь сложный белок S3 образуется из биологического окисленного кофермента дыхательного цикла (НАДН, п. 1.2.2), являющегося субcтратом S4 для ферментативных реакций окисления с участием фермента F1 – оксидоредуктазы. Добавляя эти ферменты, можно продолжить аналитическую цепочку, где место субстрата S3 займет S4:
S1+S2+S4 ® (при добавлении FL3, F1) ® свечение
(19)
Биологическое окисление НАДН из исходного субстрата S5 (НАД) катализируется другим ферментом – F2 дегидрогеназой, что позволяет измерять уже ее активность по тому же свечению, а вместо S4 использовать S5:
S1 + S2+S5 (при добавлении FL3, F1, F2) ® свечение.
(20)
При всех достоинствах подобных анализов цепочки реакций следует учитывать их недостаток – на свечение будут влиять все нестабильности концентраций исходных субстратов и ферментов.
В России производится набор КРАБ (комплекс реактивов для анализа биолюминесценции), который применяется для биохимических измерений. Ферменты КРАБ выделены из биомассы светящихся бактерий.
Приборы для измерения БЛ приведены в п. 3.1.9, а характеристики люминесцирующих БО – в табл. 5.
Запуск и блокирование реакций. Эти тест-реакции наиболее широко используются в ферментных тест-методах, предназначенных для обнаружения анализируемого вещества.
В основу ферментных тест-методов положено свойство ионов металлов или органических токсикантов ингибировать (п. 1.1.3) процессы каталитического превращения веществ в присутствии биологических катализаторов-ферментов [37]. Принцип их действия можно рассмотреть на примере тест-полоски для определения фосфорорганических веществ [14].
Она представляет собой полоску фильтровальной бумаги, на одном из концов которой иммобилизован фермент ацетилхолинэстераза, участвующий в проведении нервных импульсов (п. 1.4.1). Другой конец этой полоски содержит субстрат (ацетилхолин), скорость каталитического гидролиза которого подавляется в присутствии фосфорорганических веществ. Вместе с субстратом наносится кислотно-основной индикатор.
Наличие вещества-ингибитора выявляют по окраске зоны индикации тест-полоски после того, как полоска складывается для совмещения пятен, содержащих субстрат и фермент, и на нее, например, выжимают сок анализируемого продукта. Если продукт содержит фосфорорганический пестицид, скорость ферментативной реакции понижается, приводя к уменьшению количества выделившийся при этом кислоты, что вызывает изменение окраски индикатора. По цветовой шкале на упаковке тест-полосок можно оценить экологическую чистоту продукта питания. Аналогичная структура тест-наборов для клинической химии [1, 14].
Таблица 5
Состав и свойства светящихся смесей некоторых организмов [16]
Группа | Организм | Реагирующие | Положение |
I | Медуза (Aeguorera) | белок + Са++ | синяя |
II | Усоногие рачки | H2O2 + LH2 + E | голубая |
III | Рыба (Apagon) Простейшие Многощетинковый червь (Odontosylis) Ракообразные (Cypridina) | O2 + LH2 + E O2 + LH2 + E O2 + LH2 + E O2 + LH2 + E | 460 синяя 510 460 |
IV | Грибы (Collibia и Armillaria) Гриб (Omphaly flavida) | O2 + LH2 + E+ДПН – Н или O2 + LH2 + E+ ДПН – Н | 530 |
V | Морские анютины глазки (Renilla Reniformis) Светящиеся | O2 + LH2 + E + АМФ O2 + LH2 + E + АТФ | синяя 562 |
VI | Бактерии (Ahromobacter и другие) | O2 +LH2+E+ФМН–
| 405 |
Моллюск фаллада (Pholas Dactylus) | О2 + ДПН – Н + Е + | синяя | |
VII | Млекопитающие | О2 + липиды О2 + жиры или жирные то же + адреналин то же + эргостерин то же + лецитин то же + аминокислоты | зеленая и зеленая |
LH2 – энергетический субстрат люминесцентной реакции, Е – катализатор (люцифераза), ДПН – Н – восстановленный дифосфопириннуклеотид.
АТФ – аденозинтрифосфат, АТМ – аденозинмонофосфат, ФМН – Н2 –
восстановленный флавинмононуклеотид, 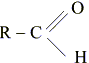 – альдегид.
– альдегид.
Общий принцип большей части химических тест-методов заключается в использовании ферментных реакций с так называемыми хромогенными (цветообразующими) реагентами [38, 41]. Реакции проводят в таких условиях, чтобы можно было визуально зафиксировать их результат. Этим результатом могут быть интенсивность окрашивания, цвет бумажной полоски или длина окрашенной части индикаторной трубки с поглощающим веществом. Большинство используемых тест-методов служат измерительной БСС однократного применения.
Тест-системы являются одним из самых коммерчески выгодных товаров. Оборот фирм, торгующих ими, составлял в 1994 г. около $100 млн.
Организация цепи тест-реакций. Метаболические ферментные процессы в организме часто образуют цепи реакций (п. 1.1.3), которые могут использоваться в БХП как тест-реакции.
Если записать формулу цепи метаболизма:
S + F1 + K + I = P1 + F1 = P2 + F1 +F2,
(21)
где S – субстрат, F1 – фермент, катализирующий реакцию образования продукта P1, являющегося субстратом для ферментов до F2, катализирующего образование продукта P2, K – кофактор, I – ингибитор (п. 1.1.3), то можно решать следующие задачи:
- выявлять субстрат-метаболит S; измерять активность ферментов по поглощению S или образованию P1 и P2; выявлять кофакторы K, запускающие работу фермента; выявлять ингибиторы I, подавляющие активность ферментов; выявлять цепочки взаимодействия ферментов.
В качестве примера можно привести другой БХП [7] на основе ацетилхолинэстеразы (F1) Для оценки активности этого важного фермента используется цепь реакций, приводящая к образованию пероксида водорода:
ацетилхолин (S) + I + F1 ® холин(P1) + уксусная кислота.
(22)
На следующем этапе фермент F2 холиноксидаза катализирует окисление P1.
холин (P1) + O2 + F2 ® H2O2 (P2) + оксихолин + F2.
(23)
Образование H2О2 будет зависеть от наличия ингибитора исходного фермента. Ингибиторами ацетилхолинэстеразы являются фосфорорганические или хлорорганические пестициды.
2.5.2. Ткани организмов
Растительные и животные ткани содержат специфические наборы ферментов, которые могут быть использованы как катализаторы соответствующих химических реакций [3, 33]. Каталитическими веществами богаты листья, цветки и плоды растений (структуры, связанные с ростом, репродукцией и накоплением питательных веществ), ткани печени, желудка, почек, слизистой оболочки животных.
Поэтому тканевые материалы успешно используют в качестве биокаталитических компонентов БХП. Ткани создают естественное окружение для требуемого фермента, в результате чего его активность стабилизируется. Во многих случаях тканевые БХП служат намного дольше, чем БХП на основе чистых ферментов. Тканевые материалы сохраняют специфичность фермента, в то время как выделенные ферменты в тех же условиях разрушаются.
Селективность тканевых БХП иногда снижается за счет присутствия в тканях не одного, а нескольких ферментов. Однако влияние «лишних» ферментов в каждом конкретном случае можно исключить или значительно ослабить подбором рН, температуры среды либо с помощью соответствующих ингибиторов, кофакторов. Наличие в ткани разных ферментов позволяет в некоторых случаях использовать один БХП для измерения концентрации нескольких субстратов.
Для БХП используют гомогенаты (измельченные ткани, п. 2.4.2) или срезы тканей в питательной среде, фиксируя их в полупроницаемой пленке (например нейлоновой) на поверхности измерительного преобразователя – ИП (разд. 3). Иногда измельченные частицы включают в порошки, пасты, гели. В результате ферментативной реакции, протекающей в ткани, выделяются вещества, концентрация которых определяет величину выходного сигнала ИП, в качестве которого чаще всего используется газочувствительный датчик (п. 3.2.4, 3.2.5). В гибридных БХП, кроме ткани, иммобилизованы еще и ферменты.
Тканевые БХП для отдельных веществ. В табл. 6 приведены примеры подобных БХП для определения различных веществ.
Зависимость скорости образования продукта от концентрации субстрата нелинейна, если количество фермента постоянно (п. 1.1.3). В табл. 6 приведен диапазон концентраций, при котором сохраняется линейная зависимость между концентрацией измеряемого и количеством выделяемого или потребляемого вещества в процессе ферментативной реакции. Время работы БХП – это время сохранения им линейного отклика на анализируемое вещество.
Таблица 6
Характеристика тканевых БХП [33]
Определяемое вещество | Биокаталитический | Вещество: выделение–В, потребление–П | Диапазон Моль | Время | Значение |
Мочевина | Мука из бобов канавалии мечевидной / уреаза | NH3 (аммиак, В) | – | – /94 дн | Болезни почек, диабет, болезни печени |
Кашица тычинок хризантемы / уреаза | NH3 (аммиак, В) | 2´10–5... 3´10–4 | – | отравления фосфором, мышьяком | |
Пируват | Срез кукурузного зерна / | CO2, В | – | – | Болезни печени, токсикозы, травмы черепа |
Пероксид водорода | Лист капусты кольраби / пероксидаза | О2, В | 4 ´10–5... 6 ´ 10–4 | 2 ... 6 с/ – | Контроль действия фармакологических |
Ткани корней хрена / пероксидаза | О2, В | 2,5´10–5... 2,3´10–4 | 3 мин / 2 мес. | препаратов, генетические патологии | |
Катехол | Срез ткани картофеля / полифенолоксидаза | О2 , П | 2,5´10–5... 2,3´10–4 | 3 мин / 3 мес. | Вещество, входящее в состав гормонов |
Ткань шпината / катехолоксидаза | О2 , П | 2,0´10–5... 8´10–4 | – / 18 дн | мозгового слоя | |
Катехоламины | Ткань печени крысы / моноаминоксидаза | Аммоний, В | – | – / 20...25 дн | (адреналина и |
Аскорбиновая кислота | Сок огурца / аскорбатоксидаза | О2 , П, вода В | 2,5´10–4... 1,6´10–3 | 3 ... 6 мин / – | Витамин |
Дофамин | Мякоть банана / полифенолоксидаза | О2, П | 1,3´10–6... 9´10–5 | 12 с /10 дн | Вещество, дейсвующее на нервную систему |
Тирозин | Срез сахарной свеклы / тирозиназа | О2, В | – /8 дн | Аминокислота гормонов (инсулина и др.) |
Помимо приведенных примеров в литературе описан целый ряд биосенсоров на пероксид водорода с применением кожуры кабачка и огурца, сенсоры на аминокислоты, содержащие в качестве биокаталитического материала компоненты цветков растений (кашицу тычинок хризантемы, ткани цветка магнолии, срезы пестика, ткани семян петрушки). Тычинки, пестики, семена содержат ферменты, катализирующие соответствующие реакции. Проведены опыты с применением в качестве БХП чешуи рыбы для определения гормона норадреналина, ткани мочевого пузыря жабы для определения антидиуретического гормона.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 6 7 8 |