![]() -
-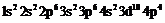 (селен);
(селен);
![]() -
-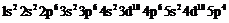 (теллур);
(теллур);
![]() -
-![]() (полоний).
(полоний).
В ряду ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() уменьшаются энергии ионизации, увеличиваются размеры атомов и ионов. Это ослабляет неметаллические признаки элементов и увеличивает металлические:
уменьшаются энергии ионизации, увеличиваются размеры атомов и ионов. Это ослабляет неметаллические признаки элементов и увеличивает металлические: ![]() – кислород,
– кислород, ![]() – сера – элементы неметаллы,
– сера – элементы неметаллы, ![]() - полоний – металл.
- полоний – металл.
Элементы VI А подгруппы имеют конфигурацию валентных электронов ![]() . В образовании связей вовлекаются непарные электроны, а также одна или две электронные пары. Поэтому наиболее устойчивые четные степени окисления: -2; +2; +4; +6.
. В образовании связей вовлекаются непарные электроны, а также одна или две электронные пары. Поэтому наиболее устойчивые четные степени окисления: -2; +2; +4; +6.
Кислород – самый распространённый элемент на Земле. По распространённости в Космосе кислород уступает только водороду и гелию. Кислород образует соединения почти со всеми элементами (кроме гелия, неона, аргона). Вследствие количественного преобладания и большой окислительной активности кислород предопределяет форму существования на Земле химических элементов. Известно свыше 1400 минералов, содержащих кислород. По электроотрицательности кислород уступает только фтору ![]() , степень окисления кислорода в подавляющем большинстве соединений равна -2 (
, степень окисления кислорода в подавляющем большинстве соединений равна -2 (![]() ,
, ![]() ,
, ![]() ,
, ![]() . Кроме того, кислород проявляет степени окисления +2 и +4, а также +1 и -1 в соединениях со связью
. Кроме того, кислород проявляет степени окисления +2 и +4, а также +1 и -1 в соединениях со связью ![]() .
.
Степени окисления +2; +1; 0 проявляются у кислорода в его соединениях со фтором, например: дифторид кислорода ![]() ; диоксидифторид
; диоксидифторид ![]() :
: 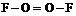 ; нитрофторид
; нитрофторид ![]() :
: 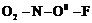 .
.
Дифторид кислорода ![]() получают при быстром пропускании фтора через 2%-ный раствор щелочи:
получают при быстром пропускании фтора через 2%-ный раствор щелочи:
![]()
Дифторид кислорода – ядовитый газ бледно-желтого цвета; термически устойчив, сильный окислитель.
Диоксидифторид ![]() образуется при взаимодействии простых веществ в электрическом разряде:
образуется при взаимодействии простых веществ в электрическом разряде:
![]()
Соединение крайне неустойчиво, что определяется низкой энергией разрыва связи ![]() (75 кДж/моль).
(75 кДж/моль).
В качестве производного, в котором кислород проявляет степень окисления +4, можно рассматривать аллотропическую (аллотропную) модификацию кислорода – озон ![]()
![]() . Молекула озона диамагнитна, имеет угловую форму и обладает некоторой полярностью (m=0,17×10-29 Кл×м).
. Молекула озона диамагнитна, имеет угловую форму и обладает некоторой полярностью (m=0,17×10-29 Кл×м).
Озон – газ синего цвета с резким раздражающим запахом, очень токсичен. Жидкий озон – темно-синяя жидкость, твердый – темно-фиолетовые кристаллы (Т пл. -192,7°С). Поскольку молекула ![]() обладает полярностью и большей поляризуемостью, озон имеет более высокую температуру кипения (-111,9°С), чем кислород.
обладает полярностью и большей поляризуемостью, озон имеет более высокую температуру кипения (-111,9°С), чем кислород.
Как сильный окислитель, к тому же экологически «чистый», озон используется для очистки питьевой воды, для дезинфекции воздуха в различных органических синтезах, для очистки морей от разлитой нефти.
Степень окисления -1 кислород проявляет в пероксидных соединениях. Наибольшее практическое значение имеет пероксид водорода (перекись) ![]() . Строение молекулы
. Строение молекулы![]() (но не линейное, а угловое).
(но не линейное, а угловое).
Пероксид – сильный окислитель. Водные растворы пероксида водорода широко используется для отбеливания различных материалов. Для обеззараживания сточных вод. При действии концентрированных растворов перекиси на бумагу, опилки или другие горючие вещества происходит их самовоспламенение. Пероксид водорода применяют как окислитель ракетного топлива.
Восстановительные свойства ![]() проявляет по отношению к таким сильным окислителям, как ионы
проявляет по отношению к таким сильным окислителям, как ионы ![]() :
:
![]()
Сера – типичный неметаллический элемент. По электроотрицательности уступает только галогенам, кислороду и азоту. Наиболее устойчивы, как уже говорилось, четные степени окисления серы (-2,+2,+4,+6). Наиболее характерны для серы высшая и низшая степени окисления. Известны соединения серы почти со всеми элементами. Сера – весьма распространенный на Земле элемент. По распространённости в Космосе сера занимает 9 место после ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() . Сера – биогенный элемент, входит в состав белков. Она содержится в нефти, углях, природных газов.
. Сера – биогенный элемент, входит в состав белков. Она содержится в нефти, углях, природных газов.
В соответствии с характерными степенями окисления сера в природе встречается в виде сульфидных (![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() и др.) и сульфатных (
и др.) и сульфатных (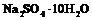 ,
, ![]() ,
, ![]() и др.) минералов, а также в самородном состоянии. Серу получают, главным образом, выплавкой самородной серы непосредственно в местах её залегания под землёй. Она применяется в производстве серной кислоты, для вулканизации каучука. Как инсектицид в сельском хозяйстве и т. д.
и др.) минералов, а также в самородном состоянии. Серу получают, главным образом, выплавкой самородной серы непосредственно в местах её залегания под землёй. Она применяется в производстве серной кислоты, для вулканизации каучука. Как инсектицид в сельском хозяйстве и т. д.
Один и тот же элемент может образовывать несколько разных типов простых веществ, называемых аллотропными модификациями. Явление аллотропии может быть обусловлено либо различным составом молекул простого вещества данного элемента (аллотропия состава), либо способом размещения молекул или атомов в кристаллах (аллотропия формы).
Сера, в отличие от кислорода, способна образовывать аллотропные модификации (гомоцепи) ![]() , имеющие зигзагообразную форму (рис.1), поскольку в их образовании принимают участие электроны взаимно перпендикулярно расположенных р-орбиталей атома. Наиболее стабильны циклические молекулы
, имеющие зигзагообразную форму (рис.1), поскольку в их образовании принимают участие электроны взаимно перпендикулярно расположенных р-орбиталей атома. Наиболее стабильны циклические молекулы ![]() , имеющие форму короны (рис.2).
, имеющие форму короны (рис.2).
Возможны молекулы ![]() ,
, ![]() и с открытыми цепями
и с открытыми цепями ![]() (пластическая сера, малоустойчивая).
(пластическая сера, малоустойчивая).
Две устойчивые в обычных условиях модификации: ромбическая a - ![]() (плотность 2,07 г/см3; Т пл. – 112,8ºС) и моноклинная b -
(плотность 2,07 г/см3; Т пл. – 112,8ºС) и моноклинная b - ![]() (плотность 1,96 г/см3; Т пл. – 119,3ºС) (
(плотность 1,96 г/см3; Т пл. – 119,3ºС) (![]() ). Неустойчивые модификации:
). Неустойчивые модификации: ![]() (пурпурная);
(пурпурная); ![]() (оранжево-желтая) и др.
(оранжево-желтая) и др.
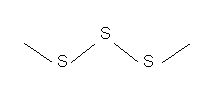
Рис. 1. Аллотропная модификация серы (гомоцепь)
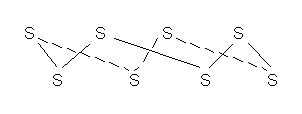
Рис. 2. Аллотропная модификация серы ![]()
Если нагревать расплавленную серу, она превращается в легко подвижную жидкость желтого цвета, при температуре t=160ºС темнеет и её вязкость повышается, при температуре 200ºС сера становится темно-коричневой и вязкой, как смола (кольцевые молекулы ![]() разрушаются и образуются цепи
разрушаются и образуются цепи ![]() ). При температуре выше 250ºС цепи разрываются и жидкость снова становится подвижной. При 444,6ºС сера закипает.
). При температуре выше 250ºС цепи разрываются и жидкость снова становится подвижной. При 444,6ºС сера закипает.
Вязкость серы h=1 при t=100ºС. Около 190ºС h вязкость примерно в 9000 раз больше, чем при 160ºС (см. рис. 3).
Сера – достаточно активный неметалл. Даже при умеренном нагревании она окисляет многие простые вещества, но и сама довольно легко окисляется кислородом и галогенами:
![]() сульфид алюминия
сульфид алюминия
![]() cульфид цинка
cульфид цинка
Сера диспропорционирует:
![]()
![]()
В технике оксид серы (VI) получают окислением ![]() в присутствии катализатора (платина или оксид ванадия):
в присутствии катализатора (платина или оксид ванадия):
![]()
а также обжигом пирита:
![]()
h
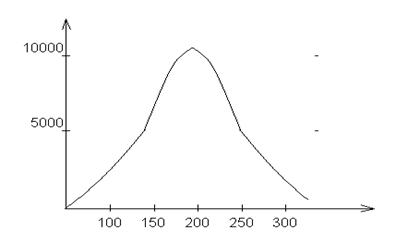
tºC
Рис. 3. Зависимость вязкости серы от температуры
Диоксиды серы ![]() применяют для получения серной кислоты; в бумажном и текстильном производстве в качестве отбеливающего средства, для консервации плодов. Жидкий
применяют для получения серной кислоты; в бумажном и текстильном производстве в качестве отбеливающего средства, для консервации плодов. Жидкий ![]() используют в качестве неводного растворителя для проведения различных синтезов.
используют в качестве неводного растворителя для проведения различных синтезов.
Малоактивные металлы ![]() ,
, ![]() и др., а также бромоводород и некоторые неметаллы восстанавливают концентрированную серную кислоту до
и др., а также бромоводород и некоторые неметаллы восстанавливают концентрированную серную кислоту до ![]() :
:
![]()
![]()
![]()
Активные металлы (![]() ,
, ![]() и т. п.) восстанавливают концентрированную
и т. п.) восстанавливают концентрированную ![]() до свободной серы или сероводорода:
до свободной серы или сероводорода:
![]()
![]()
При нагревании сульфиты диспропорционируют:
![]()
Ион ![]() легко переходит в ион
легко переходит в ион ![]() т. к. обладает довольно сильными восстановительными свойствами:
т. к. обладает довольно сильными восстановительными свойствами:
![]() ,
, ![]() .
.
Сульфиты в растворах постепенно окисляются даже кислородом воздуха:
![]()
![]()
[гидролиз 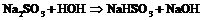 ]
]
Сера (IV) при взаимодействии с более сильным восстановителем проявляет окислительные свойства:
![]()
![]()
В щелочной среде легко смещается вправо:
![]()
![]()
![]()
[гидролиз ![]() ]
]
![]()
Сера в высшей степени окисления +6 образует различные соединения, из которых наибольший интерес представляет серная кислота. Концентрированная серная кислота является окислителем за счет серы (VI). Разбавленная серная кислота окисляет своим ионом водорода.
Лабораторная работа № 4
Элементы V группы периодической системы
1. Цель работы
1. Изучить электронное строение и свойства элементов V группы главной подгруппы.
2. Изучить окислительно-восстановительные свойства азота.
3. Познакомиться с аллотропными модификациями на примере фосфора.
4. Изучить механизм разложения солей аммония и азотной кислоты.
2. Контрольные вопросы
1. Описать конфигурацию внешнего электронного слоя атомов элементов V группы главной подгруппы? Назовите наиболее устойчивые степени окисления для этой подгруппы.
2. Почему возможно использование азота в качестве инертного наполнителя?
3. Назовите соединения азота, имеющие широкое применение.
4. Объясните, в чем заключается вертикальная периодичность на примере элементов V группы главной подгруппы.
5. До каких соединений восстанавливается ![]() в зависимости от концентрации?
в зависимости от концентрации?
6. Напишите и поясните реакцию получения азотной кислоты.
7. Расставьте коэффициенты в следующих реакциях:
![]()
![]()
8. Продолжите уравнения реакций, если известно, что окислительное действие «царской водки» обусловлено хлором. Расставьте коэффициенты:
![]()
3. Содержание работы и методические указания к её выполнению
На «рабочем столе» ПК найдите значок программы «1С:Химия».
После загрузки программы, найдите вкладку «Альбом»/»Элементы V группы».
1. Изучить строение молекул.
1.1. Зарисовать структурную и геометрическую формулы молекулы оксида фосфора (III) ![]() .
.
1.2. Зарисовать схему электронного строения атомов азота и фосфора.
1.3. Зарисовать структурную и геометрическую формулы молекулы белого фосфора ![]() .
.
1.4. Зарисовать структурную и геометрическую формулы молекулы аммиака ![]() .
.
1.5. Зарисовать структурную и геометрическую формулы молекулы азота ![]() .
.
1.6. Зарисовать структурную и геометрическую формулы молекулы фосфина ![]() .
.
1.7. Зарисовать структурную и геометрическую формулы молекулы азотистой кислоты ![]() .
.
1.8. Зарисовать структурную и геометрическую формулы молекулы азотной кислоты ![]() .
.
1.9. Зарисовать структурную и геометрическую формулы молекулы фосфорной кислоты ![]() .
.
1.10. Зарисовать структурную и геометрическую формулы молекулы фосфористой кислоты ![]() .
.
1.11. Зарисовать структурную и геометрическую формулы молекулы оксида фосфора (V) ![]() .
.
1.12. Зарисовать структурную и геометрическую формулы молекул оксидов азота: оксид азота (I) – ![]() ; оксид азота (II) –
; оксид азота (II) – ![]() ; оксид азота (IV) –
; оксид азота (IV) – ![]() .
.
2. Наблюдать опыты и написать уравнения следующих реакций:
2.1. Взаимодействие нитрата серебра с фосфатом натрия. Образуется фосфат серебра.
2.2. Разложение бихромата аммония.
2.3. Взаимодействие фосфора с концентрированной азотной кислотой.
2.4. Разложение хлорида аммония при нагревании. Образуется аммиак и хлороводород.
2.5. Разложение нитрата аммония.
2.6. Взаимодействие оксида серебра с аммиаком.
2.7. Взаимодействие амальгама натрия с хлоридом аммония.
2.8. Взаимодействие нитрата натрия с соляной кислотой. Образуется бурый газ оксида азота (IV).
2.9. Взаимодействие меди с азотной кислотой. Выделяется оксид азота (IV), при нагревании реакция ускоряется.
2.10. Разложение нитрата меди при нагревании. Образуется оксид азота (IV) бурого цвета и оксид меди (II) черного цвета.
2.11. Разложение азотной кислоты при нагревании. Образуется оксид азота (IV) ![]() .
.
2.12. Взаимодействие свинца с азотной кислотой. При нагревании выделяется оксид азота (I) ![]() . Без нагрева реакция останавливается.
. Без нагрева реакция останавливается.
2.13. Взаимодействие оксида фосфора (V) с водой.
2.14. Окисление аммиака.
3. В каждой окислительно-восстановительной реакции проставить степени окисления и записать полуреакции.
4. Написать названия соединений в химических реакциях.
Приложение
К элементам V группы главной подгруппы А относятся: ![]() – азот,
– азот, ![]() – фосфор,
– фосфор, ![]() – мышьяк,
– мышьяк, ![]() – сурьма,
– сурьма, ![]() – висмут.
– висмут.
Электронные формулы:
![]() (азот);
(азот);
![]() (фосфор);
(фосфор);
![]() (мышьяк);
(мышьяк);
![]() (сурьма);
(сурьма);
![]() (висмут).
(висмут).
Азот и фосфор относятся к типическим элементам, а мышьяк, сурьму и висмут объединяют в подгруппу мышьяка. Размеры атомов и ионов увеличиваются в группе сверху вниз по вертикали от ![]() к
к ![]() , а энергии ионизации уменьшаются. Этим обусловлено ослабление признаков неметаллических элементов.
, а энергии ионизации уменьшаются. Этим обусловлено ослабление признаков неметаллических элементов.
Азот – типичный неметаллический элемент, по электроотрицательности уступает лишь фтору и кислороду.
Элементы подгруппы мышьяка имеют неметаллические и металлические модификации. Устойчивые в обычных условиях модификации – серый мышьяк, серая сурьма, висмут – имеют металлический вид, электрическую проводимость, хрупкие из-за солистой структуры (типа черного фосфора).
Азот занимает 5 место по распространённости химических элементов в Космосе. Основная масса его входит в состав атмосферы в виде простого вещества. Азот входит в состав белковых тел всех растительных и животных организмов, обнаружен в газовых туманностях и солнечной атмосфере, на Уране и Нептуне. Степени окисления азота в соединениях -3; -1; +1; +3; +5, а также -2, +2 и +4. В обычных условиях азот непосредственно взаимодействует лишь литием с образованием ![]() . При активации молекул
. При активации молекул ![]() (нагревании, действии электроразряда или ионизирующего излучения) азот выступает как окислитель, а при взаимодействии с фтором и кислородом как восстановитель. В промышленности азот получают фракционированной перегонкой жидкого воздуха, в лаборатории – термическим разложением соединений, чаще всего нитрата аммиака
(нагревании, действии электроразряда или ионизирующего излучения) азот выступает как окислитель, а при взаимодействии с фтором и кислородом как восстановитель. В промышленности азот получают фракционированной перегонкой жидкого воздуха, в лаборатории – термическим разложением соединений, чаще всего нитрата аммиака ![]() :
:
![]()
Основная масса получаемого азота используется для синтеза аммиака, большая часть которого идет на производство азотной кислоты и других азотосодержащих веществ. Кроме того, азот применяют для создания инертной атмосферы в химических производствах, электрических лампах, при перекачке горючих жидкостей и т. п. При высоких температурах азот окисляет многие металлы и неметаллы, образуя нитриды:
![]() – нитрид магния
– нитрид магния
![]() – нитрид водорода (или
– нитрид водорода (или ![]() – аммиак)
– аммиак)
Из нитридов наибольшее практическое значение имеет аммиак. Среди водородных соединений p–элементов V группы аммиак занимает такое же особое положение, как вода среди водородных соединений p–элементов VI группы. В химическом отношении аммиак довольно активен; он вступает во взаимодействие со многими веществами. Азот в аммиаке имеет самую низкую степень окисления (-3). Поэтому аммиак обладает только восстановительными свойствами.
![]()
2 |
| восстановитель (окисление); | |
12 | |||
3 |
| окислитель (восстановление); |
![]()
В зависимости от условий окисления аммиака может протекать по реакции:
![]()
4 |
| восстановитель (окисление); | |
20 | |||
5 |
| окислитель (восстановление); |
![]()
Атом азота в молекуле аммиака связан тремя ковалентными связями с атомами водорода и сохраняет при этом одну неподелённую электронную пару:
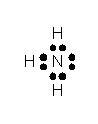 Согласно теории валентных связей это отвечает
Согласно теории валентных связей это отвечает ![]() – гибридизации валентных орбиталей атома азота. Из четырёх
– гибридизации валентных орбиталей атома азота. Из четырёх ![]() – гибридных орбиталей азота три участвуют в образовании трёх s - связей
– гибридных орбиталей азота три участвуют в образовании трёх s - связей ![]() –
–![]() , а четвертую орбиталь занимает несвязывающая электронная пара. Поскольку несвязывающее электронное облако отчётливо ориентировано в пространстве, молекула
, а четвертую орбиталь занимает несвязывающая электронная пара. Поскольку несвязывающее электронное облако отчётливо ориентировано в пространстве, молекула ![]() – резко выраженный донор электронной пары и обладает высокой полярностью (m = 0,49×10-29 Кл×м). Выступая в качестве донора электронной пары, аммиак способен вступать в реакции присоединения с образованием комплексных соединений, ионов аммония
– резко выраженный донор электронной пары и обладает высокой полярностью (m = 0,49×10-29 Кл×м). Выступая в качестве донора электронной пары, аммиак способен вступать в реакции присоединения с образованием комплексных соединений, ионов аммония ![]() , комплексных ионов:
, комплексных ионов:
![]()
![]()
![]()
Аммиак очень хорошо растворяется в воде, при этом имеет место ионизация – появляются ионы аммония ![]() и ионы
и ионы ![]() . Среда раствора щелочная. При взаимодействии ионов
. Среда раствора щелочная. При взаимодействии ионов ![]() и
и ![]() вновь образуются молекулы
вновь образуются молекулы ![]() и
и ![]() , между которыми возникает водородная связь. Ионное соединение
, между которыми возникает водородная связь. Ионное соединение ![]() (гидроксид аммония) не существует. Но по традиции водный раствор аммиака обозначает формулой
(гидроксид аммония) не существует. Но по традиции водный раствор аммиака обозначает формулой 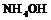 .
.
Соли аммония термически неустойчивы. При нагревании они разлагаются обратимо или необратимо в зависимости от окислительных свойств аниона. Если анион не является окислителем или в слабой степени проявляет окислительные свойства, процесс распада обратим:
![]()
Если анион проявляет резко выраженные окислительные свойства, соли распадаются необратимо:
![]()
Азот образует с кислородом ряд оксидов: оксид азота (I) ![]() (закись азота); оксид азота (II)
(закись азота); оксид азота (II) ![]() , оксид азота (IV)
, оксид азота (IV) ![]() (диоксид ли двуокись); оксид азота (III)
(диоксид ли двуокись); оксид азота (III) ![]() (азотистый ангидрид).
(азотистый ангидрид).
Наибольший интерес представляет ![]() . При растворении в воде вступает в реакцию с
. При растворении в воде вступает в реакцию с ![]() , образуют азотную
, образуют азотную ![]() и азотистую
и азотистую ![]() кислоты.
кислоты.
Азотистая кислота нестойка и быстро разлагается:
![]()
Следовательно,
![]()
![]() в присутствии кислорода воздуха окисляется до
в присутствии кислорода воздуха окисляется до ![]() и, в конечном итоге, полностью переходит в
и, в конечном итоге, полностью переходит в ![]() :
:
![]()
Диоксид азота – очень энергичный окислитель. Многие вещества могут гореть в атмосфере ![]() , отнимая от него кислород. На этом свойстве основан нитрозный метод получения серной кислоты:
, отнимая от него кислород. На этом свойстве основан нитрозный метод получения серной кислоты:
![]()
В атмосфере ![]() горят уголь, сера, фосфор. Диоксид азота применяют как нитрующий агент, например, для получения безводных нитратов.
горят уголь, сера, фосфор. Диоксид азота применяют как нитрующий агент, например, для получения безводных нитратов.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



