ФЕДЕРАЛЬНОЕ АГЕНТСТВО СВЯЗИ
ПОВОЛЖСКАЯ ГОСУДАРСТВЕННАЯ АКАДЕМИЯ ТЕЛЕКОММУНИКАЦИЙ И ИНФОРМАТИКИ
КАФЕДРА ФИЗИКИ
Проект на правах рукописи
,
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ЛАБОРАТОРНЫМ РАБОТАМ ПО КУРСУ «ХИМИЯ»
Рекомендовано УМО по образованию в области телекоммуникаций в качестве учебного пособия для студентов высших учебных заведений, обучающихся по направлениям подготовки бакалавров и магистров
550– Телекоммуникации
и подготовки дипломированных специалистов
654– Телекоммуникации
Самара
2007
УДК 54
Рецензенты
доктор технических наук, профессор
Методические указания к лабораторным работам по курсу «Химия» / , . – Самара: Изд-во ПГАТИ, 2007. – 56 с.
Настоящие методические указания разработаны для проведения лабораторных работ по химии с учетом специфики обучения студентов по направлениям подготовки бакалавров и магистров 550– Телекоммуникации и подготовки дипломированных специалистов 654– Телекоммуникации. Методические указания содержат теоретическую часть и инструкции к выполнению лабораторных работ с использованием компьютерной программы
УДК 54
, , 2007
Введение
В связи со все возрастающей компьютеризацией проведение лабораторных работ по химии для студентов академии с использованием компьютерных программ, демонстрирующих химические опыты, представляется целесообразным. Компьютерная программа по химии помимо развития практических навыков работы на персональном компьютере, дает возможность для самостоятельного и дистанционного обучения, что важно не только для студентов дневного отделения, но и для студентов заочной и дистанционной формы обучения.
Методическое пособие, содержащее необходимую теоретическую часть, создает возможность выполнения лабораторных работ на компьютере в домашних условиях. Аудиторное время занятий более полно может быть использовано для более основательного разбора теоретических основ химических процессов.
Лабораторные работы охватывают основные свойства химических элементов периодической системы по группам и подгруппам, также изучается электронное строение атомов и типы химических связей на примерах молекул некоторых веществ, наблюдаются и изучаются процессы электролиза.
В теоретической части содержатся некоторые основные понятия и представления, являющиеся общими для различных дисциплин естественно научного направления.
Лабораторная работа № I
Изучение свойств водорода
1. Цель работы
1. Познакомиться с электронным строением атома водорода, молекулы ![]() ,
, ![]() ,
, ![]() .
.
2. Изучить реакции получения водорода в лабораторных условиях.
3. Изучить окислительно-восстановительные реакции на примере взаимодействия йодида калия и перманганата калия с перекисью водорода.
2. Контрольные вопросы
1. Как получают водород в промышленности и в лаборатории? Привести уравнения реакций.
2. Описать строение молекулы водорода.
3. Описать строение молекулы воды.
4. Указать способы получения пероксида водорода. Описать строение молекулы ![]() .
.
5. Какие реакции называются окислительно-восстановительными? Дайте определения окислителям и восстановителям.
6. Какие степени окисления может принимать водород в реакциях?
7. До каких продуктов может быть окислена вода:
а) до ![]() и
и ![]() ; б) до
; б) до ![]() ; в) до
; в) до ![]() ?
?
8. Составить уравнения полуреакций окисления и восстановления для следующих реакций и определить, в каких случаях водород служит окислителем, а в каких – восстановителем:
а) ;
б) ![]() ;
;
в) 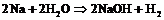 ;
;
г) 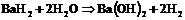 .
.
3. Содержание работы и методические указания к ее выполнению
На «рабочем столе» ПК найдите значок программы «1C: Химия». После загрузки программы, найдите вкладку «Альбом» / «Водород».
1. Изучить строение атома водорода, молекулы ![]() ,
, ![]() ,
, ![]() .
.
1.1. Зарисовать атом водорода.
1.2. Зарисовать электронное строение, геометрию и структуру молекулы водорода.
1.3. Зарисовать геометрию и структуру молекулы перекиси водорода.
1.4. Зарисовать электронное строение, геометрию и структуру молекулы воды.
1.5. Перечислите изотопы водорода.
1.6. Зарисовать структуру льда, изучить водородные связи.
2. Наблюдать проведение следующих опытов и записать уравнения реакций.
2.1. Взаимодействие цинка с соляной кислотой, в результате которой выделяется водород. При нагревании реакция ускоряется, при охлаждении замедляется.
2.2. Взаимодействие цинка с гидроксидом натрия. Водород выделяется только при нагревании.
2.3. Взаимодействие йодида калия с перекисью водорода. Выделяется йод.
2.4. Взаимодействие перекиси водорода с перманганатом калия в щелочной среде. Если прилить к перманганату калия раствор перекиси водорода, реакция не происходит. При добавлении гидроксида натрия перманганат калия восстанавливается.
2.5. Взаимодействие сульфида свинца с перекисью водорода. Перекись водорода окисляет сульфид свинца и образуется белый осадок сульфата свинца.
2.6. Взаимодействие натрия с водой. Спиртовой раствор фенолфталеина используется в качестве индикатора. Идет бурная реакция с выделением водорода.
2.7. Промышленные методы получения водорода.
2.7.1. Конверсия метана.
2.7.2. Неполное окисление метана.
2.7.3. Конверсия оксида углерода (II).
3. В каждой окислительно—восстановительной реакции проставить степени окисления и записать полуреакции.
4. Написать названия соединений в химических реакциях.
Приложение
Химия водорода
1. Распространение в природе.
2. Физико-химические свойства. Получение.
3. Применение. Токсикология.
1. Распространение. Природу водорода как особого газа впервые установил Кавендиш в 1766 г.
Водород принадлежит к распространенным в природе элементам. Он входит в состав воды, глины, каменного и бурого угля, нефти, во все животные и растительные организмы. В свободном состоянии водород встречается редко (в вулканических и природных газах). Водород – самый распространённый элемент космоса: он составляет до половины массы Солнца и большинства звёзд. Гигантские планеты солнечной системы Юпитер и Сатурн в основном состоят из водорода. Он присутствует в атмосфере ряда планет, в кометах, в газовых туманностях, в межзвёздном газе.
Его кларк равен 1%.
Кларк - относительная распространенность (в массовых долях, выраженная в %) элемента в таких составных частях Земли, как ее каменная кора глубиной до 16 км от уровня моря, воды океанов, морей, озер и рек, воздушная оболочка высотой до 50 км (граница стратосферы).
Водород не принадлежит ни к одной из групп периодической системы. Он обнаруживает те или иные физико-химические свойства, сходные с элементами почти всех А-групп. Атом водорода по сравнению со всеми остальными элементами имеет самую простую электронную конфигурацию ![]() - один электрон на одной s-АО. Основная особенность водорода заключается в том, что в отличие от всех других элементов (кроме гелия) в его атоме валентный электрон находится непосредственно в сфере действия атомного ядра – у него нет промежуточного слоя. Положительно заряженный ион водорода
- один электрон на одной s-АО. Основная особенность водорода заключается в том, что в отличие от всех других элементов (кроме гелия) в его атоме валентный электрон находится непосредственно в сфере действия атомного ядра – у него нет промежуточного слоя. Положительно заряженный ион водорода ![]() представляет собой элементарную частицу протон.
представляет собой элементарную частицу протон.
Особенность строения электронной оболочки атома водорода не позволяет однозначно решить, в какой группе периодической системы он должен находиться. Действительно, если исходить из числа валентных электронов его атома, то водород должен находиться в первой группе, что подтверждается также сходством спектров щелочных металлов и водорода. Со щелочными металлами сближает водород и его способность давать в растворах гидратированный положительный однозарядный ион ![]() (р). Однако в состоянии свободного иона
(р). Однако в состоянии свободного иона ![]() (г) – протона – он не имеет ничего общего с ионами щелочных металлов.
(г) – протона – он не имеет ничего общего с ионами щелочных металлов.
Согласно теоретическим представлениям при огромных давлениях водород должен переходить в металлическое состояние. В этих условиях должно происходить превращение молекулярного водорода в атомный и должна образовываться кристаллическая решетка, в узлах которой находятся протоны, а электроны становятся общими для всего кристалла; такой кристалл должен обладать металлической проводимостью. Но энергия ионизации атома водорода намного больше энергии ионизации атомов щелочных металлов.
Если же исходить из того, что для завершения внешнего электронного слоя атому водорода не хватает одного электрона, то водород следует поместить в VII группу. Атомы водорода, как и атомы галогенов, характеризуются высокими значениями ионизации.
Размещение водорода в I или VII группе таблицы в значительной мере условно.
Водород, встречающийся в природе, является смесью двух изотопов: - протия (99,984%) и ![]() (или
(или ![]() )- дейтерия (0,016%). Радиоактивный изотоп - тритий
)- дейтерия (0,016%). Радиоактивный изотоп - тритий ![]() или
или ![]() постоянно образуется в верхних слоях атмосферы под действием нейтронов космических лучей на атомы азота и некоторых других газов. В природных водах содержание трития не превышает 1-150 атомов на 1018 атомов протия.
постоянно образуется в верхних слоях атмосферы под действием нейтронов космических лучей на атомы азота и некоторых других газов. В природных водах содержание трития не превышает 1-150 атомов на 1018 атомов протия.
В виде простого вещества (молекул ![]() ) он встречается только на очень больших высотах, где находятся частично в атомарном, а частично в ионизированном состоянии (
) он встречается только на очень больших высотах, где находятся частично в атомарном, а частично в ионизированном состоянии (![]() ,
, ![]() ). Среднее содержание
). Среднее содержание ![]() вблизи земной поверхности составляет всего 5×10-5%.
вблизи земной поверхности составляет всего 5×10-5%.
Наиболее важные соединения водорода в природе вода, углеводороды и другие органические вещества.
2. Физико - химические свойства. Водород – газ без цвета, вкуса и запаха. Во всех трех агрегатных состояниях он находится в виде молекул ![]() . Его температура плавления – 259,20ºС, кипения – 252,80ºС. Растворимость в 1л воды при 250ºС составляет 0,0175 л (при 0ºС и 0,1 МПа). Плотность водорода по отношению к воздуху равна 0,06952. В обычных условиях водород ведет себя как идеальный газ.
. Его температура плавления – 259,20ºС, кипения – 252,80ºС. Растворимость в 1л воды при 250ºС составляет 0,0175 л (при 0ºС и 0,1 МПа). Плотность водорода по отношению к воздуху равна 0,06952. В обычных условиях водород ведет себя как идеальный газ.
Водород является смесью 25% пара-водорода и 75% орто-водорода. Он способен давать химические соединения с большинством химических элементов, за исключением благородных газов.
Водород взаимодействует с кислородом воздуха и взрывается от искры и пламени:
![]()
Смеси ![]() и
и ![]() взрываются в темноте:
взрываются в темноте:
![]()
Хлор горит в атмосфере водорода:
![]() ,
, ![]() 184 кДж.
184 кДж.
Реакции водорода с бромом и иодом протекают обратимо. С серой и селеном водород взаимодействует только при нагревании ![]() и
и ![]() . Непосредственно без катализаторов водород не реагирует с азотом, углеродом, кремнием. В обычных условиях молекулярный водород проявляет восстановительные свойства только по отношению к металлам, имеющим электродный потенциал более +0,7 В (
. Непосредственно без катализаторов водород не реагирует с азотом, углеродом, кремнием. В обычных условиях молекулярный водород проявляет восстановительные свойства только по отношению к металлам, имеющим электродный потенциал более +0,7 В (![]() ,
, ![]() ,
, ![]() ,
, ![]() ):
):
![]()
При высоких температурах ![]() является активным восстановителем, применяемым в промышленности:
является активным восстановителем, применяемым в промышленности:
![]()
![]()
![]()
Атомарный водород химически очень активен как восстановитель при Т=180ºС и более восстанавливает до металлов многие оксиды: ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() и другие.
и другие.
Некоторые металлы растворяют водород (![]() ,
, ![]() ,
, ![]() ). Щелочные, щелочно-земельные металлы, а также титан, цирконий, уран взаимодействуют с ним с образованием гидридов (
). Щелочные, щелочно-земельные металлы, а также титан, цирконий, уран взаимодействуют с ним с образованием гидридов (![]() ,
, ![]() ,
, ![]() ,
, ![]() и другие). Водород играет роль окислителя:
и другие). Водород играет роль окислителя:
![]()
Водород вызывает физическую коррозию и стали – металлы становятся хрупкими и под нагрузкой расслаиваются.
Получение. В промышленности водород получают главным образом из природных и попутных газов (до 90% метана), продуктов газификации топлива (водяного и паро-воздушного газов) и коксового газа. Производство водорода основано на каталитических реакциях взаимодействия с водяным паром (конверсии) углеводородов (главным образом метана) и оксида углерода (П), например над никелевым катализатором при Т = 800ºС:
![]() ,
, ![]() 161 кДж.
161 кДж.
![]()
![]()
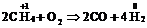
Затем из полученной смеси газов удаляют ![]() , сначала поглощая его водой под давлением, а затем – водным раствором этанол-аммиака.
, сначала поглощая его водой под давлением, а затем – водным раствором этанол-аммиака.
Наиболее чистый водород получают электрическим разложением воды, содержащей для увеличения ее электрической проводимости ![]() и
и ![]() :
:
на катоде ![]() :
: ![]() ,
,
на аноде ![]() :
:![]() .
.
Также ![]() получают по реакции:
получают по реакции:
![]()
и в лабораториях:
![]()
и из гидрида титана при терморазложении:
![]()
Гидридами называются бинарные соединения ![]() с более электроположительными элементами. По характеру химической связи все гидриды делят на ионные (солеобразные), ковалентные и металлообразные.
с более электроположительными элементами. По характеру химической связи все гидриды делят на ионные (солеобразные), ковалентные и металлообразные.
Ионные гидриды - бесцветные кристаллические вещества высокой реакционной способности. Все они сильные восстановители. Ионные гидриды в кристаллической решетке содержат катион металла и гидридный анион ![]() , который и определяет восстановительные свойства ионных гидридов. Стандартный электродный потенциал полуреакции:
, который и определяет восстановительные свойства ионных гидридов. Стандартный электродный потенциал полуреакции:
![]() ,
, ![]() 2,24 В.
2,24 В.
Поэтому анион ![]() проявляет по отношению ко многим веществам восстановительные свойства:
проявляет по отношению ко многим веществам восстановительные свойства:
![]()
![]()
Ионные гидриды образуют все щелочные и щелочно-земельные элементы и лантаноиды в степени окисления (+II), например ![]() ,
, ![]() .
.
Химическая активность ионных гидридов возрастает от ![]() к
к ![]() и от
и от ![]() к
к ![]() . Гидриды
. Гидриды ![]() и
и ![]() воспламеняются в сухом воздухе:
воспламеняются в сухом воздухе:
![]()
Они (ионные гидриды) реагируют с ![]() и
и ![]() :
:
![]()
![]()
При нагревании до Тº разложения образуются металл и водород:
![]()
Ковалентные гидриды некоторых р-элементов – газообразные бесцветные вещества со своеобразным запахом, взаимодействующие с водой и водными растворами гидроксидов щелочных металлов:
![]()
Исключением являются ![]() и
и ![]() , на которые ни вода, ни раствор
, на которые ни вода, ни раствор ![]() не действуют. Силан и диборан сгорают с образованием оксидов:
не действуют. Силан и диборан сгорают с образованием оксидов:
![]()
![]()
![]()
При нагревании гидриды распадаются:
![]()
![]()
![]()
Бор и кремний еще образуют сложные гидриды цепочного строения, могущие включать до 20 атомов бора (![]() ) и до 6 атомов кремния (
) и до 6 атомов кремния (![]() ).
).
Металлообразующие гидриды образуют некоторые d-элементы. В таких гидридах химическая связь полярная ковалентная с участием ионов ![]() или
или ![]() в зависимости от вида металла и количества связанного водорода. Их металлические свойства возникают в результате свободного перемещения электронов, оставшихся в кристаллической решетке после образования связи. Например, в гидриде
в зависимости от вида металла и количества связанного водорода. Их металлические свойства возникают в результате свободного перемещения электронов, оставшихся в кристаллической решетке после образования связи. Например, в гидриде ![]() у металла m валентных электронов, а участвуют в образовании связи только n
у металла m валентных электронов, а участвуют в образовании связи только n ![]() -ионов, то разность (m - n) дает число электронов, вызывающих металлические свойства. Когда m = n, металлические свойства исчезают и гидриды становятся ионными.
-ионов, то разность (m - n) дает число электронов, вызывающих металлические свойства. Когда m = n, металлические свойства исчезают и гидриды становятся ионными.
С кислотами они взаимодействуют, выделяя водород:
![]()
Водород широко используется как для химического синтеза веществ, так и в качестве «экологически чистого» топлива (горючего). При горении водорода в кислороде возникает высокая температура (до 2600ºС), позволяющая сваривать и резать тугоплавкие металлы, кварц и пр.
В атомной энергетике для осуществления ядерных реакций синтеза гелия имеют большое значение изотопы водорода – тритий и дейтерий.
Водород – основа химической технологии и энергетики будущего.
Лабораторная работа №2
Галогены – р-элементы VII группы периодической системы
1. Цель работы
1. Изучить электронное строение и свойства элементов VII группы главной подгруппы А периодической системы .
2. На примере галогенов проанализировать вертикальную периодичность в таблице .
3. Познакомиться с энергетическими характеристиками атомов (энергия ионизации, энергия сродства атома к электрону, электроотрицательность).
4. Познакомиться с электронным строением молекул ![]() ;
; ![]() .
.
2. Контрольные вопросы
1. Какие степени окисления характерны для галогенов?
2. Описать внешний электронный слой атомов галогенов.
3. Что называют энергией ионизации атома?
4. Что называют электроотрицательностью элемента?
5. Какие реакции называются необратимыми? Привести пример.
6. Распространение галогенов в природе.
7. Физические свойства галогенов.
8. Приведите примеры реакций, демонстрирующих окислительные свойства галогенов.
9. Назовите и приведите формулы некоторых кислородсодержащих соединений галогенов.
10. Напишите реакции образования хлорноватистой кислоты и ее превращений в растворе.
11. Как изменяется сила кислот и их окислительные свойства в ряду: хлорноватистая кислота – хлористая – хлорноватая – хлорная?
3. Содержание работы и методические указания к ее выполнению
На «рабочем столе» ПК найдите значок программы «1С:Химия».
После загрузки программы, найдите вкладку « Альбом» / «Галогены – р-элементы VII группы».
1. Изучить строение молекул ; .
1.1. Зарисовать атом хлора.
1.2. Зарисовать атом фтора.
1.3. Зарисовать структурную формулу молекулы ![]() и ее геометрию.
и ее геометрию.
1.4. Зарисовать структурную формулу и геометрию молекулы ![]() .
.
2. Наблюдать проведение следующих опытов и записать уравнения реакций.
2.1. Взаимодействие хлорида натрия с серной кислотой. Выделяется хлороводород.
2.2. Взаимодействие нитрата серебра с хлоридом калия, бромидом калия, йодидом калия. Выпадают осадки солей серебра.
2.3. Взаимодействие бромида натрия с серной кислотой. Выделяется бромоводород и бром.
2.4. Взаимодействие алюминия с йодом. Образуется йодид алюминия.
2.5. Взаимодействие брома и йодида калия.
2.6. Взаимодействие бромида свинца с йодидом калия. Образуется осадок йодида свинца.
2.7. Взаимодействие оксида меди (II) с соляной кислотой.
2.8. Взаимодействие бромида калия с броматом калия в кислой среде. Выделяется бром.
2.9. Взаимодействие брома со щелочью. Образуется бромид и бромат натрия.
2.10. Взаимодействие перманганата калия с йодидом калия. Образуется йод.
2.11. Взаимодействие перманганата калия с соляной кислотой. Выделяется хлор.
3. В каждой окислительно – восстановительной реакции проставить степени окисления и записать полуреакции.
4. Написать названия химических соединений, участвующих в реакциях.
Приложение
Элементы главной подгруппы А VII группы имеют групповое название «галогены», иначе «солеобразователи». К этим элементам относятся ![]() – фтор,
– фтор, ![]() – хлор,
– хлор, ![]() – бром,
– бром, ![]() – йод,
– йод, ![]() – астат.
– астат.
Электронные формулы:
![]() –
– ![]() (фтор);
(фтор);
![]() –
– 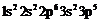 (хлор);
(хлор);
![]() –
– 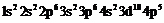 (бром);
(бром);
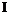 –
– 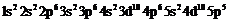 (йод);
(йод);
![]() -
- ![]() (астат).
(астат).
Все свойства элементов, определяемые электронной оболочкой атома, закономерно изменяются по периодам и группам периодической системы. В ряду элементов-аналогов электронные структуры сходны, но нетождественны.
У галогенов в их соединениях встречаются нечетные степени окисления от (-I) до (+VII), равной номеру группы. Только фтор имеет одну степень окисления (-I), так как является всегда акцептором электрона (табл. 1).
Таблица 1
Степени окисления галогенов и отвечающие им соединения
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вследствие большой химической активности, галогены находятся в природе только в связанном состоянии (например, в виде солей галогеноводородных кислот).

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



