Азотистая кислота обладает сильно выраженными окислительными свойствами:
![]()
![]()
Она разрушает животные и растительные ткани, окисляет почти все металлы и неметаллы. Образование тех или продуктов взаимодействия зависит от концентрации ![]() , активности простого вещества и температуры. Достаточно разбавленная кислота восстанавливается до
, активности простого вещества и температуры. Достаточно разбавленная кислота восстанавливается до 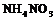 , с повышением её концентрации более характерно образование
, с повышением её концентрации более характерно образование![]() ; концентрированная
; концентрированная ![]() восстанавливается до
восстанавливается до ![]() :
:
![]()
![]()
![]()
Фосфор вследствие легкой окисляемости в свободном состоянии в природе не встречается. Из природных соединений фосфора самым важным является ортофосфат кальция ![]() , который в виде минерала фосфорита иногда образует большие залежи. Минерал апатит содержит, кроме
, который в виде минерала фосфорита иногда образует большие залежи. Минерал апатит содержит, кроме ![]() , еще
, еще ![]() или
или ![]() . Для получения фосфора природный фосфорит или апатит измельчают, смешивают с песком и углем и накаливают в печах с помощью электрического тока без доступа воздуха:
. Для получения фосфора природный фосфорит или апатит измельчают, смешивают с песком и углем и накаливают в печах с помощью электрического тока без доступа воздуха:
![]()
![]()
Фосфор выделяется в виде паров, которые конденсируются в приемнике под водой.
Фосфор образует несколько аллотропных видоизменений: белый фосфор, красный и черный.
Одна из сфер применения фосфора – получение некоторых полупроводников: фосфида галлия ![]() , фосфида индия
, фосфида индия ![]() . В состав других полупроводников он вводится в очень небольших количествах в качестве необходимой добавки.
. В состав других полупроводников он вводится в очень небольших количествах в качестве необходимой добавки.
Оксид фосфора (III), или фосфористый ангидрид, ![]() получается при медленном окислении фосфора или когда фосфор сгорает при недостаточном доступе кислорода. Это белые кристаллы, плавящиеся при 23,8ºС. При действии холодной воды
получается при медленном окислении фосфора или когда фосфор сгорает при недостаточном доступе кислорода. Это белые кристаллы, плавящиеся при 23,8ºС. При действии холодной воды ![]() медленно взаимодействует с ней, образуя фосфористую кислоту
медленно взаимодействует с ней, образуя фосфористую кислоту ![]() . Оксид и кислота обладают сильно выраженными восстановительными свойствами.
. Оксид и кислота обладают сильно выраженными восстановительными свойствами.
Оксид фосфора (V), или фосфорный ангидрид, ![]() образуется при горении фосфора на воздухе или в кислороде в виде белой объемистой снегообразной массы; жадно соединяется с водой и потому применяется как очень сильное водоотнимающее средство. Оксиду фосфора (V) отвечает несколько кислот. Важнейшая из них – это ортофосфорная кислота
образуется при горении фосфора на воздухе или в кислороде в виде белой объемистой снегообразной массы; жадно соединяется с водой и потому применяется как очень сильное водоотнимающее средство. Оксиду фосфора (V) отвечает несколько кислот. Важнейшая из них – это ортофосфорная кислота ![]() . Она образует бесцветные прозрачные кристаллы, плавящиеся при 42,35ºС. В воде она растворяется очень хорошо.
. Она образует бесцветные прозрачные кристаллы, плавящиеся при 42,35ºС. В воде она растворяется очень хорошо.
Ортофосфорная кислота не принадлежит к числу сильных кислот. Константы ее диссоциации равны: ![]() ,
, ![]() ,
, 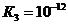 . Будучи трехосновной, она образует три ряда солей: средние и кислые с одним или с двумя атомами водорода в кислотном остатке:
. Будучи трехосновной, она образует три ряда солей: средние и кислые с одним или с двумя атомами водорода в кислотном остатке:
![]() ;
; ![]() - трехзамещенные, или средние фосфаты
- трехзамещенные, или средние фосфаты
![]() ;
; ![]() - двухзамещенные фосфаты, или гидрофосфаты
- двухзамещенные фосфаты, или гидрофосфаты
![]() ;
; ![]() - однозамещенные фосфаты, или дигидрофосфаты.
- однозамещенные фосфаты, или дигидрофосфаты.
В лаборатории фосфорную кислоту можно получать окислением фосфора 30%-ной ![]() . Реакция протекает согласно уравнению:
. Реакция протекает согласно уравнению:
![]()
В промышленности фосфорную кислоту получают двумя методами: экстракционным и термическим. В основе экстракционного метода лежит обработка природных фосфатов серной кислотой:
![]()
Образующуюся фосфорную кислоту отфильтровывают от сульфата кальция и концентрируют выпариванием. Термический метод состоит в восстановлении природных фосфатов до свободного фосфора с последующим его сжиганием и растворением образующегося фосфорного ангидрида в воде. Получаемая по этому методу термическая фосфорная кислота отличается более высокой чистотой и повышенной концентрацией.
Лабораторная работа № 5
р-Элементы IV группы периодической системы
1. Цель работы
1. Изучить электронное строение и свойства элементов IV группы главной А подгруппы на примере типических элементов углерода ![]() и кремния
и кремния ![]() .
.
2. На примере соединений углерода проанализировать образование ![]() -связей и гибридизацию атомных орбиталей (
-связей и гибридизацию атомных орбиталей (![]() ,
, ![]() ,
, ![]() ).
).
2. Контрольные вопросы
1. Охарактеризовать аллотропные модификации углерода и указать причину различия их свойств.
2. Какие типы гибридизации атомных орбиталей характерны для углерода?
3. В каких случаях при горении угля образуется оксид углерода (II) - ![]() ?
?
4. Дать краткую характеристику кремнию, указав: а) электронное строение атома и его валентные возможности; б) химические свойства свободного кремния.
5. Описать свойства угольной кислоты.
6. Указать тип гибридизации атомных орбиталей кремния в молекулах ![]() и
и ![]() . Полярны ли эти молекулы?
. Полярны ли эти молекулы?
7. Водяной газ представляет собой смесь равных объемов водорода и оксида углерода (II). Найти количество теплоты, выделяющейся при сжигании 112 л водяного газа, взятого при нормальных условиях.
3. Содержание работы и методические указания к ее выполнению
На «рабочем столе» ПК найдите значок программы « 1C: Химия». После загрузки программы, найдите вкладку «Альбом» / «Элементы IV группы: , ».
1. Изучить строение атомов и и молекул образуемых ими оксидов и кислот.
1.1. Зарисовать электронное строение атомов ![]() и
и ![]() .
.
1.2. Зарисовать структурную формулу молекулы оксида кремния ![]() .
.
1.3. Зарисовать структурную и геометрическую формулы молекулы оксида углерода (II) ![]() .
.
1.4. Зарисовать структурную и геометрическую формулы молекулы оксида углерода (IV) ![]() .
.
1.5. 3арисовать структурную и геометрическую формулы молекулы угольной кислоты ![]()
1.6. Зарисовать структурную формулу молекулы кремниевой кислоты ![]() .
.
2. Наблюдать проведение следующих опытов и записать уравнения реакций:
2.1. Взаимодействие карбида кальция с водой в присутствии индикатора фенолфталеина. Выделяется ацетилен.
2.2. Взаимодействие мрамора (или мела) с соляной кислотой. Выделяется
углекислый газ.
2.3. Взаимодействие карбоната натрия с водой. Выделяется углекислый газ. Изменение среды со щелочной на кислую и вновь на щелочную.
2.4. Взаимодействие гидроксида кальция с угольной кислотой. Выделяется осадок карбоната кальция, который растворяется при избытке угольной кислоты.
2.5. Взаимодействие силиката натрия с соляной кислотой. Выделяется осадок кремниевой кислоты.
2.6. Промышленные методы получения оксида углерода (II).
2.6.1. Пропускание воздуха или углекислого газа через раскаленный уголь.
2.6.2. Газификация угля.
3. В каждой окислительно-восстановительной реакции проставить степени окисления и записать полуреакции.
4. Написать названия соединений в химических реакциях.
5. Для реакций, в которых происходит гидролиз какого-либо продукта, написать уравнение гидролиза.
Приложение
В IV группу входят углерод ![]() , кремний
, кремний ![]() , германий
, германий ![]() , олово
, олово ![]() и свинец
и свинец ![]() . Электронная конфигурация невозбужденных атомов элементов
. Электронная конфигурация невозбужденных атомов элементов ![]()
![]() (валентные электроны), причем на р-орбиталях находится 2 неспаренных электрона (правило Гунда):
(валентные электроны), причем на р-орбиталях находится 2 неспаренных электрона (правило Гунда):
![]()
![]()
|
|
|
В своих соединениях элементы IV-A- группы, имеют, как правило, две степени окисления: (+II) или (+IV). Устойчивость соединений со степенью окисления (+II) увеличивается от С к Рb, что подтверждается в частности изменением энергии Гиббса:
![]()
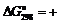 41 кДж
41 кДж
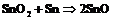
![]() 6 кДж
6 кДж
![]() ,
, ![]() 185 кДж
185 кДж
Из значений ![]() следует, что соединения
следует, что соединения ![]() (II) должны быть сильными восстановителями, а соединения
(II) должны быть сильными восстановителями, а соединения ![]() (IV) - сильными окислителями (
(IV) - сильными окислителями (![]() ,
, ![]() ).
).
Элементы IV - А - группы в степени окисления (+IV) образуют слабые кислоты (![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() ), а со степенью окисления (+II) – малорастворимые основания составов
), а со степенью окисления (+II) – малорастворимые основания составов 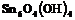 ,
, ![]() , которые проявляют амфотерные свойства. Устойчивость гидридов резко падает от метана
, которые проявляют амфотерные свойства. Устойчивость гидридов резко падает от метана ![]() (
(![]() 51 кДж/моль) к плюмбату
51 кДж/моль) к плюмбату ![]() . Уже моносилан
. Уже моносилан ![]() является эндотермическим соединением (
является эндотермическим соединением (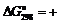 57кДж/моль).
57кДж/моль).
Гидролиз всех тетрагалогенов термодинамически возможен:
![]()
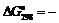 380 кДж
380 кДж
![]()
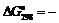 278 кДж
278 кДж
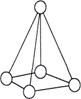 Углерод, кремний и германий имеют несколько аллотропных модификаций, одной из которых является модификация с атомной кристаллической решеткой алмаза.
Углерод, кремний и германий имеют несколько аллотропных модификаций, одной из которых является модификация с атомной кристаллической решеткой алмаза.
Алмаз - метастабильная модификация углерода. В его кристаллах каждый атом углерода окружен 4 такими же атомами, располагающимися в вершинах правильного тетраэдра.
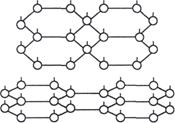 Графит - стабильная аллотропная модификация углерода со слоистой структурой, состоящая из шестичленных бесконечных колец.
Графит - стабильная аллотропная модификация углерода со слоистой структурой, состоящая из шестичленных бесконечных колец.
Кристаллическую решётку графита можно считать переходной между молекулярной и металлической решетками.
Кристаллическая решётка третьей аллотропной модификации углерода - карбина состоит из линейных цепей:
Расстояние между ними меньше, чем между слоями графита, за счет более сильного межмолекулярного взаимодействия. Карбин образует кристаллы белого цвета. У углерода допускают существование еще двух малоизученных модификации металлического углерода (углерод (III) и углерода ![]() ). Химическая активность возрастает от углерода (графит) к германию, а среди аллотропных модификаций углерода наименее химически активен алмаз. При пропускании, водяного пара через сильно нагретые
). Химическая активность возрастает от углерода (графит) к германию, а среди аллотропных модификаций углерода наименее химически активен алмаз. При пропускании, водяного пара через сильно нагретые ![]() ,
, ![]() или
или ![]() можно наблюдать реакции:
можно наблюдать реакции:
![]()
![]()
В кислороде при высоких температурах ![]() ,
, ![]() ,
, ![]() сгорают с образованием оксидов
сгорают с образованием оксидов ![]() ,
, ![]() ,
, ![]() и
и ![]() .
.
С водородом ![]() ,
, ![]() ,
, ![]() непосредственно не взаимодействуют, а с
непосредственно не взаимодействуют, а с ![]() вступает в реакцию только
вступает в реакцию только ![]() с образованием при t выше 1300 °С белого вещества состава тетранитрида трикремния
с образованием при t выше 1300 °С белого вещества состава тетранитрида трикремния ![]() . Кремний, в отличие от
. Кремний, в отличие от ![]() , может взаимодействовать с углеродом при температуре около
, может взаимодействовать с углеродом при температуре около ![]() с образованием карбида кремния
с образованием карбида кремния ![]() - химически инертного вещества, по твердости уступающего только алмазу.
- химически инертного вещества, по твердости уступающего только алмазу.
На углерод и кремний азотная, серная, хлорная и галогенводородные кислоты в обычных условиях не действуют.
В присутствии порошка меди кремний взаимодействует с безводным ![]() :
:
![]()
Эта реакция используется для промышленного получения трихлорсилана.
Аморфный углерод ![]() (активированный или древесный уголь) более химически активен. Азотная кислота
(активированный или древесный уголь) более химически активен. Азотная кислота ![]() окисляет его до
окисляет его до ![]() :
:
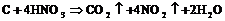
В ![]() германий подвергается пассивированию, но при нагревании медленно взаимодействует по реакции:
германий подвергается пассивированию, но при нагревании медленно взаимодействует по реакции:
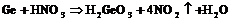
Он взаимодействует с растворами ![]() и
и ![]() :
:
![]()
![]()
Расплавы и водные растворы ![]() и
и ![]() взаимодействуют только с
взаимодействуют только с ![]() и
и ![]() :
:
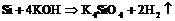
![]()
Углерод вступает в реакции с галогенами при нагревании. Со фтором углерод образует продукты состава ![]() , где n ≥ 1 (
, где n ≥ 1 (![]() ,
, ![]() ,
, ![]() и т. д.), а с другими галогенами «n» уменьшается до n=4, например
и т. д.), а с другими галогенами «n» уменьшается до n=4, например ![]() ,
,![]() .
.
Известно несколько оксидов углерода (![]() ,
, ![]() ,
, ![]() ) и по 2 оксида
) и по 2 оксида ![]() и
и ![]() (
(![]() ,
, ![]() ,
, ![]() ,
, ![]() ). Восстановительные свойства
). Восстановительные свойства ![]() при повышенной температуре сильнее, чем у водорода в реакции:
при повышенной температуре сильнее, чем у водорода в реакции:
![]()
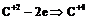 - восстановитель
- восстановитель
![]() - окислитель
- окислитель
![]() участвует в реакции присоединения:
участвует в реакции присоединения:
![]() - формиат калия
- формиат калия
0,5 мПа
С металлами ![]() образует комплексные соединения карбониды:
образует комплексные соединения карбониды:
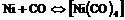
Для синтеза ![]() применяют главным образом следующие реакциии:
применяют главным образом следующие реакциии:
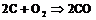 - в промышленности
- в промышленности
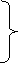 t
t
|
t
![]() Диоксид углерода -
Диоксид углерода - ![]() - газ без цвета и запаха, тяжелее воздуха. Твердый
- газ без цвета и запаха, тяжелее воздуха. Твердый ![]() возгоняется без плавления при 78°C. В жидком состоянии он может находиться только под давлением. Молекула
возгоняется без плавления при 78°C. В жидком состоянии он может находиться только под давлением. Молекула ![]() линейная, длина связи
линейная, длина связи ![]() -
- ![]() равна
равна
116 пм:
В воде ![]() растворяется: 1 л воды при 25°С и 0,1 мПа поглощает 0,76 л
растворяется: 1 л воды при 25°С и 0,1 мПа поглощает 0,76 л ![]() . Только 1%
. Только 1% ![]() взаимодействует с водой, образуя угольную кислоту:
взаимодействует с водой, образуя угольную кислоту:
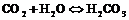
Диоксид углерода превращает водные растворы щелочных и щелочноземельных металлов и магния в гидрокарбонаты при избытке ![]() :
:
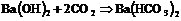
Гидроксиды и оксиды этих же элементов поглощают ![]() из воздуха:
из воздуха:
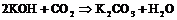
Диоксид углерода и водорода взаимодействуют (![]() ,
, ![]() ) в присутствии катализатора (смесь
) в присутствии катализатора (смесь ![]() и
и ![]() ) с образованием метанола:
) с образованием метанола:
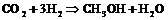
![]() получают в промышленности при разложении известняка:
получают в промышленности при разложении известняка:
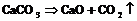
В лаборатории его получают по реакции:
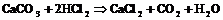
В свободном виде мономерные кислородные кислоты углерода, кремния и Германия (![]() ,
, ![]() ,
, ![]() ) не получены.
) не получены.
Карбонаты под действием кислот выделяют ![]() :
:
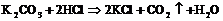
Протолиз ![]() в водном растворе протекает в основном до образования гидрокарбонатных анионов.
в водном растворе протекает в основном до образования гидрокарбонатных анионов.
![]()
![]()
Анионная кислота ![]() является еще более слабой:
является еще более слабой:
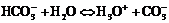
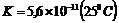
Кремниевые и германиевые кислоты слабее угольной, они выпадают в осадок при пропускании ![]() через их водный раствор.
через их водный раствор.
Лабораторная работа № 6
Электролиз
1. Цель работы
1. Познакомиться с электрохимическими процессами, происходящими при электролизе.
2. Научиться записывать уравнения процессов электролиза растворов и расплавов солей, щелочей и кислот.
2. Контрольные вопросы
1. Какой процесс называется электролизом?
2. Какая величина называется «потенциалом разложения»?
3. Каким закономерностям подчиняются количественные соотношения при электролизе?
4. От каких факторов зависит процесс электролиза, на какие группы он делится?
5. .Будут ли отличаться по составу продукты электролиза расплава и водного раствора ![]() ?
?
6. Составить схемы электролиза водных растворов ![]() ,
, ![]() ,
, ![]() с платиновыми электродами.
с платиновыми электродами.
7. Написать уравнения электродных процессов, протекающих при электролизе водных растворов ![]() и
и ![]() с инертным анодом.
с инертным анодом.
8. Составить схемы электролиза водного раствора сульфата меди, если:
а) анод медный; б) анод угольный.
9. В какой последовательности будут выделяться металлы при электролизе раствора, содержащего в одинаковой концентрации сульфаты никеля, серебра, меди?
10. При электролизе растворов ![]() на аноде выделилось 560 мл газа (условия нормальные). Найти массу меди, выделившейся на катоде.
на аноде выделилось 560 мл газа (условия нормальные). Найти массу меди, выделившейся на катоде.
11. Вычислить массу серебра, выделившегося на катоде при пропускании тока силой 6А через раствор нитрата серебра в течение 20 минут.
3. Содержание работы и методические указания к ее выполнению
На «рабочем столе» ПК найдите значок программы « 1C: Химия». После загрузки программы, найдите вкладку «Альбом».
1. Постепенно открывая гипертекстовые ссылки, указанные ниже, наблюдайте проведение опытов и запишите уравнения реакций для следующих процессов электролиза:
· ссылка «Водород»
1.1.Электролиз водного раствора гидроксида калия.
· ссылка «Галогены»
1.2.Электролиз фтороводорода.
1.3.Электролиз хлорида натрия.
· ссылка « Элементы III группы»
1.4.Электролиз раствора оксида алюминия в расплавленном криолите.
· ссылка « Элементы II группы»
1.5.Электролиз расплава хлорида кальция.
· ссылка « Элементы I группы»
1.6 Электролиз расплава гидроксида натрия.
1.7 Электролиз расплава хлорида калия.
· ссылка « Переходные металлы»
1.8 Электролиз водного раствора сульфата марганца.
1.9 Электролитическое рафинирование меди.
2. Составьте схемы процессов электролиза.
Приложение
Электролизом называется окислительно-восстановительный процесс, протекающий при прохождении электрического тока, подаваемого от внешнего источника, через раствор или расплав электролита. При этом энергия постоянного тока превращается в химическую.
Электролизером называют ячейку с электролитом, в которую помещены два электрода, соединенных с внешним источником постоянного тока. Для исключения взаимодействия продуктов электролиза, образующихся на катоде и аноде, применяют диафрагмы или мембраны. Например, ионообменные мембраны, проницаемые только для ионов одного знака. Обычно катоды изготавливают из графита, стали, ртути, платины и никеля; аноды - из нержавеющей стали, графита, платины, никеля, а также из титана, покрытого оксидами металлов.
Электролиз протекает при определенном значении внешней разности потенциалов, называемом напряжением (потенциалом) разложения U нр. Потенциал разложения - это минимальное значение внешней разности потенциалов, приложенной к электродам, при котором начинается электролиз данного соединения. Это характерная для каждого соединения величина, стандартное значение которой приводится в справочниках.
Для простых соединений типа ![]() ,
, ![]() ,
, ![]() и др. U нр почти совпадает со стандартными окислительными потенциалами процессов их образования.
и др. U нр почти совпадает со стандартными окислительными потенциалами процессов их образования.
Количественные соотношения при электролизе подчиняются общим закономерностям всех электрохимических систем - законам Фарадея. Их общая формулировка: масса электролита, подвергающаяся превращению при электролизе, а так же масса образующихся на электродах веществ прямо пропорциональны количеству электричества, прошедшего через раствор или расплав электролита, и эквивалентным массам соответствующих веществ:
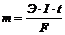 , где
, где
m – масса образовавшегося или подвергшегося превращению вещества; Э – его эквивалентная масса; I – сила тока; t – время; ![]() - число Фарадея, т. е. количество электричества, необходимое для осуществления электрохимического превращения одного эквивалента вещества.
- число Фарадея, т. е. количество электричества, необходимое для осуществления электрохимического превращения одного эквивалента вещества.
Характер протекания электродных процессов при электролизе зависит от многих факторов, важнейшими из которых являются состав электролита, материал электродов и режим электролиза (температура, напряжение, плотность тока и др.).
Процессы, протекающие при электролизе можно разбить на группы:
1. электролиз, сопровождающийся химическим разложением электролита;
2. электролиз, сопровождающийся химическим разложением растворителя;
3. электролиз растворов солей ряда металлов с растворимыми анодами из тех же металлов.
Часто 1 и 2 группы объединяют под общим названием электролиза с нерастворимыми (инертными) анодами. Инертные аноды в процессе электролиза химически не изменяются, а служат лишь для передачи электронов во внешнюю цепь.
Примеры электролиза:
1) Электролиз водного раствора ![]() с инертным анодом.
с инертным анодом.
Ионы ![]() и
и ![]() , образующиеся при диссоциации
, образующиеся при диссоциации ![]() , переносят электричество и участвуют в электродных процессах, что приводит к разложению электролита –
, переносят электричество и участвуют в электродных процессах, что приводит к разложению электролита – ![]() :
:
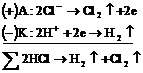
Схематически весь процесс можно представить следующим образом:
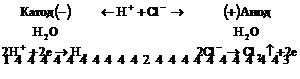
![]()
В ходе электролиза уменьшается содержание ![]() в электролите.
в электролите.
2) Электролиз водного раствора ![]() с платиновыми электродами.
с платиновыми электродами.
Ионы ![]() и
и ![]() , образующиеся при диссоциации
, образующиеся при диссоциации ![]() , переносят электричество, но в электродном процессе (анодном) участвует только один вид ионов,
, переносят электричество, но в электродном процессе (анодном) участвует только один вид ионов, ![]() , что не ведет к разложению электролита:
, что не ведет к разложению электролита:
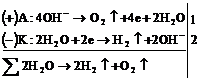
![]()
На катоде при более высоком катодном потенциале возможен процесс:
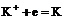 ;
; 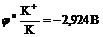
Однако преимущественно протекает процесс разложения молекул воды, разложение ![]() не происходит, его содержание в растворе не меняется, но среда у анода становится более кислотной, а у катода более щелочной. Схема процесса:
не происходит, его содержание в растворе не меняется, но среда у анода становится более кислотной, а у катода более щелочной. Схема процесса:
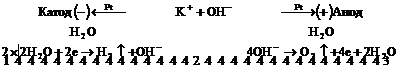
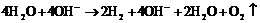
![]()
Аналогично происходит электролиз водных растворов ![]() ,
, ![]() и кислородсодержащих кислот.
и кислородсодержащих кислот.
3) Электролиз водного раствора ![]() с медными электродами.
с медными электродами.
Ионы ![]() и
и ![]() , образующиеся при диссоциации
, образующиеся при диссоциации ![]() , являются переносчиками электричества, но в электродных процессах принимают участие лишь ионы
, являются переносчиками электричества, но в электродных процессах принимают участие лишь ионы ![]() , поэтому катодный процесс обратен анодному:
, поэтому катодный процесс обратен анодному:
![]()
![]()
Химического разложения электролита не происходит, если значения выходов по току одинаковы для катодного и анодного процессов. Вследствие электродных процессов и переноса ионов изменяется содержание ![]() около электродов: в катодном пространстве оно уменьшается, а в анодном - увеличивается. Схема процесса:
около электродов: в катодном пространстве оно уменьшается, а в анодном - увеличивается. Схема процесса:
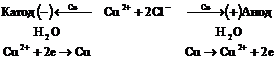

![]()
Электролиз расплавов электролитов протекает наиболее просто, поскольку в электролите находится лишь один вид катионов и один вид анионов:
![]()
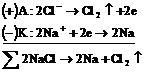
Схема всего процесса:
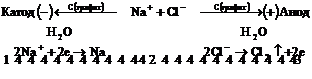
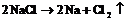
Электролиз растворов электролитов сложен из-за присутствия нескольких видов катионов и анионов, а так же недиссоциированных молекул воды. Когда на одном и том же электроде возможно протекание двух или более процессов, наиболее вероятен тот, осуществление которого связано с минимальной затратой энергии. Последовательность протекания электродных процессов определяется значениями их потенциалов и величиной поляризации. Поэтому на катоде восстанавливаются в первую очередь окисленные формы окислительно-восстановительных систем (окислители) с наибольшим (наиболее положительным) электродным потенциалом, а на аноде окисляются восстановленные формы (восстановители) с наименьшим (наиболее отрицательным) электродным потенциалом.
Литература
1. Степин, химия / , . – М.: Высшая школа, 1994. – 608 с.
2. Глинка, химия: Учебное пособие для вузов / / под ред. . – Л.: Химия, 1985. – 704 с.
3. Швехгеймер, химия / , . – М.: Высшая школа, 1994. – 544 с.
4. Глинка, и упражнения по обшей химии: Учебное пособие для вузов / / под ред. и . – М.: Интеграл-пресс, 1997. – 240 с.
5. Ахметов, и неорганическая химия: Учеб. для вузов / Н. С Ахметов. – М.: Высшая школа, 2003. – 743 с.
6. Угай, химия / . – Высшая школа, 1984. – 590 с.
7. Угай, и неорганическая химия / . – М.: Высшая школа, 1997. – 605 с.
содержание
Введение……………………………………………………………….…3
Лабораторная работа № 1……………………………………….…… . .4
Лабораторная работа № 2………………………………………… …..12
Лабораторная работа № 3…………………………………………… ..25
Лабораторная работа № 4…………………………………………… ..33
Лабораторная работа № 5…………………………………………… ..41
Лабораторная работа № 6………………………………………… …..47
Литература………………………………………………………………53
Учебное издание
Гончарова Галина Николаевна
Картавых Татьяна Николаевна
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ЛАБОРАТОРНЫМ РАБОТАМ ПО КУРСУ «ХИМИЯ»
Компьютерная верстка______________
Подписано в печать_________
Формат_______.Бумага_______.Печать________.
Объем 1,72 усл. Печ. Л. Тираж 500 экз. Заказ____
Отпечатано с готового оригинал-макета
В типографии______________________
__________________________________
Лицензия__________________________
Тел._______________________________

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |



