На правах рукописи
БАЛЫМ ЮРИЙ ПЕТРОВИЧ
ЭКСПЕРИМЕНТАЛЬНАЯ И КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ
ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ ПРЕПАРАТОВ СЕЛЕНА И ЭФФЕКТИВНОСТЬ ПРИМЕНЕНИЯ ИХ В ВЕТЕРИНАРИИ
16.00.04 – ветеринарная фармакология с токсикологией
Автореферат
диссертации на соискание ученой степени
доктора ветеринарных наук
Воронеж - 2009
Работа выполнена в отделе фармакологии и токсикологии
ГНУ «Всероссийский научно-исследовательский ветеринарный институт патологии, фармакологии и терапии» РАСХН
Научный консультант: доктор ветеринарных наук, профессор
Официальные оппоненты: доктор ветеринарных наук, профессор
доктор ветеринарных наук
доктор ветеринарных наук, профессор
Ведущая организация: ФГОУ ВПО Белгородская государственная
сельскохозяйственная академия
Белгородская обл., пос. Майский,
ул. Вавилова, 24
Защита состоится «23» октября 2009 г. в 10 часов на заседании совета
ДМ 006.004.01 при ГНУ Всероссийский научно-исследовательский ветеринарный институт патологии, фармакологии и терапии РАСХН 14б.
С диссертацией можно ознакомиться в библиотеке ГНУ ВНИВИПФиТ.
Автореферат разослан «___» __________ 2009 г.
Ученый секретарь
диссертационного совета
1. Общая характеристика работы
Актуальность темы. Создание широкой сети промышленных животноводческих
комплексов поставило перед ветеринарной наукой ряд проблем, связанных с совершенствованием технологических систем сельскохозяйственных предприятий, обеспечивающих получение здорового приплода с высокой резистентностью и реактивностью, с одной стороны, разработкой более эффективных средств и способов общей неспецифической и специфической профилактики и терапии болезней животных, особенно молодняка, с другой ( с соавт., 1987; , 2000; с соавт., 1997, 2000 и др.). Вместе с тем, очевидно, что применение лекарственных средств специфического этиопатогенного действия не может устранить основную причину патологического состояния, являющегося в большинстве случаев следствием нарушения метаболизма – высокоинтегрированного и целенаправленного процесса, обеспечивающего обмен веществ и энергии между клеткой и средой (, 2007; с соавт. 2008).
одной из причин замедления роста, дегенеративных изменений мышечной ткани и печени, кардиомиопатии, нарушений эмбриогенеза и репродуктивной функции может служить дефицит селена в рационе питания сельскохозяйственных животных (, 2003).
Негативные изменения в функционировании органов, систем органов и организма как единого целого при низком содержании селена обусловлены тем, что на клеточном уровне данный микроэлемент играет ключевую роль в поддержании целостности мембран, формирует активные центры таких ферментов, как глутатионпероксидаза, глицинредуктаза, формиатдегидрогеназа препятствует накоплению внутриклеточного кальция, участвует в метаболизме аминокислот и кетокислот, а так же целого ряда энергопродуцирующих превращений ( с соавт., 2002; с соавт., 2004; , 2004). Указанные свойства свидетельствуют об участии селена в первой и второй фазе биохимической адаптации: окисление чужеродных веществ с образованием органических окисей и перекисей, связывание и выведение активных метаболитов ( с соавт, 1998; с соавт., 2007).
В последние годы разработаны и предложены для практического применения комплексные препараты на основе селенита натрия (селерол, Е-селен, селевит, седимин и др.) и органические соединения селена: селенофилы, биоселен, дрожжевой селен, селенопиран, ДАФС-25. Вместе с тем, перечень селенсодержащих лекарственных средств не так велик, а некоторые из них обладают целым рядом недостатков, таких как, высокая токсичность, быстрый срок выведения из организма и некоторые др. В связи с чем, разработка новых комплексных селенсодержащих препаратов, проведение исследования по выяснению их фармакологических и токсикологических свойств, оценка эффективности органических и неорганических соединений селена является весьма перспективным для ветеринарии.
С учетом вышеизложенного, были определены общая направленность исследований, выбор методических подходов и объектов исследований, объем и разнообразие экспериментальных работ и клинической апробации новых препаратов.
Цель и задачи исследований. Целью данной работы было исследование токсических свойств и фармакологического действия новых селенсодержащих препаратов: селемаг (комплексный неорганический препарат селена), селеноорганического - селеданта и его субстанции – диметилдипиразолилселенида, оценка профилактической и лечебной эффективности селеданта и селемага при акушерско-гинекологических болезнях коров и свиней, заболеваниях новорожденных телят и поросят, и их влияние на продуктивность и качество продукции.
Для достижения данной цели на разрешение были поставлены следующие задачи:
- изучить биологическую активность и токсикологические свойства комплексного неорганического препарата селена – селемага;
- определить токсикологические параметры 4,4-ди-[3-(5-метилпиразо-лил)]селенид (ДМДПС) и препарата на его основе – селеданта;
- изучить биологическую активность ДМДПС;
- изучить фармакологическое действие селемага и селеданта на гомеостаз и репродуктивную функцию крупного рогатого скота и свиней;
- выявить влияние селеданта и селемага на рост, развитие, молочную и мясную продуктивность и качество молока и мяса крупного рогатого скота и свиней;
- изучить эффективность применения селеданта и селемага для профилактики болезней телят и поросят;
- разработать нормативную документацию и наставления по применению ДМДПС, селеданта и селемага.
Научная новизна. Впервые экспериментально разработаны и клинически оценены новые высокоэффективные препараты на основе неорганических и органических соединений селена для профилактики и лечения заболеваний продуктивных животных, улучшения роста и развития молодняка.
Изучены фармакологические свойства и определены параметры токсичности препаратов селена: селемага, селеданта и субстанции - диметилдипиразолилселенида.
В опытах на лабораторных и сельскохозяйственных животных установлено, что данные препараты обладают выраженными адаптогенными и антиоксидантными свойствами; их применение нормализует гомеостаз, повышает продуктивность, качество молозива, молока и мяса, репродуктивные функции коров и свиноматок, рост и развитие телят и поросят.
Конкретизированы и систематизированы данные о механизме действия препаратов селена. Установлено, что направленность биологической активности селенсодержащих препаратов зависит от химической природы соединений, входящих в состав лекарственного средства (неорганическая и органическая формы).
Показано, что применение селеданта, препарата органической природы, в большей степени способствует коррекции гомеостаза: снижению дисбаланса про - и антиоксидантных процессов, нормализации морфологических и биохимических показателей крови у крупного рогатого скота и свиней, чем использование селенита натрия и селемага. установлено более выраженное положительное действие селеданта, чем селемага на рост и развитие телят и поросят, молочную и мясную продуктивность, воспроизводительную способность животных, профилактику и лечение болезней коров, свиноматок, телят и поросят.
Результаты проведенных исследований вносят определенный вклад в развитие теории рационального использования различных форм микроэлемента селена для профилактики заболеваний, повышения продуктивности сельскохозяйственных животных и качества получаемого молока и мяса.
Научная новизна исследований подтверждена двумя патентами РФ № 000 и № 000.
Практическая значимость. Полученные результаты послужили основанием для разработки технологии получения, контроля качества и инструкции по применению субстанции ДМДПС для производства лекарственных средств для животных, которые вошли в разработанную и утвержденную нормативную документацию на 4,4-ди-[3-(5-метилпиразолил)]селенид
(СТО 08-2006) и инструкцию, утвержденную Россельхозназдором РФ (ПВР-2-1.7/01907 от 01.01.2001).
Разработаны технология производства, контроль качества и инструкция по применению лекарственного средства селеданта для регуляции окислительно-восстановительных процессов, нормализации обмена веществ, регуляции репродуктивной функции и профилактики послеродовых патологий, повышения резистентности животных к заболеваниям, которые вошли в нормативно-техническую документацию на препарат (СТО 05-2007) и инструкцию, утвержденную Россельхозназдором РФ (ПВР-2-1.7/01895 от 01.01.2001).
Разработаны технология производства, контроль качества и инструкция по применению лекарственного средства селемаг для профилактики и лечения заболеваний, развивающихся на фоне недостаточности витамина Е и селена, которые вошли в нормативную документацию на препарат селемаг
(ТУ от 01.01.2001 г.) и инструкцию по применению, утвержденную Россельхознадзором РФ (ПВР -2-4.3/01388 от 01.01.2001).
Разработаны и научно обоснованы показания к применению селемага и селеданта для повышения воспроизводительных функций коров и свиноматок, профилактики послеродовых заболеваний коров, свиноматок и желудочно-кишечных болезней телят и поросят, повышения молочной и мясной продуктивности, качества молока и мяса, роста и развития телят и поросят.
Апробация результатов исследований. Основные материалы диссертации доложены и обсуждены на ежегодных отчетных конференциях и заседаниях Ученого совета ВНИВИ патологии, фармакологии и терапии (Воронеж, гг.); Российском ветеринарном конгрессе, XV Московском международном ветеринарном конгрессе (2007); Всероссийской научно-практической конференции «Молочное и мясное скотоводство: состояние и перспективы развития в южном федеральном округе» (г. Черкесск, 2007); X Международной научно-практической конференции, посвященной 40-летию образования кафедры крупного животноводства и переработки животноводческой продукции и кафедры свиноводства и мелкого животноводства Белорусской ГСХА «Актуальные проблемы интенсивного развития животноводства» (Республика Беларусь, г. Горки, 2007); научно-практической конференции «Научное обеспечение ветеринарного обслуживания животноводства в условиях реформирования сельскохозяйственного производства» (г. Вологда, 2007); первом съезде ветеринарных фармакологов России (г. Воронеж, 2007); 16-й Всероссийской научно-методической конференции по патологической анатомии животных
(г. Ставрополь, 2007); XIV Международной научно-практической конференции «Современные проблемы интенсификации производства свинины» (г. Ульяновск, 2007); Международной научно-практической конференции «Современные проблемы ветеринарного обеспечения репродуктивного и продуктивного здоровья животных» (г. Воронеж, 27-29 мая 2009 г.).
Публикация результатов исследований. По теме диссертации опубликована 1 монография, 35 печатных работ, из них 12 в журналах, рекомендованных ВАК РФ, 2 патента.
Объем и структура диссертации. Диссертация изложена на 350 страницах компьютерного текста и состоит из введения, обзора литературы, материалов и методов исследований, результатов собственных исследований, обсуждения, выводов, практических предложений, списка литературы, включающего 217 отечественных и 117 иностранных авторов и приложения. Работа содержит 130 таблиц, иллюстрирована 14 рисунками.
Основные положения, выносимые на защиту:
- токсикометрические параметры ДМДПС, селеданта и селемага;
- фармакологические свойства ДМДПС, селеданта и селемага;
- состояние гомеостаза, продуктивность и качество продукции крупного рогатого скота и свиней при применении селеданта и неорганических препаратов селена;
- клиническая эффективность применения различных препаратов селена для профилактики послеродовых заболеваний коров, свиноматок и желудочно-кишечных болезней новорожденных телят и поросят.
2. Материал и методы исследования
Работа выполнена в гг. в отделе фармакологии и токсикологии ГНУ «Всероссийский научно-исследовательский ветеринарный институт патологии, фармакологии и терапии» Россельхозакадемии в соответствии с планами НИР по Государственной теме: "Изучить на молекулярно-биохимическом, структурно-функциональном, системно-физиологическом и экологическом уровнях и определить причины и механизмы перехода организма из нормального состояния в патологическое и на этой основе разработать средства, методы и технологии защиты здоровья и продуктивности животных" (№ гос. регистрации 01.200.117018).
Отдельные исследования по определению параметров токсичности изучаемых препаратов и по их влиянию на животных проведены при участии сотрудников ГНУ ВНИВИПФиТ , , В проведении научно-хозяйственных экспериментов принимали участие (ГНУ ВНИВИПФиТ), () и другие, которым автор выражает искреннюю признательность за оказанную помощь и плодотворное сотрудничество.
Научно-производственные опыты проведены на базе хозяйств Харьковской области: ЗАТ «Шебелинское» Балаклевского района; ПСП «Родина» Двуречанского района; ЗАСТ «Украина» Чугуевского района, с/комплекса «Слобожанский» Чугуевского района.
Экспериментальные и научно-производственные опыты проведены в соответствие с требованиями к врачебно-биологическому эксперименту по подбору аналогов, постановке контроля, соблюдению одинаковых условий кормления и содержания животных в период проведения работы и учета результатов (, 1965).
Для оценки биологической активности и изучения фармакотоксиколгических свойств диметилдипиразолилселенида, селеданта и селемага использовали культуру Paramecium caudatum, 660 белых мышей, 1316 белых крыс, 35 кроликов, 134 поросенка, 74 теленка и 20 морских свинок.
Для определения фармакологических свойств изучаемых препаратов в научно-хозяйственных опытах материалом для исследований служили 60 дойных и 96 сухостойных коров, 60 новорожденных телят, 45 телят на откорме, 60 свиноматок, 1400 новорожденных поросят, 45 поросят на откорме.
С целью выявления адаптогенных свойств ДМДПС проводили иммобилизацию белых крыс, являющуюся интегральной моделью острого стресса ( с соавт, 2000).
Стресс-корректорные свойства ДМДПС оценивали на модели эмоционально-физической нагрузки в условиях плавания мышей с грузом 5 % от веса тела ( с соавт., 1997).
Оценку антиоксидантных свойств препаратов селена проводили на модели «оксидативного стресса» путем введения животным 5,6-диоксиурацил-моногидратом (ДОУМГ), механизм общетоксического воздействия, которого реализуется посредством образования активных форм кислорода и запуском в клетке цепи свободнорадикальных реакций ( с соавт.,1986). ДОУМГ компании «Sigma» (коммерческое название – аллоксан) вводили в дозе 140,0 мг/кг однократно подкожно, длительность эксперимента - 14 дней. Массу тела животных определяли до введения ДОУМГ и на 14-е сутки эксперимента. Оценку эффективности защитного действия ДМДПС проводили на основании сравнения выживаемости и динамики изменения массы тела животных опытных групп по отношению к контрольной группе.
Токсические свойства препаратов оценивали методом определения острой и хронической токсичности, а отдаленных последствий – изучением аллергенной, эмбриотоксической, тератогенной и мутагенной активности в соответствии с «Методическими указаниями по определению токсических свойств препаратов, применяемых в ветеринарии и животноводстве» (ГУВ СССР, 1991) и руководством по экспериментальному (доклиническому) изучению новых фармакологических веществ (Москва, 2000).
Для оценки общего действия препаратов в крови определяли: количество эритроцитов (1012/л) и лейкоцитов (109/л) на счетчике частиц Культер-Каунтер, гемоглобина (г/л) – гемоглобинцианидным методом и с помощью гемометра Сали, глюкозу (мМ/л) ортотолуидиновым методом Гультмана в модификации Хиваринена-Никкила (, 1983); в сыворотке крови: общий белок (г/л) рефрактометрически, белковые фракции электрофорезом в агаровом геле (,1985), содержание мочевины (мМ/л) по цветной реакции Фирона в модификации (1976), общий кальций (мМ/л) комплексометрическим способом по Уилкинсону (, 1985), неорганический фосфор (мМ/л), активность щелочной фосфотазы, активность АЛАТ и АСАТ (мМ/л´ч) – колориметрическим методом с использованием спектрометра Specol 211, содержание общих липидов (г/л) – по цветной реакции с сульфофосфованилиновым реактивом (Кнайт с соавт., 1972), содержание холестерина (мМ/л) с помощью наборов фирмы «Lachema» на спектрофотометре СФ-46, содержание меди, цинка, марганца (мкМ/л), железа, магния, натрия (мМ/л) на атомно-абсорбционном спектрометре РЕ-703 фирмы «Perkin Elmer».
Для определения интенсивности процессов перекисного окисления липидов и состояния системы антиоксидантной защиты организма в крови определяли: содержание малонового диальдегида (мМ/л) (, , 1977), диеновых конъюгатов и кетодиенов (ед. опт. пл./мг липидов) ( с соавт., 1978); активность глутатионпероксидазы (мкМG-SH/л х мин х 103 (, , 1976); в сыворотке крови: содержание флуоресцирующих оснований Шиффа (опт. ед./мл) (W. R. Bidlack, A.L. Tappel,1973), витамина Е (мкМ/л) (, , 1972), витамина А (мкМ/л) по Бессею в модификации (1969); в плазме крови - содержание витамина С (мкМ/л) (, 1985).
Для изучения неспецифической резистентности и иммунологической реактивности организма животных в сыворотке крови определяли бактерицидную активность (БАСК) по и (1966), лизоцимную (ЛАСК) – по К. Кагромановой, (1966), комплементарную (КАСК) – по (1963), классы иммуноглобулинов G, M, А (мг/мл) – методом иммунодиффузии в агаровом геле по Манчини (1965); в крови: фагоцитарную активность лейкоцитов с антигеном Staph. аureus по (1950).
Молочную продуктивность коров учитывали путем проведения ежемесячных контрольных доек в течение двух смежных дней. Состав и свойства молозива и молока изучались в соответствии с методическими рекомендациями по технике анализа молока и молочных продуктов (ВИЖ, 1983) и по методике и (1988) с использованием следующих стандартов: органолептическая оценка, ГОСТ Р; определение чистоты молока, ГОСТ 8218-89; определение белка – методом формольного титрования, ГОСТ ; количество жира – стандартным сернокислым способом, ГОСТ 5867-90; плотность – с помощью ареометра типа АМ, ГОСТ 3625-84; кислотность – титрометрическим методом, ГОСТ 3624-92; размер и количество жировых шариков – подсчетом в камере Горяева.
Для изучения роста и развития подопытных животных проводили взвешивание их при рождении, а затем ежемесячно. На основании этих данных вычисляли абсолютную и относительную скорость роста по периодам выращивания по формуле С. Броди.
Для изучения мясной продуктивности проводили контрольной убой по методике ВИЖ (1977). У трех животных из каждой группы определяли: морфологический и химический состав туши, выход мышечной, жировой и костной ткани, проводили органолептическую оценку мяса.
Для характеристики клинического состояния животных при проведении экспериментов, определяли температуру тела, частоту пульса и дыхания, поедаемость кормов. Учитывали продолжительность беременности, характер течения родов, количество новорожденных телят и поросят, их массу при рождении и динамику роста, заболеваемость коров и свиноматок послеродовыми, а телят и поросят - желудочно-кишечными болезнями.
Расчет экономической эффективности проводили по в соответствии с «Методикой определения экономической эффективности использования в сельском хозяйстве результатов научно-исследовательских и опытно-конструкторских работ» (М.,1988).
Все полученные данные подвергали статистической обработке, с определением достоверности различий между соответствующими показателями контрольных, опытных и интактных групп животных, с использованием общепринятых методов математической статистики (, 1990; 1999) и прикладных программ «Statistica 5.5», «Excel» на РС «Celeron 2000».
3. Результаты собственных исследований
В экспериментах использовали: неорганическое соединение – селенит натрия, комплексный препарат на его основе – селемаг и органическое – субстанция - 4,4-ди-[3(5-метилпиразолил)]селенид (диметилдипиразолилселенид, ДМДПС) и препарат, созданный на основе ДМДПС – селедант.
3.1. Токсикометрическая и фармакологическая оценка
4,4-ди[3(5-метилпиразолил)] селенида
3.1.1. Острая и хроническая токсичность ДМДПС
При анализе результатов определения острой токсичности ДМДПС (табл. 1) установлено, что при внутрижелудочном введении его ЛД50 для белых мышей составляет 5800 мг/кг, белых крыс – 8079 мг/кг, а при внутрибрюшинном – соответственно 527,5 и 912,0 мг/кг массы тела, что позволило отнести ДМДПС к IV классу опасности – малоопасные вещества (ГОСТ 12.1.007-76).
Таблица 1
Параметры острой токсичности ДМДПС при однократном введении для
лабораторных животных (мг/кг)
Вид животных | Параметры токсичности | Ошибка, SLD50 | ||||
МПД | LD16 | LD50 | LD84 | LD100 | ||
Per os | ||||||
Белые мыши | 4850,0 | 5474,4 | 5800,0 | 6172,2 | 6650,0 | ±67,9 |
Белые крысы | 4000,0 | 5803,0 | 8079,0 | 10150,0 | 13000,0 | ±463,9 |
Внутрибрюшинно | ||||||
Белые мыши | 440,0 | 494,1 | 527,5 | 585,9 | 640,0 | ±8,70 |
Белые крысы | 450,0 | 686,0 | 912,0 | 1087,0 | 1350,0 | ±44,6 |
Симптомы отравления дмдпсом были однотипны и проявлялись пугливостью, адинамией, снижением роговичного рефлекса и реакции на внешние раздражители. Движения животных становились нескоординированными, учащенное дыхание сменялось редким. Они принимали боковое положение и погибали в глубокой коме. Латентный период отравления длился 15-90 минут в зависимости от введенной дозы. Смерть наступала в течение первых суток, а при введении высоких доз – через 1,5-2 часа.
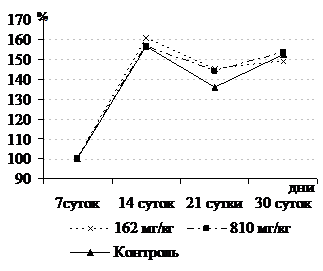
Хроническую токсичность ДМДПС оценивали при его многократном (в течение 30 дней) пероральном введении в дозах 162 и 810 мг/кг массы тела (1/50 и 1/10 дозы от LD50). Применение ДМДПС в указанных дозах не вызывало существенных изменений в клиническом состоянии животных: поведение, груминг, аппетит, частота дыхания крыс, как в период применения препарата, так и в течение одной недели после были в норме. Случаев гибели подопытных животных не было, они не отличались от контрольных по приросту массы тела и относительной массе внутренних органов (рис. 1).
Рис.1. Динамика массы тела белых крыс при многократном применении ДМДПС | При исследовании крови животных, которым вводили ДМДПС перорально в дозе 162,0 мг/кг массы тела, не отмечено существенных изменений в морфологических, биохимических показателях крови, по сравнению с таковыми у контрольных животных. Наиболее характерным изменением крови крыс, получавших ДМДПС в дозе 810 мг/кг, на 30-й день была незначительная гипопротеинемия и гипербетаглобулинемия, увеличение в сыворотке крови активности АлАТ, АсАТ – на 26,2 и 23,0 % соответственно, и на |
20,0% - уровня билирубина, однако средние значения этих показателей не выходили за верхние границы нормы для данного вида животных.
При гистологическом исследовании органов подопытных, животных получавших перорально ДМДПС в дозах 162,0 и 810,0 мг/кг в течение 30 дней, и павших в остром эксперименте при определении ЛД50 установлено следующее:
В печени отмечены слабо выраженные дистрофические изменения гепатоцитов, которые сохранялись и спустя 15 дней после окончания введения препарата.
В почках выявлено малокровие, в эпителии околоклубочковых канальцев слабо выраженные дистрофические изменения. В строме отмечена очаговая лимфоцитарная инфильтрация, клубочки разной величины, просвет капсулы либо сужен, либо отсутствует, в эпителии канальцев мутное набухание, дистрофические изменения. Однако, спустя 15 дней после окончания введения ДМДПС, в почках остаются лишь незначительные дистрофические изменения.
В селезенке у всех видов опытных животных отклонения от контроля однотипны и сохраняются без динамики вне зависимости от сроков исследования. Селезенка полнокровна, ее фолликулы округлые, разной величины, зародышевые центры крупные, в крупных фолликулах светлые, в мелких – темные, перифолликулярный пояс широкий и рыхлый, богат малыми лимфоцитами, лимфобластами, эозинофилами, сегментоядерными нейтрофилами. В межфолликулярной зоне умеренное количество клеток, среди которых встречаются плазматические.
Патологические изменения в остальных органах (миокард, легкие, тонкий кишечник, мозг и надпочечники) характеризовались полнокровием, кровоизлиянием, чаще периваскулярного характера, отложением гематогенного пигмента вокруг сосудов и прилежащей к ним ткани, незначительными дистрофическими изменениями.
Изучение общекомпенсаторных реакций при действии на организм животных ДМДПС проведено на белых мышах при пероральном и внутримышечном способах введения препарата в пробе плавания с грузом 5% от массы тела. Установлено, что однократное введение ДМДПС не оказывает влияния на работоспособность мышей. Длительное же 20-кратное введение ДМДПС в дозе 1/10 ЛД50 снизило работоспособность белых мышей в разной степени в зависимости от способа введения. При одинаковой массе животных в опытной и контрольной группах продолжительность плавания в первой группе (580,0 мг/кг – внутрь) уменьшилась почти в 2,3 раза, во второй (53,0 мг/кг – в/м) – 1,7 раза. препарат в дозах 10,0 (в/м) и 116,0 (внутрь) мг/кг снижал работоспособность мышей при динамической нагрузке всего на 6,0 и 8,2 % соответственно (табл. 2).
При определении коэффициента кумуляции дробное введение ДМДПС белым крысам в возрастающих дозах в начале первых четырех периодов не влияло значительно на прирост массы тела животных по сравнению с контрольной группой. К началу 6-го периода (0,75 ЛД50) отмечено снижение интенсивности роста крыс по сравнению с контролем, которое продолжалось до конца опыта.
Таблица 2
Влияние ДМДПС на выносливость белых мышей при динамической нагрузке
Кратность введения препарата | Продолжительность плавания животных (сек), доза, мг/кг | |||
11,0 (в/м) (n=10) | 116,0 (внутрь) (n=10) | 53,0 (в/м) (n=10) | 580,0 (внутрь) (n=10) | |
Контроль | 217,1±10,3 | 217,1±10,3 | 217,1±10,3 | 217,1±10,3 |
Однократное | 224,7±10,3 | 213,8±10,3 | 216,5±10,3 | 215,3±10,3 |
20-кратное | 204,1±7,4 | 199,4±11,7 | 126,7±8,1* | 94,5±4,2* |
*- Р < 0,05 по отношению к контролю

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |