Анализ истории болезни пациентов с ХСН позволяет отметить, что еще не редко в историях болезни встречаются диагностические заключения, использующие термин миокардит Абрамова-Фидлера. Это не удивительно, так как значительное число врачей старшего поколения в период обучения в институте изучало эту нозоологическую форму как самостоятельное заболевание. К сожалению, этот диагноз относится к числу укоренившихся врачебных заблуждений:
- во-первых Абрамов и Fiedler никогда не имели совместных работ. Fiedler опубликовал в 1900 г. работу, где описал картину острого воспаления в миокарде (воспалительная инфильтрация, отек, некротические изменения кардиомиоцитов). , цитирую по клинике «Ошибки в диагностике болезней сердца» - описал смерть пациента с симптомами ХСН и выраженной дилятацией полостей сердца, поступившей через 4 месяца от начала заболевания. Таким образом, термин миокардит Абрамова-Фидлера подразумевает тяжелое течение болезни.
- во-вторых: применяя термин "миокардит Абрамова-Фидлера" - врач упрощает ситуацию, исключая из рассмотрения клинические формы, которые приводят к тяжелому течению миокардитов - молниеносную форму, гигантоклеточный миокардит и т. д.
Таким образом, в современной клинике целесообразно воздержаться от вынесения в диагноз форм, не предусмотренных классификациями.
Особенностью миокардитов хронического течения является стертое, зачастую трудно определяемое начало заболевания и нередко рецидивирующий характер процесса. В отличие от острых, хронические миокардиты часто могут не иметь прямой связи с инфекцией. Как правило, это миокардиты, развивающиеся в рамках системных аутоиммунных заболеваний. Формально они могут быть отнесены к миокардитам вторичного характера, однако, скорее всего, это не совсем точно, поскольку сердце при диффузных заболеваниях соединительной ткани и системных васкулитах также является одним из плацдармов патологического процесса. Важно отметить, что поражение миокарда в таких случаях является далеко не основной причиной развития возможной сердечной недостаточности (СН), которая на фоне аутоиммунных болезней в основном развивается вследствие поражения клапанного аппарата.
Однако основную проблему для клиницистов представляют все-таки инфекционнообусловлепные хронические миокардиты. Эти миокардиты, в отличие от развивающихся в рамках системных аутоиммунных заболеваний, характеризуются наличием весьма большого количества жалоб у пациентов и сопровождаются разнообразными нарушениями сердечного ритма, а также развитием не связанной с поражением клапанного аппарата ХСН. Инфекционный процесс, приводящий к формированию хронических миокардитов, чаще всего имеет генерализованный характер и обусловлен возбудителями, развивающимися внутриклеточно.
Обычно для обозначения хронических инфекционoобусловленных миокардитов используют термин «инфекционно-аллергический миокардит». Этот термин нельзя не признать правомочным, поскольку он отражает наиболее частую суть этиологии данного патологического процесса - наличие инфекции и один из важнейших элементов его патогенеза - избыточный иммунный ответ. Однако современные данные свидетельствуют о том, что наряду с избыточностью иммунного ответа существуют другие важные особенности патогенетических механизмов развития хронического миокардита. Применение же пока еще сохраняющегося в некоторых лечебных учреждениях термина «неревматический миокардит» в сущностном и практическом отношении не имеет никакого смысла, кроме как исключение диагноза «ревматизм».
Комитет экспертов ВОЗ [20] для обозначения всех воспалительных заболеваний сердца предлагает использовать термин «воспалительная кардиомиопатия». Воспалительная кардиомиопатия (inflammatory cardiomyopathy) - это целая группа заболеваний, которая включает в себя все хронические воспалительные поражения мышцы сердца, все случаи дилатационной кардиомиопатии с воспалительной инфильтрацией в миокарде, все острые или хронические миокардиты, ассоциированные с перикардитом и с сердечной дисфункцией, все случаи идиопатических, аутоиммунных и инфекционных поражений миокарда, связанных с инфекцией и систолической дисфункцией, а также все случаи миокардитического кардиосклероза [10, 11]. Важным является то, что понятие «воспалительная кардиомиопатия» включает в себя не только процесс воспаления, но и его исход - миокардитический кардиосклероз.
Использование данного термина на практике значительно упрощает задачу врача, поскольку действительно бывает трудно определить - имеет данный процесс острый (конечный) характер или же он впоследствии может проявить себя в виде рецидива воспаления или развития СН вследствие кардиосклероза. И все же в большинстве случаев на практике хватает критериев, позволяющих уточнить диагноз, хотя бы в системе координат «острый - хронический», «инфекционнообусловленный или неинфекционнообусловленный» миокардит.
Таким образом, достаточно высокая частота заболевания, нередко имеющего стертое начало, сложность верификации процесса воспаления именно в ткани сердца, еще большая сложность обнаружения инфекционного возбудителя и его идентификации обусловливают особенную значимость хронических инфекционнообусловленных миокардитов в практике кардиолога.
 Алгоритм диагностики хронических инфекционнообусловленных миокардитов
Алгоритм диагностики хронических инфекционнообусловленных миокардитов
Диагностика хронических инфекционнообусловленных миокардитов весьма затруднительна. Несмотря на множество клинических симптомов, изменений лабораторных и инструментальных показателей, в большом числе случаев диагноз устанавливается лишь после очень тщательного анализа результатов обследования, при этом существенное значение имеют опорные клинико-инструментальных критерии заболевания. Наиболее известными являются схемы клинико-инструментальной диагностики миокардита NYHA (1964, 1973) и J. H.Goodwin [27]. По этим алгоритмам диагноз устанавливается на основе комбинации рутинных неспецифических клинико-лабораторных и инструментальных критериев воспаления и синдрома поражения миокарда при наличии факта перенесенной инфекции. Однако они не лишены существенных недостатков, поскольку не позволяют судить ни о протяженности воспалительной инфильтрации, ни о наличии миокардитического кардиосклероза.
С появлением новых методов диагностики воспаления в миокарде возникла возможность усовершенствования диагностического алгоритма с возможностью подтверждения именно хронического инфекционно обусловленного миокардита, как наиболее сложного для распознавания и верификации. При обследовании больных необходимо выполнить комплекс методов, сгруппированных в своеобразные диагностические направления:
- верификация повреждения кардиомиоцитов и иммунного воспаления;
- верификация нарушения электрической и механической функций сердца;
- выявление воспалительной инфильтрации (и ее протяженности) и фиброза в миокарде;
- выявление этиологических факторов (обнаружение вирусов и бактерий, очагов хронической инфекции).
Основой для начала диагностических исследований, безусловно, является постановка предварительного диагноза миокардита на основании данных анализа жалоб, анамнеза и физикального обследования. Реализация необходимых диагностических процедур не предполагает строго определен-
ной последовательности. Окончательный диагноз устанавливался при исключении других синдромосходных заболеваний (ИБС, не воспалительные кардиомиопатии, ревматическое поражение сердца, соединительнотканные дисплазии, пороки сердца, миокардиодистрофии па фоне эндогенных интоксикаций, эндокринной патологии и анемий и др.).
Анализ жалоб, данных анамнеза заболевания, результатов физикального обследования
Патогномоничных клинических симптомов хронического инфекционно-обусловленного миокардита не существует. Клиническая картина заболевания зависит от выраженности воспаления и миокардитического кардиосклероза и варьирует от малосимптомного течения до жизнеугрожающих нарушений сердечного ритма, тяжелой сердечно - сосудистой недостаточности и внезапной смерти. Иногда хроническое воспаление мышцы сердца начинается весьма отчетливо через 2-3 педели после перенесенной инфекции, но чаще больные затрудняются указать время начала заболевания, но при этом все же связывают ухудшение состояния на фоне переносимых инфекций или переохлаждений.
Основными жалобами при хронических инфекционно-обусловленных миокардитах являются боли в области сердца различной интенсивности, локализации и продолжительности, возникающие у 50-80% больных, сердцебиение (30-70%), перебои в работе сердца (25-60%), одышка при физической нагрузке и в покое (40-60%), отеки на нижних конечностях (5-15%), рецидивирующая субфебрильная лихорадка (10-25%). При объективном обследовании у 30-50% больных отмечается бледность кожных покровов, у 5-10% - акроцианоз, у 20-40% - лимфоаденопатия. В 10-30% случаев выявляется увеличение размеров сердца, в 20-50% - тахикардия, в 10-30% приглушение сердечных тонов, в 5-20% - ритм галопа.
Уровень артериального давления зависит от степени поражения миокарда и от его исходных значений. При тяжелом поражении мышцы сердца систолическое давление понижается, а диастолическое повышается. В период реконвалесценции артериальное давление может повышаться (как систолическое, так и диастолическое).
Признаки хронической ХСН выявляются у 15-36% больных миокардитом хронического течения. При хроническом воспалительном поражении миокарда проявления ХСН связаны и с протяженностью лейкоцитарной инфильтрации в миокарде, и с патологическим ремоделированием ЛЖ (увеличением диастолических размеров сердца и индекса массы миокарда), и с выраженностью миокардитического кардиосклероза [5].
Инструментальная верификация дисфункции сердца
На рентгенограмме органов грудной клетки у 15-30% больных миокардитом отмечается увеличение тени сердца и усиление легочного рисунка за счет венозного застоя, что косвенно свидетельствует о снижении сократительной способности миокарда.
Изменения, выявляемые при электрокардиографии (ЭКГ)
Электрокардиографические изменения при миокардитах наблюдаются у 50-90% больных, они неспецифичны и могут быть обусловлены как воспалительной инфильтрацией, так и миокардитическим кардиосклерозом и дистрофией кардиомиоцитов. В зависимости от локализации воспалительного процесса отмечается значительная вариабельность изменений па ЭКГ. Внедрение в широкую клиническую практику суточного мониторировапия ЭКГ позволяет регистрировать у больных миокардитом преходящие нарушения ритма и проводимости. Если патологические изменения на ЭКГ регистрируются в 30-50% случаев, то при проведении суточного мониторирования ЭКГ они выявляются у 70-90% больных.
У больных хроническим инфекционнообусловленным миокардитом при ЭКГ мониторировании чаще всего наблюдаются преходящие нарушения ритма и проводимости регистрировались у 92% пациентов, что было в два раза чаще, чем на ЭКГ в покое (47%). Структура нарушений ритма и проводимости была следующей: реполяризационные изменения (62%), синусовая тахикардия (51%), блокады ножек пучка Гиса (46%), частая наджелудочковая экстрасистолия (39%), синусовая брадикардия (38%), частая желудочковая экстрасистолия (32%), миграция водителя ритма (33%). Реже выявлялись мерцательная аритмия (26%), желудочковая тахикардия (18%) и предсердно-желудочковая блокада (9%). Установлено, что одни нарушения ритма и проводимости связаны преимущественно с признаками воспаления, а другие - с преобладанием процессов фиброза. Так, в дебюте воспаления миокарда, более характерными являются атриовентрикулярная блокада, синусовая тахикардия и миграция водителя ритма, в развернутой стадии процесса - наджелудочковая и желудочковая экстрасистолии и даже желудочковая тахикардия, а для рецидивов воспаления на фоне уже выраженного фиброза - блокады ножек пучка Гиса (нередко транзиторного характера).
В редких случаях (у 0,5-3% больных) миокардит может стать причиной развития крупных очагов некроза. В подобных случаях на ЭКГ в динамике отмечаются изменения, характерные для развития крупноочагового некроза миокарда в соответствующих отведениях (формируется патологический зубец QS).
Возникновение очаговоподобных изменений па электрокардиограмме (ЭКГ) отмечается практически при всех формах некоронарогенных заболеваний миокарда (ПЗМ) [1].
По нашим данным, приблизительно у 19% больных ПЗМ возникают трудности их дифференциации с ИБС, встречающейся значительно чаще. В настоящем сообщении рассматриваются лишь очаговоподобные изменения при доброкачественных (очаговых) инфекционно-аллергических (иммунологических) миокардитах (ИАМ), диффузных инфекционно-аллергических миокардитах (ДИАМ) и своеобразной форме ИАМ - миоперикардите.
Следует отметить, что патогенез очаговоподобных изменений при трех вышеназванных формах существенно отличается.
При относительно доброкачественной форме ИАМ изменения касаются преимущественно зубца Т; инвертированные зубцы Т локализуются в правой и левой группах грудных отведений. Отсутствует связь выявленных ЭКГ изменений с кардиалгиями, которые носят подчас длительный, изнуряющий пациента характер, отсутствуют определенные зоны иррадиации болевого синдрома в сердце, обычно (не всегда!) нитраты не эффективны. Могут определяться некоторые острофазовые лабораторные сдвиги, наблюдаемые при ИАМ (положительные реакция торможения миграции лимфоцитов - РТМЛ и тест дегрануляции базофилов - ТДБ, увеличение содержания продуктов перекисного окисления липидов и др.) [2].
Положительная динамика зубцов Т при ИАМ завершается в среднем в течение 4-9 педель. Однако в ряде наблюдений негативность зубцов Т была достаточно стабильной, что, по-видимому, указывает на значительные нарушения метаболизма миокарда - повреждение кардиомиоцитов, ускорение апоптоза, активизацию фагоцитарной функции макрофагов с выделением цитотоксина TNF и др.[3, 4].
Для целей дифференциальной диагностики доброкачественно протекающих
очаговых ИАМ и ИБС могут быть использованы (нередко забываемые) пробы с хлоридом калия, пропранололом (обзиданом), велоэргометрия (гипервентиляция).
Перечисленные пробы следует проводить только у больных с изначально отрицательным зубцом Т в двух и более отведениях ЭКГ.
Изменения ЭКГ, по-видимому, обусловлены наличием клеточного дефицита калия и выраженной катехоламиновой стимуляцией у рассматриваемого контингента больных.
Следует подчеркнуть появление у больных с исходно отрицательным зубцом Т положительных изменений этого зубца, существенной же динамики сегмента ST не отмечалось. Наблюдаемые сдвиги полностью противоположны фиксируемым при ИБС.
Следовательно, особенностью электрофизиологии миокарда у больных с доброкачественно протекающими ИАМ является выраженная лабильность фазы реполяризации в форме отчетливой «позитивной» динамики зубца Т в ответ на различные стимулы (симпатомиметические препараты, физическая нагрузка). Примечательно, что нитроглицерин у подобного контингента больных практически не меняет морфологию зубцов и интервалов ЭКГ.
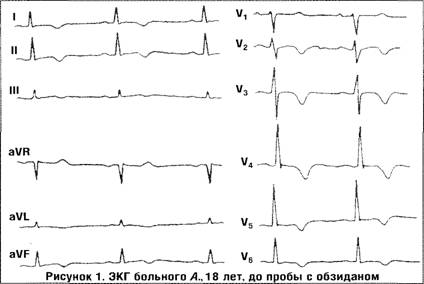
В качестве иллюстрации приводим наблюдение молодого пациента А. 18 с очаговым доброкачественным вариантом ИАМ.
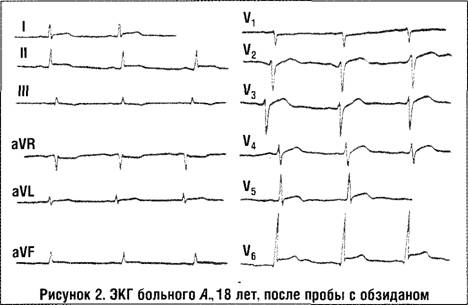
Больному проведена проба с обзиданом, которая дала положительный результат через 20 минут (рис. 1, 2). Таким образом, формы ИАМ, протекающие с относительно доброкачественным течением, характеризуются инвертированными зубцами Т, отсутствием изменений сегмента ST, острофазовыми лабораторными сдвигами, положительной динамикой зубца Т в ответ на определенные стимулы. Гемодинамические параметры не претерпевают значительных изменений и в случаях их возникновения отличаются обратимостью, нет тенденции к прогрессированию дилатации сердца, систолической и диастолической дисфункции.
Это подтверждено данными секторальной эхокардиографии (ЭхоКГ), зондированием правых отделов сердца; отсутствовали выраженные сегментарные нарушения.
Очаговоподобные ЭКГ изменения при ДИАМ заключаются в изменениях зубца Т, сегмента ST и появлении в ряде случаев патологического зубца Q. В подобных случаях дифференциация с ИБС встречает значительные трудности и иногда требует проведения сложных дополнительных методов исследования – вентрикуло - и коронарографии, субэндокардиальной биопсии миокарда.
При наличии патологического зубца Q во многих отведениях встает вопрос о возможности некоронарогенных крупноочаговых повреждений миокарда вплоть до формирования диффузных мышечных аневризм сердца. Патогенез очаговых повреждений миокарда при ДИАМ практически не отличается от такового при дилатационной кардиомиопатии (ДКМП) [5]. В формировании очаговых повреждений миокарда принимают участие гемодинамические факторы - снижение систолической функции ЛЖ, повышение постнагрузки вследствие неадекватности компенсаторной гипертрофии степени нарастания дилатации левого желудочка (ЛЖ).
Прогрессирующее увеличение дилатации ЛЖ приводит к перерастяжению, особенно субэндокардиальных участков миокарда с развитием «микронекрозов» по [6]. Нарушения трофики миокарда при ДИАМ способствуют суммации «микронекрозов» и возможному развитию крупноочаговых повреждений миокарда вплоть до формирования диффузных мышечных аневризм. Увеличение экстраваскулярного компонента коронарного сопротивления (рост конечного диастолического давления ЛЖ и напряжения его стенки) приводит к перераспределению коронарного кровотока, обеднению кровоснабжения миокарда, значительной редукции миофибрилл [7].
Обнаруживаемое в капиллярном русле микротромбозирование способствует диффузной ишемии миокарда. В случаях выраженной дилатации сердца отмечается также дилатация коронарных артерий, увеличение объемной плотности васкуляризации миокарда, выраженная дилатация микрососудов с перестройкой капиллярной сети; отмечается увеличение массы и объема миокарда обоих желудочков [8]. Выявляемая гиперваскулиризация, неадекватная выраженной дилатации основных отделов сердца, лишь способствует его декомпенсации. Следует также учитывать значительные электролитные и гипоксические нарушения при ДИАМ, которые способны приводить к метаболическому повреждению миокарда. Экспериментальные работы позволили выявить при миокардите увеличение эффективного рефрактерного периода и длительности потенциала действия, что с увеличением экспрессии ионных каналов было названо авторами «электрическим ремоделированием» миокарда [9].
Наконец, необходимо иметь в виду непосредственное (вирусно-иммунологические) токсическое повреждение миокарда и кардиомиоцитов, иммуноклеточную реакцию.
Весь вышеперечисленный комплекс изменений способствует прогрессированию дилатации сердца, приводит к систолической и диастолической дисфункции, ухудшению насосной функции сердца, оно приобретает сферическую форму. Процессы дилатации заметно преобладают над процессами гипертрофии, способствуя бивентрикулярному ремоделированию. Гуморальные и гемодинамические аспекты прогрессировавия ДИАМ (активизация нейрогуморальной системы, вазоконстрикция, дисфункция миокарда и др.) возникают на фоне дальнейшей хронизации воспалительного процесса.
При диффузных миокардитах отмечаются кардиомегалия, сердечная недостаточность, расстройства ритма и проводимости. На ЭКГ могут наблюдаться прямые признаки крупноочагового кардиосклероза - патологические зубцы Q, QS, однако соответствующих динамических изменений ST-T не отмечается («формальные» признаки очаговости). При ЭхоКГ и рентгенометрии выявляются дилатация всех камер сердца, значительные расстройства гемодинамики и сократительной функции сердца. В подобных сложных диагностических случаях приходится прибегать к субэндокардиальной биопсии миокарда, а иногда - к коронаро - и вентрикулографии.
Острофазовые гуморальные сдвиги (за исключением ТДБ) менее выражены, чем при очаговом НАМ.
Приводим соответствующее наблюдение. 22 лет, поступила в клинику в тяжелом состоянии с явлениями тотальной застойной сердечной недостаточности (одышка, цианоз, периферические и полостные отеки, гепатомегалия и др.), упорные кардиалгии.
Заболевание возникло через 3-4 недели после перенесенной пневмонии. На ЭКГ наряду с проявлениями легочной гипертензии - увеличенные зубцы Р I—II, V), отмечались глубокие патологические зубцы Q (QS) в отведениях I, aVL, V4, что не исключало возможности крупноочагового некоронарогенного повреждения миокарда (рис. 4).
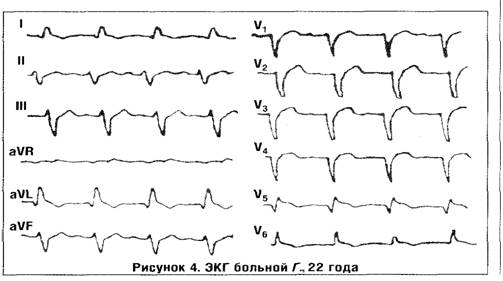
При рентгенологическом исследовании выявлена кардиомегалия. Субэндомиокардиальная биопсия миокарда свидетельствовала об активном аутоиммунном миокардиальном процессе с обнаружением гистиолимфо - цитарных инфильтратов. Для подтверждения крупноочагового повреждения миокарда с возможным формированием мышечной аневризмы была произведена коронаро-вентрикулография, которая при наличии интактных венечных артерий выявила аневризму ЛЖ. Течение заболевания характеризовалось неуклонным прогрессированием сердечной недостаточности, присоединением тромбоэмболических осложнений. Повторные госпитализации в клинику давали лишь кратковременный результат. Заболевание закончилось смертельным исходом.
Патологоанатомическое исследование подтвердило основной диагноз и возникшие осложнения, в том числе мышечную аневризму передней стенки ЛЖ диаметром 3 см при полной проходимости венечных артерий.
Специально следует остановиться на своеобразной форме ИАМ - миоперикардите, при котором определенная монофазность ЭКГ кривой вызывает изначальные дифференциально-диагностические трудности.
Приводим наблюдение больного А., 18 лет, находившегося в клинике кардиологии с диагнозом инфекционно-аллергический миоперикардит. Диагноз был поставлен на основании соответствующих клинико-анамнестических (связь заболевания с острой респираторной вирусной инфекцией, упорные кардиалгии, тахикардия и др.), лабораторных (повышенные значения ТДБ до 40%, РТМЛ), инструментальных данных (ЭКГ, ЭхоКГ, рентгенометрия).
На ЭКГ (рис. 5) определялась выраженная конкордантность сегмента ST с появлением инвертированных зубцов Т.
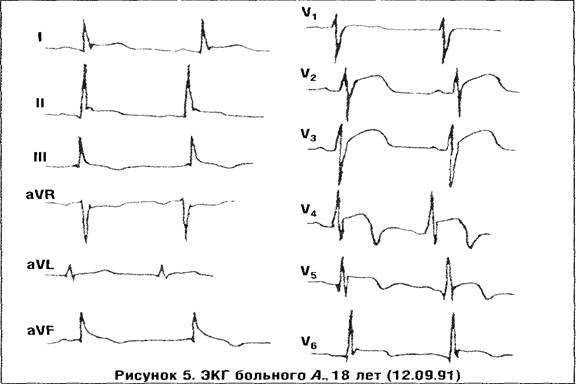
При динамическом клиническом и ЭКГ наблюдении клиническая картина и ЭКГ нормализовались (рис. 6).
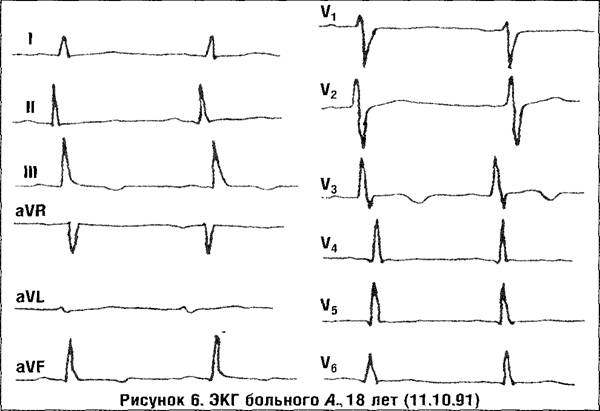
Дифференциация с ИБС не представляла значительных трудностей.
Течение заболевания, несмотря на начальную выраженность клинических (упорные кардиалгии) и ЭКГ проявлений, характеризовалось доброкачественностью, отсутствием гемодинамических изменений, позитивной эволюцией ЭКГ параметров. При вовлечении перикарда в аутоиммунный процесс с наличием конкордантного подъема сегмента ST во многих отведениях, длительного болевого синдрома в сердце нами не отмечено формирования патологического зубца Q. Следует подчеркнуть, что при ЭхоКГ в случаях миоперикардита не обнаруживался экссудат в полости перикарда, что свидетельствует о преимущественно фибринозном («сухом») характере перикардиальных изменений.
По данным Millaire и соавт. [10], с 1980 по 1993 г. в госпитале г. Лилля обследовано 47 больных с изменениями на ЭКГ, напоминающими инфаркт миокарда. У всех больных отмечался приступ болей за грудиной, у 9 из них ошибочно была использована тромболитическая терапия, причем у 2 - на догоспитальном этапе. Перикардиальных спаек и зубца Q отмечено не было, уровень креатининкиназы был нормальным. У всех больных наблюдалась полная нормализация ЭКГ. Длительный прогноз (46±29 мес.) был благоприятный.
Очаговоподобные формы миокардитов имеют множественный патогенез, требуют своеобразных диагностических подходов, характеризуются различной прогностической оценкой.
Изменения, выявляемые при эхокардиографии (Эхо КГ)
Косвенными признаками воспалительного поражения миокарда могут являться дилатация камер сердца (кардиомегалия), снижение систолической функции (фракции выброса - ФВ) и наличие жидкости в полости перикарда. Дилатация камер сердца может быть равномерной или аневризматической. Аневризматическое расширение левого желудочка (ЛЖ) при миокардитах в основном связано с развитием крупноочагового миокардитического кардиосклероза. Увеличение систолических и диастолических размеров ЛЖ может сопровождаться компенсаторной гипертрофией миокарда. Важным показателем, позволяющим объективно отслеживать увеличение камер сердца при динамическом наблюдении, является индекс сферичности. В норме он составляет 1,8- 1,6; снижение этого показателя (в динамике) ниже 1,5 свидетельствует о прогрессирующей дилатации ЛЖ.
 При воспалительном поражении миокарда в 10-20% случаев па Эхо КГ выявляется сопутствующий перикардит в виде сепарации листов перикарда в систолу. Очень редко перикардит бывает «сухим» (1 -3% случаев) с характерными аускультативными феноменами, в основном это экссудативный перикардит с незначительным количеством жидкости (с расхождение листов перикарда в области задней стенки ЛЖ до 1,0 см).
При воспалительном поражении миокарда в 10-20% случаев па Эхо КГ выявляется сопутствующий перикардит в виде сепарации листов перикарда в систолу. Очень редко перикардит бывает «сухим» (1 -3% случаев) с характерными аускультативными феноменами, в основном это экссудативный перикардит с незначительным количеством жидкости (с расхождение листов перикарда в области задней стенки ЛЖ до 1,0 см).
В 25-40% случаев у больных миокардитом снижается систолическая функция ЛЖ (ФВ), а изменение диастолической функции ЛЖ выявляется у 35-50%.
По нашим данным, расширение камер сердца и систолическая дисфункция в большей степени зависят от длительности заболевания и выраженности миокардитического кардиосклероза и в меньшей степени от воспалительной инфильтрации. Нарушение диастолической функции ЛЖ при миокардите отмечается при комбинации нескольких факторов: воспалительной инфильтрации в миокарде, миокардитического кардиосклероза и увеличении индекса массы миокарда ЛЖ [7].
Доказательство повреждения кардиомиоцитов и наличия иммуновоспалительного процесса.
Воспаление сердечной мышцы влечет за собой изменение биохимических и иммунологических показателей крови. Отмечается повышение концентрации кардиоспецифических ферментов и белков миокарда: креатининфосфокиназы (КФК), ее сердечного изоэнзима (КФК-МВ), лактатдегидрогеназы (ЛДГ). тропонина Т и I. Учитывая то, что разрушение кардиомиоцитов при миокардитах не столь значительно, как например, при инфаркте миокарда, повышение КФК, КФК-МВ и ЛДГ выявляется только у 25-40% больных, а превышение нормативных значений этих показателей отмечается не более, чем па 20-40%. Кроме того, отмечается лабильность вышеуказанных ферментов, которые нормализуются через 2-5 дней постельного режима и метаболической терапии. Кардиальные белки тропонин Т и I появляются в крови также при разрушении кардиомиоцитов. Они выявляются в крови всего у 30-40% больных, но сохраняются в циркуляции до 10-20 суток.
У больных миокардитом отмечается изменение белкового состава крови - α-, β- и γ-глобулинов, повышается концентрация сиаловой кислоты и С-реактивного белка, фибриногена. В целом повышение биохимических маркеров воспаления отмечается у 25-60% больных миокардитом, но, как правило, затрагивает только 1 -2 лабораторных теста.
Очень важно в диагностическом процессе использовать иммунологические тесты, свидетельствующие о поражении миокарда, т. к. иммунные диспропорции сохраняются достаточно длительное время - до 1,5 лет и более. У 40% больных миокардитом в сыворотке крови выявляются кардиальные антигены (являющиеся аутоантигенами), которые циркулируют до 4 месяцев, а у 70% пациентов выявляются антикардиальные антитела к различным белкам цитоскелета кардиомиоцита, находящиеся в циркуляции до 1,5 лет. Отмечается гиперчувствительность лимфоцитов к ткани миокарда, которая может быть выявлена в реакции торможения миграции лимфоцитов с кардиальным антигеном (РТМЛ).
Из неспецифических иммунологических тестов целесообразно отслеживать повышение концентрации интерлейкинов 1β 8,10, ФНО-α, адгезивных молекул, IgM, IgG, IgA и циркулирующих иммунных комплексов, которые являются показателями острого или хронического иммунного воспаления [3].
Начальная стадия заболевания (длительность 10±5 мес.) характеризуется распространенной лейкоцитарной инфильтрацией в миокарде без нарушения перфузии (кардиосклероз пока не выражен) и сопровождается повышением концентрации кардиоселективпых ферментов, биохимических маркеров воспаления, высвобождением и поступлением в кровоток кардиальных антигенов, а также минимальным уровнем спонтанной и индуцированной продукции ФНО-а при максимальном индексе стимуляции Ил-8. Следующая стадия заболевания (длительность 18+9 мес.) связана со специфическим иммунным ответом: на кардиальные антигены, при этом отмечается накопление в циркуляции специфических антикардиальных антител и сенсибилизированных к кардиальному антигену лимфоцитов. Этой стадии хронического миокардита соответствует ограниченный характер накопления меченых лейкоцитов в миокарде и появление фиброза. И, наконец, третья стадия (длительность 32±12 мес.) характеризуется отчетливым развитием фиброза при минимальной воспалительной инфильтрации в сердечной мышце. Для этой стадии миокардита типично наличие в крови специфических антител к миокарду, повышение спонтанной и индуцированной продукции ФНО-а при минимальном Ил-8. При этом параллельно отмечаются нарушение систолической, диастолической функции ЛЖ, реполяризационные изменения и блокады ножек пучка Гиса. Специфическая сенсибилизация лимфоцитов к тканям миокарда, определяемая в РТМЛ, выявлена у 87,5% больных миокардитом, но встречается с одинаковой частотой при различных вариантах воспалительной инфильтрации и фиброза в миокарде [8].
Верификация воспаления и фиброза в миокарде
При миокардитах хронического течения воспаление дистрофия и кардиосклероз за исключением самой ранней стадии процесса являются не последовательными, а параллельными патологическими процессами, происходящими в миокарде. Так, в одном гистологическом препарате можно обнаружить все эти изменения одновременно.
Выраженность (протяженность) воспалительной инфильтрации во многом определяется фазой воспалительного процесса. Она имеет максимальную распространенность (что соответствует понятию «диффузный миокардит») в дебюте заболевания и в период его рецидивов. Стихание же клинических проявлений воспалительного процесса сопровождается значительным сокращением площади инфильтрации в миокарде и ее своеобразным «рассыпанием» па отдельные зоны, что, видимо, соответствует понятию «очаговый миокардит».
Определение соотношения выраженности процессов воспаления и кардиосклероза весьма важно, так как клиническая картина хронического миокардита в значительной степени зависит от их баланса. Миокардит без выраженного кардиосклероза, особенно у больных молодого возраста, очень часто протекает малосимптомно (незначительные кардиалгии, изменение кардиоселективных ферментов и нарушения ритма), а манифестировать заболевание может только при его значимом развитии. При этом заболевание может обнаруживать черты не воспалительных форм поражения миокарда, т. к. на первый план выходят проявления ХСП, что существенно затрудняет диагностику [12].
Референтными методами обнаружения воспаления и фиброза являются методы морфометрии миокарда: биопсия эндомиокарда с последующим гистологическим изучением микропрепаратов; томосцинтиграфия миокарда с «воспалительными» и кардиотропными радиофармпрепаратами; магнитно-резонансная томография сердца с контрастированием и ультразвуковая денситометрия [3, 14, 17].
 Эндомиокардиальная биопсия
Эндомиокардиальная биопсия
Одним из методов диагностики воспалительной инфильтрации и фиброза в мышце сердца является эндомиокардиальная биопсия (ЭМБ). Для морфологического подтверждения диагноза считается необходимым взять от 3 до 7 биоптатов сердца (но не менее 3). При миокардитах в биоптатах сердца обнаруживаются специфические и неспецифические изменения. Основным морфологическим признаком воспаления является клеточная инфильтрация, которая может состоять из лимфоцитов, нейтрофилов, эозинофилов и гистиоцитов. Помимо воспалительной инфильтрации, в биоптатах можно выявить неспецифические изменения: отек межклеточного пространства, полнокровие сосудов микроциркуляторного русла, набухание эндотелия, дистрофические изменения кардиомиоцитов и миокардитический кардиосклероз.
Оценку результатов биопсии сердца проводят по критериям Далласской морфологической классификации миокардита [15]. При первичной эндомиокардиальной биопсии различают: а) активный миокардит с фиброзом или без фиброза; б) пограничный миокардит с фиброзом или без фиброза (в этом случае возможна повторная биопсия); в) отсутствие миокардита. При повторной эндомиокардиальной биопсии выделяют: а) продолжающийся миокардит с фиброзом или без него; б) разрешающийся миокардит с фиброзом или без него; в) разрешившийся миокардит с фиброзом или без него. Количественные морфометрическис критерии активного миокардита заключаются в обнаружении 14 лимфоцитов и более в ноле зрения (при увеличении микроскопа в 400 раз), пограничного от 5 до 14 клеток воспаления в поле зрения, при отсутствии миокардита - в поле зрения находят менее 5 клеток.
В соответствии с Марбургским соглашением Комитета экспертов ВОЗ (1997) рекомендовано выделять активный миокардит с фиброзом или без фиброза, хронический миокардит с фиброзом или без него и отсутствие миокардита. Отличие новых морфологических критериев от Далласских заключается в том, что оценка гистологического препарата проводится не в одном поле зрения, а на площади 1 мм2, т. е. количество клеток воспаления при активном миокардите должно быть не менее 14 на площади 1 мм2. Для верификации хронического миокардита целесообразно проведение иммуногистохимического исследования для определения специфических Т-лимфоцитов (CD-45) в мышце сердца, которые являются признаком именно хронического характера воспаления.
Следует учитывать, что ЭМБ не дает полной гарантии постановки диагноза, поскольку достаточно высока вероятность забора неизмененной ткани и получения «ложноотрицательного» результата. Опыт многих авторов показал, что ЭМБ подтверждает клинический диагноз миокардита только в 17-50% случаев.
Сцинтиграфия сердца с тропными к элементам воспаления радиофармпрепаратами
Для определения наличия и протяженности лейкоцитарной инфильтрации в мышце сердца используется томосцинтиграфия сердца с радиофармпрепаратами (РФП), тропными к элементам воспаления. К этим РФП относят цитрат галлияGa), аутолейкоциты, меченные технецием-99ш (99тТс) или индием-111-оксимом (ш1п), и антитела к миозину, меченные ш1п. Однофотонная эмиссионная компьютерная томография сердца (ОФЭКТ) позволяет получать качественные многомерные изображения миокарда с толщиной каждого томографического скана до 0,88 см, и таким образом по серии компьютерных срезов сердца определить наличие и протяженность лейкоцитарной инфильтрации в миокарде. Параллельно целесообразно проведение томосцинтиграфии с РФП, позволяющими оценить состояние перфузии миокарда, для чего используют 99гаТс (технетрил или 99mTc-MIBI) или 201Т1. РФП накапливается в интактной ткани сердечной мышце, оставляя участки ишемии, некроза и кардиосклероза в виде «дефектов накопления». При этом у мужчин старше 40-45 лет желательно исследование состояния коронарных артерий для исключения ишемического генеза кардиосклероза.
Таким образом, радиоизотопная диагностика в комплексе из двух исследований (определение воспалительной инфильтрации и перфузии миокарда) позволяет оценить наличие воспалительной инфильтрации в миокарде, а также определить нарушение перфузии, связанной с развитием миокардитического кардиосклероза.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 5 |


