Федеральное государственное образовательное учреждение
среднего профессионального образования
«Омский колледж торговли, экономики и сервиса»
ФИЗИЧЕСКАЯ И КОЛЛОИДНАЯ ХИМИЯ
опорный конспект лекций
для специальности:
260502 Технология продукции общественного питания
2010
ББК 74.5 Ф 48 | ОДОБРЕНО Цикловой методической комиссией естественно-математических дисциплин Протокол № 10 Дата 15.06.2010 Председатель |
Физическая и коллоидная химия: опорный конспект лекций для специальности: 260502 Технология продукции общественного питании / . – Омск: ФГОУ СПО «ОКТЭС», 2010. – 67с.
Опорный конспект лекций составлен в соответствии с требованиями Государственного образовательного стандарта среднего профессионального образования к минимуму содержания по дисциплине «Физическая и коллоидная химия» для специальности: 260502 Технология продукции общественного питания.
Работа с опорным конспектом лекций способствует переходу от обычного описательного восприятия физико-химических данных к количественным представлениям, т. е. приводит к глубокому и правильному их пониманию и, как следствие, к предсказательности протекающих процессов в коллоидных и других системах. Это помогает профессионально разрабатывать, используя научные основы физической и коллоидной химии, подходы к технологии получения, хранения и переработки продуктов питания.
Пособие предназначено для организации аудиторной и внеаудиторной работы студентов по дисциплине «Физическая и коллоидная химия».
Рецензенты: , преподаватель естественный дисциплин ФГОУ СПО «ОКТЭС»;
, преподаватель, председатель ПУК химических дис-
циплин ФГОУ СПО «Омский химико-механический колледж».
![]() © ФГОУ СПО «ОКТЭС», 2010
© ФГОУ СПО «ОКТЭС», 2010
Оглавление
Введение……………………………………………………………………………..4
Раздел 1. Физическая химия
Тема 1.1. Основные понятия и законы термодинамики. Термохимия …………5
Тема 1.2. Агрегатные состояния веществ, их характеристика …………………12
Тема 1.3. Химическая кинетика и катализ. Химическое равновесие. ………....18
Тема 1.4. Свойства растворов……………………………………………………..22
Тема 1.5. Поверхностные явления. Адсорбция…………………………………..32
Раздел 2. Коллоидная химия
Тема 2.1. Предмет коллоидной химии. Дисперсные системы ………………….38
Тема 2.2. Коллоидные растворы ………………………………………………….41
Тема 2.3. Грубодисперсные системы ……………………………………………...46
Тема 2.4. Физико-химические изменения органических веществ пищевых
продуктов…………………………………………………………………52
Библиографический список ………………………………………………………...64
Введение
Физическая химия – это наука, изучающая связь химических и физических свойств веществ, химических и физических явлений и процессов.
Физическую химию можно считать пограничной наукой между химией и физикой. Она имеет не только теоретическое, но и практическое значение.
Только на основе законов физической химии могут быть понятны, и осуществлены такие распространенные в различных отраслях пищевой промышленности процессы, как выпаривание, кристаллизация, сушка, сублимация, сепарация, дистилляция, экстрагирование и растворение. Без знаний методов физической химии невозможен технологический контроль пищевых производств: определение влажности, кислотности, содержание сахаров, белков, жиров, витаминов и т. д.
Основоположником физической химии является . Он в гг. первым из ученых прочитал студентам курс физической химии. Чтение курса сопровождалось демонстрацией опытов и проведением лабораторных работ. Ломоносов первый предложил термин «физическая химия» и дал этой научной дисциплине следующее определение: «Физическая химия есть наука, объясняющая на основе положений и опытов физики то, что происходит в смешанных телах при химических операциях». Таким образом, рассматривал физическую химию как науку, призванную дать физическое объяснение сущности химических процессов.
был написан первый в мире учебник по физической химии. Открытие великим ученым закона сохранения материи и энергии, учение о существовании абсолютного нуля, кинетическая теория газов, ряд работ по исследованию растворов явились основой зарождающейся физической химии, способствовали оформлению ее в самостоятельную науку. Период выделения в отдельную науку длился более 100 лет. Курс физической химии за это время никем из ученых не читался.
Одним из разделов физической химии, который превратился в самостоятельную науку, является коллоидная химия.
Коллоидная химия – это наука, изучающая свойства гетерогенных высокодисперсных систем и растворов полимеров.
Кулинарные процессы: коагуляция белков (при тепловой обработке мяса, рыбы, яиц и т. п.), получение стойких эмульсий (многие соусы), пен (взбивание сливок, белков, муссов), старение студней (очерствение хлеба, отделение жидкости от киселей, желе и т. п.), адсорбция (осветление бульонов) – относятся к коллоидным процессам. Они лежат в основе всех пищевых производств.
Законы физической и коллоидной химии лежат в основе мероприятий по охране окружающей среды. Как правило, сточные воды, дым заводских труб – также коллоидные системы. Методы разрушения этих коллоидных систем основаны на законах физколлоидной химии.
Раздел 1. Физическая химия
Тема 1.1. Основные понятия и законы термодинамики.
Термохимия
1. Основные понятия термодинамики.
2. Первый закон термодинамики.
3. Термохимия.
4. Второй закон термодинамики.
1. Основные понятия термодинамики
Термодинамика – наука, которая изучает общие законы взаимного превращения энергии из одной формы в другую.
Химическая термодинамика количественно определяет тепловые эффекты различных процессов, выясняет принципиальную возможность самопроизвольного течения химических реакций и условия, при которых химические реакции могут находиться в состоянии равновесия.
Объектом изучения в термодинамике является система – тело или группа тел, фактически или мысленно отделенных от окружающей среды. Системой можно назвать кристалл минерала, раствор любого вещества в какой-либо емкости, газ в баллоне и т. д.
Систему называют термодинамической, если между телами, ее составляющими, может происходить обмен теплотой, веществом и если система описывается полностью термодинамическими параметрами.
Виды систем
(в зависимости от характера взаимодействия с окружающей средой)
Открытая | Закрытая | Изолированная |
Обменивается энергией и веществом с окружающей средой. | Не может обмениваться с окружающей средой веществом, но может обмениваться с ней энергией и работой. | Не имеет обмена веществом и энергией с внешней средой. Внутри системы могут происходить передача теплоты, взаимные превращения энергии, выравнивание концентраций, но внутренняя энергия системы остается постоянной. |
Примеры | ||
Открытая колба с раствором, из которой может испаряться растворитель, и которая может нагреваться и охлаждаться. | Плотно закрытая колба с веществом. | Реакция, идущая в термостате. |
Система может быть гомогенной – состоит из одной фаза (воздух, кристалл, соли) и гетерогенной – состоит из нескольких фаз (лед-вода, вода-бензол).
Фаза – часть гетерогенной системы, отделенная поверхностями раздела и характеризующаяся одинаковыми физическими свойствами во всех своих точках.
Окружающая среда – это все, что находится в прямом или косвенном контакте с системой. Принято считать, что окружающая среда имеет такой большой размер, что отдача или приобретение ею теплоты не изменяет ее температуру.
Состояние термодинамической системы определяется массой, объемом, давлением, составом, теплоемкостью и др. характеристикам, которые называются параметрами состояния.
Если параметры состояния системы со временем не изменяются, то такое состояние считается равновесным. В равновесной термодинамической системе параметры состояния связаны между собой определенными математическими уравнениями – уравнениями состояния (например, уравнение Клайперона-Менделеева для состояния идеального газа).
Параметры, которые поддаются непосредственному измерению, называют основными параметрами состояния. Параметры состояния, которые не поддаются непосредственному измерению (внутренняя энергия, энтальпия, энтропия, термодинамические потенциалы), рассматривают как функции основных параметров состояния.
Термодинамические процессы – изменения параметров состояния системы:
· изотермический (Т=const);
· изобарный (Р=const);
· изохорный (V=const).
Все тела в природе независимо от агрегатного состояния обладают определенным запасом внутренней энергии.
Энергия складывается из кинетической энергии молекул, включающей энергию поступательного и вращательного движения, энергии движения атомов в молекулы, электронов в атомах, внутриядерной энергии, энергии взаимодействия частиц друг с другом и т. п. Кинетическая и потенциальная энергия самого тела во внутреннюю энергию не входит. Внутренняя энергия является функцией состояния. Абсолютное значение внутренней энергии определить нельзя, можно только измерить изменение внутренней энергии (DU). Изменение внутренней энергии не зависит от пути перехода, а зависит только от начального и конечного состояния системы.
Теплота (Q) (или тепловой эффект процесса) – это количественная характеристика энергии, которую система в ходе данного процесса получает (отдает) от окружающей среды. Теплота является формой передачи энергии, реализуемой путем изменения кинетической энергии теплового (хаотического) движения частиц (атомов, молекул). Если процесс сопровождается переходом энергии от окружающей среды к системе, он называется эндотермическим, в противном случае – экзотермическим. Любая экзотермическая реакция в прямом направлении становится эндотермической, если она идет в обратном направлении, и наоборот.
Работа (А), совершаемая системой, обусловлена взаимодействием системы с внешней средой, в результате чего преодолеваются внешние силы, т. е. работа является одной из форм обмена энергией с окружающей средой и служит количественной характеристикой переданной энергии, причем передача энергии реализуется путем упорядоченного (организованного) движения молекул под действием определенной силы.
2. Первый закон (первое начало) термодинамики. Это всеобщий закон природы, закон сохранения и превращения энергии, соответствующий основному положению диалектического материализма о вечности и неуничтожимости движения. Впервые этот закон в 1842 г. сформулировал выдающийся немецкий физик Ю. Мейер.
Энергия не исчезает и не возникает из ничего, а только превращается из одного вида в другой в строго эквивалентных соотношениях.
В зависимости от вида системы первый закон термодинамики имеет различные формулировки.

 Для закрытой системы этот закон термодинамики устанавливает связь между теплотой, полученной или выделенной системой в некотором процессе, изменением внутренней энергии системы и произведенной при этом работой.
Для закрытой системы этот закон термодинамики устанавливает связь между теплотой, полученной или выделенной системой в некотором процессе, изменением внутренней энергии системы и произведенной при этом работой.
В изобарно-изотермических условиях, в которых функционируют живые организмы:
А=рDV, (1.2)
где:
р – внешнее давление,
DV – изменение объема системы.
Подставим (1.2) в (1.1).
Qр = DU+рDV = (Uкон – Uнач) + (рVкон – рVнач) = (Uкон + рVкон) – (Uкон + рVнач) (1.3)
Сумма внутренней энергии системы и произведения объема на давление (U+рV) называется энтальпией (Н) – термодинамическая функция, характеризующая энергетическое состояние системы при изобарно-изотермических условиях. Таким образом:
Qр=DН (1.4)
Энтальпия – это сумма всех видов энергии, сосредоточенной в данной системе, включая и механическую энергию частиц, которая может проявиться в виде работы при расширении. Химические реакции и физико-химические процессы могут протекать с выделением и поглощением энергии. Их делят на экзотермические и эндотермические.
Процессы, в которых теплота выделяется, называются экзотермическими, процессы, протекающие с поглощением теплоты, – эндотермическими.
В экзотермических процессах энтальпия уменьшается (Нкон < Ннач), следовательно:
ΔH = (Hкон – Hнач)
ΔHэкзо < 0
В эндотермических процессах энтальпия увеличивается (Нкон > Ннач), следовательно:
ΔH = (Hкон – Hнач) > 0
ΔHэндо > 0
Энтальпия системы зависит от давления, температуры, количества вещества.
В изобарно-изотермических условиях количество теплоты, которое выделяется или поглощается в ходе химической реакции, характеризуется изменением энтальпии и называется энтальпией реакции DН. Изменение энтальпии реакции, определенное при стандартных условиях, называется стандартной энтальпией реакции и обозначается DН0.
Стандартные условия:
· количество вещества 1 моль;
· давление 760 мм. рт. ст. или 101,325 кПа;
· температура 2980К или 250С.
3. Термохимия
Химическое уравнение, в котором указано значение энтальпии (или тепловой эффект) реакции, называется термохимическим.
Термохимическими уравнениями пользуются в термохимии. Термохимия определяет тепловые эффекты химической реакции и переходов из одного состояния в другое. Термохимическое уравнение отличается от химического тем, что в термохимических уравнениях указывают абсолютную величину и знак теплового эффекта реакции, который относят к одному молю исходного или полученного вещества, поэтому стехиометрические коэффициенты в термохимических уравнениях могут быть дробными. В термохимических уравнениях отмечают также агрегатное состояние и кристаллическую форму.
 Энтальпию реакции можно определить как экспериментально, так и методом расчета с использованием энтальпий образования веществ, участвующих в химической реакции на основе закона Гесса (1840 г.):
Энтальпию реакции можно определить как экспериментально, так и методом расчета с использованием энтальпий образования веществ, участвующих в химической реакции на основе закона Гесса (1840 г.):
В термохимических расчетах большое значение имеют следствия из закона Гесса:
1 следствие. Энтальпия реакции равна разности алгебраической суммы энтальпий образования продуктов и исходных веществ с учетом стехиометрических коэффициентов в уравнении реакции.
 2 следствие. Энтальпия прямой реализации численно равна энтальпии обратной реакции, но с противоположным знаком.
2 следствие. Энтальпия прямой реализации численно равна энтальпии обратной реакции, но с противоположным знаком.
4. Второй закон термодинамики. Это закон имеет следующие формулировки:
Перенос теплоты от холодного тела к горячему связан с компенсацией, т. е. с необходимостью дополнительной затраты работы, которая переходит в конечном счете в теплоту, поглощаемую горячим телом (так, в домашнем холодильнике происходит перенос теплоты от предметов к деталям прибора, а затем к воздуху. Этот перенос требует затраты электроэнергии). Процессы, реализация которых связаны с компенсацией, называют необратимыми.

Тепло океана, например, может быть в принципе превращено в работу (согласно первому закону термодинамики), однако только при наличии соответствующего холодильника (согласно второму закону термодинамики).

Применительно к химическим реакциям (при Р, Т=const) это положение выражается следующим математическим уравнением:
DH = DG + TDS или DG = DH – TDS, (1.5)
где
DН – тепловой эффект реакции, наблюдаемый при ее необратимом течении;
DG – изменение свободной энергии Гиббса (свободной энергии при постоянном давлении), или изменение изобарно-изотермического потенциала, то есть это та максимальная часть энергии системы, которая в данных условиях может превратиться в полезную работу. При DG < 0 реакция протекает самопроизвольно.
Введенная в уравнение (1.5) функция S получила название энтропии.
Энтропия является функцией каждого конкретного, стационарного состояния и не зависит от пути к достижению нового состояния (например, от того, какие промежуточные стадии проходит система при переходе из состояния 1 в состояние 2).
Произведение TDS – переносимое тепло (Q), которое не может быть превращено в работу даже при обратимом ходе реакции (величина «связанной энергии»). Это произведение показывает количество внутренней энергии, теряемой в форме теплоты:
TDS = Q, или DS = Q/T, (1.6)
где
DS = S2-S1 – изменение энтропии системы при реакции, равное сообщенному системе теплу, деленному на абсолютную температуру, при которой система эту теплоту получает (отдает).
Кроме термодинамического потенциала – свободной энергий Гиббса G, в термодинамике в качестве вспомогательной функции для описания процессов большое значение имеет также и другой введенный термодинамический потенциал – свободная энергия Гельмгольца F (свободная энергия при постоянном объеме), или изохорно-изотермический потенциал:
DF = DU –TDS (при V, T=const) (1.7)
Самопроизвольные процессы могут производить работу. Равновесие наступает тогда, когда эта возможность исчерпывается. Поскольку самопроизвольным процессам соответствуют отрицательные изменения DF и DG, то знак изменения функции G (при Р, Т=const) или функции F (при V, T=const) и будет показывать возможность или невозможность самопроизвольного протекания реакции. Если изменения этих функций для состояния системы 1 и 2 равны нулю, то система находится в равновесии.
Энтропия отличается от других параметров состояния системы (P, T, V) тем, что ее численное значение и значение ее изменения не поддаются непосредственному измерению и могут быть получены только косвенным, расчетным путем. Для расчета DS энтропии реакции аА+bB=cC=dD надо из суммы энтропий веществ правой части уравнения вычесть сумму энтропий веществ левой части уравнения (с учетом стехиометрических коэффициентов). Так, для стандартных условий:
DS0298K = SDS0298K (продуктов) – SDS0298K (реагентов), (1.8)
Самопроизвольно в изолированной системе могут протекать только те процессы, которые связаны с увеличением энтропии, т. е. система из менее вероятного состояния переходит в более вероятное и достигает такого макроскопического состояния, которому соответствует небольшое число микроскопических состояний. Другими словами, процессы бывают самопроизвольными, когда конечное состояние может быть реализовано большим числом микросостояний и энтропия является мерой стремления системы к равновесию. Такие процессы должны сопровождаться увеличением энтропии.
Вопросы для самоконтроля:
1. Какие принципиальные вопросы решает химическая термодинамика?
2. Что называют системой, термодинамической системой?
3. Что называется параметрами состояния? Какие бывают параметры состояния?
4. Что называют термодинамическим процессом?
5. Как формулируется первое начало термодинамики?
6. В каком соотношении находятся энтальпия внутренняя энергия системы?
7. Что такое стандартная энтальпия образования?
8. Чем отличаются химические уравнения от термохимических?
9. Что определяет второе начало термодинамики?
10. Что нужно знать, чтобы определить принципиальную возможность той или иной реакции в данных условиях?
11. Какие термодинамические факторы определяет направление химических реакций?
12. Как изменяются изобарно-изотермический и изохорно-изотермический потенциалы в самопроизвольно идущем процессе?
13. Как рассчитать изменение изобарно-изотермического потенциала в реакции?
Тема 1.2. Агрегатные состояния веществ, их характеристика
1. Характеристика газообразного состояния вещества.
2. Характеристика жидкого состояния вещества.
3. Характеристика твердого состояния вещества.
В зависимости от внешних условий (температуры и давления) каждое вещество может находиться в одном из трех агрегатных состояний: твердом, жидком или газообразном. Эти состояния называются агрегатными состояниями. Для некоторых веществ характерно только два или даже одно агрегатное состояние. Например, нафталин, йод при нагревании в обычных условиях из твердого состояния переходят в газообразное, минуя жидкое. Такие вещества, как белки, крахмал, каучуки, имеющие огромные макромолекулы, не могут существовать в газообразном состоянии.
Газы не имеют постоянной формы и постоянного объема. Жидкости имеют постоянный объем, но не имеют постоянной формы. Твердые характеризуются постоянством формы и объема.
1. Характеристика газообразного состояния вещества
Для газов характеры следующие свойства:
- равномерное заполнение всего предоставленного объема;
- малая плотность по сравнению с жидкими и твердыми веществами и большая скорость диффузии;
- сравнительно легкая сжимаемость.
Эти свойства определяются силами межмолекулярного притяжения и расстоянием между молекулами.
В газе молекулы находятся на очень большом расстоянии друг от друга, силы притяжения между ними ничтожно малы. При низких давлениях расстояния между молекулами газа настолько велики, что по сравнению с ними размером молекул, а, следовательно, объемом молекул в общем объеме газа можно пренебречь. При больших расстояниях между молекулами практически отсутствуют силы притяжения между ними. Газ в таком состоянии называется идеальным. При нормальных условиях Т=2730К (00С) и p=101,325 кПа реальные газы независимо от природы можно считать идеальными и применять к ним уравнение состояния идеального газа (уравнение Клайперона-Менделеева):
PV = n RT, (2.1)
где
Р – давление газа,
V – объем газа,
n – количество вещества,
R – универсальная газовая постоянная (в единицах СИ R =8,314 Дж/мольК),
Т – абсолютная температура.
Реальные газы при высоких давлениях и низких температурах не подчиняются уравнению состояния идеального газа, так как в этих условиях начинают проявляться силы взаимодействия между молекулами и уже нельзя пренебрегать собственным объемом молекул по сравнению с объемом тела. Для математического описания поведения реальных газов используют уравнение Ван-дер-Ваальса:
(р + n2 a/V2) (V - nb) = vRT, (2.2)
где
а и b – постоянные,
a/V2 – поправка на взаимное притяжение,
b – поправка на собственный объем молекул,
n – число молей газа.
С увеличением давления и понижением температуры расстояния между молекулами уменьшаются, а силы взаимодействия увеличиваются так, что вещество из газообразного состояния может перейти в жидкое. Для каждого газа существует предельная критическая температура, выше которой газ не может быть превращен в жидкость ни при каком давлении. Давление, необходимое для сжижения газа при критической температуре, называется критическим давлением, а объем одного моля газа при этих условиях критическим объемом.
 Состояние газа при критических параметрах называют критическим состоянием. В критическом состоянии исчезает различие между жидкостью и газом, они имеют одинаковые физические свойства.
Состояние газа при критических параметрах называют критическим состоянием. В критическом состоянии исчезает различие между жидкостью и газом, они имеют одинаковые физические свойства.
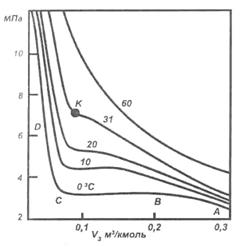
Переход газа в жидкость можно показать графически. На рисунке 1 приведена графическая зависимость между объемом и давлением при постоянных температурах. Такие кривые называются изотермами. У изотерм можно выделить три участка: АВ, ВС, CD при низких температурах. АВ – соответствует газообразному состоянию, ВС – отвечает переходу газа в жидкость, CD – характеризует жидкое состояние. С повышением температуры участок ВС уменьшается и превращается в точку перегиба К, называемую критической точкой.
Сжиженные газы находят большое промышленное применение. Жидкий СО2 используется для газирования фруктовых и минеральных вод, приготовления шипучих вин. Жидкий SO2 используют как дезинфицирующее средство для уничтожения плесневых грибков в подвалах, погребах, винных бочках, бродильных чанах. Жидкий азот широко применяют в медицине и биологии для получения низких температур при консервировании, замораживании крови и биологических тканей. Жидкие газы удобнее транспортировать.
2. Характеристика жидкого состояния вещества
В отличие от газов между молекулами жидкости действуют достаточно большие силы взаимного притяжения, что определяет своеобразный характер молекулярного движения. Тепловое движение молекулы жидкости включает колебательное и поступательное движения. Каждая молекула в течение какого-то времени колеблется около определенной точки равновесия, затем перемещается и снова занимает новое равновесное положение. Это определяет ее текучесть. Силы межмолекулярного притяжения не дают молекулам при их движении далеко отходить друг от друга. Суммарный эффект притяжения молекул можно представить как внутреннее давление жидкостей, которое достигает очень больших значений. Этим и объясняются постоянство объема и практическая несжимаемость жидкостей, хотя они легко принимают любую форму.
Свойства жидкостей зависят также от объема молекул, формы и полярности их. Если молекулы жидкости полярны, то происходит объединение (ассоциация) двух и более молекул в сложный комплекс. Такие жидкости называют ассоциированными жидкостями. Ассоциированные жидкости (вода, ацетон, спирты) имеют более высокие температуры кипения, обладают меньшей летучестью, более высокой диэлектрической проницаемостью. Например, этиловый спирт и диметиловый эфир имеют одинаковую молекулярную формулу (С2Н6О). Спирт является ассоциированной жидкостью и кипит при более высокой температуре, чем диметиловый эфир, который относится к неассоциированным жидкостям.
Жидкое состояние характеризуют такие физические свойства, как плотность, вязкость, поверхностное натяжение.
Поверхностное натяжение.
Состояние молекул, находящихся в поверхностном слое, существенно отличается от состояния молекул в глубине жидкости. Рассмотрим простой случай – жидкость – пар (рис. 2).
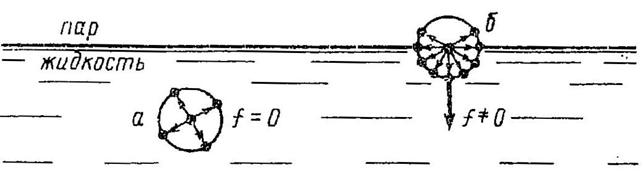 Рис.2. Действие межмолекулярных сил на поверхности раздела и внутри жидкости
Рис.2. Действие межмолекулярных сил на поверхности раздела и внутри жидкости
На рис. 2 молекула (а) находится внутри жидкости, молекула (б) – в поверхностном слое. Сферы вокруг них – расстояния, на которые распространяются силы межмолекулярного притяжения окружающих молекул.
На молекулу (а) равномерно действуют межмолекулярные силы со стороны окружающих молекул, поэтому силы межмолекулярного взаимодействия компенсируются, равнодействующая этих сил равна нулю (f=0).
Плотность пара значительно меньше плотности жидкости, так как молекулы удалены друг от друга на большие расстояния. Поэтому молекулы, находящиеся в поверхностном слое, почти не испытывают силы притяжения со стороны этих молекул. Равнодействующая всех этих сил будет направлена внутрь жидкости перпендикулярно ее поверхности. Таким образом, поверхностные молекулы жидкости всегда находятся под действием силы, стремящейся втянуть их внутрь и, тем самым, сократить поверхность жидкости.
Чтобы увеличить поверхность раздела жидкости, необходимо затратить работу А (Дж). Работа, необходимая для увеличения поверхности раздела S на 1 м2, является мерой поверхностной энергии или поверхностным натяжением.
Таким образом, поверхностное натяжение δ (Дж/м2 = Нм/м2 = Н/м) – результат некомпенсированности межмолекулярных сил в поверхностном слое:
δ = F/S (F – поверхностная энергия) (2.3)
Существует большое число методов определения поверхностного натяжения. Наиболее распространены сталагмометрический метод (метод счета капель) и метод наибольшего давления газовых пузырьков.
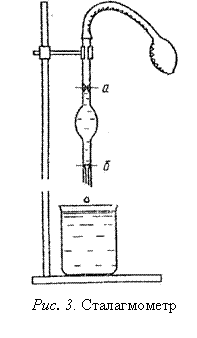
 Сталагмометр (рис.3) представляет собой толстостенную капиллярную трубку с расширением посередине; выше и ниже расширения находятся две метки (а и б), ограничивающие определенный объем. Нижняя часть сталагмометра заканчивается капилляром с отшлифованной поверхностью. Метод заключается в определении массы капли, вытекающей из капилляра. В момент отрыва масса капли преодолевает силу поверхностного натяжения, которое удерживает каплю на конце трубки. Чем больше капля, тем больше поверхностное натяжение.
Сталагмометр (рис.3) представляет собой толстостенную капиллярную трубку с расширением посередине; выше и ниже расширения находятся две метки (а и б), ограничивающие определенный объем. Нижняя часть сталагмометра заканчивается капилляром с отшлифованной поверхностью. Метод заключается в определении массы капли, вытекающей из капилляра. В момент отрыва масса капли преодолевает силу поверхностного натяжения, которое удерживает каплю на конце трубки. Чем больше капля, тем больше поверхностное натяжение.
При помощи методов рентгеноструктурного анализа было установлено, что в жид-костях есть некоторая упорядоченность пространствен-ного расположения молекул в отдельных микрообъемах. Вблизи каждой молекулы наблюдается так называемый ближний порядок. При удалении от нее на некоторое расстояние эта закономерность нарушается. И во всем объеме жидкости порядка в расположении частиц нет.
Вязкость η (Па·с) – свойство оказывать сопротивление перемещению одной части жидкости отно-сительно другой. В практической жизни человек сталкивается с большим множеством жидких систем, вязкость которых различна, – вода, молоко, растительные масла, сметана, мед, соки, патока и т. д.
Вязкость жидкостей обусловлена межмолекулярным воздействием, ограничивающим подвижность молекул. Она зависит от природы жидкости, температуры, давления.
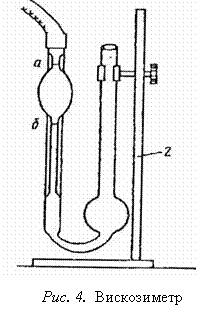
Для измерения вязкости служат приборы, называемые вискозиметрами. Выбор вискозиметра и метода определения вязкости зависит от состояния исследуемой системы и ее концентрации.
Для жидкостей с малой величиной вязкости или небольшой концентрацией широко используют вискозиметры капиллярного типа.
3. Характеристика твердого состояния вещества
Твердые тела в отличие от жидкостей и газов сохраняют свою форму. Силы притяжения между частицами, составляющими твердое тело, настолько велики, что они не могут двигаться свободно относительно друг друга, а только колеблются около какого-то среднего положения.
Все твердые тела делят на кристаллические и аморфные. В кристаллических телах частицы расположены в определенном характерном для каждого вещества порядке и этот порядок распространяется на весь объем. Во всем объеме аморфного тела порядка в расположении частиц нет. В этом отношении аморфные тела можно рассматривать как жидкости с аномально большой вязкостью.
Очень часто аморфная и кристаллическая формы являются различными состояниями одного и того же вещества. Так, диоксид кремния встречается в природе и в форме кристаллов кварца (горный хрусталь), и в аморфном виде – минерал кремень. Известен кристаллический и аморфный углерод.
Кристаллическая форма – наиболее устойчивая, вещества постепенно переходят из аморфного состояния в кристаллическое. В обычных условиях этот процесс идет очень медленно, повышение температуры может его ускорить. Например, сахар может быть в кристаллическом (сахар-песок, кусковой сахар) и в аморфном (карамелизованный) состояниях. Со временем карамель может кристаллизоваться, что нежелательно в кондитерском производстве.
Порядок в пространственном расположении частиц и кристаллических тел – кристаллическая решетка – определяет внешние признаки кристаллического состояния. К ним относятся: 1) определенная и резко выраженная температура плавления; 2) определенная геометрическая форма одиночных кристаллов; 3) анизотропия.
Вопросы для самоконтроля:
1. При каких условиях свойства реального газа приближаются к свойствам идеального?
2. Можно ли безгранично сжимать реальный газ?
3. Каков физический смысл постоянных в уравнении состояния реального газа?
4. Можно ли, зная температуру и давление, определить число молекул в единице объема?
5. Чем обусловлена малая сжимаемость жидкостей?
6. Как влияет на свойства жидкости образование водородной связи между молекулами?
7. Чем объяснить, что с повышением температуры уменьшаются поверхностное натяжение и вязкость?
8. По каким признакам можно отличить кристаллическое тело от аморфного?
9. В чем состоит основное различие в строении кристаллических и аморфных тел?
Тема 1.3. Химическая кинетика и катализ. Химическое равновесие
1. Скорость химической реакции.
2. Катализ и катализаторы.
3. Химическое равновесие.
1. Скорость химической реакции
Кинетика – учение о скорости и механизме химических реакций.
Вопрос о скорости химической реакции имеет большое практическое и теоретическое значение. От скорости реакции зависит течение биохимических процессов в организме, физико-химические изменения пищевых продуктов при тепловой обработке, производительность заводской аппаратуры.
Скорость химических процессов можно регулировать, изменяя условия их протекания. В некоторых случаях желательно интенсифицировать процесс, чтобы получить больше продукта в единицу времени. Иногда требуется уменьшить скорость химической реакции, например, замедлить окисление жиров в пищевых продуктах. Все эти задачи можно решить, применяя законы химической кинетики.

|
Из за большого объема этот материал размещен на нескольких страницах:
1 2 3 4 |




